11 березня, 2021
Нові підходи до лікування цукрового діабету: чи можлива перемога?
Майже 100 років пацієнти різних країн світу використовують для лікування цукрового діабету інсуліни виробництва компанії Novo Nordisk, яка здійснює постійний пошук нових можливостей для покращення життя хворих на діабет.
22 жовтня 2020 року, за підтримки фармацевтичної компанії Novo Nordisk (Данія), відбувся міжнародний симпозіум, де обговорювалися нові опубліковані дані, які можуть змінити підхід до лікування цукрового діабету (ЦД) 2-го типу. У заході взяли участь провідні фахівці з України, Хорватії та Італії.
Одним із вагомих продуктів у портфелі компанії Novo Nordisk є препарат групи сучасних неінсулінових цукрознижувальних препаратів – Віктоза®. Це давно й добре відомий препарат, проте науково-дослідницький інтерес до нього зберігається. На останньому конгресі Європейської асоціації з вивчення діабету (EASD) влітку 2020 року були оголошені перші результати дослідження LIRA-PRIME, які продемонстрували досягнення тривалого глікемічного контролю ЦД 2 типу на тлі прийому препарата Віктоза®.
Для більш детального розгляду всіх отриманих клінічних даних щодо результатів дослідження та обговорення інших клінічно значущих даних стосовно препарату Віктоза® було проведено міждисциплінарну зустріч національних і міжнародних експертів. Участь у цій зустрічі взяли член-кореспондент НАМН України, завідувачка відділення ендокринної гінекології, заступниця директора з наукової роботи ДУ «Інститут педіатрії, акушерства та гінекології імені О.М. Лук’янової НАМН України», доктор медичних наук, професор Тетяна Феофанівна Татарчук, керівниця відділу діабетології Інституту ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України, доктор медичних наук Любов Костянтинівна Соколова, завідувачка відділу гіпертонічної хвороби ДУ«Національний науковий центр «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України, доктор медичних наук Лариса Анатоліївна Міщенко, а також професор Університету Палермо (Італія), професор внутрішньої медицини Університету Південної Каліфорнії (США) Ріцо Манфреді та провідний європейський діабетолог, керівник клініки діабету, ендокринології та обміну речовин при Університеті ім. Врховача (Хорватія), професор Даріо Рахеліч.
Саме з доповіді професора Ріцо Манфреді про особливості дослідження корекції кардіоваскулярних ризиків у хворих на ЦД 2 типу й способи покращення цих ризиків розпочалася зустріч науковців.
про особливості дослідження корекції кардіоваскулярних ризиків у хворих на ЦД 2 типу й способи покращення цих ризиків розпочалася зустріч науковців.
Учений зазначив, що серцево-судинні захворювання (ССЗ) є основною причиною смерті хворих на ЦД 2 типу.
Підвищена частота ССЗ у пацієнтів із діабетом пов’язана з небажаними патофізіологічними механізмами гіперглікемії, включаючи безпосередній вплив підвищеного рівня глюкози в крові, ендотеліальну дисфункцію через оксидативний стрес та активацію атерозапальних цитокінів. Крім цього, зміни ліпідного метаболізму та складу ліпопротеїнів унаслідок інсулінорезистентності призводять до утворення менших і щільніших частинок холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ), роблячи їх, таким чином, більш атерогенними.
Головною метою лікування діабету є запобігання смертності та захворюваності на серцево-судинні та мікросудинні патології. Компанія Novo Nordisk допомогла провести міжнародне дослідження Capture.
CAPTURE – це перше глобальне неінтервенційне дослідження, метою якого було вивчення поширеності ССЗ, СС ризиків та підходів до лікування пацієнтів із ЦД 2 типу. Завданнями було виявити осіб із ЦД 2 типу з високим ризиком ССЗ та атеросклеротичними ССЗ, а також задокументувати використання серцево-судинних препаратів, які знижують подібний ризик, у пацієнтів із ЦД 2 типу та встановленими ССЗ. Атеросклеротичні ССЗ визначали як цереброваскулярні захворювання (зокрема, захворювання сонної артерії), ішемічну хворобу серця та/або хворобу периферичних артерій. Дослідження CAPTURE проводилося в Аргентині, Австралії, Бразилії, Чехії, Китаї, Франції, Угорщині, Ізраїлі, Італії, Японії, Мексиці, Саудівській Аравії та Туреччині із залученням майже 10 тис пацієнтів із ЦД 2 типу, діагностованим щонайменше 180 днів тому. Вік учасників мав бути не менше 18 років.
У ході дослідження виявилося, що 1 із 3 хворих на ЦД 2 типу буде мати ССЗ, і з більшою вірогідністю це буде атеросклеротичне ССЗ. Саме в такій ситуації на допомогу приходить аналог нативного глюкагон-пептидного гормону, що належить до родини інкретинів. Інкретини – це гормони, що сінтезуються в кишечнику, головним чином ГПП‑1 та глюкозозалежний інсулінотропний пептид (ГІП), які секретуються на низькому базальному рівні в стані голодування. Як ГПП‑1, так і ГІП після секреції піддаються розщепленню ферментом iДПП‑4.
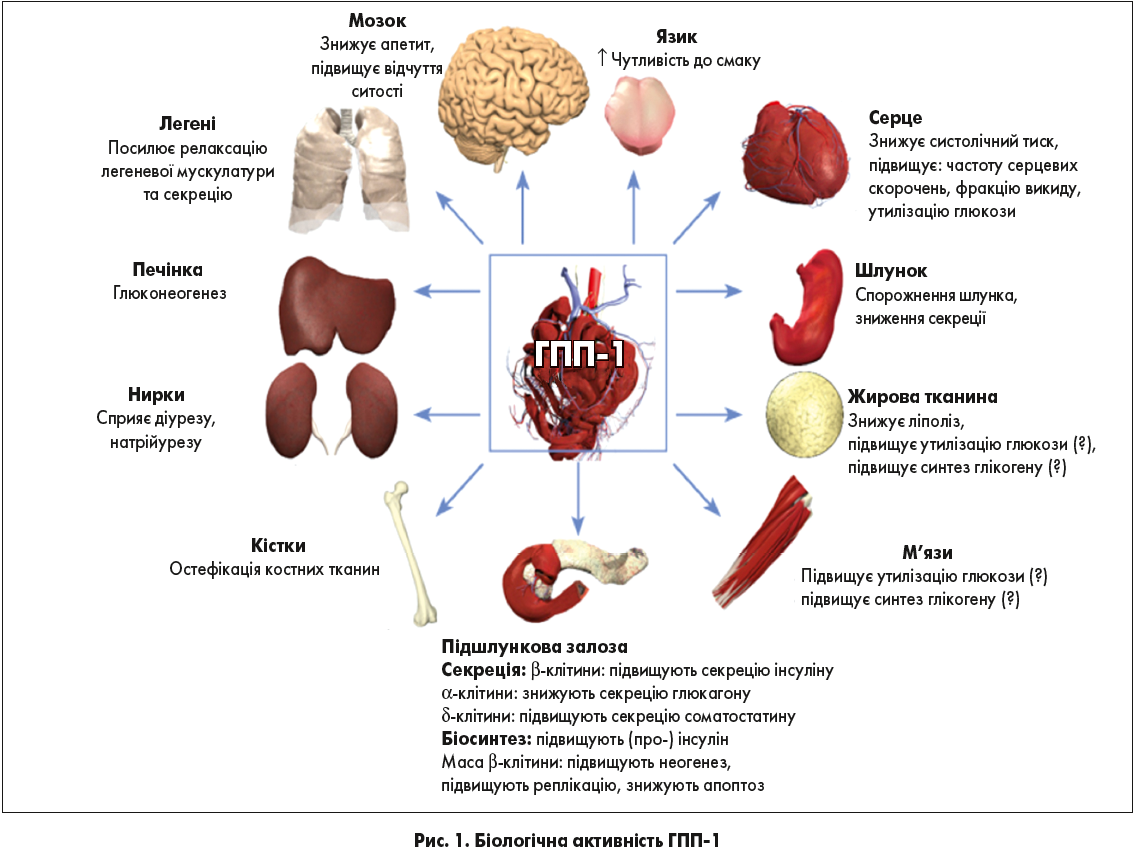
Глюкагоноподібний пептид‑1 (ГПП‑1) – багатогранний гормон із широким фармакологічним потенціалом. Серед численних метаболічних ефектів y ГПП‑1 є глюкозозалежна стимуляція секреції інсуліну, зменшення спорожнення шлунка, інгібування споживання їжі, збільшення натрійдіурезу. ГПП‑1 також має кардіо- та нейропротекторні ефекти, допомагає знизити запалення судин і є доклінісчні дані що свідчать про здатність впливати на апоптоз бета-клітин підшлункової залози.
ГПП‑1 чинить позитивну дію на функцію серця та судин, впливає на артеріальний тиск та обмін липідів, допомагає знизити масу тіла, впливаючи на центр апетиту в головному мозку (рис. 1).
Є два типи терапії, що базується на інкретині. Це лікування ЦД 2 типу агоністами рецепторів ГПП‑1 (арГПП‑1) чи інгібіторами дипептидилпептидази‑4 (iДПП‑4), дія яких відбувається внаслідок посилення сигналізації рецепторів інкретину.
Лікування, яке базується на арГПП‑1, рекомендоване науковими міжнародними настановами в якості препаратів вибору у хворих на ЦД 2 типу. Виділяють препарати на основі:
- аналогів людського ГПП‑1 – дулаглутид, ліраглутид;
- ексендинів – ексенатид, ліксисенатид.
Різниця між ними – це відсоток гомогенності або афінітивності до природного складника. Ліраглутид гомогенний на 97% до нативного ГПП-1. З огляду на особистий клінічний досвід, професор Ріцо Манфреді зазначив, що ліраглутид у вигляді препарату Віктоза® мав значний позитивний ефект на важливі кардіометаболічні показники в пацієнтів із ЦД 2 типу: зниження великих серцево-судинних макроваскулярних подій, зменшення обхвату талії, індекса маси тіла, зниження рівня глікованого гемоглобіну, покращення ліпідограми.
Оскільки деякі цукрознижувальні препарати (ЦЗП) викликали занепокоєння щодо підвищеного мікро- та макросудинного ризику, Управління із санітарного нагляду за якістю харчових продуктів і медикаментів США (FDA) ухвалило в 2008 р. рішення про дослідження серцево-судинних наслідків при ЦД (CVOT), щоб запобігти небажаному збільшенню ризику ССЗ.
У своєму виступі професор Ріцо Манфреді акцентував увагу на результатах відомого дослідження LEADER, в якому вивчався вплив ліраглутиду в дозі 1,8 мг на серцево-судинні ризики в пацієнтів із ЦД 2 типу. Дослідження було завершено в 2015 році. Воно було багатоцентровим, рандомізованим, подвійним сліпим та плацебо-контрольованим. У дослідженні LEADER брали участь пацієнти з ЦД 2 типу (HbA1с ≥7,0%), з факторами ризику ССЗ або з діагностованими ССЗ.
Загалом 9340 пацієнтів пройшли рандомізацію з вересня 2010 по квітень 2012 року; 4668 пацієнтам було довільно призначено ліраглутид, а 4672 – плацебо. Середній час прийому ліраглутиду або плацебо становив 3,5 року. Середня добова доза ліраглутиду дорівнювала 1,78 мг (міжквартильний діапазон від 1,54 до 1,79).
Демографічні та клінічні характеристики пацієнтів були однаковими в двох групах. З 9340 пацієнтів у 7598 (81,3%) були встановлені: ССЗ (6764 (72,4%) пацієнти), хронічна хвороба нирок ≥3 стадії (2307 (24,7%) пацієнтів) або обидві патології (1473 (15,8%) пацієнти). На початковому рівні середня тривалість діабету становила 12,8 року, а середній рівень HbA1с – 8,7%.
Було показано: 13,0% хворих, яким призначили ліраглутид, пережили першу смерть унаслідок ССЗ, нефатального (у тому числі так званого тихого) ІМ або інсульту, що не призвів до летального результату, проти 14,9% пацієнтів, які отримували плацебо. За результатами дослідження смерть через ССЗ наступила в 4,7% у групі ліраглутиду проти 6,0% у групі плацебо, рівень смертності від будь-якої причини – у 8,2 проти 9,6% відповідно, а частота нефатального ІМ та нефатального інсульту в групі ліраглутидів була нижчою за таку в групі плацебо. Автори дійшли висновку, що в пацієнтів із ЦД 2 типу, які приймають ліраглутид, рівень випадків першої смертності внаслідок ССЗ, нефатального ІМ або інсульту, що не призвів до летального результату, був нижчим за такий у групі плацебо.
Професор Ріцо Манфреді дав пояснення механізмам кардіоваскулярного впливу ліраглутиду при ЦД 2 типу.
Ліраглутид зменшує формування та прогресію атеросклеротичних бляшок. Головним чином це відбувається завдяки зменшенню рівня запалення, оксидації, формуванню ЛПНЩ, підвищенню та покращенню ендотеліальної функції, контролю рівня глюкози в крові. Рецептори ГПП‑1 експресуються в кардіоміоцитах та ендотеліальних клітинах, і доклінічні дослідження демонструють, що активація рецепторів ГПП‑1 покращує функцію ендотелію судин. Обмежені дані свідчать про те, що ГПП‑1 також можуть зберігати шлуночкову функцію.
Це дає підстави сподіватися, що своєчасне призначення ліраглутиду пацієнтам із високими / дуже високими кардіоваскулярними ризиками на тлі ЦД 2 типу або встановленими ССЗ атеросклеротичного генезу може позитивно вплинути на зменшення частоти серцевосудинних подій.
Тему необхідності контролю глікемії у хворих на ЦД 2 типу продовжив у своєму виступі професор Даріо Рахеліч (Хорватія).
Передусім він наголосив, що пацієнти з ЦД найбільш чутливі до інфікування на COVID‑19 та більш складного перебігу інфекції. Смертність у таких хворих вища майже на 40%.
Висока поширеність діабету робить його важливим коморбідним захворюванням у пацієнтів із COVID‑19. ЦД і супутні ускладнення можуть збільшити ризик захворюваності та смертності під час гострих інфекцій через пригнічені вроджені та гуморальні імунні функції.
Рівні HbA1c >9% пов’язані з 60% підвищеним ризиком госпіталізації та тяжкістю пневмонії під час бактеріальної інфекції. Наявність діабету втричі збільшила ризик госпіталізації та вчетверо – ризик потрапляння до відділення інтенсивної терапії в період спалаху грипу А (H1N1) у 2009 році. Під час спалаху 2012 року Близькосхідного респіраторного синдрому коронавірусу (MERS-CoV) ЦД був поширений майже в 50% світової популяції. Рівень смертності у хворих на MERS-CoV, які страждали на діабет, становив 35%.
Саме тому Американська діабетологічна асоціація та Європейська асоціація з вивчення цукрового діабету (ADA/EASD) наголошують на постійному контролі глікемії в пацієнтів із COVID‑19 та інтенсифікації лікування ЦД для полегшення перебігу та запобігання ускладненням.
Професор Рахеліч презентував дані останнього дослідження ліраглутиду 1,8 мг, анонсовані на конгресі УФІВ 2020. Багатьом лікарям знайома властивість ліраглутиду впливати на масу тіла в пацієнтів із ЦД 2 типу. Унікальність цього дослідження полягала в тому, що в його фокусі була здатність ліраглутиду впливати на рівень глікемії.
У дослідженні LIRA-PRIME порівнювали ефективність контролю глікемії за допомогою ліраглутиду з пероральними ЦЗП (ПЦЗП) у пацієнтів із неконтрольованим ЦД 2 типу з монотерапією метформіном в умовах первинної медичної допомоги.
Це 104-тижневе відкрите активне контрольоване дослідження проводилося в 9 країнах (n=1991). Під час скринінгу пацієнти з ЦД 2 типу (середній вік – 57,4 року; жінок – 47,6%; середня вага – 94,8 кг; середня тривалість діабету – 7,2 року) понад 3 міс застосовували стабільну добову дозу метформіну ≥1500 мг або максимальну переносиму дозу протягом ≥60 днів; рівні HbA1c складали від 7,5 до 9,0%, виміряні протягом ≤90 днів до скринінгу. Учасникам було довільно призначено або ліраглутид у дозі 1,8 мг (n=996), або ПЦЗП (n=995) на додаток до метформіну протягом 104 тижнів. Індивідуальні ПЦЗП були обрані лікуючим лікарем відповідно до місцевих рекомендацій. Найбільш поширеними ПЦЗП в контрольній групі, що їх додавали до метформіну, були інгібітори НЗКТГ‑2 (47,9%) та іДПП‑4 (39,7%), тоді як 10,8; 1,1 та 0,5% припадало на препарати сульфонілсечовини, тіазолідиндіони та інгібітори α-глюкозидази відповідно. Первинною кінцевою точкою став час неадекватного контролю глікемії, визначений як HbA1c >7,0% у ході двох запланованих послідовних візитів після перших 26 тиж лікування.
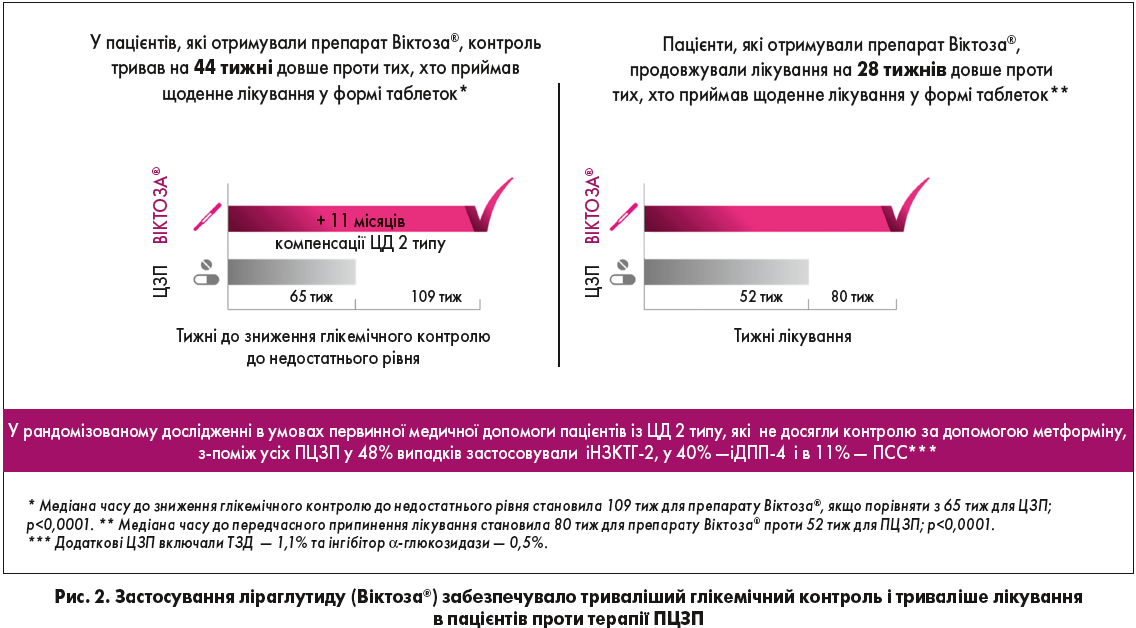
Відповідно до результатів дослідження LIRA-PRIME, додавання ліраглутиду до метформіну сприяло значно більшій тривалості контролю глікемії в пацієнтів із ЦД 2 типу проти групи контролю (рис. 2).
Ключовим результатом дослідження стала довготривала компенсація ЦД 2 типу в основній групі пацієнтів. Глікемічна компенсація, якщо порівняти з контрольною групою, тривала на 44 тиж довше (109 проти 65 тиж відповідно; р<0,0001).
Реципієнти ліраглутиду також досягли більш тривалого середнього часу до передчасного припинення лікування з будь-якої причини, якщо порівняти з реципієнтами ПЦЗП (80 проти 52 тиж відповідно; р<0,0001).
Наприкінці доповіді професор Даріо Рахеліч підбив підсумки дослідження і наголосив на тому, що ми не маємо забувати, Віктоза – це передусім потужний цукрознижувальний препарат, який допомогає тримати значно довшу глікемічну компенсацію ЦД 2 типу аніж деякі інші цукрознижувальні препарати. Це має дуже велике значення, оскільки дає можливість відкласти його подальшу інтенсифікацію та спростити менеджмент ЦД 2 типу в умовах первинної медичної допомоги.
У ході зустрічі експертів відбувся медичний консіліум, в якому взяли участь: старша наукова співробітниця ННЦ «Інститут кардіології ім. М.Д. Стражеска», доктор медичних наук Лариса Анатоліївна Міщенко, старша наукова співробітниця відділу діабетології Інституту ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України, доктор медичних наук Любов Костянтинівна Соколова та член-кореспондент НАМН України, завідувачка відділення ендокринної гінекології, заступниця директора з наукової роботи ДУ «Інститут педіатрії, акушерства та гінекології ім. О.М. Лук’янової НАМН України», доктор медичних наук, професор Тетяна Феофанівна Татарчук.
Клінічний випадок
Пацієнтка 54 років, з менопаузою протягом 3 років, була направлена лікарем-психіатром, в якого вона спостерігалася з приводу тривожно-депресивного синдрому, до гінеколога. В анамнезі пацієнтки перенесена транзиторна ішемічна атака. Із ліків приймала пароксин та гідазепам.
На момент консультації у хворої були скарги на підвищення АТ, постійну спрагу, відчуття тривоги та нестачу повітря, панічні атаки, сухість, печію в піхві, припливи до 10 разів на добу з 2017 року. Хвора скаржиться також, що, попри здоровий спосіб життя, не може скинути вагу. Сімейний анамнез обтяжений онкологічним захворюванням, у бабусі з боку батька був рак молочної залози. Із супутніх патологій у пацієнтки ожиріння ІІ ст. та ЦД 2 типу, хронічний панкреатит, хронічний холецистит, мікролітіаз.
При більш детальному опитуванні жінки лікарем-гінекологом було визначено, що в анамнезі присутні такі зміни, як порушення менструального циклу та овуляції, синдром полікістозу яєчників, гестаційний діабет, що в клімактеричному періоді привело до ризиків надмірної маси тіла в менопаузі, а також до остеоартрозу, ССЗ, неалкогольної жирової хвороби печінки, варикозної хвороби серця, дисліпідемії, артеріальної гіпертензії, депресії. Також жінка зазначає, що в анамнезі були мимовільні викидні.
Після огляду, збору анамнезу лікарем-гінекологом встановлено попередній діагноз: Постменопауза. Клімактеричний синдром тяжкого ступеня. Ожиріння ІІ ст. З огляду на дані анамнезу та об’єктивні дані: тривожно-депресивний стан, хронічний холецистит, хронічний панкреатит, мікролітіаз, ЦД 2 типу, гіпертонічна хвороба?
Лікарем було рекомендовано дообстеження:
- Звернутися за консультацією до мамолога, зробити мамографію.
- Звернутися за консультацією до ендокринолога та кардіолога.
- Зробити коагулограму, ліпідний спектр, печінкові проби, перевірити пролактин, вітамін D, глікований гемоглобін, холестерин та його фракції.
Тиждень потому лікар отримав результати дообстеження пацієнтки. Було виявлено: підвищення глюкози натще – до 9,8 ммоль/л, HbA1c – до 8,2 ммоль/л, тригліцеридів – до 2,2 ммоль/л, холестерину – до 5,3 ммоль/л, ЛПНЩ – до 3,4 ммоль/л, зниження ліпопротеїнів високої щільності (ЛПВЩ) – до 0,9 ммоль/л. Показники демонстрували наявність у хворої ЦД 2 типу в стадії декомпенсації, що потребувало достатньо інтенсивного лікування ЦД на додаток до метформіну, який вона приймає.
Лікар-кардіолог зазначила, що в пацієнтки комбінована дісліпідемія (підвищені рівні ЛПНЩ і ТГ, знижений рівень ЛПВЩ), мікроальбумінурія та в анамнезі перенесена транзиторна ішемічна атака. На доплерографії судин виявлено дві атеросклеротичні бляшки: за діаметром 30 і 40% від діаметру внутрішньої сонної артерії. Під час уточнення кардіологічних скарг хвора вказала на значне покращення стану на тлі прийому пароксетину – майже відсутні різкі підйоми АТ до 180/100 мм рт. ст. Проте все ще турбує головний біль, переважно ввечері, пов’язаний із підвищенням АТ. Коливання АТ з 120/70 мм рт. ст. зранку до 150/100 мм рт. ст. ввечері. Із препаратів жінка приймала небіволол 2,5-5 мг на добу та ацетилсаліцилову кислоту (АСК) 100 мг на день.
Встановлено діагноз: Гіпертонічна хвороба ІІІ ст. ([транзиторна ішемічна атака] ТІА в басейні лівої [середньої мозкової артерії] СМА 2019 р.), 1 ступеня ризик (дуже високий), СН 0. Стенозуючий атеросклероз сонних артерій. Комбінована дисліпідемія.
Проаналізувавши всі дані та результати інструментальних і лабораторних досліджень, лікар-гінеколог порекомендував таке лікування:
- Клімадінон по 1 таблетці двічі на день.
- Амарелін по 1 супозиторії на ніч.
- Декрістол 4000 МО 1 раз на добу.
- Хепі Фем по 1 таблетці двічі на день.
- Продовжувати виконувати призначення психіатра.
Лікар-кардіолог доповнив:
- Фіксована комбінація периндоприлу/індапаміду/5/1,25 мг на добу.
- АСК 100 мг на добу.
- Розувастатин 20 мг на добу.
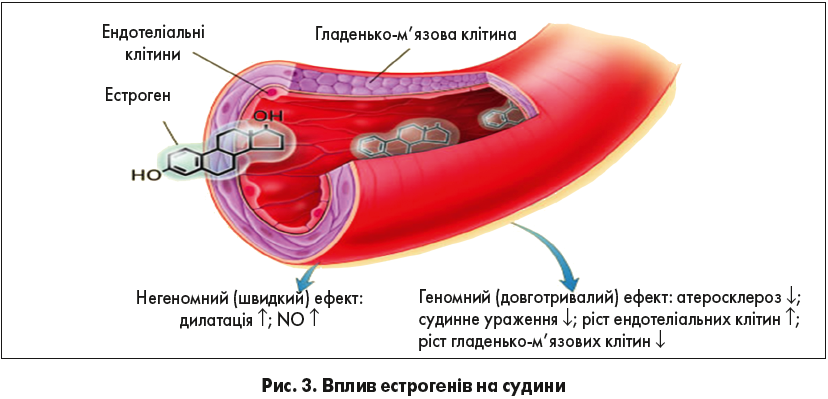
З огляду на виявлені атеросклеротичні бляшки, хворій протипоказана менопаузальна гормональна терапія. Це пов’язано з тим, що естрогени викликають підвищення синтезу метилопротеїнази 9 типу, яка стимулює розвиток центрального некрозу в наявних бляшках, що може призвести до дестабілізації бляшки та атеротромбозу (рис. 3).
Але, зважаючи на необхідність сфокусувати лікування на зниження ризиків ССЗ у пацієнтки з ЦД 2 типу, необхідно провести нейтралізацію факторів ризику та застосування сучасних ЦЗП із доведеним позитивним впливом на серцево-судинний прогноз.
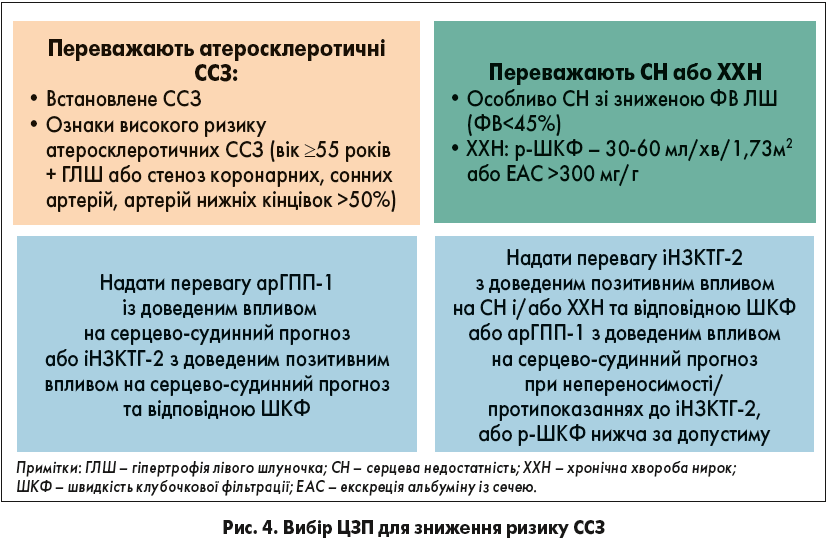
За останніми рекомендаціями вибором ЦЗП для зниження ризику ССЗ є агоністи ГПП‑1 та інгібітори НЗКТГ‑2 (рис. 4).
У разі встановленого атеросклеротичного ССЗ, як в нашому випадку, рекомендовано надавати перевагу агоністам ГПП‑1 із доведеним впливом на серцевий прогноз (ESC 2019, ADA 2020).
У процесі дослідження LEADER був доказаний вплив ліраглутиду на стійке зменшення ризику нефатальних інсультів. Для перевірки цих даних при застосуванні арГПП-1 був зроблений метааналіз 8 рандомізованих клінічних досліджень. Згідно з його результатами арГПП-1 достовірно знижували ризик розвитку нефатального інсульту на 16% (Subodh V. et al., 2018).
Саме тому пацієнтці для максимального зниження ризику атеросклеротичних ССЗ, перш за все інсульту, ендокринологом був рекомендований ліраглутид у вигляді препарату Віктоза®.
Після консультації пацієнтки лікарем-ендокринологом було встановлено діагноз: Постменопауза. Клімактеричний синдром тяжкого ступеня. Ожиріння ІІ ст. Тривожно-депресивний синдром. Хронічний холецистит. Хронічний панкреатит. Мікролітеаз. ЦД 2 типу. Гіпертонічна хвороба.
В якості гіпоглікемічного лікування рекомендовано залишити метформін у дозі 2000 мг на добу і додати препарат Віктоза® в кінцевій дозі 1,8 мг на добу з покроковою титрацією, аби запобігти виникненню можливих побічних ефектів. Вибір препарату був підтверджений лікарем-ендокринологом з огляду на мультифакторний вплив на рівень глікемії та зниження кардіоваскулярних ризиків цього лікарського засобу.
***
З огляду на особисту клінічну практику, експерти зазначили, що додавання ліраглутиду сприяє тривалішому глікемічному контролю в пацієнтів. Ті хворі, які отримували препарат Віктоза®, продовжували лікування на 44 тиж довше тих, кому було призначене щоденне лікування у вигляді пероральної цукрознижувальної терапії.
Як свідчать результати клінічної практики, у хворих, які отримували препарат Віктоза®, компенсований вуглеводний обмін був довшим.
Довідка ЗУ
Фармацевтична компанія Novo Nordisk була заснована в 1923 р. датським подружжям Августом та Марі Крог. Август Крог обіймав посаду професора факультету зоофізіології Копенгагенського університету. Лауреат Нобелівської премії. Марія була лікарем та вченим, яка вивчала ЦД 1 типу.
У 1921 р., за запрошенням дослідників Єльського університету (США), сімейна пара читала лекції про свої медичні дослідження після отримання 1920 року Романської премії з фізіології.
Під час свого туру Август та Марі отримували багато повідомлень про хворих на ЦД. Найцікавішою новиною для них стало виділення гормону підшлункової залози – інсуліну, який було відкрито в 1921 р. двома канадськими дослідниками Бантінгом та Бестом. Марі Крог почала збирати та вивчати всю інформацію щодо лікування ЦД, оскільки вона сама хворіла на діабет 2 типу. Через деякий час Август і Марі зв’язались із вченими, які відкрили інсулін, та отримали патент і дозвіл на виробництво інсуліну в скандинавських країнах. Повернувшися додому зі США, подружжя Крог разом із доктором Хансом Крістіаном Хагедорном заснували фірму Nordisk Insulinlaboratorium. Фармацевт Август Конгстед, власник компанії Leo Pharmaceuticals, надав необхідну фінансову підтримку, що дало можливість створити компанію.
Підготувала Юлія Золотухіна
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (52) 2020 р.