8 вересня, 2021
Цукровий діабет та артеріальна гіпертензія
 За даними Всесвітньої організації охорони здоров’я, артеріальна гіпертензія (АГ) та цукровий діабет (ЦД) 2 типу є одними з провідних чинників серцево-судинного ризику. За останні 30 років поширеність АГ зменшилася до 1/4 населення світу, але захворюваність на ЦД зросла з 4,7 до 8,5%, і прогноз на майбутнє свідчить про подальший драматичний приріст. Покращання обізнаності щодо цих захворювань, їх лікування та контролю є основною метою глобальної системи охорони здоров’я. Розповсюдженість АГ у хворих на ЦД 2 типу до 3 разів вища, ніж у пацієнтів без ЦД, а поєднання ЦД та АГ істотно збільшує ймовірність розвитку серцево-судинних захворювань (ССЗ). Несприятливий взаємозв’язок цих двох станів, прискорюючи процеси атеросклерозу, може спричинити негативні патофізіологічні зміни серцево-судинної системи. Крім того, кардіоваскулярна автономна нейропатія (КАН), що виникає в результаті пошкодження вегетативних нервових волокон, які іннервують серце та судини, є вагомим ускладненням ЦД 2 типу, особливо за системної АГ.
За даними Всесвітньої організації охорони здоров’я, артеріальна гіпертензія (АГ) та цукровий діабет (ЦД) 2 типу є одними з провідних чинників серцево-судинного ризику. За останні 30 років поширеність АГ зменшилася до 1/4 населення світу, але захворюваність на ЦД зросла з 4,7 до 8,5%, і прогноз на майбутнє свідчить про подальший драматичний приріст. Покращання обізнаності щодо цих захворювань, їх лікування та контролю є основною метою глобальної системи охорони здоров’я. Розповсюдженість АГ у хворих на ЦД 2 типу до 3 разів вища, ніж у пацієнтів без ЦД, а поєднання ЦД та АГ істотно збільшує ймовірність розвитку серцево-судинних захворювань (ССЗ). Несприятливий взаємозв’язок цих двох станів, прискорюючи процеси атеросклерозу, може спричинити негативні патофізіологічні зміни серцево-судинної системи. Крім того, кардіоваскулярна автономна нейропатія (КАН), що виникає в результаті пошкодження вегетативних нервових волокон, які іннервують серце та судини, є вагомим ускладненням ЦД 2 типу, особливо за системної АГ.
ЦД 2 типу й АГ мають декілька спільних патофізіологічних механізмів, які виправдовують існування їх коморбідності. Інсулінорезистентність (ІР), гіперінсулінемія (ГІ), активація оксидантного стресу (ОС) і субклінічне хронічне системне низькоінтенсивне запалення (ХСНЗ) є найбільш вивченими. Зокрема, ГІ індукує ІР і зумовлює розвиток АГ у нормотензивних пацієнтів без ЦД; спричиняє реконструкцію та ригідність артерій, підвищує активність симпатичної нервової системи, стимулює ренін-ангіотензин-альдостеронову систему (РААС) і реабсорбцію Na+ в нирках. Окрім того, надмірний оксидантний стрес і субклінічне ХСНЗ є визначальними чинниками дисфункції ендотелію, порушень реактивності судин, підвищеної опірності периферичних судин і порушень обміну глюкози та ліпідів. Усі ці механізми призводять до підвищення рівня артеріального тиску (АТ) і глюкози в плазмі крові шляхом змін гемодинамічного та гліколіпідного обмінів. ГІ, абдомінальне ожиріння, субклінічне ХСНЗ і клас використовуваних антигіпертензивних препаратів можуть мати більше значення при розвитку ЦД 2 типу, ніж безпосередньо АГ. З іншого боку, ГІ, ригідність артерій, порушення функції нирок і гіперглікемія спричиняють приєднання/прогресування АГ.
Отже, ЦД 2 типу є причинним фактором розвитку АГ. Однак у складній мережі взаємопов’язаних станів, причетних до АГ та ЦД 2 типу, слід шукати більш релевантні чинники. Менделівська рандомізація може неабияк допомогти в ідентифікації таких шляхів.
Діагностика
Відомо, що фізіологічний циркадний профіль АТ характеризується зниженням рівня АТ під час сну й підвищенням при пробудженні. Варіативність параметрів АТ вночі характеризується зниженням АТ перед сном, базальним рівнем під час сну й підвищенням АТ перед пробудженням. За ступенем нічного зниження АТ розрізняють такі категорії: достатнє зниження АТ вночі (10-20%) оцінюють як фізіологічне (dippers), >20% – over-dippers, недостатнє зниження АТ вночі (>10%) – non-dippers, підвищення АТ вночі – night-peakers. Розподіл хворих на ці категорії зумовлює необхідність аналізу впливу активності пацієнта протягом дня, особливостей і відмінностей сну та/або положення тіла тощо.
Частка пацієнтів із ЦД, у яких при амбулаторному обстеженні вперше діагностовано АГ, становить 32%, у разі проведення добового моніторингу АТ (ДМАТ) – додатково +17%. Верифікація прихованої амбулаторної АГ вказує на її особливе значення в «масках» АГ у хворих на ЦД. Окрім того, висока поширеність категорії non-dippers при ЦД (≈70%) може безпосередньо стосуватися прогнозування смертності в цій та інших групах пацієнтів з АГ.
Пригнічення біологічно опосередкованих процесів зниження АТ вночі (non-dippers) у хворих на ЦД 2 типу з АГ, а також фізіологічним рівнем АТ може спричиняти високий ризик приєднання/прогресування мікро- та макросудинних ускладнень. Повідомляється, що порушення циркадного ритму АТ / параметрів циркадного профілю АТ із формуванням моделі non-dippers потребує проведення скринінгу щодо синдрому апное уві сні, особливо в разі резистентної АГ (РАГ), а також постуральної гіпотензії (однієї з ознак діабетичної КАН). У хворих на ЦД із приєднанням та/або прогресуванням КАН часто спостерігається постпрандіальна гіпотензія (ще один важливий компонент 24-годинної мінливості АТ), яка може бути виявлена за допомогою ДМАТ. Зокрема, проведення ДМАТ у хворих на ЦД 2 типу з КАН виявило, що клінічні форми, тяжкий перебіг захворювання асоціюються з вищими показниками систолічного АТ (САТ) і пульсового АТ, особливо вночі та в ранні ранкові години, більшим відсотком пацієнтів зі статусом non-dippers.
ДМАТ доцільно проводити при високому нормальному АТ за даними неодноразових клінічних вимірювань із метою діагностики прихованої АГ; у разі суттєвої різниці офісного й домашнього АТ; за підозри на АГ «білого халата»; при значних коливаннях офісного АТ під час одного чи різних відвідувань лікаря; РАГ; епізодах гіпотензії; для оцінки ступеня зниження нічного АТ. У нормі відзначається зниження нічного АТ.
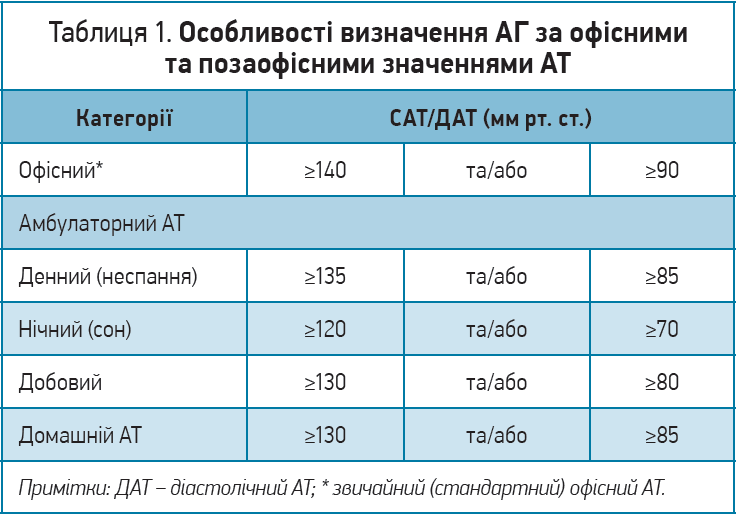
Особливості визначення АГ за офісними та позаофісними значеннями АТ наведено в таблиці 1 (ESC/ESH, 2018; Rabi D.M. et al., 2020).
Лікування
Раціональне харчування та фізична активність
Дієтичні принципи включають отримання необхідної кількості енергії в поєднанні з фізіологічним раціоном харчування. Традиційна середземноморська дієта (Греція та Південна Італія) пов’язана з довголіттям та/або низькою смертністю внаслідок ускладнень ССЗ, зменшенням захворюваності на ЦД 2 типу, низькою частотою широкого спектра хронічних захворювань, включаючи ревматоїдний артрит, хворобу Паркінсона тощо. Середземноморська дієта сприяє зниженню АТ, позитивним змінам ліпідного спектра крові; має багато спільного з DASH-дієтою й OmniHeart-дієтою (збільшення вмісту ненасичених жирів і білка в раціоні), що сприяє зниженню АТ, вмісту холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) і тригліцеридів.
Довголанцюгові ω‑3 та ω‑6 поліненасичені жирні кислоти (ПНЖК) позитивно впливають на перебіг ССЗ при ЦД 2 типу. Зокрема, лінолева ω‑6 ПНЖК покращує чутливість до інсуліну, знижує рівень загального холестерину та сприяє вираженому зниженню співвідношення ХС ЛПНЩ / ХС ліпопротеїнів високої щільності (ЛПВЩ) у крові. Мононенасичені жирні кислоти (оливкова олія або олія ріпаку та горіхів) також покращують чутливість до інсуліну, сприяють зниженню співвідношення ХС ЛПНЩ / ХС ЛПВЩ у крові. Оливкова олія, особливо нерафінована, має низку фітохімічних характеристик, які виявляють сприятливий вплив на чинники ризику ССЗ, а олія рапсу містить α-ліноленову й ω‑3 ПНЖК, що асоціюється із захисним впливом щодо розвитку ССЗ і зниженням частоти хронічного коронарного синдрому (ХКС).
Фізичне навантаження є наріжним каменем у профілактиці та лікуванні ССЗ, ЦД 2 типу та метаболічного синдрому. Зокрема, результати епідеміологічних досліджень свідчать, що фізична активність може зменшити ризик ССЗ та ЦД 2 типу на 50%.
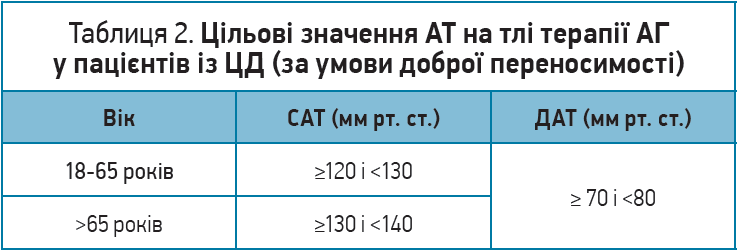
Цільові значення АТ на тлі терапії АГ у пацієнтів із ЦД (за умови доброї переносимості) наведено в таблиці 2 (Rabi D. M. et al., 2020).
Основні положення стосовно лікування АГ у хворих на ЦД (ADA, 2017; 2020):
- Пацієнти з коморбідними ЦД й АГ належать до груп високого та дуже високого ризику ССЗ, відповідно до якого визначається стратегія антигіпертензивного лікування.
- Діагностика та визначення ступеня АГ у хворих на ЦД проводиться за тими самими принципами, що й у загальній популяції.
- Цільові значення АТ на тлі застосовуваної терапії залежать від віку пацієнтів і переносимості досягнутих показників АТ.
- Пацієнтам із ЦД й АГ доцільно призначати метаболічно нейтральні лікарські засоби (ЛЗ).
- Необхідно забезпечити найбільш ранній початок лікування з досягненням оптимальної підтримувальної дози антигіпертензивних засобів і регулярною її корекцією протягом життя хворого.
- Необхідно забезпечити початок лікування із застосуванням мінімальних ефективних доз одного чи двох препаратів із метою досягнення максимального ефекту при мінімальному відсотку побічних ефектів.
- Медикаментозна антигіпертензивна терапія призначається в разі збільшення показників АТ ≥140/90 мм рт. ст. Мета: досягнення цільового рівня <130/80 мм рт. ст. (<140/80 – у пацієнтів літнього віку).
- Цільовий рівень АТ має становити 140/90 мм рт. ст. Однак у хворих без надмірного навантаження ліками, молодих пацієнтів з альбумінурією та/або АГ у поєднанні з чинниками ризику атеросклерозу цільовий рівень АТ має бути <130/80 мм рт. ст.
- Медикаментозна терапія АГ при ЦД передбачає застосування антигіпертензивних ЛЗ, насамперед тих, які мають ангіо- та нефропротекторні властивості, а саме препаратів із групи блокаторів РААС.
- Стратегія лікування має включати інгібітор РААС і дигідропіридинові блокатори кальцієвих каналів (ДГП-БКК) та/або тіазидоподібні діуретики (ТПД).
- При АТ <160/100 мм рт. ст. у хворих на ЦД лікування рекомендовано починати з одного препарату – інгібітора ангіотензинперетворювального ферменту (ІАПФ) або блокатора рецепторів ангіотензину ІІ (БРА), при АТ >160/100 мм рт. ст. – із двох ЛЗ.
- Необхідно забезпечити своєчасне використання комбінованої терапії тоді, коли неможливо досягти цільових рівнів АТ за монотерапії.
- При РАГ до основної трикомпонентної фіксованої терапії додають антигіпертензивні ЛЗ другого ряду (резерву).
- Якщо рівень ХС ЛПНЩ >1,8 ммоль/л (ЦД з ураженням органів-мішеней) або >2,6 ммоль/л (неускладнений ЦД), необхідно призначити статини з метою первинної профілактики.
- Зниження рівня глюкози та корекція дисліпопротеїнемії згідно з наявними рекомендаціями.
Бажані характеристики антигіпертензивних препаратів наведено в таблиці 3 (Unger T. et al., 2020).
Блокатори РААС
Інгібітори РААС переважно включають ІАПФ та БРА й демонструють сприятливий ефект щодо зменшення альбуміну в сечі. Ці препарати, враховуючи їхній позитивний вплив на ІР та нефропротекторні властивості, належать до антигіпертензивних засобів першої лінії для хворих на ЦД. Інгібітори РААС рекомендують хворим на ЦД із мікроальбумінурією та/або протеїнурією. Проте з результатів метааналізу декількох досліджень за участю хворих на ЦД з АГ випливає, що інгібітори РААС як антигіпертензивні ЛЗ першого ряду не проявили себе краще за інші категорії препаратів. Зокрема, аналізували ефективність інгібіторів РААС щодо ступеня зменшення серцево-судинної смертності, смертності від усіх причин, частоти порушення функції нирок і ССЗ. Узагальнені ефекти продемонстрували менші ризики, але статистично значущої різниці не виявлено.
Існує кілька клінічних настанов щодо раціонального лікування хворих на ЦД з АГ, в яких інгібітори РААС рекомендовано як антигіпертензивні препарати першої лінії. Проте з точки зору статистичного аналізу в певних протоколах досліджень подеколи спостерігаються суттєві відмінності. Зокрема, ймовірні чинники полягають у такому:
- порівняння ефективності інгібіторів РААС із ББК, або блокаторами β-адренергічних рецепторів (ББ), або діуретиками;
- запропоновані цільові показники АТ;
- достатня ефективність призначених препаратів;
- період спостереження за протоколом дослідження;
- критерії включення/виключення осіб із порушеннями функції нирок;
- серцево-судинні події в анамнезі (позитивні/негативні).
За результатами численних досліджень сформульовано положення, що блокатори РААС, а саме ІАПФ та БРА, є пріоритетними при лікуванні АГ у хворих на ЦД 1 та 2 типів, хоча в кількох попередніх дослідженнях не виявлено переваг ІАПФ/БРА над іншими антигіпертензивними ЛЗ щодо запобігання серцево-судинним подіям у пацієнтів із ЦД. Препаратам цієї групи властива не тільки виражена антигіпертензивна дія, а й здатність не погіршувати або, згідно з даними низки авторів, навіть поліпшувати чутливість тканин до інсуліну та гальмувати розвиток ЦД 2 типу. Фармакологічні агенти з груп ІАПФ та БРА характеризуються кардіо- й нефропротекторними ефектами у хворих на ЦД та знижують ризик розвитку серцево-судинних подій і прогресування діабетичної хвороби нирок (ДХН). При лікуванні пацієнтів із ЦД й АГ препарати груп ІАПФ та БРА загалом виявляють зіставну антигіпертензивну, кардіо- й нефропротекторну ефективність. Але хворим на ЦД необхідно уникати одночасного прийому двох блокаторів РААС, зокрема й інгібітора реніну аліскірену, через підвищений ризик тяжких ниркових ускладнень, гіперкаліємії та гіпотензії.
У літературі триває дискусія щодо можливих переваг якогось із цих класів препаратів. Зокрема, серед результатів дослідження ONTARGET, у якому порівнювали ефективність раміприлу й телмісартану, такі:
- раміприл не має переваг над телмісартаном;
- телмісартан статистично значуще не поступається раміприлу за частотою серцево-судинних подій, інсульту та загальної смертності;
- спростовано припущення, що активність телмісартану стосовно рецепторів активації проліферації пероксисом-γ може зробити цей препарат ефективнішим щодо запобігання чи затримки розвитку ЦД.
Головні положення щодо ІАПФ/БРА:
- не виявляють негативного впливу на вуглеводний і ліпідний обміни, знижують ІР периферичних тканин;
- мають нефропротекторну дію, яка не залежить від їхнього антигіпертензивного ефекту;
- ІАПФ із метою нефропротекції призначають хворим на ЦД 1 та 2 типів у разі виявлення мікроальбумінурії та протеїнурії навіть при нормальному значенні АТ;
- терапію ІАПФ/БРА варто проводити під контролем рівня креатиніну та калію плазми (особливо за наявності ДХН);
- варто скасувати через 2 тиж після ініціації терапії, якщо гіперкаліємія >6 ммоль/л або креатинін плазми >30% від вихідного значення;
- протипоказані при двобічному стенозі ниркових артерій, вагітності та лактації, гіперкаліємії >5,5 ммоль/л.
Блокатори кальцієвих каналів
БКК – препарати першої лінії, які використовуються в лікуванні хворих на ЦД з АГ. Загалом БКК: метаболічно нейтральні, мають виражені антигіпертензивні, антиоксидантні, протизапальні, антипроліферативні й антиагрегаційні властивості, суттєво поліпшують функцію ендотелію. Крім того, ДГП-БКК пролонгованої дії сприяють покращанню чутливості тканин до інсуліну. Необхідно зазначити, що ДГП-БКК третього покоління (амлодипін), БКК бензотіазепінового та фенілалкіламінового ряду мають кардіо-, вазо- та нефропротекторні ефекти.
Головні положення щодо БКК:
- метаболічно нейтральні, суттєво не впливають на стан вуглеводного, ліпідного та пуринового обмінів і не підвищують ризик розвитку ЦД 2 типу;
- характеризуються нефропротекторними ефектами, знижують вираженість мікроальбумінурії, сповільнюють прогресування ДХН;
- ДГП-БКК тривалої дії – препарати вибору для лікування ізольованої систолічної АГ;
- є препаратами першої лінії, що використовуються для лікування АГ при вагітності. Їх бажано призначати жінкам з АГ репродуктивного віку, які планують вагітність.
Увага до комбінації ІАПФ із БКК зумовлена такими її перевагами:
- ефективне зниження як САТ, так і ДАТ;
- вплив на судинну стінку (зменшення жорсткості судин);
- вазодилатувальний ефект;
- кардіопротекторний ефект;
- нейрорегуляторний вплив на механізми підвищення АТ;
- нефропротекторний ефект;
- покращання стану метаболізму.
Тіазидні й тіазидоподібні діуретики
Тіазидні діуретики (ТД) і ТПД належать до препаратів першої лінії в лікуванні АГ. Основні показання/протипоказання до використання діуретиків у лікуванні хворих на ЦД з АГ такі:
- ТД у дозах 12,5-25 мг/добу не спричиняють гіперглікемії, дисліпідемії, гіпокаліємії;
- ТД і ТПД протипоказані хворим зі швидкістю клубочкової фільтрації (ШКФ) <30 мл/хв/1,73 м2 і пацієнтам із подагрою;
- петльові діуретики призначають пацієнтам із ЦД й АГ за наявності хронічної серцевої недостатності (ХСН), а також хворим на АГ при ШКФ <30 мл/хв/1,73 м2;
- вживання калійзберігальних діуретиків можна розглянути при РАГ у схемі з використанням понад трьох антигіпертензивних препаратів, якщо ШКФ >60 мл/хв/1,73 м2;
- призначення спіронолактону й еплеренону при показниках ШКФ <60 мл/хв/1,73 м2 зумовлене високим ризиком погіршення функції нирок і приєднанням гіперкаліємії;
- з метою корекції АТ при ХСН у пацієнтів із первинним гіперальдостеронізмом доцільно використовувати калійзберігальні діуретики;
- при ЦД осмотичні діуретики не використовуються.
Блокатори β-адренергічних рецепторів
Основні показання/протипоказання до використання ББ у лікуванні АГ у хворих на ЦД такі:
- ББ призначають пацієнтам із ЦД й АГ, хворим на ХКС (перенесений інфаркт міокарда), при фібриляції передсердь, вагітності або її плануванні (перевага віддається селективним);
- неселективні ББ не рекомендується використовувати в пацієнтів із ЦД для корекції АТ. Фармакологічні агенти цієї групи препаратів негативно впливають на стан ліпідного обміну, глікемічний контроль, підвищують ризик ЦД 2 типу внаслідок посилення периферичної ІР;
- пацієнтам із ЦД й АГ рекомендується призначення кардіоселективних ББ (бісопролол, метопролол) і ББ із вазодилатувальними ефектами (карведилол, небіволол), які не впливають негативно на вуглеводний і ліпідний обміни, здатні підвищувати чутливість тканин до інсуліну.
Препарати четвертої лінії в лікуванні АГ: α-адреноблокатори
Результати дослідження ALLHAT показали, що використання блокаторів α-адренорецепторів (АБ) порівняно з ТД призводило до підвищення частоти розвитку серцевих і цереброваскулярних ускладнень. Отже, АБ (доксазозин, празозин) недоцільно застосувати як ЛЗ першої лінії при лікуванні АГ. Найраціональніше застосовувати їх у комбінованій терапії хворих на ЦД з АГ як препарати третьої або четвертої лінії, насамперед у разі резистентної форми АГ, а також РАГ з ожирінням. Загалом АБ:
- характеризуються сприятливим метаболічним профілем дії;
- слід застосовувати у складі комбінованої терапії АГ у хворих на ЦД із доброякісною гіперплазією передміхурової залози;
- слід з обережністю призначати хворим на ЦД із клінічними формами автономної нейропатії, що проявляються ортостатичною гіпотензією, яку може провокувати прийом цієї групи препаратів.
Резистентна АГ
РАГ передбачає утримання показників АТ на рівні 140/90 мм рт. ст., незважаючи на терапевтичну стратегію, що включає модифікацію способу життя, використання діуретичних фармакологічних агентів у поєднанні з двома іншими антигіпертензивними препаратами, які належать до різних класів, у відповідних дозах. Перш ніж діагностувати РАГ, слід виключити інші захворювання та стани.
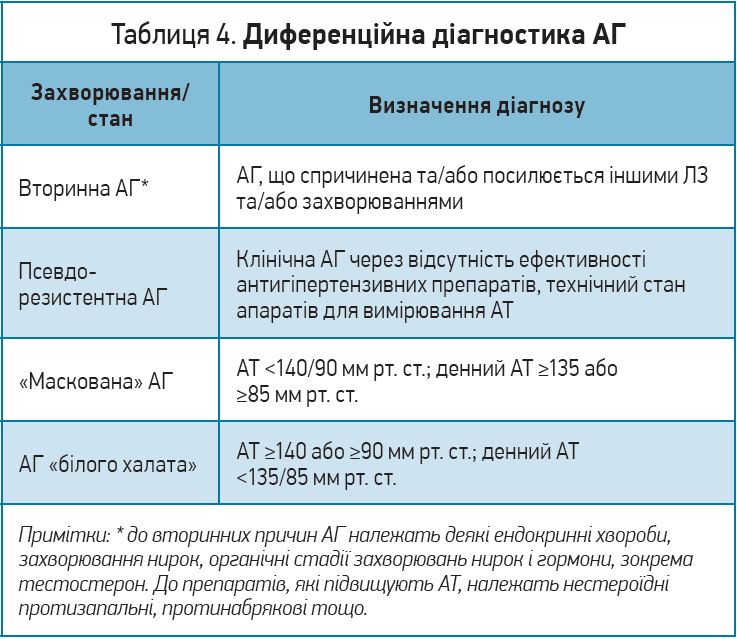
Диференційні діагнози АГ наведено в таблиці 4 (ADA, 2017; 2020).
Антагоністи мінералокортикоїдних рецепторів (антагоністи альдостерону)
Антагоністи мінералокортикоїдних рецепторів (АМР) ефективні для лікування РАГ у хворих на ЦД 2 типу в комбінації з інгібіторами РААС, БКК та діуретиками, частково тому, що зменшують активність симпатичної ланки автономної нервової системи. АМР також зменшують альбумінурію та мають додаткові переваги щодо впливу на стан серцево-судинної системи. Однак АМР у поєднанні з ІАПФ або БРА можуть збільшити ризик епізодів гіперкаліємії. Профілактика гіперкаліємії полягає в обмеженні вживання продуктів, багатих на калій, запобіганні втраті калію при використанні діуретиків або препаратів, які зв’язують калій. Утім, необхідні довгострокові дослідження, щоб оцінити роль АМР у цих процесах.
Комбінована терапія
До переваг комбінованої антигіпертензивної терапії слід віднести:
- ефективність у зниженні АТ;
- зручність у застосуванні (особливо фіксованих комбінацій);
- підвищення прихильності пацієнта до лікування;
- синергізм антигіпертензивних ефектів ЛЗ;
- можливість зниження побічних ефектів за рахунок зменшення дози одного або обох препаратів комбінації.
Хворі на ЦД 2 типу з АГ переважно потребують комбінованої антигіпертензивної терапії, оскільки контроль АТ у цих хворих є дуже складним. Отже, якщо цільовий рівень АТ не досягається при монотерапії стандартними дозами, слід застосовувати додаткову антигіпертензивну терапію. Для осіб, у яких розглядається комбінована терапія з ІАПФ, ДГП-БКК є кращим вибором, аніж ТД/ТПД. Зокрема, рекомендації, що свідчать на користь використання комбінованої терапії ІАПФ/БКК у пацієнтів із ЦД 2 типу, базуються на результатах дослідження ACCOMPLISH, у якому порівнювали ефективність комбінованого лікування беназеприлом/амлодипіном і беназеприлом/хлорталідоном. У дослідженні взяли участь 6946 хворих на ЦД 2 типу, 2842 з яких віднесені до групи з особливо високим ризиком через серцеву, цереброваскулярну патологію чи ХСН в анамнезі. Первинна комбінована кінцева точка – інфаркт міокарда, інсульт, смерть унаслідок ССЗ, госпіталізація з приводу ХКС, реанімаційні заходи при зупинці серця та коронарна реваскуляризація. Встановлено, що беназеприл/амлодипін зменшували настання первинної комбінованої кінцевої точки порівняно з беназеприлом/хлорталідоном у всіх пацієнтів із ЦД 2 типу.
Серед найадекватніших комбінацій антигіпертензивних препаратів, які мають доказову базу та можуть застосовуватися у хворих на ЦД з АГ, доцільно рекомендувати:
- ІАПФ + ДГП-БКК + ТПД;
- БРА + ДГП-БКК + ТПД;
- ІАПФ + ТПД;
- БРА + ТПД;
- ДГП-БКК + ТПД;
- ДГП-БКК (амлодипін, лерканідипін) + АБ (із вазодилатувальною дією).
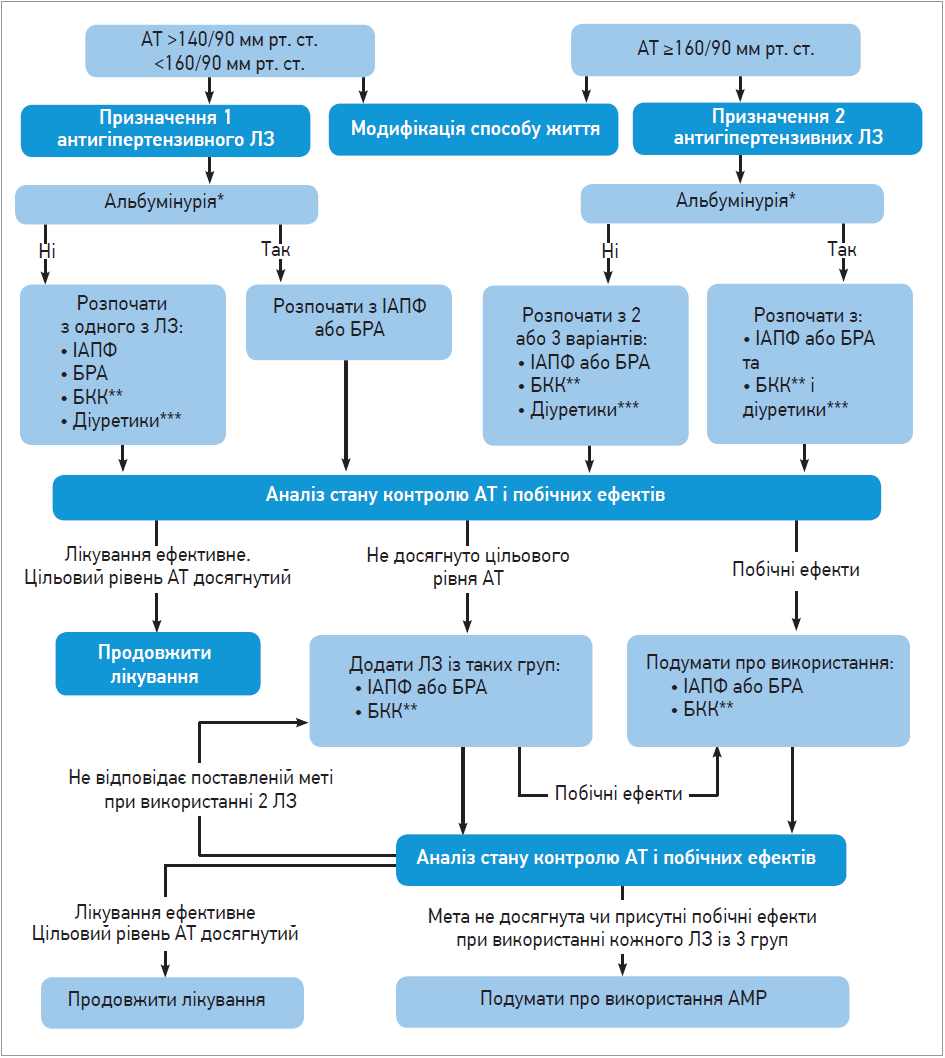
Рекомендації щодо лікування АГ у хворих на ЦД продемонстровано на рисунку.
Рис. Рекомендації щодо лікування АГ у хворих на ЦД (ADA, 2017; 2020)
Примітки: * ІАПФ або БРА рекомендуються для лікування АГ у пацієнтів із співвідношенням альбумін/креатинін у сечі (САКС) 30-299 мг/г креатиніну й обов’язково призначаються хворим із САКС 300 мг/г креатиніну. ** Дигідропіридинові. *** Тіазидоподібні (хлорталідон та індапамід) – нетіазидні діуретики тривалої дії, показані для зменшення частоти серцево-судинних подій.
Висновки
Проблема ефективності лікування та поліпшення прогнозу хворих на ЦД з АГ залишається складною. Успіх у лікуванні залежить від дотримання таких положень: ефективність антигіпертензивних властивостей ЛЗ, здатність досягнути цільового рівня офісного АТ, показників ДМАТ, оскільки хворі на ЦД з АГ переважно належать до категорії non-dippers; досягнення та збереження високої прихильності до терапії протягом багатьох років; виражені нефропротекторні ефекти.
Метою майбутніх досліджень має бути визначення й опрацювання конкретних завдань із причинно-наслідковим значенням для запобігання ЦД 2 типу й АГ. У цьому плані ГІ може бути хорошим кандидатом.