26 жовтня, 2022
Лікування діабету при хронічній хворобі нирок: консенсусні рекомендації ADA і KDIGO
Коморбідність цукрового діабету (ЦД) і хронічної хвороби нирок (ХХН) спричиняє високий ризик розвитку ниркової недостатності, атеросклеротичних серцево-судинних захворювань (ССЗ), серцевої недостатності та передчасної смерті. Останні клінічні дослідження підтвердили ефективність нових підходів до менеджменту діабету в пацієнтів із ХХН. Американська діабетична асоціація (ADA) та Глобальна ініціатива з покращення результатів лікування захворювань нирок (KDIGO) у 2022 році випустили об’єднані консенсусні рекомендації з лікування ЦД при ХХН.
Скринінг і діагностика ХХН
Поширеність ХХН серед пацієнтів із ЦД перевищує 25%. У 40% осіб із ЦД протягом життя розвивається ХХН. Остання визначається як стійка розрахункова швидкість клубочкової фільтрації (ШКФ) <60 мл/хв/1,73 м2, альбумінурія (співвідношення альбумін/креатинін ≥30 мг/г) або наявність інших маркерів ураження нирок, таких як гематурія або аномалії структури. Важливо, що результати аналізів можуть змінюватися в окремих осіб із часом, тому для встановлення діагнозу необхідна стійкість показників протягом щонайменше 3 місяців.
У більшості випадків ХХН не проявляється симптомами, тому її часто діагностують під час планового скринінгу. Як ADA, так і KDIGO рекомендують щорічний скринінг на ХХН пацієнтів із діабетом. Скринінг ХХН слід розпочинати з моменту встановлення діагнозу ЦД 2 типу, оскільки на цей час ознаки ХХН часто вже є очевидними. Натомість при ЦД 1 типу скринінг рекомендується розпочинати через 5 років після встановлення діагнозу, до цього часу ХХН є рідкістю.
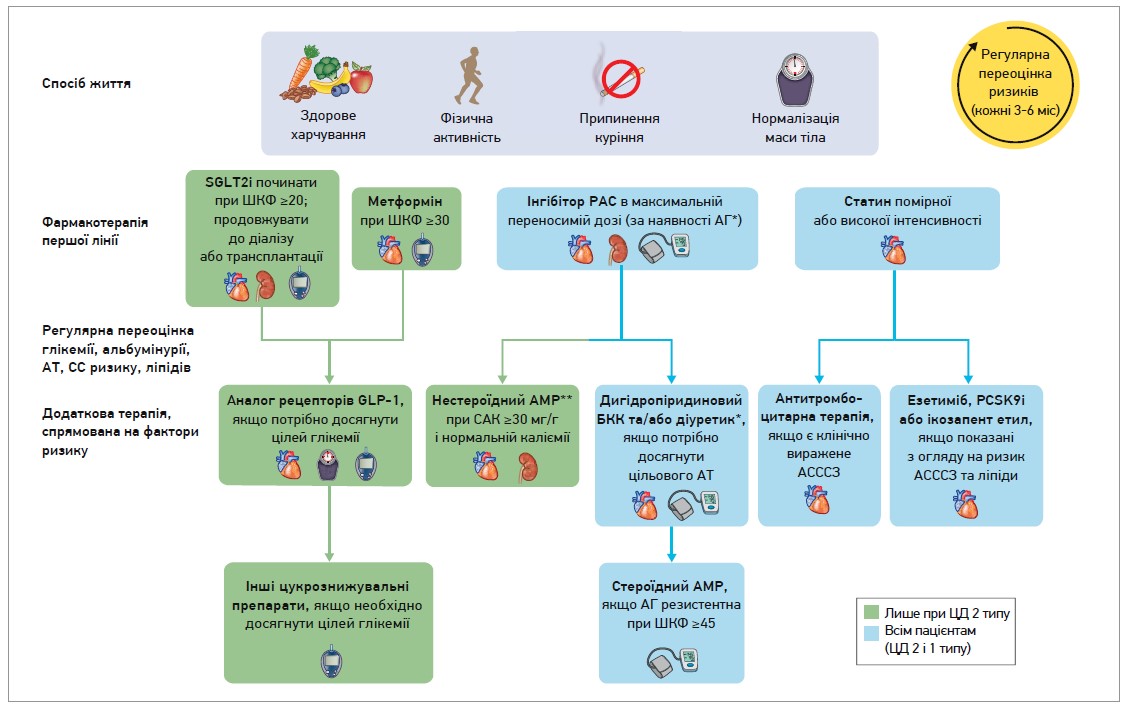
Мультиморбідність є типовою для пацієнтів із діабетом і ХХН. Вони мають високий ризик прогресування ХХН, серцево-судинних подій і передчасної смерті. Тому як ADA, так і KDIGO підкреслюють важливість комплексної, цілісної, орієнтованої на пацієнта медичної допомоги для покращення загальних результатів лікування. Цей підхід потребує оптимізації способу життя, фармакологічної терапії, спрямованої на збереження функції органів, і додаткового лікування, націленого на покращення проміжних факторів ризику, таких як глікемія, артеріальний тиск (АТ) і ліпідний обмін (рис.).
Рис. Цілісний підхід до покращення прогнозу в пацієнтів із ЦД і ХХН
Примітки: * ІАПФ або БРА (в максимальних переносимих дозах) мають бути терапією першої лінії гіпертензії за наявності альбумінурії. В іншому випадку також можна розглянути дигідропіридиновий блокатор кальцієвих каналів або діуретик; усі три класи часто необхідні для досягнення цільових показників АТ.
**Фінеренон наразі є єдиним нестероїдним АМР із доведеними клінічними перевагами для нирок і серцево-судинної системи. АГ – артеріальна гіпертензія; БКК – блокатор кальцієвих каналів; РАС – ренін-ангіотензинова система; САК – співвідношення альбумін/креатинін.
Консенсусні рекомендації ADA/KDIGO
- Всі пацієнти із ЦД 1 або 2 типу та ХХН повинні отримувати комплексне лікування за планом, розробленим й узгодженим фахівцями охорони здоров’я спільно з пацієнтом. Цей план має включати оптимізацію харчування, фізичні вправи, відмову від куріння та нормалізацію маси тіла, засновану на доказах фармакотерапію, спрямовану на збереження функції органів, а також на досягнення проміжних цілей – нормалізацію глікемії, АТ і ліпідного профілю.
- Інгібітор ангіотензинперетворювального ферменту (ІАПФ) або блокатор рецепторів ангіотензину ІІ (БРА) рекомендовано призначати пацієнтам із ЦД 1 або ЦД 2 типу, які мають артеріальну гіпертензію та альбумінурію, титрувати до максимальної антигіпертензивної або найвищої переносимої дози.
- Терапія статинами рекомендована для всіх пацієнтів із ЦД 1 або 2 типу та ХХН: помірної інтенсивності – для первинної профілактики атеросклеротичних ССЗ (АСССЗ), високої інтенсивності – для пацієнтів із наявним АСССЗ і деяких пацієнтів із множинними факторами ризику АСССЗ.
- Метформін рекомендований для пацієнтів із ЦД 2 типу, ХХН і розрахунковою ШКФ ≥30 мл/хв/1,73 м2. Дозу слід зменшити до 1000 мг/добу в пацієнтів із ШКФ 30-44 мл/хв/1,73 м2 і в деяких пацієнтів із ШКФ 45-59 мл/хв/1,73 м2, які мають високий ризик розвитку лактоацидозу.
- Інгібітор натрій-глюкозного котранспортера 2 (SGLT2i) з доведеною користю для нирок або серцево-судинної системи рекомендований пацієнтам із ЦД 2 типу, ХХН і розрахунковою ШКФ ≥20 мл/хв/1,73 м2. Після початку терапії SGLT2i вона може бути продовжена і при нижчих рівнях ШКФ.
- Агоніст рецептора глюкагоноподібного пептиду 1 (GLP‑1) із доведеною користю для серцево-судинної системи рекомендовано призначати пацієнтам із ЦД 2 типу та ХХН, які не досягають індивідуального цільового рівня глюкози крові за допомогою прийому метформіну та/або SGLT2i, чи тим, хто не може використовувати ці препарати.
- Нестероїдний антагоніст мінералокортикоїдних рецепторів (АМР) із доведеною користю для нирок і серцево-судинної системи рекомендований пацієнтам із ЦД 2 типу, ШКФ ≥25 мл/хв/1,73 м2, нормальною концентрацією калію в сироватці крові та альбумінурією (співвідношення альбуміну до креатиніну ≥30 мг/г), незважаючи на максимальну переносиму дозу інгібітора ренін-ангіотензинової системи.
Цукрознижувальні засоби при ЦД 2 типу та ХХН
ADA та KDIGO рекомендують ранній початок лікування метформіном разом з інгібітором SGLT2 у більшості пацієнтів із ЦД 2 типу та ХХН. У подальшому можна додавати інші цукрознижувальні агенти, якщо це необхідно, щоб досягти індивідуальних цільових показників глікемії. Призначення цукрознижувальних препаратів може бути обмежене низькою ШКФ. Тому відповідна корекція дози на основі розрахункової ШКФ важлива для ліків, які підвищують ризик побічних ефектів за низької ШКФ або виводяться нирками. За необхідності рекомендується обережне застосування та титрування інсуліну й препаратів сульфонілсечовини, щоб уникнути гіпоглікемії.
Метформін
Метформін рекомендований для застосування в більшості пацієнтів із ЦД 2 типу та ХХН, які мають розрахункову ШКФ ≥30 мл/хв/1,73 м2. Доведено, що метформін є безпечною, ефективною та доступною основою для контролю глікемії при ЦД 2 типу. Метформін виводиться із сечею в незміненому вигляді. В інструкції для медичного застосування міститься попередження про підвищений ризик лактоацидозу в пацієнтів із ХХН через порушення виведення метформіну. Проте дослідження свідчать, що загальний ризик лактоацидозу, пов’язаного з метформіном, низький, тому Управління з контролю за якістю продуктів харчування і лікарських засобів США (FDA) переглянуло інструкцію щодо метформіну, щоб відобразити його безпеку для більшості пацієнтів із ШКФ ≥30 мл/хв/1,73 м2.
У пацієнтів із ХХН для безпечної терапії метформіном ШКФ слід контролювати принаймні раз на рік, при цьому рекомендований інтервал моніторингу зменшують до 3-6 місяців, якщо ШКФ знижується до <60 мл/хв/1,73 м2. Рекомендовано зменшити дозу метформіну до 1000 мг/добу для пацієнтів із ШКФ у діапазоні від 30 до 44 мл/хв/1,73 м2. Також слід розглянути можливість зниження дози для пацієнтів із ШКФ 45-59 мл/хв/1,73 м2 за наявності в них супутньої патології, яка піддає їх підвищеному ризику лактоацидозу через гіпоперфузію та гіпоксемію. Більшість епізодів лактоацидозу, пов’язаного з метформіном, виникають одночасно з іншими гострими захворюваннями, часто коли гостре ураження нирок сприяє зниженню кліренсу метформіну. Тому під час гострого захворювання застосовується принцип пропуску доз, коли дозу метформіну тимчасово зменшують або припиняють прийом препарату, щоб знизити ризик асоційованого з метформіном лактоацидозу.
Інгібітори натрій-глюкозного котранспортера 2
SGLT2i рекомендовано призначати більшості пацієнтів із ЦД 2 типу та ХХН із ШКФ ≥20 мл/хв/1,73 м2 незалежно від рівня HbA1c або необхідності додаткового зниження рівня глюкози. Ця рекомендація ґрунтується на переконливих доказах того, що SGLT2i знижує ризик прогресування ХХН, розвитку серцевої недостатності й атеросклеротичних захворювань у пацієнтів із ЦД 2 типу та ХХН. Ці переваги не залежать від рівня глюкози крові. SGLT2i доцільно призначати пацієнтам із ЦД 2 типу та ХХН, навіть якщо глікемічна ціль вже досягнута. Хоча SGLT2i зазвичай додають до модифікації способу життя та базисної терапії метформіном, лікування SGLT2i без метформіну також може бути доцільним для пацієнтів із занадто низькою ШКФ, а також для тих, хто не переносить метформін або кому не потрібен метформін для досягнення цільових показників глікемії.
Використання додаткових цукрознижувальних засобів
На думку експертів KDIGO, додавання агоніста рецептора GLP‑1 тривалої дії є кращим варіантом продовження терапії для пацієнтів, які не досягають індивідуальних цільових показників глікемії попри терапію метформіном та/або SGLT2i, або для осіб, які не можуть приймати ці ліки. Подібним чином ADA рішуче підтримує використання агоністів рецепторів GLP‑1 у пацієнтів із ЦД 2 типу та ХХН або АСССЗ, враховуючи їхні первинні переваги для серцево-судинної системи та вторинної переваги для нирок, що були показані у великих дослідженнях. Слід зазначити, що агоністи рецепторів GLP‑1 зберігають глікемічний ефект і безпеку навіть на пізніх стадіях ХХН.
Агоністи рецепторів GLP‑1 зменшують альбумінурію й уповільнюють зниження ШКФ, про що свідчать вторинні результати, отримані в дослідженнях серцево-судинних наслідків і клінічному випробуванні ефективності та безпеки агоніста GLP‑1 у пацієнтів із ЦД 2 типу та ШКФ 15-59 мл/хв/1,73 м2. У дослідженнях серцево-судинних наслідків агоністи рецепторів GLP‑1 знижували ризик великих несприятливих серцево-судинних подій у пацієнтів із ЦД 2 типу.
Висновки
Існує гостра потреба в лікуванні хворих на ЦД і ХХН відповідно до найсучасніших рекомендацій. ADA та KDIGO пропонують чіткі вказівки щодо вибору та пріоритетності терапії. Цукрознижувальними засобами першої лінії для більшості пацієнтів із ЦД 2 типу та ХХН є метформін з огляду на його добре вивчену безпеку й ефективність у досягненні цілей глікемії, а також інгібітор SGLT2 з урахуванням його доведеного позитивного впливу на прогноз.
Джерело: de Boer I. H., Khunti K., Sadusky T. et al. Diabetes Management in Chronic Kidney Disease: A Consensus Report by the American Diabetes Association (ADA) and Kidney Disease: Improving Global Outcomes (KDIGO). Diabetes Care. 2022 Oct 3: dci220027. doi: 10.2337/dci22-0027.
Підготував Ігор Петренко
Медична газета «Здоров’я України 21 сторіччя» № 13 (530), 2022 р.