1 грудня, 2024
Альфа-ліпоєва кислота для лікування діабетичної периферичної нейропатії: позиція експертів у 2024 році
Постійне збільшення тягаря цукрового діабету (ЦД) у всьому світі супроводжується поширенням його хронічних ускладнень, зокрема діабетичної нейропатії (ДН). Її найпоширенішою формою (75%) є дистальна симетрична полінейропатія, яку також називають діабетичною периферичною нейропатією (ДПН). ДПН уражає до 50% пацієнтів із ЦД 1 та 2 типів, а також щонайменше 10% осіб із переддіабетом.
У червні 2024 року в журналі Frontiers of Endocrinology опубліковано міждисциплінарний консенсус щодо ведення пацієнтів із ДПН. Група експертів із 4 різних спеціальностей (ендокринологія, неврологія, внутрішня медицина, фізична медицина та реабілітація) проаналізувала наявні рекомендації, а також дані доказової медицини; крім того, проведено зустріч для пошуку консенсусної думки щодо концептуальних, клінічних та терапевтичних аспектів ДПН.
Зокрема, були детально розглянуті основні принципи лікування ДПН:
- оптимальне лікування ЦД (інтенсивний глікемічний контроль, модифікація способу життя та багатофакторне зменшення ризиків);
- патогенетично орієнтована фармакотерапія з особливим акцентом на альфа-ліпоєвій кислоті (АЛК);
- симптоматичне полегшення болю при больовій ДПН.
Особливе місце в сучасній парадигмі лікування ДПН посідає АЛК, ліцензована як лікарський засіб у багатьох країнах. Її унікальні антиоксидантні ефекти, спрямовані на патогенез ДПН, були ретельно досліджені в регіонах, де широко використовується АЛК, як-от Німеччина, Східна Європа та Далекий Схід. Нижче узагальнена консенсусна позиція експертів щодо ролі АЛК у лікуванні ДПН.
АЛК як патогенетично спрямований і хворобомодифікувальний засіб при ДПН
У разі ЦД унаслідок інгібування ключових гліколітичних ферментів активуються хибні метаболічні шляхи (поліоловий, гексозаміновий, шлях протеїнкінази С тощо), задіяні в розвитку ДПН. Усі ці шляхи зумовлюють посилення клітинного окисного стресу, спричиненого утворенням реактивних сполук кисню (РСК), а також зниженням антиоксидантного захисту. Саме тому АЛК вважається перспективною першою лінією антиоксидантної терапії ДПН. АЛК модифікує перебіг хвороби завдяки її здатності запобігати ранньому розвитку та прогресуванню ДПН шляхом здійснення прямого (гальмування утворення РСК) і непрямого (збільшення ендогенного антиоксиданту глутатіону) антиоксидантного ефекту, що згодом проявляється в помітному клінічному покращенні (рис.). Крім того, AЛК може бути ефективним агентом, спрямованим на патогенез, із погляду мікросудинної гіпотези ДПН, оскільки потенційно здатна знижувати рівень гомоцистеїну. АЛК зменшує індукований гіпергомоцистеїнемією стрес ендоплазматичного ретикулуму та окислення в ендотеліальних клітинах.
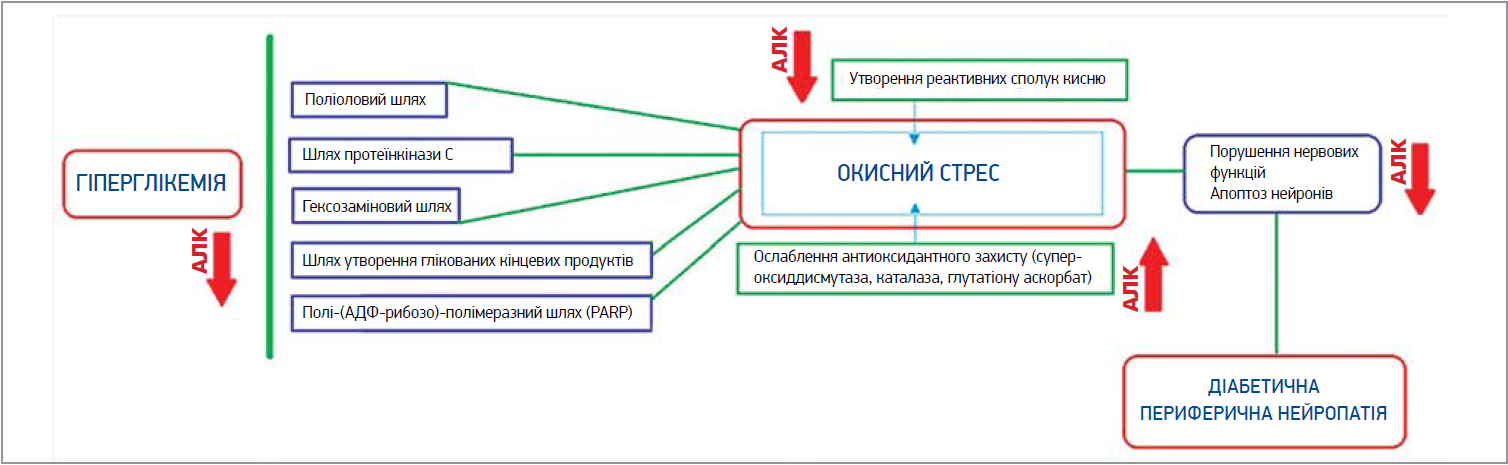 Рис. AЛК як агент, що модифікує захворювання: прямі та непрямі антиоксидантні ефекти щодо основних шляхів, залучених до патогенезу ДПН
Рис. AЛК як агент, що модифікує захворювання: прямі та непрямі антиоксидантні ефекти щодо основних шляхів, залучених до патогенезу ДПН
Клінічна ефективність: результати опорних досліджень та метааналізів
У дослідженні ALADIN II застосування АЛК (спочатку внутрішньовенно, а згодом перорально, впродовж 2 років) зумовило покращення функції рухових і сенсорних нервів (підвищення швидкості провідності) та полегшення симптомів нейропатії (Reljanovic M. et al., 1999). У дослідженні SYDNEY2 пероральне лікування 600 мг АЛК 1 р/день протягом 5 тиж поліпшило невропатичні симптоми (колючий/пекучий біль, парестезії, оніміння стоп уві сні) та неврологічний дефіцит при ДПН за шкалою оцінки симптомів, а також їхніх змін у разі нейропатії (NSC), шкалою оцінки порушень функцій за нейропатії (NIS) (Ziegler D. et al., 2006).
У метааналізі 3 рандомізованих контрольованих досліджень (РКД) за участю пацієнтів із симптоматичною ДПН було показано, що режими терапії АЛК у дозі 600 мг перорально чи внутрішньовенно значно полегшують невропатичні симптоми (Mijnhout G.S. et al., 2012). Інший метааналіз 4 РКД (ALADIN I, ALADIN III, SYDNEY, NATHAN I за участю загалом 1258 пацієнтів) підтвердив, що 3 тижні терапії АЛК значно покращили загальну оцінку симптомів нейропатії (TSS; відносна різниця порівняно із плацебо – 24,1% зі значним впливом на біль, печіння й оніміння) та оцінку симптомів нейропатії у нижніх кінцівках (NIS-LL; відносна різниця порівняно із плацебо – 16,0% зі значним впливом на гомілковостопні рефлекси, відчуття уколу та дотику) (Ziegler D. et al., 2004).
За даними метааналізу 9 досліджень ДПН, пероральний прийом АЛК порівняно із плацебо сприяв покращенню оцінок NIS (м’язова слабкість, втрата рефлексів, відчуття тиску, дотику, вібрації, положення суглобів і рухів), NIS-LL (функція рухових нервів, рефлекси), NDS (ушкодження черепних нервів, сила м’язів, втрата рефлексів / відчуттів) на додачу до полегшення симптомів нейропатії за TSS (Cassanego G. et al., 2022). Метааналіз у підгрупах виявив статистично значуще зменшення колючого болю, печіння, парестезії та оніміння в пацієнтів, які отримували AЛК, порівняно із плацебо. Отже, пероральне застосування АЛК було визнано оптимальним варіантом для лікування ДПН щодо покращення симптомів болю, моторики та функції нервів разом із відмінним профілем безпеки.
Довготривала терапія, досвід застосування АЛК у рутинній практиці
В дослідженні NATHAN І нейропатичний дефіцит покращився після 4 років лікування АЛК у пацієнтів із легкою або помірною (переважно безсимптомною) ДПН (Ziegler D. et al., 2011). За допомогою апостеріорного аналізу дослідження NATHAN І вдалося зрозуміти, який саме вплив мають різні початкові чинники на ефективність АЛК. Поліпшення та запобігання прогресуванню ДПН, за оцінками NIS-LL (ΔNIS-LL ≥2 бали), при застосуванні АЛК порівняно із плацебо впродовж 4 років було досягнуто переважно в чоловіків старшого віку з нижчим індексом маси тіла, нормальним артеріальним тиском, але вищим тягарем серцево-судинних захворювань в анамнезі, які отримували лікування інсуліном, мали більшу тривалість діабету та нейропатії, а також вищу стадію нейропатії (Ziegler D. et al., 2016). У висновках автори зазначили, що оптимальний контроль факторів ризику серцево-судинних захворювань може сприяти підвищенню ефективності АЛК у пацієнтів із вищим тягарем захворювання. Також експерти пов’язують ефективність АЛК з інтенсивнішим лікуванням ЦД. Вважається, що поганий контроль глікемії зумовлює вищу частоту та гірший прогноз макро- і мікросудинних ускладнень діабету. Без досягнення глікемічного контролю неможливо запобігти ускладненням, а також сповільнити прогресування в будь-якого хворого. Жоден із засобів, що використовуються для лікування нейропатії, не може запобігти ускладненням, доки зберігається глюколіпотоксичність.
АЛК (особливо її внутрішньовенна форма) також є ефективним засобом для полегшення невропатичного болю; вона навіть може скорочувати використання аналгетиків (наприклад, прегабаліну, дулоксетину й тапедантолу). В реальній когорті 443 діабетичних хворих із хронічною больовою нейропатією отримували АЛК у дозі 600 мг 1 р/добу перорально протягом середнього періоду (5 років). Довгострокова терапія виявилася безпечним та ефективним варіантом лікування амбулаторних пацієнтів із ДПН у Німеччині (Ruessmann H.J., 2009). Слід зауважити, що припинення прийому АЛК після 5 років лікування спричинило рецидив симптомів через 2 тиж. За переходу від тривалого прийому АЛК на центральні аналгетики, як-от габапентин, пацієнти спостерігали підвищення частоти побічних ефектів, що потребувало більше амбулаторних візитів, щоденних витрат на лікування. Ці результати свідчать про те, що лікування ДПН має бути тривалим і безперервним (навіть у періоди відсутності симптомів), а також потребує призначення препаратів із патогенетичними властивостями, як-от АЛК (Ruessmann H.J., 2009).
Ретроспективний аналіз національної бази даних в Угорщині виявив нижчу частоту серцево-судинної та цереброваскулярної захворюваності (гострий інфаркт міокарда, інсульт, госпіталізація щодо серцевої недостатності), а також онкологічних випадків, крім того, загальної смертності в пацієнтів із ДПН, котрі отримували патогенетично-орієнтовану АЛК, порівняно з тими, хто мав симптоматичну аналгетичну фармакотерапію (Jermendy G. et al., 2023).
У метааналізі 24 РКД у пацієнтів із метаболічними захворюваннями було виявлено, що АЛК покращує гомеостаз глюкози (зниження рівня глюкози натще, інсуліну, індексу інсулінорезистентності HOMA-IR та глікованого гемоглобіну HbA1c), а також ліпідний профіль (зниження тригліцеридів, загального холестерину, холестерину ліпопротеїнів низької щільності) (Akbari M. et al., 2018). Потенційні механізми, що лежать в основі здатності АЛК покращувати гомеостаз глюкози, продемонстровані в деяких експериментальних дослідженнях – здебільшого на основі AЛК-опосередкованого збільшення поглинання глюкози м’язами в тварин із ожирінням (Ghibu S. et al., 2009; Eason R.C. et al., 2002), стимуляції поглинання глюкози шляхом транслокації глюкозних транспортерів до плазматичної мембрани, збільшення фосфорилювання тирозину субстрату рецептора інсуліну‑1 (Konrad D. et al., 2001). Вплив АЛК на ДПН вважається більшим, якщо вона використовується як складова традиційного лікування ЦД 2 типу, тобто разом із метформіном, глімепіридом, інгібіторами натрій-глюкозного котранспортера‑2, аналогами ГПП‑1.
Висновки
- AЛК є патогенетичною терапією першої лінії для лікування ДПН, що модифікує перебіг захворювання завдяки прямим та непрямим антиоксидантним ефектам.
- Ефективність АЛК при ДПН була послідовно продемонстрована в багатьох клінічних випробуваннях, дослідженнях в умовах реальної практики і метааналізах, які виявили покращення швидкості рухової та сенсорної нервової провідності, полегшення нейропатичних симптомів.
- Об’єктивними індикаторами ефективності АЛК, окрім полегшення симптомів нейропатії, є вплив на різні неврологічні порушення (слабкість м’язів, втрата рефлексів, відчуття тиску, дотику, вібрації, положення суглобів і рухів).
- АЛК – корисне доповнення для покращення гомеостазу глюкози та ліпідного профілю при застосуванні разом із традиційним лікуванням ЦД 2 типу.
- Лікування ДПН має бути тривалим; навіть у періоди відсутності симптомів пацієнти потребують патогенетичної терапії, якою є АЛК. Доведена безпека й ефективність терапії з безперервним використанням АЛК упродовж 5 років.
Джерело: Atmaca A. et al. (2024). Expert opinion on screening, diagnosis and management of diabetic peripheral neuropathy: a multidisciplinary approach. Front. Endocrinol. 15: 1380929.
doi: 10.3389/fendo.2024.1380929.
Реферативний огляд підготував Ігор Петренко
Довідка «ЗУ»
В Україні АЛК (тіоктова кислота) європейського виробництва представлена, зокрема, лінійкою препаратів Берлітіон® від компанії «Берлін-Хемі». Берлітіон® має статус лікарського засобу, показаний для лікування парестезій при ДН. Препарат доступний у двох лікарських формах (обидві виробляються в Німеччині). Одна капсула Берлітіон® 600 капсули містить 600 мг тіоктової кислоти. Одна ампула Берлітіон® 300 ОД містить 12 мл концентрату для розчину для інфузій етилендіамінової солі тіоктової кислоти 388 мг, що відповідає 300 мг тіоктової кислоти, Берлітіон® 600 ОД – 24 мл розчину, який містить еквівалент 600 мг тіоктової кислоти. Такі дозування дозволяють підбирати оптимальний режим лікування для кожного пацієнта, а також проводити ступінчасту терапію. За інтенсивних парестезій рекомендується внутрішньовенне введення препарату в дозі від 12 (1 ампула 300 ОД) до 24 мл (2 ампули 300 ОД або 1 ампула 600 ОД) на добу. Таку терапію можна проводити в стаціонарі чи денній амбулаторії. Для подальшої терапії застосовують Берлітіон® 600 капсули в дозі 300-600 мг/добу.
Медична газета «Здоров’я України 21 сторіччя» № 19/1 (581), 2024 р




