7 грудня, 2024
Глімепірид у сучасному веденні цукрового діабету: фармакологічні переваги та клінічне застосування
Цукровий діабет (ЦД) 2 типу – комплексне захворювання, на розвиток якого впливають різноманітні генетичні та зовнішні фактори. Важливу роль у його прогресуванні відіграє недостатність β-клітин підшлункової залози, які поступово втрачають здатність ефективно підтримувати рівень інсуліну [1, 2]. Цей процес відбувається в кілька етапів: початкова схильність (генетика, внутрішньоутробний вплив, харчування в перші місяці життя), період адаптації (тимчасове збільшення маси β-клітин у відповідь на інсулінорезистентність) і власне недостатність із симптомами [2]. Хронічна гіперглікемія утворює хибне коло, яке не лише погіршує стан β-клітин, а й підвищує ризик ускладнень і смерті, пов’язаних із діабетом [3-5]. Саме тому ефективний контроль глікемії на ранніх стадіях захворювання є критично важливим для зниження ризику цих ускладнень у довготривалій перспективі [6, 7].
Похідні сульфонілсечовини (ПСС) – пероральні протидіабетичні препарати, які вже понад 60 років є важливою складовою фармакотерапії ЦД 2 типу завдяки своїй здатності стимулювати вивільнення інсуліну з β-клітин підшлункової залози. У такий спосіб вони полегшують наслідки дисфункції β-клітин і сприяють досягненню цільового глікемічного контролю. До переваг зазначених препаратів належать висока антигіперглікемічна активність, добра довготривала переносимість та економічна доступність [8-11]. Цей огляд присвячений глімепіриду – ПСС третього покоління з унікальними фармакологічними властивостями – в аспекті сучасних підходів до ведення пацієнтів із ЦД 2 типу.
Критична роль раннього та довготривалого глікемічного контролю
Традиційно ведення ЦД 2 типу передбачало поетапний підхід, коли новий препарат додавали до вже наявної схеми лікування. Однак на сьогодні накопичено достатньо доказів на користь проактивнішої стратегії, за якої комбінацію цукрознижувальних засобів призначають уже з моменту встановлення діагнозу [12].
Раннє застосування комбінацій препаратів дозволяє досягти кращого контролю рівня глюкози порівняно з монотерапією окремими препаратами, тому комбіноване лікування рекомендоване для пацієнтів, у яких рівень глікованого гемоглобіну (HbA1c) перевищує цільовий показник на >16,3 ммоль/моль (>1,5%) на момент діагностики (тобто ≥70 ммоль/моль, або >8,5%, для більшості пацієнтів) [12]. У спільних європейських та американських настановах (ADA/EASD), зокрема, зазначено, що в молодих дорослих із ЦД 2 типу слід прагнути негайного і стійкого глікемічного контролю, орієнтуючись на рівень HbA1c <53 ммоль/моль (7%) або навіть нижче [13]. Це забезпечує найкращу можливість уникнути ускладнень діабету протягом життя. Крім того, патофізіологія мікро- та макросудинних ушкоджень має більше спільного, ніж колись вважали, що свідчить про можливість зменшення макросудинних ускладнень у довготривалій перспективі завдяки профілактиці мікросудинних порушень [14].
Раннє застосування комбінацій цукрознижувальних засобів виглядає особливо доцільним, якщо зважати на багатофакторний характер ЦД 2 типу [15]. Комбінована терапія дозволяє не тільки швидше досягти цільових показників HbA1c, а й ефективніше впливати на різні патофізіологічні аспекти захворювання, що стає визначальним фактором у попередженні ускладнень. Раціональним компонентом такого підходу є призначення глімепіриду, який завдяки своїм фармакологічним властивостям здатен оптимально доповнити комбіноване лікування.
Похідні сульфонілсечовини: класифікація та механізми дії
Похідні сульфонілсечовивни поділяють на три покоління, кожне з яких відрізняється за фармакологічними характеристиками, ефективністю та профілем безпеки [16].
До першого покоління належать такі препарати, як толбутамід, хлорпропамід і толазамід. Це найстаріші ПСС, розроблені в 1950-х роках. Вони мали низьку селективність дії, що призводило до вищого ризику гіпоглікемії та частіших побічних ефектів, зокрема з боку кардіоваскулярної системи.
До другого покоління відносять глібенкламід, гліпізид і гліклазид. Ці ПСС мають вищу селективність дії та ефективні в нижчих дозах. Гліклазид і гліпізид випускаються також у формі з модифікованим вивільненням (MR); це сприяє поступовому всмоктуванню та стабільнішому контролю рівня глюкози, але може мати й певні недоліки.
Єдиним ПСС третього покоління є глімепірид – найновіший і найсучасніший представник цього класу, який став доступним у 1990-х роках. Глімепірид відрізняють покращений профіль безпеки завдяки високій селективності до рецепторів β-клітин підшлункової залози, подвійний механізм дії, справжня (обумовлена властивостями молекули, а не лікарською формою) тривала дія, низький ризик гіпоглікемій, відсутність збільшення маси тіла та низка корисних позапанкреатичних ефектів [17].
Загальний механізм дії ПСС полягає в стимуляції секреції інсуліну з β-клітин підшлункової залози шляхом блокування АТФ-залежних калієвих каналів, що веде до деполяризації клітинної мембрани та виділення інсуліну (рис. 1) [18]. Через це ПСС ефективні тільки в пацієнтів з ЦД 2 типу, у яких збережена функція β-клітин.
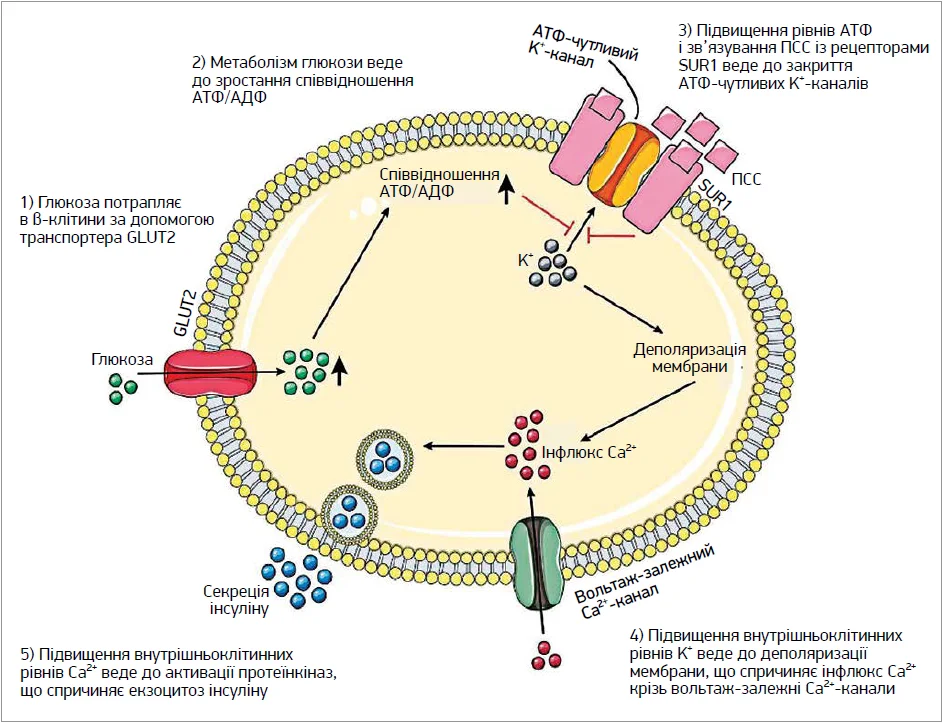 Рис. 1. Схематичне зображення механізму дії ПСС на β-клітину підшлункової залози (адаптовано за Hendriks A.M. et al., 2019)
Рис. 1. Схематичне зображення механізму дії ПСС на β-клітину підшлункової залози (адаптовано за Hendriks A.M. et al., 2019)
Глімепірид у веденні ЦД 2 типу
Контроль глікемії
Максимальна цукрознижувальна активність і рівень інсуліну у хворих на ЦД 2 типу досягаються через 2-3 години після прийому глімепіриду. Дія триває до 24 годин, тому режим прийому 1 р/добу дозволяє ефективно контролювати глікемію. Глімепірид можна приймати безпосередньо перед сніданком або під час нього з однаковими результатами [35].
Цукрознижувальна ефективність глімепіриду в монотерапії (зниження HbA1c на 1,5-2%) подібна до такої метформіну та агоністів рецепторів глюкагоноподібного пептиду 1 (ГПП‑1) і краща, ніж у нових препаратів – інгібіторів натрійзалежного контранспортера глюкози 2 (НЗКТГ-2; зниження HbA1c на 0,5‑1,0%) та інгібіторів дипептидилпептидази‑4 (ДПП‑4; зниження HbA1c на 0,4-0,9%) [27-32].
Подвійний механізм дії та позапанкреатичні ефекти
Крім стимуляції секреції інсуліну β-клітинами, глімепірид також помітно підвищує чутливість периферичних тканин до інсуліну. Ця дія може проявлятися завдяки таким механізмам:
- вплив на транспортери глюкози (GLUT4): глімепірид активує сигнальний шлях інсуліну в м’язовій та жировій тканині, стимулюючи переміщення транспортерів глюкози GLUT4 на поверхню клітин. Це сприяє ефективнішому захопленню глюкози периферичними тканинами [19];
- збільшення активності ферментів, які беруть участь у метаболізмі глюкози: глімепірид стимулює активність гексокінази та піруваткінази, що посилює процес утилізації глюкози в клітинах [20];
- вплив на рецептори інсуліну: глімепірид може сприяти підвищенню чутливості інсулінових рецепторів периферичних тканин, що також підвищує ефективність внутрішньоклітинних сигнальних шляхів [21]. Це сприяє поліпшенню засвоєння глюкози без необхідності надмірного вивільнення інсуліну з підшлункової залози.
Крім того, глімепірид має низку корисних позапанкреатичних ефектів: антиагрегантний (інгібує агрегацію тромбоцитів сильніше, ніж гліклазид); ендотелій-протекторний (стимулює продукування оксиду азоту ендотеліальними клітинами судин); антихолестеринемічний (зменшує зростання атеросклеротичної бляшки; підвищує рівень адипонектину); антиішемічний (полегшує ішемічне прекондиціювання міокарда), антиоксидантний (зменшує рівні пероксидів і малонового альдегіду в умовах гіперглікемії) [22-26].
Кардіоваскулярна безпека
У настановах ADA/EASD глімепірид відзначено як єдиний представник класу ПСС із доведеною кардіоваскулярною безпекою [13]. Підґрунтям для такого висновку стали результати великого (n=6033) рандомізованого контрольованого дослідження CAROLINA, в якому глімепірид порівнювали з інгібітором ДПП‑4 лінагліптином – кардіоваскулярно нейтральним протидіабетичним препаратом (за даними дослідження CARMELINA [36]). Отже, в дослідженні CAROLINA не було виявлено різниці в частоті серйозних несприятливих кардіоваскулярних подій у пацієнтів з високим кардіоваскулярним ризиком, які отримували глімепірид або лінагліптин. Первинна кінцева точка (смерть від кардіоваскулярних захворювань, нефатальний інфаркт міокарда або нефатальний інсульт) спостерігалася в 356 із 3023 учасників (11,8%) у групі лінагліптину та в 362 із 3010 (12,0%) у групі глімепіриду (р=0,76) [37].
Нещодавнє дослідження W. He та співавт. також продемонструвало, що в пацієнтів із ЦД 2 типу та хронічною серцевою недостатністю тривале безперервне лікування глімепіридом пов’язане зі зниженням кардіоваскулярної смертності та частоти госпіталізацій. Особливо відчутний позитивний вплив на прогноз відзначено у хворих зі збільшеним >50 мм лівим шлуночком і попередньо досягнутим контролем глікемії (HbA1c <8%) [38].
Вплив на масу тіла
Більшість пацієнтів із ЦД 2 типу мають надлишкову масу тіла [39]; її зниження веде до значного покращення клінічних і метаболічних профілів, у т. ч. сприяє досягненню цільового рівня HbA1c. Ефект набирання маси тіла вважають недоліком класу ПСС, а також тіазолідиндіонів та інсуліну. Проте порівняльні дослідження свідчать, що глімепірид не впливає на масу тіла пацієнтів із ЦД [40]. Кілька спостережних когортних досліджень навіть показали втрату маси тіла при застосуванні глімепіриду. Так, в одному дослідженні було зареєстровано середню втрату маси тіла на 3 кг після 1-5 років лікування глімепіридом [41]. В іншому дослідженні при лікуванні глімепіридом пацієнти позбавилися 2,2 кг протягом 8 тижнів [42].
Остаточного пояснення нейтральності глімепіриду щодо маси тіла нема, проте її пов’язують з ощадливою стимуляцією секреції інсуліну та позапанкреатичними ефектами [17]. Для пацієнтів із ЦД 2 типу це додаткова перевага як з естетичної точки зору, так і в аспекті довготривалих клінічних наслідків, адже нормалізація маси тіла – це, зокрема, усунення важливого фактора кардіоваскулярного ризику.
Зменшений ризик гіпоглікемії
Гіпоглікемія є потенційно небезпечним для життя станом та однією з найпоширеніших побічних реакцій, пов’язаних із ПСС. Однак глімепірид асоціюється з нижчою частотою гіпоглікемії порівняно з іншими ПСС завдяки своїм фармакологічним особливостям.
По-перше, глімепірид селективно взаємодіє з рецепторами сульфонілсечовини типу 1 (SUR1) на β-клітинах підшлункової залози [38]. Це дозволяє прицільніше стимулювати секрецію інсуліну в умовах гіперглікемії, зменшуючи стимуляцію секреції інсуліну на тлі нормального або низького рівня глюкози.
По-друге, глімепірид має двофазний вплив на секрецію інсуліну: викликає початковий швидкий викид інсуліну (подібний до фізіологічного), а потім спричиняє поступову, контрольовану стимуляцію секреції інсуліну, яка адаптується до рівня глюкози в крові [43]. Це забезпечує м’якший і стабільніший контроль глікемії, без надмірних коливань рівня інсуліну.
Зрештою, глімепірид додатково підвищує чутливість периферичних тканин до інсуліну, що дозволяє організму ефективніше використовувати інсулін, знижуючи потребу в надмірній його секреції [17].
Ще одним ПСС із низьким ризиком гіпоглікемії вважають гліклазид MR. Проте в нещодавньому дослідженні було продемонстровано, що в пацієнтів старшого віку спостерігається підвищена частота тяжкої гіпоглікемії при застосуванні гліклазиду MR порівняно з глімепіридом [44]. Гліклазид MR також асоціювався зі значно вищим ризиком тяжкої глікемії, що потребувала невідкладної госпіталізації, вищим ризиком переломів, невідкладної госпіталізації з кардіоваскулярних причин і повторних невідкладних госпіталізацій. Одне з можливих пояснень – недолік форми з модифікованим вивільненням: у пацієнтів із порушеннями травлення чи зміненою моторикою кишечника (зокрема, при гастропарезі – частому ускладненні діабету) швидкість і рівень всмоктування гліклазиду з MR-форми можуть змінюватися [45], що, своєю чергою, може призводити до коливань рівнів препарату в крові та менш контрольованого ефекту.
Прихильність до лікування та фармакоекономічний аспект
Глімепірид поєднує високу ефективність у зниженні рівня глюкози, безпеку та доступність за ціною, тому в багатьох випадках може бути раціональною альтернативою іншим, навіть сучаснішим протидіабетичним препаратам. Пероральний шлях застосування, а також схема дозування 1 р/день забезпечують кращу прихильність пацієнтів до лікування [46].
У дослідженні GRADE пацієнтів із ЦД 2 типу розподілили на чотири групи для лікування глімепіридом, ситагліптином, ліраглутидом або інсуліном гларгін на додаток до метформіну. Результати показали, що протягом першого року лікування ліраглутид і глімепірид були найефективнішими щодо утримання рівня HbA1c <7% [47]. А після 4 років терапії не було відмінностей за частотою мікросудинних ускладнень залежно від виду втручання [48]. Не спостерігали також істотних відмінностей щодо ризику розвитку серйозних несприятливих кардіоваскулярних подій, менш значущих несприятливих кардіоваскулярних подій чи смерті в досліджуваних групах. Отже, з урахуванням співвідношення ефективності, безпеки, вартості та зручності застосування, а також беручи до уваги відсутність суттєвих відмінностей щодо впливу на жорсткі кінцеві точки найраціональнішим із фармакоекономічного погляду вбачається додавання до метформіну саме глімепіриду.
Клінічні сценарії застосування
Глімепірид може використовуватися у веденні осіб із ЦД 2 типу в різних клінічних ситуаціях, які залежать від рівня HbA1c, наявності супутніх захворювань, відповіді на інші цукрознижувальні препарати, а також індивідуальних потреб пацієнта. Нижче наведені основні сценарії застосування глімепіриду відповідно до сучасних настанов [13].
- Монотерапія. Глімепірид може бути призначений у вигляді монотерапії для пацієнтів, які не досягають цільового рівня глікемічного контролю тільки за рахунок модифікації способу життя. Монотерапія глімепіридом є доцільною для пацієнтів із помірним підвищенням HbA1c (зазвичай до 1,5% від цільового рівня) та відсутністю значних кардіометаболічних ризиків.
- Комбінація з метформіном. Найпоширенішою комбінацією для пацієнтів із ЦД 2 типу є поєднання глімепіриду з метформіном. Цей підхід рекомендований для пацієнтів, у яких глікемічний контроль на тлі монотерапії метформіном недостатній. Метформін знижує інсулінорезистентність і пригнічує продукцію глюкози печінкою, натомість глімепірид посилює секрецію інсуліну. Це забезпечує синергічний ефект, що дозволяє досягти кращого глікемічного контролю з мінімальним ризиком гіпоглікемії та зниженням впливу на масу тіла.
- Потрійна терапія (глімепірид, метформін та інший препарат). Для пацієнтів, які не досягають цільового рівня HbA1c на фоні двокомпонентної терапії (глімепірид + метформін), доцільним є додавання третього препарату іншого класу, наприклад інгібітора ДПП‑4, агоніста рецепторів ГПП‑1 або інгібітора НЗКТГ-2. Така потрійна терапія забезпечує комплексний підхід до лікування, впливаючи на кілька механізмів гіперглікемії одночасно (завдяки стимуляції секреції інсуліну, зниженню інсулінорезистентності, зменшенню реабсорбції глюкози в нирках). Це дозволяє знижувати HbA1c до цільового рівня з мінімізацією ризиків побічних ефектів.
- Застосування в рамках інтенсифікації терапії. У випадках, коли пацієнти не досягають цільового рівня глікемії навіть на потрійній терапії, або при значному підвищенні HbA1c (понад 2% від цільового рівня) настанови ADA/EASD рекомендують розглядати інтенсифікацію терапії, яка може включати додавання інсуліну або інтенсивніших комбінацій цукрознижувальних засобів. Глімепірид можна використовувати разом із базальним інсуліном для підтримання стабільного рівня глікемії протягом доби, особливо в пацієнтів із вираженою потребою в посиленні інсулінової секреції.
- Особливі клінічні сценарії. Глімепірид може бути корисним для пацієнтів літнього віку або тих, хто має обмежені фінансові можливості, оскільки цей препарат є доступним та ефективним. Водночас необхідно враховувати загалом підвищений ризик гіпоглікемії в цих пацієнтів і ретельно контролювати дозування.
Приклад титрування дози глімепіриду наведено на рисунку 2.
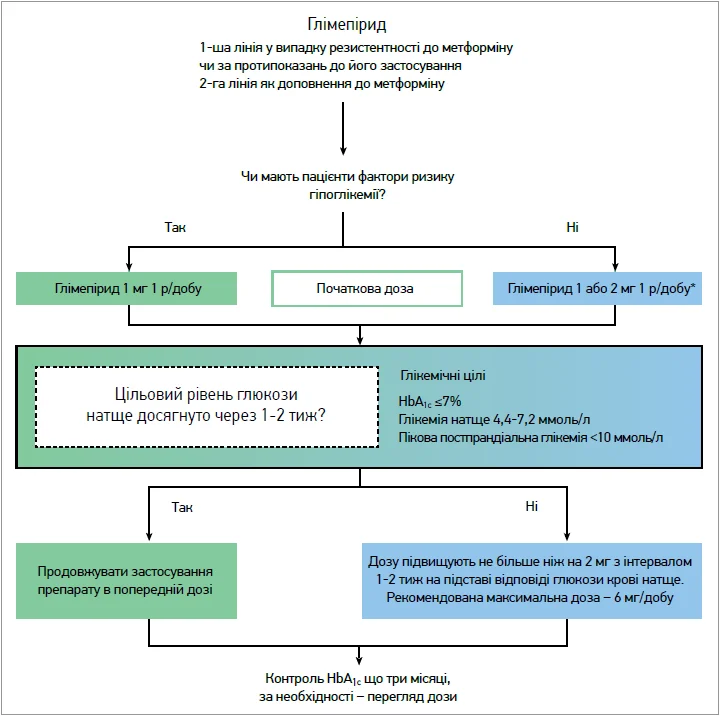 Рис. 2. Алгоритм початку терапії та титрування дози глімепіриду
Рис. 2. Алгоритм початку терапії та титрування дози глімепіриду
Примітка: * за рекомендацією FDA. В Україні, відповідно до інструкції із застосування лікарського засобу Олтар®, початкова доза глімепіриду становить 1 мг 1 р/добу [35].
Висновки
Глімепірид як представник ПСС третього покоління займає важливе місце в сучасних схемах ведення ЦД 2 типу. Завдяки здатності ефективно стимулювати секрецію інсуліну та впливати на чутливість до інсуліну периферичних тканин глімепірид забезпечує значне зниження рівня глюкози в крові, дозволяючи досягти і підтримувати цільові показники HbA1c.
Використання глімепіриду в різних клінічних сценаріях – від монотерапії до комбінованої та інтенсифікованої терапії – відповідає сучасним рекомендаціям та дозволяє індивідуалізувати лікування залежно від потреб пацієнтів. Крім того, глімепірид добре переноситься та є економічно доступним, що робить його оптимальним вибором для пацієнтів з обмеженими фінансовими ресурсами.
Доведена кардіоваскулярна безпека, відносно низький ризик гіпоглікемії та нейтральний вплив на масу тіла сприяють тривалому застосуванню глімепіриду як ефективного компонента терапії. Отже, він залишається перспективним препаратом у лікуванні ЦД 2 типу, особливо в складі комбінованих схем, котрі дозволяють забезпечити ранній і стабільний контроль глікемії і в такий спосіб мінімізувати ризики віддалених ускладнень.
Олтар®
В Україні глімепірид європейського виробництва представлений компанією «Берлін-Хемі» під назвою Олтар®. Олтар® показаний для лікування ЦД 2 типу в дорослих, коли лише дієти, фізичного навантаження та зниження маси тіла виявляється недостатньо для підтримання рівня глюкози в крові. Лінійка дозувань 2, 3, 4 або 6 мг глімепіриду в 1 таблетці дозволяє індивідуально підбирати цукрознижувальну терапію та плавно титрувати добову дозу з інтервалом 1 мг.
Список літератури знаходиться в редакції.
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 20 (582), 2024 р




