26 грудня, 2020
Роль молекулярно-генетичного тестування у веденні пацієнтів із вогнищевою патологією щитоподібної залози
 9-12 вересня 2020 року, у рамках науково-освітнього проекту регіонального циклу «Школа ендокринолога», спрямованого на поглиблення обізнаності медичної спільноти стосовно першочергових питань діагностики, лікування й профілактики ендокринних захворювань, було прослухано доповідь заступника директора з наукової роботи клініки ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (м. Київ), віце-президента Асоціації ендокринологів України, доктора медичних наук , професора Андрія Миколайовича Кваченюка, присвячену веденню пацієнтів із вогнищевою тиреоїдною патологією.
9-12 вересня 2020 року, у рамках науково-освітнього проекту регіонального циклу «Школа ендокринолога», спрямованого на поглиблення обізнаності медичної спільноти стосовно першочергових питань діагностики, лікування й профілактики ендокринних захворювань, було прослухано доповідь заступника директора з наукової роботи клініки ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (м. Київ), віце-президента Асоціації ендокринологів України, доктора медичних наук , професора Андрія Миколайовича Кваченюка, присвячену веденню пацієнтів із вогнищевою тиреоїдною патологією.
Вузли щитоподібної залози (ЩЗ) – доволі поширена причина звернень пацієнтів до лікарів-ендокринологів. Рівні поширеності вузлових захворювань ЩЗ різняться залежно від досліджуваної популяції та діагностичних методів виявлення вузлів. При пальпаторному обстеженні їх виявляють у 2-6% загальної популяції, при ультразвуковому дослідженні – у 19-35%, а за даними аутопсії – у 8-65% випадків. Саме завдяки широкому впровадженню в клінічну практику більш чутливих методів інструментальної візуалізації вузли ЩЗ все частіше стають випадковою знахідкою при обстеженні (Dean D.S. et al., 2008).
Незважаючи на те що в більшості випадків вогнищеві зміни є доброякісними і не потребують лікування, підхід до ведення даної категорії пацієнтів залишається предметом суперечок. Недостатнє розуміння спектра станів, які можуть проявлятися у вигляді тиреоїдних вузлів, та страх перед онкопатологією призвели до зростання частоти невиправданих оперативних втручань на ЩЗ. Останнє прямо корелює з поширеністю в популяції гіпотиреозу, який негативно впливає на якість життя пацієнтів, погіршує перебіг супутньої патології та потребує пожиттєвої замісної терапії.
Є безліч стратифікаційних систем для визначення ризику злоякісності вузлової патології ЩЗ, однак більшість із них вельми суб’єктивні, і тому їх використання в клінічній практиці швидше породжує нові сумніви, ніж дає відповіді.
Найбільш популярними шкалами для оцінки онкологічного потенціалу є такі системи (Tessler F.N. et al., 2017; Cibas E.S. et al., 2017):
- TIRADS (Thyroid Imaging, Reporting and Data System) – дає можливість визначити ризик злоякісності за ультразвуковими (УЗ) критеріями та відібрати пацієнтів для проведення пункційної біопсії;
- TBSRTC (The Bethesda System for rеporting Thyroid Cytopatology) – забезпечує стратифікацію онкологічного ризику за цитологічними критеріями для визначення показів для хірургічного лікування.
У 2018 р. були опубліковані результати дослідження, в якому оцінювалася стабільність початкового ризику злоякісності за УЗ критеріями протягом 5-річного періоду спостереження. Було використано 5 стандартних класифікаційних систем (АТА, ААСЕ/АСЕ/АМЕ, К-TIRADS, EU-TIRADS і TI-RADS).
Як показали результати, УЗ характеристики умовно доброякісних вузлів ЩЗ з часом залишаються стабільними, а зміни, які потребують біопсії, зазначалися лише в 6-8% випадків. Нові вузли з’являються часто, але тільки в 5% випадків вони належать до групи високого ризику.
Сукупність отриманих даних підтверджує, що пацієнти з імовірно доброякісними вузлами ЩЗ можуть безпечно продовжувати УЗ моніторинг без проведення тонкоголкової аспіраційної пункційної біопсії (ТАПБ) (Grani G. et al., 2018).
Сьогодні є безліч модифікацій TIRADS, однак у більшості з них основні УЗ ознаки злоякісності залишаються незмінними з 2002 року, коли вперше були представлені Е. Papini та співавт.: це виражена гіпоехогенність, неправильна форма «вище-ніж-ширше», нерівні і/або нечіткі контури та мікрокальцифікати.
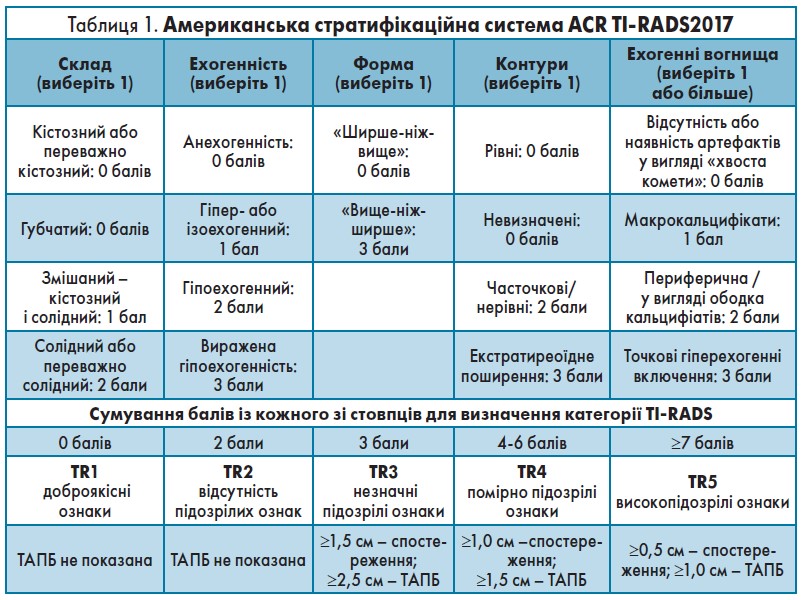
Перевагою ACR TI-RADS перед іншими варіантами класифікацій є бальна система оцінки злоякісності. Оцінюються окремі УЗ ознаки та їхні характеристики: склад, ехогенність, форма, контури, ехогенні вогнища. Доброякісні УЗ характеристики анулюються, а підозрілі – оцінюються певною кількістю балів, сума яких визначає категорію TI-RADS та покази до ТАПБ (табл. 1).
Отже, ТАПБ показана пацієнтам:
- категорії TR3, які мають вузли розміром ≥2,5 см;
- категорії TR4, які мають вузли розміром ≥1,5 см;
- категорії TR5, які мають вузли розміром ≥0,5 см.
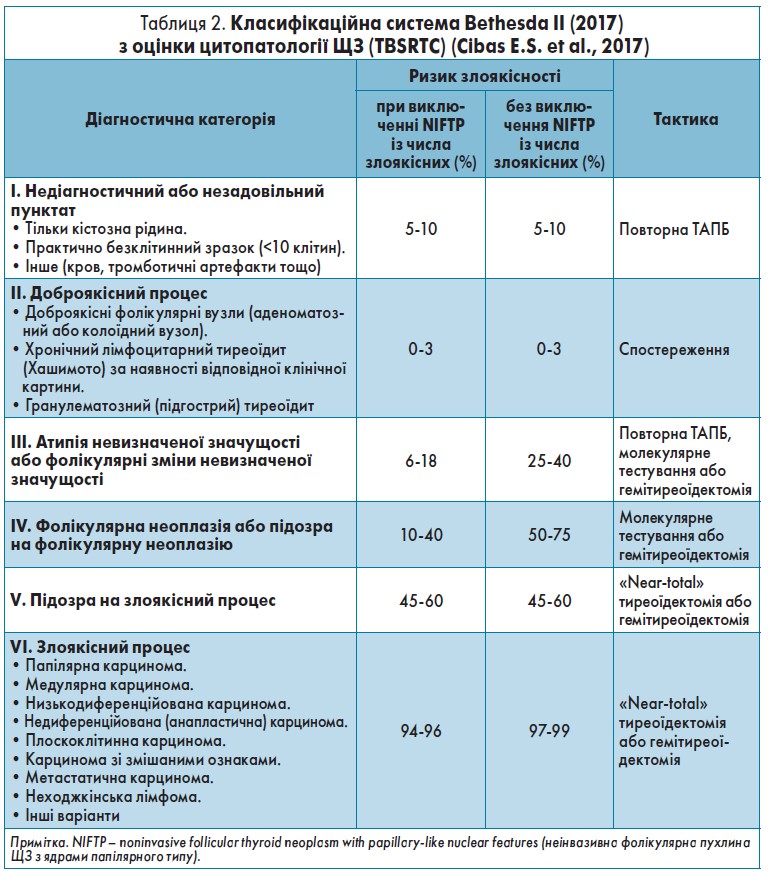
Для визначення термінології та вирішення інших питань, пов’язаних із ТАПБ ЩЗ, Національний інститут раку США провів наукову конференцію в місті Бетесда (Bethesda, штат Меріленд) та сформував систему Bethesda з оцінки цитології ЩЗ, 6 основних діагностичних категорій якої відображені в таблиці 2.
У випадках, коли отриманий діагностичний матеріал потрапляє під ІІІ-V діагностичні категорії, пацієнтам показане молекулярно-генетичне тестування (МГТ), яке дасть можливість уточнити діагноз та оптимізувати терапевтичну тактику. Поєднання ТАПБ і МГТ підвищує чутливість щодо злоякісності до 80% та знижує кількість хибно-негативних ТАПБ результатів із 2,1 до 0,9%. Для порівняння, чутливість щодо злоякісності ізольованої ТАПБ складає лише 44%.
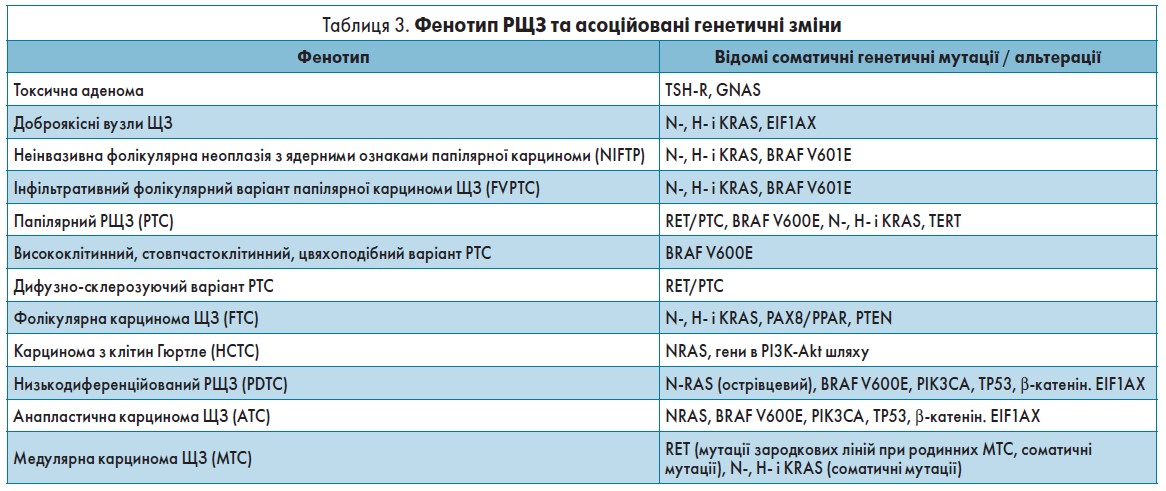
До 2017 року, з огляду на результати гістопатологічного дослідження, пухлини розподіляли на 2 великі категорії: доброякісні та злоякісні. Сьогодні ж виділяють безліч фенотипів раку ЩЗ (РЩЗ) з асоційованими генетичними змінами (табл. 3).
Кожна генетична зміна РЩЗ по-різному впливає на агресивність перебігу та відповідь на лікування. Так, при папілярному РЩЗ мутація BRAF дає можливість передбачити агресивність перебігу, мутація RET/PTC пов’язана з низькоагресивним перебігом, а відсутність мутацій забезпечує найкращий прогноз. Саме тому в разі появи цитопатологічних ознак злоякісного новоутворення (діагностична категорія VІ) МГТ допоможе виявити генетичні маркери, базуючись на яких визначають подальший терапевтичний алгоритм і прогнозують швидкість та тяжкість перебігу захворювання та успішність лікування.
Ще однією категорією пацієнтів, яким показане МГТ, є вагітні. Якщо раніше такі пацієнтки з цитологічним діагнозом «фолікулярна неоплазія» підлягали обов’язковому оперативному втручанню в післяпологовому періоді, то сучасна методика МГТ дає можливість визначити потребу в операції відразу після постановки діагнозу, що зменшує психологічне навантаження на вагітну та, за потреби, прискорює надання необхідної медичної допомоги, що напряму впливає на прогноз.
МГТ рекомендоване трьома основоположними клінічними настановами, побудованими згідно з принципами доказової медицини:
- Протоколом ведення дорослих пацієнтів із вузлами ШЗ та диференційованим РЩЗ Американської асоціації щитоподібної залози (American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer) 2015 року (Haugen B.R. et al., 2016);
- Настановою Європейської асоціації щитоподібної залози щодо молекулярної діагностики цитологічного матеріалу вузлів ЩЗ, отриманого за допомогою ТАПБ (European Thyroid Association Guidelines regarding Thyroid Nodule Molecular Fine-Needle Aspiration Cytology Diagnostics) 2017 року (Paschke R. et al., 2017);
- Клінічними рекомендаціями Національної глобальної онкологічної мережі США з лікування карциноми щитоподібної залози (National Comprehensive Cancer Network. Thyroid Carcinoma. Clinical Practice Guidelines in Oncology) 2017 року (NCCT, 2017).
Викладені в цих документах рекомендації дають можливість побудувати діагностичний алгоритм ведення пацієнтів категорій ТАПБ ІІІ-V:
Крок 1. Пацієнту проведено ТАПБ – отримано цитологічне заключення – категорія ТАПБ ІІІ, або ІV, або V.
Крок 2. З вузла/вузлів із зазначеною категорією ТАПБ взяти повторну ТАПБ – пунктат не на скельця, а в ПЦР-контейнер для молекулярно-генетичного дослідження.
При цьому варто пам’ятати, що хоча взяття біоматеріалу для молекулярно-генетичного дослідження під час першої ТАПБ не регламентовано, однак на практиці воно можливе і має клінічний сенс, якщо кваліфікація пунктолога дає йому можливість відразу запідозрити можливий результат ТАПБ «невизначена цитологія».
Отримання достовірних результатів МГТ можливе лише за умов строгого дотримання лабораторією, яка проводить дослідження, вимог чинних регламентуючих документів. На сьогодні цим критеріям повністю відповідає мережа медичних лабораторій «ДІЛА».
Переваги МЛ «ДІЛА» при проведенні МГТ:
1. Дослідження панелі генетичних мутацій, регламентованої основоположними світовими настановами.
2. Оцінка регламентованого спектра генетичних порушень, зокрема мутацій BRAFV600E, NRAS, KRAS, HRAS, RET/PTC (RET/PTC1 та RER/PTC3), PAX8/PPARg.
3. Застосування регламентованої методики ПЦР у реальному часі, яка забезпечує високу точність підтвердження доброякісності/злоякісності вузла та зниження кількості хибно-позитивних результатів.
4. Використання транспортного середовища з муколітиком, який забезпечує захист нуклеїнових кислот від спонтанної деградації в щойно відновленому біологічному матеріалі, зокрема при транспортуванні або зберіганні.
Таким чином, переваги МГТ біоптату з вузлів щитоподібної залози в МЛ «ДІЛА» мають:
- пацієнти категорії ТАПБ ІІІ, або ІV, або V – для визначення потреби в хірургічному лікуванні;
- пацієнти категорії ТАПБ VІ – для оцінки агресивності злоякісного новоутворення, оптимізації терапії та визначення прогнозу;
- вагітні пацієнтки з діагнозом «фолікулярна неоплазія» – з метою вибору оптимальної тактики (спостереження чи оперативне втручання).
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (51) 2020 р.