27 грудня, 2020
Вплив допоміжних речовин на стабільність таблеток левотироксину натрію
Останнім часом захворювання щитоподібної залози (ЩЗ) привертають до себе все більше уваги. Загалом, це пов’язано з погіршенням екології. Як і щодо інших нозологічних одиниць, спостерігається поступове збільшення кількості випадків розвитку гіпотиреозу (ГТ). За 10 років вона зросла на 38,9% і складає майже 50 випадків на 100 тис населення.
Золотим стандартом лікування ГТ є левотироксин (L-Тироксин). В аптеках є декілька різних препаратів L-Тироксину. Вони відрізняються наявністю допоміжних речовин (ДР), які, своєю чергою, впливають на стабільність левотироксину.
Як відомо, при виробництві лікарських препаратів використовуються допоміжні речовини: групи речовин органічної і неорганічної природи, необхідні для надання препарату корисних властивостей. Зазвичай зміст ДР у готових лікарських формах значно перевищує концентрацію діючих речовин. Наприклад, у таблетках понад 90% маси складають саме ДР. Останні мають низку функціональних властивостей, здатних чинити значущий вплив на стабільність та біодоступність діючих речовин, а отже, на якість і ефективність лікарських засобів.
Зокрема, таблетки, у складі яких є безводна лактоза, крохмаль або мікрокристалічна целюлоза (МКЦ), перестали відповідати вимогам Фармакопеї США (The United States Pharmacopeia – USP) через 3 міс при температурі 40 °C та 75% вологості. Таблетки, виготовлені з двоосновним фосфатом кальцію або манітолом, через той же проміжок часу відповідали вимогам USP.
Для успішного лікування гіпотиреозу важливо підібрати адекватну дозу для замісної терапії. Навіть незначні відхилення в кількості отриманого левотироксину можуть призводити до появи в пацієнта симптомів гіпотиреозу або тиреотоксикозу. Тому стабільне надходження чітко визначеної дози L-тироксину є запорукою успішного лікування гіпотиреозу. Для цього лікарю необхідні знання деяких фармакологічних характеристик препаратів тиреоїдних гормонів.
Синтетичний левотироксин використовується переважно для лікування ГТ та як пригнічувач тиреотропного гормону (ТТГ) в лікуванні або профілактиці різних типів еутиреоїдного зобу (Гудман і Гілман, 2001).
Історія замісної терапії налічує не один десяток років. Першим препаратом був екстракт ЩЗ вівці, який G. Murray у 1891 р. застосував у вигляді внутрішньом’язових ін’єкцій, а вже через рік – перорально. Подальші зусилля вчених були спрямовані на виділення тиреоїдних гормонів. У 1915 р. E. Kendall вдалося отримати чистий гормон ЩЗ в кристалічному вигляді, у 1926 р. C.R. Harrington здійснив його синтез – синтезував тироксин.
1952 року був відкритий другий гормон ЩЗ – трийодтиронін. Беручи до уваги, що ЩЗ продукує два гормони – тироксин (Т4) і трийодтиронін (Т3), довгий час вважали, що для лікування ГТ краще використовувати комбінацію Т4 і Т3. Але в 1970 р. L.E. Braverman, K. Sterling та співавт. відкрили периферичне перетворення тироксину в трийодтиронін. Згодом це послужило основою для використання в клінічній практиці переважно синтетичного L-Тироксину.
Починаючи з 1970-х рр. терапія синтетичним левотироксином поступово заміняла застосування екстрактів ЩЗ тварин. Вони складалися переважно з тиреоглобуліну, а також йодтиронінів і йоду в різних пропорціях. До їхніх недоліків слід віднести ненадійну стандартизацію, занадто високий вміст йоду, посилений перехід Т4 в Т3 при тривалому зберіганні, можливість утворення антитіл до тваринного білка.
Сьогодні для терапії ГТ застосовують синтетичні аналоги тиреоїдних гормонів, які позбавлені цих недоліків. Перший синтетичний продукт левотироксину був зареєстрований у США в 1955 р. Відтоді було багато відкликано препаратів левотироксину різних фармакологічних компаній. Майже всі відкликання були розпочаті через сумніви, що продукт буде підтримувати активність своєї дії протягом усього терміну придатності. Відсутність стабільності та суперечлива ефективність дії могла б спричинити серйозні наслідки для здоров’я тих, хто потребував прийому левотироксину.
Левотироксин має складний профіль стабільності, чутливий до світла, температури, вологи, рН і окислення (Post and Warren, 1976; Won, 1992; Kazemifard et al., 2001; Garnick et al., 1984; Wortsman et al., 1989). Won (1992) вивчав кінетику деградації левотироксину натрію в розчині та твердому стані. Він дійшов висновку, що в рідині левoтироксин натрію дотримується кінетики першого порядку деградації і при збільшенні рН розчину деградація зменшується. Запропонована деградація відбувалася шляхом дейодування. Кінетика деградації твердого стану виявилася двофазною, та запропонований метод здійснювався шляхом дезамінації.
Родс (1998) повідомив, що стабільність таблеток левотироксину – це складна проблема і наукові дослідження процесу деградації призведуть до виявлення основних методів формулювання та обробки, що ефективно усуне поточні проблеми.
Для високої ефективності низькодозового препарату (наприклад, левотироксин) очікується значна деградація активної речовини лікарського продукту завдяки високому вмісту ДР (Badaway et al., 1999).
Таким чином, метою цього дослідження було визначити вплив ДР на стабільність левотироксину натрію пентагідрат та відповідні йому таблетки.
Матеріали та методи
У досліджені були використані: левотироксину натрію пентагідрат, двоосновний фосфат кальцію, безводна лактоза, манітол, МКЦ та крохмаль, магнію стеарат, алюміній озерно-синій № 2, повідон, гідроксипропілметилцелюлоза (HPMC), натрію кроскармелоза, крохмаль гліколят натрію, кросповідон, стеаринова кислота, димний кремнезем (діоксид кремнію), HYDRANAL® Composite 2 та HYDRANAL® Methanol. Ацетонітрил, вода, трифтороцтова кислота, фосфорна кислота, трийод-L-тиронін, гідроксид натрію, соляна кислота, натрію карбонат, натрію бікарбонат, оксид магнію, винна й лимонна кислоти – були отримані від Fisher Scientific (Fair Lawn, NJ, USA). Дійодо-L-тиронін, тетрайодтирооцтова кислота, трийодтирооцтова кислота та дійодтирооцтова кислота – від Sigma Chemical Co. Для зберігання таблеток використовувалися пляшки, виготовлені з поліетилену високої щільності низького тиску з позначкою HDPE.
Аналіз
Для аналізу всіх зразків Garnick та співавт. (1984) використовували систему високоефективної рідинної хроматографії (ВЕРХ) з автоматичним пробовідбірником і УФ-детектором, встановленим на 25 нм. Під час рухомої фази при швидкості 0,3 мл/хв використовували метод ВЕРХ з оберненою фазою за допомогою колонок Waters®Spherisorb Cyano 25 см×2 мм (частинка розміром 5 м) та з ацетонітрилом: суміш води (40:60) з 0,5 мл/л фосфорної кислоти. Для аналізу зразків таблеток, виготовлених із модифікаторами рН, фосфорна кислота в рухомій фазі була замінена (0,3 мл/л) трифтороцтовою кислотою, оскільки це посилювало відновлення левотироксину.
Визначення вологи
Уміст вологи в зразках визначали за допомогою титрування Карла Фішера за титриметричним методом USP для визначення води. Приблизно 100 мг кожного порошкоподібного зразка титрували з реагентом Карла Фішера, HYDRANAL® Composite 2.
Стійкість та гігроскопічність левотироксину натрію
Порошок левотироксину натрію пентагідрат зберігався у відкритих і закритих флаконах при температурі 40 °C та 75% відносної вологості (ВВ) (ICH Q1A (R), 2000; FDA, 1998) загалом 6 місяців. Аналіз і визначення вологості проводили через 0; 3 та 6 місяців. Гігроскопічність левотироксину натрію пентагідрат визначали із сорбційним балансом вологи. Левотироксин натрію пентагідрат встановлювали на ваги та збільшували ВВ навколишнього середовища на 5%. Кожна наступна зміна ВВ проводилася після стабілізації зразка. Для цього був встановлений час – 2 години. Загальні зміни ВВ були в межах від 30 до 100%. Згодом вологість подібним чином поступово знижували до 10% ВВ.
Стійкість левотироксину натрію в таблетках
Виготовлення з різними розчинниками
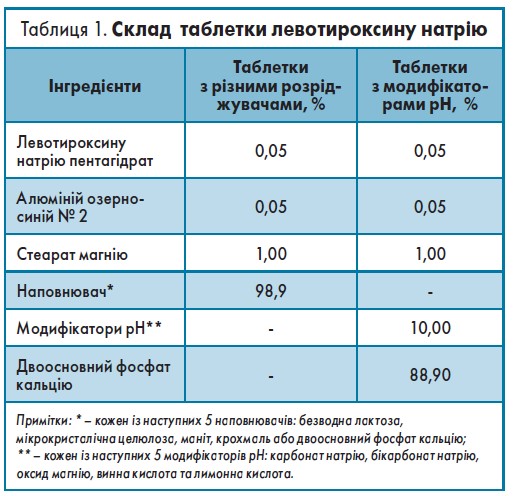 Різні партії таблеток левотироксину натрію 50 г виготовляли за допомогою одного з наступних п’яти наповнювачів: безводна лактоза, МКЦ, маніт, крохмаль та/або двоосновний фосфат кальцію. Усі таблетки містили магній стеарат та алюміній озерно-синій № 2 (табл. 1).
Різні партії таблеток левотироксину натрію 50 г виготовляли за допомогою одного з наступних п’яти наповнювачів: безводна лактоза, МКЦ, маніт, крохмаль та/або двоосновний фосфат кальцію. Усі таблетки містили магній стеарат та алюміній озерно-синій № 2 (табл. 1).
Виготовлення з модифікаторами рН
Різні партії таблеток левотироксину натрію 50 мкг виготовляли з двоосновним кальцію фосфатом та різними основними модифікаторами рН, а саме карбонатом натрію, бікарбонатом натрію, оксидом магнію та кислими модифікаторами рН, а саме винною і лимонною кислотами. рН насиченого розчину кожного з використовуваних модифікаторів становив: 8,1; 11,9; 10,3; 1,7 та 0,4 для бікарбонату натрію, натрію карбонату, оксиду магнію, винної та лимонної кислот відповідно (це відповідало б приблизному рН мікросередовища). Серія таблеток без модифікатора рН була контролем (табл. 1).
Усі таблетки зберігалися в поліетиленових пляшках з позначкою HDPE з осушувачем і без нього. Партії були протестовані на однорідність дозованих одиниць (USP 25). Стабільність активної речовини таблеток оцінювали протягом 6 міс в прискореному тесті стабільності згідно з нормативними вимогами ICH (40 °C та 75% вологості). Аналіз і визначення вологості проводили відразу після виготовлення та після 3 і 6 міс зберігання.
 Мас-спектроскопію таблеток, виготовлених із різними розчинниками, проводили на зразках 6 міс зберігання (Jin et al., 2001).
Мас-спектроскопію таблеток, виготовлених із різними розчинниками, проводили на зразках 6 міс зберігання (Jin et al., 2001).
Результати та обговорення
Стійкість та гігроскопічність левотироксину натрію
Лікарська речовина левотироксину натрію була стабільною при зберіганні протягом 6 міс в умовах прискореного тесту стабільності (температура/вологість 40 °C/75%) у відкритому або закритому контейнері (табл. 2).
У разі ВВ від 30 до 90% левотироксину натрію дещо збільшує вологість (приблизно на 1%) при дослідженні адсорбції-десорбції вологи (рис. 1), але при ВВ від 30 до 10% він швидко втрачав вологу (3,5% зміни ваги). Це показує, що левотироксин натрія є негігроскопічним за нормальних умов обробки (ВВ >30%), а при нижчій ВВ він втрачає вологу.
Вплив допоміжних речовин на стабільність таблетки левотироксину натрію
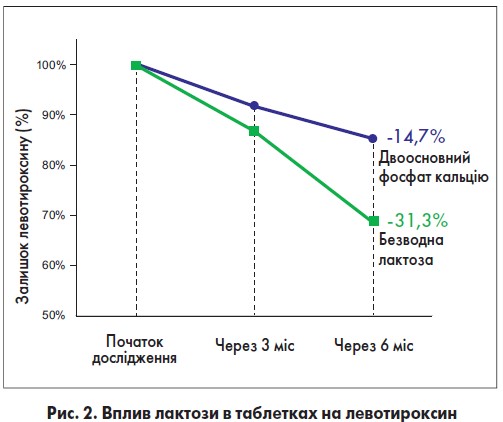
Як показано в таблиці 2, найкраща стабільність левотироксину натрію пентагідрат була досягнута з двоосновним фосфатом кальцію та манітом, які використовували як допоміжні речовини для таблеток. Через 6 міс зберігання при температурі 40 °C та 75% вологості таблетки в комбінації з цими наповнювачами мали суттєво менший вміст вологи (<1%) проти таблеток, виготовлених із МКЦ, крохмалем або безводною лактозою (≥5%). Однак ці таблетки не відповідали вимогам USP для аналізу ефективності дії через 6 міс за прискорених умов (рис. 2). Тобто хоча контроль вологості покращує стабільність, це все одно недостатньо для забезпечення стабільного складу.
.jpg) Первинними шляхами деградації, які спостерігалися під час мас-спектроскопії, були дейодування і дезамінування. Ці спостереження відповідали попереднім висновкам Андре та співавт. (1996) та Kazemifard і співавт. (2001). Також були виявлені продукти декарбоксилювання. Рацемізації не спостерігалося в жодній партії таблеток.
Первинними шляхами деградації, які спостерігалися під час мас-спектроскопії, були дейодування і дезамінування. Ці спостереження відповідали попереднім висновкам Андре та співавт. (1996) та Kazemifard і співавт. (2001). Також були виявлені продукти декарбоксилювання. Рацемізації не спостерігалося в жодній партії таблеток.
Учені дійшли висновку, що тип наповнювача, що його було використано для виготовлення таблеток левотироксину натрію, впливає на його стабільність. Таким чином, належний вибір ДР у виробництві таблеток левотироксину натрію був критичним.
Хоча сьогодні можна придбати препарати левотироксину, у складі яких використані такі допоміжні речовини, як лактоза та МКЦ, у згаданому дослідженні вони не виявилися найбільш підходящими розчинниками.
Це узгоджено з Гуптою та співавт. (1990), які вивчали таблетки левотироксину двох різних виробників. Автори зазначили, що таблетки одного виробника можуть мати різні варіації ДР. Ученими також було виявлено, що таблетки від конкретних виробників містили ДР, які діють як каталізатор для пришвидшення розкладання.
 Таблетки левотироксину натрію, які містять основні модифікатори рН, а саме карбонат натрію, бікарбонат натрію або оксид магнію, відповідали вимогам аналізу USP (90-110%), через 0; 3 та 6 міс зберігання при температурі/вологості 40 °C/75%.
Таблетки левотироксину натрію, які містять основні модифікатори рН, а саме карбонат натрію, бікарбонат натрію або оксид магнію, відповідали вимогам аналізу USP (90-110%), через 0; 3 та 6 міс зберігання при температурі/вологості 40 °C/75%.
За результатами дослідження було вдосконалено використання основного модифікатору рН – двоосновного фосфату натрію для покращення стабільності таблеток левотироксину натрію пентагідрат. На відміну від використання кислих модифікаторів рН виявлялася посилена деградація.
Був зроблений висновок, що використання основних модифікаторів рН є потенційною методикою підвищення стабільності таблетки левотироксину натрію.
Висновки
Левотироксину натрію пентагідрат – лікарська речовина, яка зберігає свою стабільність в умовах прискореного тесту за нормативними вимогами ICH протягом 6 міс і є негігроскопічною в нормальних умовах обробки.
На розпад таблеток левотироксину натрію впливає тип використаних у рецептурі ДР. Таблетки, виготовлені з деяких із найбільш часто використовуваних допоміжних речовин: безводної лактози, крохмалю та МКЦ, продемонстрували значно більші втрати ефективності через 6 міс зберігання в умовах температури 40 °C і 75% вологості, ніж таблетки, виготовлені з манітолом або двоосновним фосфатом кальцію. Втрата ефективності на 30% супроводжувалася значущим збільшенням вологи (лактоза, 0,8-5%; крохмаль, 7,8-10,25%) або була пов’язана з початково високим її вмістом (МКЦ, 6,2%). Ліки, виготовлені з манітолом або двоосновним фосфатом кальцію, показали лише приблизно 15% втрати потенції, і ці таблетки містили <1% вологи спочатку і через 6 місяців.
Попри те що контроль вологості покращував стабільність, він був недостатнім для стабілізації рецептури та задоволення ICH критеріїв стабільності. Це було продемонстровано в таблетках, які містили 88,9% двоосновного фосфату кальцію та 10% кислотного модифікатора рН (лимонна або винна кислота). Ці таблетки мали <1% вологи, проте втрати ефективності становили майже 25% через 6 міс при температурі 40 °C та 75% вологості. Однак таблетки, виготовлені з 88,9% двоосновного фосфату кальцію і 10% основного модифікатора рН (натрію карбонат, бікарбонат натрію або оксид магнію), відповідали критеріям стабільності ICH щодо потенції протягом 6 міс при температурі/вологості 40 °C/75%.
Як показало дослідження, левотироксин натрію в таблетках найбільш стабільний в присутності наповнювача з низьким умістом вологи та низьким поглинанням, а саме з двоосновним фосфатом кальцію.
В Європі в 2012 р. під час аналізу препаратів із левотироксином було виявлено, що майже всі ліки містять деякі спільні ДР (кукурудзяний крохмаль, желатин, лактоза моногідрат), але більшість ДР різні. Загалом у 53% пацієнтів, які застосовували >100 мкг/день левотироксину зі спільними ДР (кукурудзяний крохмаль, желатин, лактоза моногідрат), спостерігалися біохімічні ознаки надмірного вживання добавок. У відповідь було видано загальну пораду перевірити рівень ТТГ у сироватці крові через 6 тиж після будь-якої зміни марки та врахувати зменшення дози в пацієнтів, які отримували >100 мкг/день.
У результаті перевірки Британське агентство з контролю якості лікарських засобів та медичних продуктів призупинило дію ліцензії на таблетки левотироксину, що містили лактозу, унаслідок зниженої активності препаратів.
Серед виробників, які працюють на українському фармацевтичному ринку, міжнародна компанія «Берлін-Хемі/Менаріні» (Німеччина) також дотримується такої політики, зокрема вона виключила лактозу й барвники зі складу препарату L-тироксину (L-Тироксин від «Берлін-Хемі/Менаріні» – таблетки по 50; 75; 100; 125 і 150 мкг).
Заміна лактози на інші допоміжні речовини, як показали дослідження Н. Patel та співавт., підвищує стабільність таблеток L-Тироксину, подовжує час активності діючої речовини при зберіганні. Проведення адекватної замісної терапії гіпотиреозу безлактозними формами L-тироксину не тільки сприятиме покращанню соматичного стану пацієнта, а й слугуватиме профілактикою численних органних порушень, що виникають на тлі зниженої функції щитоподібної залози.
Patel H. et al. The effect of excipients on the stability of levothyroxine sodium pentahydrate tablets, International Journal of Pharmaceutics. Vol. 264, Is. 1-2, 2 October 2003, P. 35-43.
Список літератури знаходиться в редакції.
Реферативний огляд підготувала Юлія Золотухіна
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (51) 2020 р.



