7 грудня, 2024
Синдром подразненого кишечнику: у фокусі – терапія спазму та болю
 Не згасає інтерес у сучасній медицині до вивчення найрозповсюдженіших функціональних гастроінтестинальних розладів (ФГІР). ФГІР – група хвороб, яким притаманні хронічні симптоми з боку травного тракту (біль у животі, дисфагія, диспепсія, діарея, закрепи та здуття живота) за відсутності видимого при обстеженнях патологічного стану. ФГІР виникають унаслідок порушень міжорганної комунікації між мозком і кишечником [12]. З урахуванням біопсихосоціальних факторів, використанням даних інтегративного опитувальника наразі встановлюють нові підтипи ФГІР. Ідентифіковано 4 підтипи ФГІР: легкий, тяжкий, а також із переважанням розумових і тілесних симптомів [13].
Не згасає інтерес у сучасній медицині до вивчення найрозповсюдженіших функціональних гастроінтестинальних розладів (ФГІР). ФГІР – група хвороб, яким притаманні хронічні симптоми з боку травного тракту (біль у животі, дисфагія, диспепсія, діарея, закрепи та здуття живота) за відсутності видимого при обстеженнях патологічного стану. ФГІР виникають унаслідок порушень міжорганної комунікації між мозком і кишечником [12]. З урахуванням біопсихосоціальних факторів, використанням даних інтегративного опитувальника наразі встановлюють нові підтипи ФГІР. Ідентифіковано 4 підтипи ФГІР: легкий, тяжкий, а також із переважанням розумових і тілесних симптомів [13].
У структурі ФГІР однією з найпоширеніших нозологічних одиниць є синдром подразненого кишечнику (СПК). Незважаючи на значну кількість досліджень, які проводили з метою пояснити причини виникнення СПК, це захворювання продовжує бути складною проблемою ХХІ ст.
СПК – поширений хронічний рецидивувальний ФГІР із ремітувальним перебігом, за якого біль у животі пов’язаний з дефекацією, зміною частоти та характеру випорожнень. Симптоми СПК з’являються і зникають із часом, вони асоціюються з іншою функціональною та позакишковою соматичною патологією. Показники поширеності СПК варіюються від 1,1 до 45% на основі досліджень населення в країнах усього світу. Поширеність коливається від 6,0 до 12% у Європі, США та Японії [15], в Україні становить 16-20%. Із 2022 р. збільшується кількість хворих на СПК. СПК із діареєю зустрічається в 37% хворих, із закрепом – у 25%, зі змішаним субтипом – у 19%, некласифікований СПК спостерігається в 19% [4]. Жінки в 2-4 рази частіше страждають через СПК, ніж чоловіки. Симптоми виникають переважно в пацієнтів віком до 45 років. Останніми роками спостерігається зростання поширеності ФГІР‑патології серед людей літнього віку [20]. Поява клінічної симптоматики в осіб віком >40 років не виключає СПК, але передбачає ретельний пошук недіагностованої органічної патології. Поширеність захворювання варіює у різних країнах і залежить від використаних діагностичних критеріїв [14].
Уперше СПК описано в XIX ст. Джоном Хаушіпом у 1830 р. зі шпиталю Святого Георгія в Лондоні. Надалі Вільям Ослер у 1892 р. позначив цей стан як слизовий коліт. За тривалий час його вивчення СПК отримав значну кількість синонімічних визначень, як-от спастичний коліт, невроз кишечнику. Перші критерії СПК запропоновані A. P. Manning і співавт. у 1978 р. Міжнародна робоча група з вивчення функціональної патології травного тракту на чолі з професором Д. А. Дроссманом уперше офіційно затвердила термін СПК у 1992 р. під час роботи IX Всесвітнього конгресу гастроентерологів у Римі та надала його критерії для установлення діагнозу, які отримали назву «Римські критерії СПК». У 1999, 2006 і 2016 рр. критерії були модернізовані – Римські критерії II, Римські критерії III, Римські критерії IV [14].
Л. Енжел запропонував біопсихосоціальну модель розвитку СПК, згідно з якою він розвивається в результаті стресового втручання в біологічні, психологічні та соціальні сфери, що взаємодіють на різних рівнях. Подальші психосоціальні дослідження продемонстрували, що розвиток СПК зумовлюють порушення взаємодії центральної нервової системи (ЦНС) та автономної ентеральної нервової системи [18].
Вагому роль у патофізіології СПК відіграють порушення перистальтики, проникності кишкової стінки, гіперчутливість шлунково-кишкового тракту (ШКТ), стресорні фактори, порушення мікробного пейзажу, що сприяють розвитку мікрозапалення [6]. Незважаючи на те що СПК належить до групи функціональних хвороб, із кожним роком збільшується кількість доказів наявності мікроморфологічних ознак цього захворювання. Нині численними дослідженнями доведено, що 25% випадків розвитку СПК передують гострі інфекційні захворювання, а в 40% випадків прогресування СПК відбувається на тлі порушеного мікробного пейзажу кишечнику [18].
Ролі генетичної схильності у виникненні СПК приділяється багато уваги. Обтяжений сімейний анамнез СПК мають приблизно 33% пацієнтів. Під час низки досліджень вивчався можливий вплив поліморфізму генів, що кодують протизапальні та прозапальні інтерлейкіни, α2-адренергічні, серотонінові й холецистокінінові рецептори. Зафіксовано значний взаємозв’язок між поліморфізмом серотонінових рецепторів і ступенем вираженості симптомів СПК [16].
Феномен вісцеральної гіперчутливості в пацієнтів із СПК виявив Вільям Е. Вайтхед за допомогою балонно-дилатаційного тесту за швидкого механічного розтягування стінки прямої кишки [21]. Клінічні прояви СПК високо корелюють з вираженістю вісцеральної гіперчутливості. Розвиток вісцеральної гіперчутливості може обумовлюватися двома механізмами: зниженням порогу сприйняття болю та інтенсивнішим відчуттям болю за нормального порогу сприйняття. СПК притаманний дифузний характер порушення сприйняття болю протягом усього кишечнику. Основними клінічними ознаками вісцеральної гіперчутливості є симптоми гіпералгезії та алодинії. Гіпералгезія проявляється як підвищеною чутливістю до больових стимулів, так і відчуттям болю, що виникає у відповідь на дію небольових стимулів. Алодинія проявляється розладами різних функцій у відповідь на дію больових стимулів [10]. Вісцеральна гіперчутливість – багатофакторний процес, який може зачіпати периферичну і ЦНС, а також відігравати основну роль у патогенезі СПК. Селективна гіперчутливість розвивається внаслідок стимуляції різних рецепторів вісцеральних аферентних нервових волокон у кишковій стінці, крім того, провокує розтягування чи здуття кишечнику, що може пояснити виникнення різних симптомів СПК [8].
Традиційно СПК – стан, що супроводжується зміною моторики кишечнику (із зумовленням діареї чи закрепу), вісцеральною гіперчутливістю (зі спричиненням абдомінального дискомфорту або болю), психопатологією. Зміна моторики кишечнику в хворих на СПК, емоційний стрес або сильні емоції через вісь «головний мозок – кишечник» можуть сприяти порушенню моторики (особливо тонкого та товстого кишечнику). Кишечник хворих на СПК є чутливішим до впливу стресових факторів порівняно зі здоровими особами. Порушення моторики тонкого кишечнику може маніфестувати прискоренням транзиту їжі, схиляючи до появи діареї, а також уповільненням її проходження із зумовленням закрепу [14].
З огляду на обмежений успіх у лікуванні ФГІР за допомогою традиційних методів існує нагальна потреба в індивідуальному лікуванні, яке враховує гетерогенність і біопсихосоціальні фактори, пов’язані з ФГІР [13]. Ідентифікація нових підтипів ФГІР пропонує основу для персоналізованих стратегій лікування, потенційно покращуючи терапевтичні результати через унікальні біопсихосоціальні профілі пацієнтів із ФГІР.
Сучасні стратегії менеджменту хворих цієї групи передбачають, що діагностика і тактика терапії СПК здійснюються з позиції Римських критеріїв IV [7]. Згідно з ІV Римськими рекомендаціями медикаментозну терапію пропонується призначати з урахуванням переважання в пацієнтів із СПК тих чи інших клінічних симптомів. Абдомінальний біль – головна ознака СПК, відсутність болю в животі виключає цей клінічний діагноз. Абдомінальний біль – значущий фактор, що зумовлює суттєве зниження якості життя пацієнтів, тому саме лікування спазмолітичними препаратами, які впливають на вісцеральну гіперчутливість, може бути патогенетично обґрунтованим. Спазмолітики – препарати вибору в пацієнтів із дискомфортом або абдомінальним болем, котрі сприяють релаксації гладкої мускулатури кишечнику, зменшують або усувають абдомінальний біль та спазм. Важливою умовою призначення спазмолітиків є тривалість терапії з можливістю застосування лікарського препарату не менш ніж 1 місяць, надалі – тривало в режимі «за потреби». Тому доцільним є застосування міотропних спазмолітиків із вибірковою дією на гладенькі м’язи травного тракту, що підтвердили як свою високу клінічну ефективність, так і високий ступінь безпеки саме при тривалому використанні [5].
Одним із найвивченіших селективних міотропних спазмолітиків для ШКТ є мебеверину гідрохлорид. Експериментальні дослідження показали, що мебеверин має два ефекти. Перший – блокада швидких натрієвих каналів клітинної мембрани міоциту, що порушує процеси надходження натрію до клітини, сповільнює процеси деполяризації, припиняє надходження кальцію до клітини через повільні канали. В результаті знижуються процеси фосфорилювання міозину, швидко знімається спазм м’язового волокна (антиспастичний ефект). Другий ефект обумовлений зниженням поповнення внутрішньоклітинних кальцієвих депо, що зумовлює лише короткочасний вихід іонів калію із клітини та її гіперполяризацію, а це, своєю чергою, запобігає розвитку гіпотонії м’язового волокна після усунення спазму. Цей ефект мебеверину вигідно відрізняє його від дії інших міотропних спазмолітиків, які зумовлюють тривалу гіпотонію. Поряд зі спазмолітичною дією мебеверину гідрохлорид має прокінетичну активність [9].
Наразі в Україні в розпорядженні лікарів є оригінальний препарат мебеверину (Дуспаталін®) [2]. Нами проведено дослідження, метою якого була оцінка клінічної ефективності оригінального препарату мебеверину в купіюванні абдомінального больового синдрому та порушень випорожнення за різних клінічних фенотипів СПК.
Матеріали та методи
До випробування залучили 72 пацієнтів (жінки – 51, чоловіки – 21) віком від 18 до 57 років. Медіана віку складала 35,7 (30,6; 46,5) року. Критерії включення: вік >18 років, наявність у хворих клінічних симптомів СПК (абдомінальний біль, здуття живота, діарея, закрепи, чергування діареї та закрепів), відсутність органічної патології, яка могла пояснити симптоми. Критерії виключення пацієнтів із дослідження: вагітність або період годування грудьми, одночасне застосування інших спазмолітиків, наявність онкологічних захворювань, депресії, тривоги, психічних розладів, патології ШКТ, що потребує хірургічного лікування, перенесені в анамнезі операції на черевній порожнині, за винятком апендектомії та холецистектомії, наявність хвороби Крона, виразкового коліту чи іншого захворювання кишечнику у фазі загострення, а також декомпенсованих захворювань інших органів і систем, що перешкоджають достовірній оцінці ефективності препарату. Діагноз СПК установлювали на основі ІV Римських критеріїв [7]. За нозологічним принципом і методом лікування сформували 3 групи: групу 1 склали 26 пацієнтів із СПК із діареєю (СПК-Д); групу 2 – 24 хворі з СПК із закрепами (СПК-З); до групи 3 увійшли 22 пацієнти із СПК змішаного варіанту (СПК-ЗВ). Групи хворих були зіставними за гендерною структурою, віком, індексом маси тіла (табл. 1).
|
Таблиця 1. Характеристика пацієнтів із СПК залежно від клінічного фенотипу |
||||
|
Параметр |
Група 1 |
Група 2 |
Група 3 |
р |
|
Клінічний фенотип СПК |
СПК |
СПК |
СПК |
- |
|
Загальна кількість |
26 |
24 |
22 |
0,64 |
|
Чоловіки |
8 |
7 |
6 |
0,36 |
|
Жінки |
18 |
17 |
16 |
0,84 |
|
Медіана віку |
32 (29,2; 45,3) |
35,5 (30,4; 48,1) |
37,5 (31,8; 48,8) |
0,49 |
|
Індекс маси тіла |
22,6 (20,6; 32,7) |
24,85 (21,8; 33,3) |
30,5 (23,2; 34,1) |
0,52 |
|
Пацієнти із супутніми хронічними |
9 |
13 |
12 |
0,78 |
|
Пацієнти, котрі |
3 |
6 |
5 |
0,61 |
Усі хворі приймали оригінальний препарат мебеверину (Дуспаталін®) по 135 мг 3 р/добу за 20 хвилин до прийому їжі протягом 8 тижнів [2]. Хворим із діареєю додатково призначали кишкові адсорбенти (діосмектит у загальноприйнятих дозах) через 1 годину після вживання їжі до нормалізації випорожнень. Хворі із закрепами додатково отримували лактулозу в індивідуально підібраних дозах до відновлення випорожнень. Усім пацієнтам рекомендували дотримання дієти відповідно до типу CПК.
Методи дослідження включали загальноклінічне обстеження (збір скарг, анамнезу, клінічний огляд, антропометричні показники). Всім хворим робили загальний аналіз крові, копрограму, УЗД органів черевної порожнини. Пацієнтам із діареєю призначали дослідження для визначення показників С‑реактивного білка, кальпротектину калу, антитіл до ендомізію (IgA, IgG), антитіл до тканинної трансглутамінази (IgA, IgG); за потреби досліджували показники еластази калу та рівень тиреотропного гормона (ТТГ). Пацієнтам із закрепами визначали рівні ТТГ, Са крові. Колоноскопію не проводили через відсутність у всіх хворих симптомів тривоги. Пацієнтам віком >50 років на момент дослідження колоноскопія не проводилася; діагноз СПК у цієї вікової категорії був установлений у віці <50 років.
Оцінка ефективності лікування проводилася клінічно щодо зменшення (зникнення) болю, діареї, закрепів на 1-й та 7-й дні лікування, на 2-му та 4-му тижні лікування, а також через 2 місяці після лікування.
Визначення інтенсивності болю проводилося за візуальною аналоговою шкалою (ВАШ). ВАШ – це горизонтальна 10-сантиметрова лінія, на одному кінці якої зазначено «немає болю», а на іншому – «найсильніший біль, який можна уявити». Пацієнта просять поставити на цій лінії крапку, яка відповідає рівню пережитих ним больових відчуттів. Відстань, виміряна між кінцем лінії «відсутність болю» та зазначеною точкою, є цифровою оцінкою болю. ВАШ – проста, ефективна та мінімально обтяжлива для хворого методика, яка добре корелює з іншими достовірними тестами. ВАШ визначає лише інтенсивність болю, не надаючи інформації про якісні характеристики [1].
У дослідженні використовували два опитувальники: валідований неспецифічний опитувальник якості життя SF‑36; валідований специфічний опитувальник Gastrointestinal Symptom Rating Scale (GSRS).
У гастроентерологічній практиці найпоширенішим опитувальником є специфічний опитувальник GSRS – шкала оцінки шлунково-кишкових симптомів; саме тому в нашому дослідженні для оцінки вираженості гастроентерологічної симптоматики і якості життя (ЯЖ) використовувалася україномовна версія спеціального опитувальника GSRS [11, 3]. Спеціальний опитувальник GSRS складається з 15 запитань, згрупованих у 5 шкал: абдомінальний больовий синдром (AP), рефлюкс-синдром (RS), діарейний синдром (DS), диспепсичний синдром (IS), синдром закрепів (CS), шкала сумарного вимірювання. Виразність симптомів оцінювалася в балах від 1 до 7, де 1 бал відповідав повній відсутності суб’єктивних проявів симптому, а 7 балів – дуже сильному суб’єктивному прояву симптому. Сума балів певних номерів запитань становить значення шкали. Отже, вищі значення відповідають вираженішим симптомам, тому і нижчій ЯЖ. Опитувальник GSRS може застосовуватися для оцінки абдомінальних симптомів у пацієнтів із СПК [17].
ЯЖ, пов’язану зі здоров’ям, вивчали за допомогою української версії валідованого стандартизованого неспецифічного опитувальника The 36-Item Short Form Health Survey (SF‑36) [11], який містить 36 запитань, об’єднаних у 8 шкал, і 2 інтегральні показники.
Вони дозволяють оцінити всі компоненти ЯЖ:
- фізичне функціонування (ФФ) – оцінка буденних фізичних навантажень;
- рольове ФФ (РФФ) – обмеження життєдіяльності за рахунок фізичних проблем;
- інтенсивність тілесного болю характеризує роль больових відчуттів в обмеженні життєдіяльності;
- загальний стан здоров’я людини – суб’єктивна оцінка пацієнтом свого здоров’я на час анкетування;
- життєва активність – суб’єктивна оцінка хворим життєвого тонусу;
- рольове емоційне функціонування – обмеження життєдіяльності за рахунок емоційних проблем;
- соціальне функціонування (СФ) – оцінка пацієнтом рівня відносин із рідними, друзями, колегами;
- психічне здоров’я – оцінка настрою.
За цими шкалами розраховують інтегральні показники – фізичний компонент здоров’я і психічний компонент. Результати за кожною шкалою визначаються в балах від 0 до 100, де 100 відповідає повному здоров’ю. Градація показника ЯЖ для різних доменів відповідає таким інтервалам: низький показник ЯЖ – 0-20 балів; знижений – 21-40 балів; середній – 41-60 балів; підвищений – 61-80 балів; високий – 81-100 балів. Опитувальник не є специфічним для вікових груп, певних нозологій або програм лікування.
Перед проведенням випробування всіх пацієнтів проінструктували щодо того, як заповнювати щоденник хворого для реєстрації зменшення / зникнення абдомінального болю, метеоризму, частоти випорожнень, інших диспепсичних симптомів і проявів астенічного синдрому.
Пацієнти досліджуваних груп були зіставними за статтю, віком та інтенсивністю болю за ВАШ.
Статистичний аналіз
Статистична обробка отриманих даних проводилася з використанням ліцензійної програми STATISTICA та Microsoft Excel. Використовували методи непараметричної статистики, визначали медіану показників (Ме), межі інтерквартильного відрізка (25; 75%) під час опису кількісних ознак, якісних – у відсотках за допомогою критерію χ2. Для порівняння показників у двох незалежних групах використовували U‑критерій Манна – Вітні та критерій Вілкоксона (W) для порівняння двох залежних груп. Оцінка ступеня взаємозв’язку між парами незалежних ознак, виражених у кількісній шкалі, проводилася за допомогою коефіцієнта рангової кореляції Спірмана (r). Статистично значущі відмінності результатів досліджень визначали за рівня p<0,05.
Результати та обговорення
При аналізі характеристик больового синдрому на початку спостереження встановлено, що хворі з різними фенотипами СПК не мали достовірних відмінностей в інтенсивності абдомінального болю за шкалою ВАШ (табл. 2). За основними характеристиками больового синдрому групи були зіставними. Водночас варто зауважити, що достовірно більший відсоток хворих з абдомінальним болем після стресу в групі СПК із діареєю порівняно з 2-ю та 3-ю групами становив 92,3; 58,3 та 68,2% відповідно (p<0,05).
|
Таблиця 2. Характеристика больового синдрому в пацієнтів із СПК на початку спостереження залежно від клінічного фенотипу |
|||
|
Параметр |
Група 1 – СПК із діареєю, n=26 |
Група 2 – СПК із закрепами, n=24 |
Група 3 – СПК змішаного варіанту, n=22 |
|
Періодичний абдомінальний біль, n |
21 |
18 |
16 |
|
Постійний абдомінальний біль, n |
5 |
7 |
6 |
|
Ниючий абдомінальний біль, n |
11 |
8 |
6 |
|
Розпираючий абдомінальний біль, n |
16 |
17 |
13 |
|
Колючий абдомінальний біль, n |
13 |
9 |
12 |
|
Невизначений абдомінальний біль, n |
4 |
3 |
4 |
|
Абдомінальний біль після вживання їжі, n |
8 |
9 |
7 |
|
Абдомінальний біль у разі порушення дієти, n |
18 |
16 |
16 |
|
Абдомінальний біль після стресу, n |
24* |
14 |
15 |
|
Абдомінальний біль після перевтоми, n |
12 |
12 |
10 |
|
Інтенсивність абдомінального болю за шкалою ВАШ у початковому стані |
7 (5,2; 8,9) |
6 (4,8; 8,2) |
7 (5,0; 8,6) |
|
Примітка: * р<0,05 порівняно з 2-ю та 3-ю групами. |
|||
Усі 72 пацієнти, включені в дослідження, були комплаєнтні за препаратами, які призначалися. Під час лікування небажані явища були поодинокими (p>0,05) і не пов’язувалися із симптомами СПК. Під час аналізу динаміки інтенсивності больового синдрому встановлено, що в усіх трьох групах хворих із СПК інтенсивність больового синдрому за шкалою ВАШ достовірно знизилася наприкінці спостереження (рис. 1). Отже, в групі 1 інтенсивність абдомінального болю зменшилася на 85,7%, а в групах 2 і 3 – на 90% та 88,6% відповідно (р<0,05).
Динаміку абдомінального больового синдрому в групі пацієнтів із СПК на тлі лікування оригінальним препаратом мебеверину продемонстровано на рисунку 2. Встановлено, що зменшення інтенсивності больового синдрому спостерігалося в більшості пацієнтів уже на 1-й день лікування, котрий повністю купіювався протягом 1 тижня незалежно від клінічного фенотипу СПК. Слід зазначити, що повне зникнення абдомінального болю через 2 місяці спостереження встановлено в усіх хворих із СПК.
При аналізі часу виникнення протибольового ефекту оригінального препарату мебеверину (Дуспаталін®) встановлено, що в середньому ефект відбувався на 15,06 (9,2; 16,2) хвилину від прийому препарату та не залежав від клінічного фенотипу СПК (рис. 3).
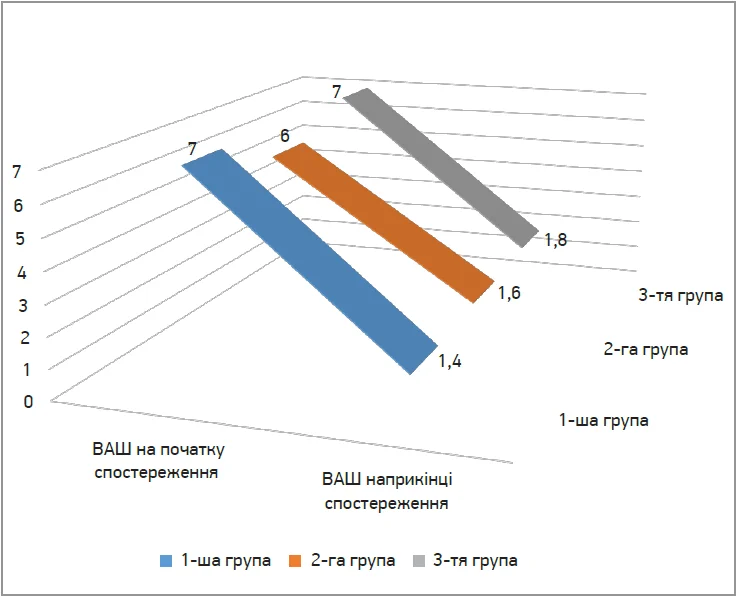 Рис. 1. Динаміка інтенсивності больового синдрому на тлі лікування оригінальним препаратом мебеверину в хворих із СПК залежно від клінічного фенотипу
Рис. 1. Динаміка інтенсивності больового синдрому на тлі лікування оригінальним препаратом мебеверину в хворих із СПК залежно від клінічного фенотипу
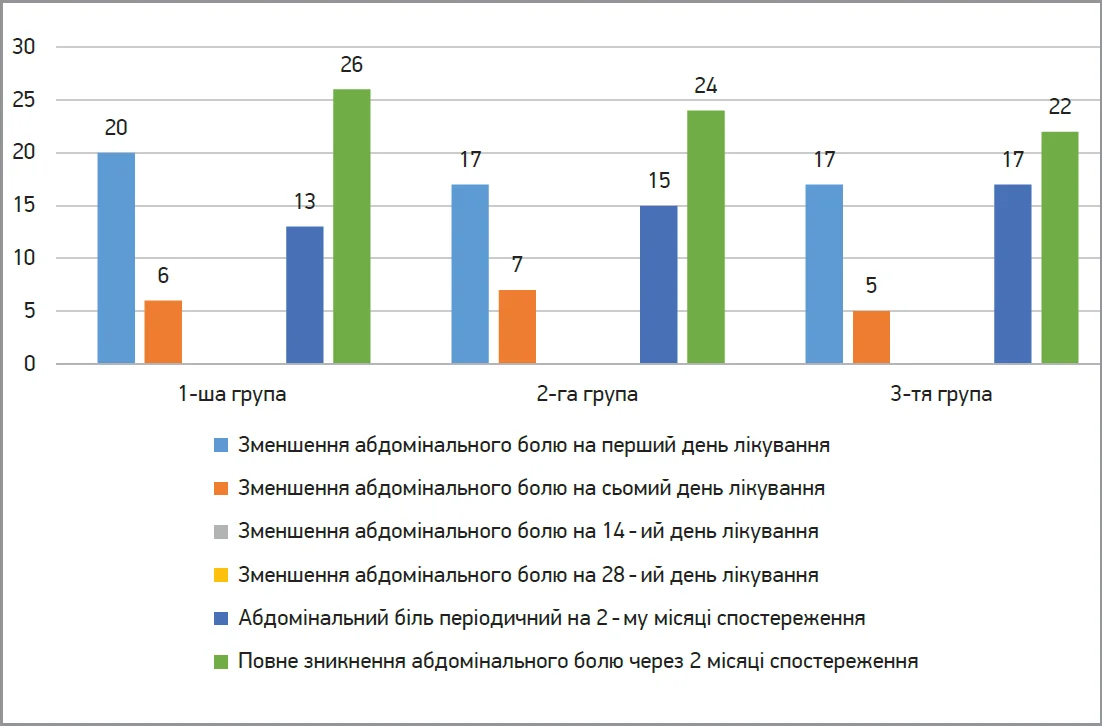
Рис. 2. Динаміка больового синдрому в пацієнтів із СПК на тлі лікування оригінальним препаратом мебеверину (Дуспаталін®) залежно від клінічного фенотипу
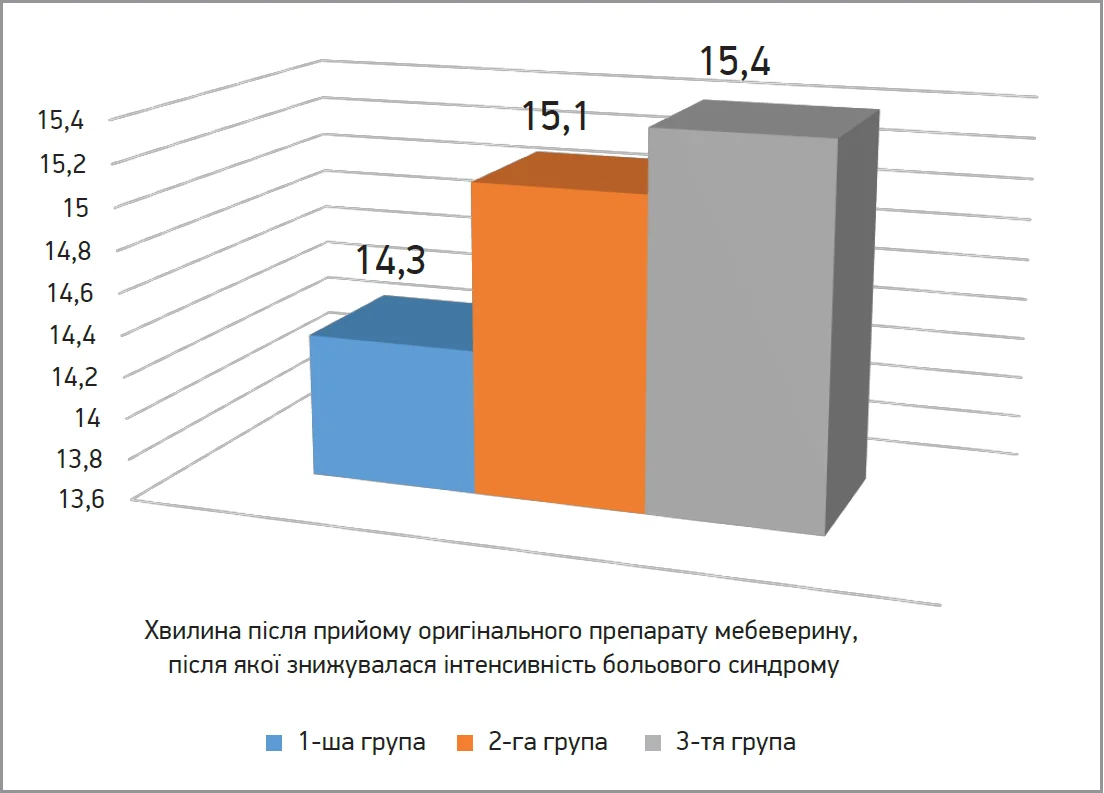
Рис. 3. Медіана часу настання ефекту зниження інтенсивності болю після прийому оригінального препарату мебеверину в хворих із СПК залежно від клінічного фенотипу
Диспепсичний синдром у вигляді метеоризму виявили в 58,3% обстежених хворих, при цьому групи хворих за формами СПК достовірно не відрізнялися на початку спостереження. В більшості пацієнтів спостерігалося зменшення метеоризму на 1-й день лікування оригінальним препаратом мебеверину – в 65,3% хворих; найзначиміша динаміка зниження встановлена в пацієнтів із варіантом СПК з діареєю із повним зникненням симптомів у 73,1% хворих після 2 місяців спостереження (табл. 3). Зменшення проявів діареї / закрепу на 1-й день лікування встановлено в 53,7% хворих із СПК, у 93,1% пацієнтів симптоми зменшилися протягом 1-го тижня лікування, при цьому в 96,2% пацієнтів 1-ї групи після 2 місяців лікування симптоми діареї були повністю відсутні.
|
Таблиця 3. Динаміка диспепсичного синдрому в пацієнтів із СПК на тлі лікування оригінальним препаратом мебеверину залежно від клінічного фенотипу |
|||
|
Параметр |
Група 1 – СПК із діареєю, n=26 |
Група 2 – СПК із закрепами, n=24 |
Група 3 – СПК змішаного варіанту, n=22 |
|
Зменшення проявів метеоризму на 1-й день лікування |
20* |
18 |
15 |
|
Зменшення проявів метеоризму на 7-й день лікування |
6 |
6 |
7 |
|
Зменшення проявів метеоризму на 14-й день лікування |
0 |
0 |
0 |
|
Зменшення проявів метеоризму на 28-й день лікування |
0 |
0 |
0 |
|
Метеоризм періодичний на 2-му місяці спостереження |
12 |
13 |
3 |
|
Повне зникнення симптомів метеоризму через 2 місяці спостереження |
19* |
12 |
14 |
|
Зменшення проявів діареї / закрепу на 1-й день |
12 |
15 |
11 |
|
Зменшення проявів діареї / закрепу на 7-й день |
12 |
9 |
8 |
|
Зменшення проявів діареї / закрепу на 14-й день |
2 |
2 |
3 |
|
Зменшення проявів діареї / закрепу на 28-й день |
0 |
0 |
0 |
|
Епізоди діареї / закрепу на 2-му місяці спостереження |
7 |
2 |
7 |
|
Повне зникнення епізодів діареї / закрепу через 2 місяці спостереження |
25* |
16 |
15 |
|
Примітка: * достовірність відмінностей (р<0,05). |
|||
На початку спостереження в 93,2% хворих із СПК установлено ознаки астенічного синдрому, при цьому в структурі симптомів переважало відчуття постійної слабкості – в 55,6% пацієнтів (рис. 4). У хворих 1-ї групи достовірно частіше спостерігалися симптоми постійної слабкості, надмірної стомлюваності та пригніченого настрою; водночас у пацієнтів 2-ї групи – достовірно частіше відчуття втрати інтересу до звичайної діяльності.
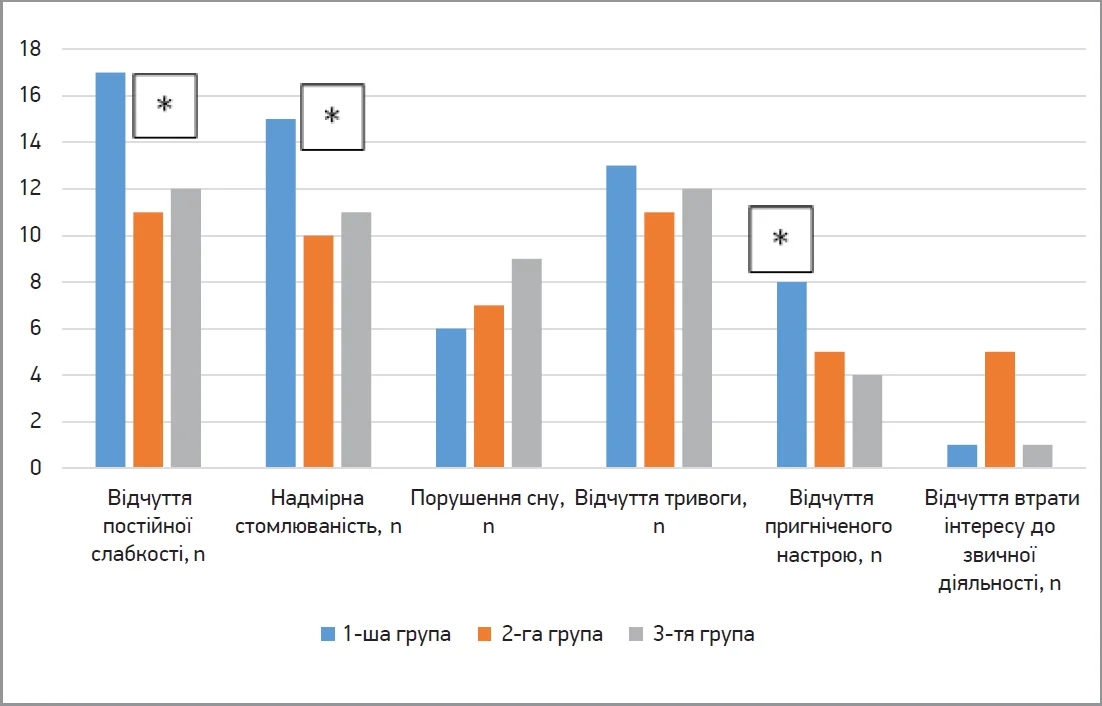
Рис. 4. Характеристика астенічного синдрому в пацієнтів із СПК залежно від клінічного фенотипу
|
Таблиця 4. Динаміка астенічного синдрому в пацієнтів із СПК на тлі лікування оригінальним препаратом мебеверину на 1-му місяці спостереження залежно від клінічного фенотипу |
||||||||||||
|
Параметр |
Група 1 – СПК із діареєю, n=26 |
Група 2 – СПК із закрепами, n=24 |
Група 3 – СПК змішаного варіанту, n=22 |
|||||||||
|
|
1-й день |
7-й |
14-й день |
28-й день |
1-й день |
7-й |
14-й день |
28-й день |
1-й день |
7-й |
14-й день |
28-й день |
|
Зменшення проявів слабкості |
4 |
8 |
7 |
2 |
4 |
6 |
7 |
0 |
3 |
10 |
4 |
0 |
|
Зменшення проявів втомлюваності |
5 |
11* |
7 |
4 |
5 |
8 |
6 |
0 |
0 |
13* |
6 |
0 |
|
Зменшення проявів порушення сну |
0 |
12 |
13 |
12 |
0 |
8 |
10 |
7 |
4 |
12 |
7 |
14* |
|
Зменшення проявів тривоги |
0 |
10* |
8 |
0 |
0 |
5 |
9 |
5 |
4 |
6 |
10 |
5 |
|
Зменшення проявів пригніченого настрою |
0 |
13 |
14 |
0 |
0 |
9 |
11 |
9 |
0 |
0 |
14 |
8* |
На тлі терапії оригінальним препаратом мебеверину встановлено зменшення проявів астенічного синдрому у 89,7% хворих із СПК переважно на 2-му тижні лікування із вираженішою динамікою серед хворих 1-ї групи (табл. 4). Отже, найбільша динаміка зниження на 1-му місяці лікування спостерігалася серед проявів втомлюваності, порушення сну та пригніченого настрою – на 56,7; 62,3 та 60,3% відповідно.
На 2-му місяці спостереження на тлі терапії оригінальним препаратом мебеверину в пацієнтів із СПК повне зникнення симптомів слабкості та втомлюваності спостерігалося в переважної більшості на рівні 53,4%. Слід зазначити, що хворі 1-ї групи мали достовірно кращу динаміку зниження проявів тривоги та пригніченого настрою. Повне зникнення симптомів слабкості та втомлюваності через 2 місяці спостереження встановлено в 71,6% пацієнтів із СПК (табл. 5). Зникнення симптомів тривожності та пригніченого настрою спостерігалося в 54,95% пацієнтів із СПК із діареєю, що достовірно частіше ніж у 2-й та 3-й групах (р<0,05).
|
Таблиця 5. Динаміка астенічного синдрому в пацієнтів із СПК на тлі лікування оригінальним препаратом мебеверину на 2-му місяці спостереження залежно від клінічного фенотипу |
|||
|
Параметр |
Група 1 – СПК |
Група 2 – СПК |
Група 3 – СПК змішаного варіанту, n=22 |
|
Слабкість періодично на 2-му місяці спостереження |
12 |
11 |
12 |
|
Повне зникнення симптомів слабкості через 2 місяці спостереження |
14 |
11 |
12 |
|
Епізоди втомлюваності на 2-му місяці спостереження |
11 |
10 |
9 |
|
Повне зникнення епізодів утомлюваності через 2 місяці спостереження |
15 |
10 |
13 |
|
Епізоди порушення сну на 2-му місяці спостереження |
12 |
12 |
14 |
|
Повне зникнення епізодів порушення сну через 2 місяці спостереження |
14 |
11 |
13 |
|
Епізоди тривоги на 2-му місяці спостереження |
12 |
11 |
13 |
|
Повне зникнення епізодів тривоги через 2 місяці спостереження |
14* |
8 |
8 |
|
Епізоди пригніченого настрою на 2-му місяці спостереження |
2* |
13 |
11 |
|
Повне зникнення епізодів пригніченого настрою через 2 місяці спостереження |
17* |
10 |
11 |
Під час аналізу показників ЯЖ за опитувальником SF‑36 у хворих із СПК залежно від клінічного фенотипу на початку спостереження встановлено достовірно нижчі показники, що характеризують СФ, психологічне здоров’я, РФФ серед пацієнтів 1-ї групи, – 46,2 та 47,7% відповідно (р<0,05) (табл. 6).
На тлі лікування із включенням оригінального препарату мебеверину через 2 місяці у хворих із СПК установлено достовірне поліпшення показників ЯЖ за опитувальником SF‑36, що характеризують ФФ, РФФ, загальне здоров’я та зниження інтенсивності болю у всіх групах пацієнтів, на 42,8%; 36,7%; 32,6% та 40,7% відповідно. Водночас у пацієнтів 1-ї групи встановлено достовірне поліпшення показників, що характеризують СФ, у хворих 2-ї та 3-ї груп – показників психологічного здоров’я.
При опитуванні хворих із СПК із діареєю за шкалою GSRS на початку спостереження встановлено достовірно вищі бали, що характеризують рефлюкс, – на 38,9%, діарею – на 30,8% та диспепсичний синдром – на 27,5%. Сумарний бал за опитувальником GSRS у хворих 1-ї групи був також достовірно вищим (на 28,3%) порівняно із 2-ю групою (р<0,05) (рис. 5).
На тлі лікування із включенням оригінального препарату мебеверину через 2 місяці у хворих із СПК установлено достовірне поліпшення показників за опитувальником GSRS, що характеризують больовий синдром, діарею, диспепсію, закреп на 28,7%; 35,1%; 34,9% та 32,7% відповідно, при цьому найзначиміша динаміка спостерігалася в пацієнтів 1-ї групи (рис. 6).
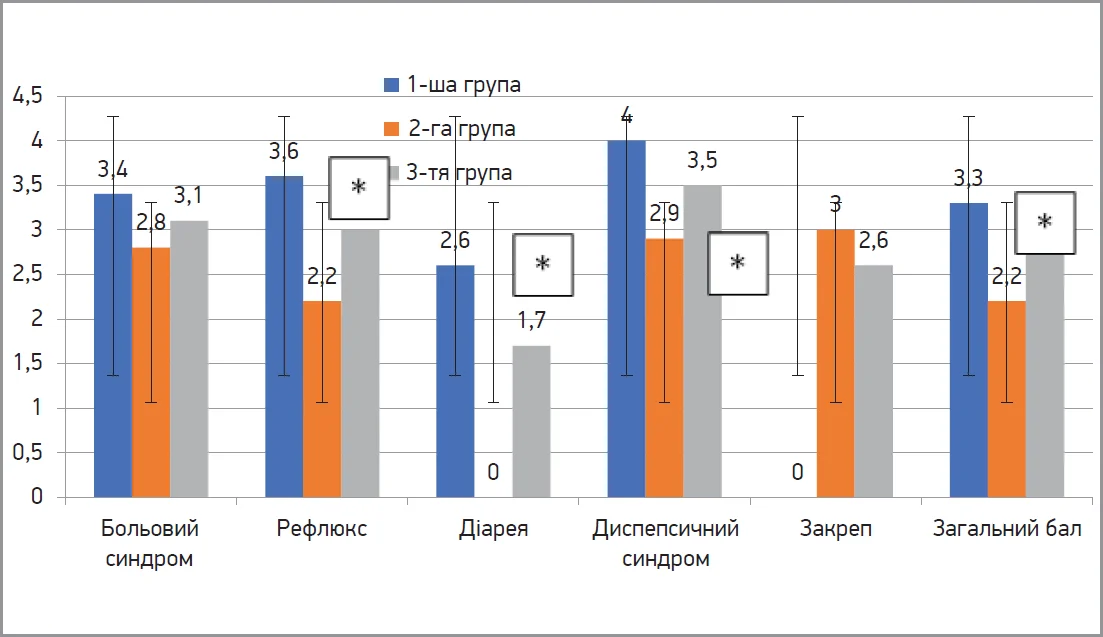 Рис. 5. Показники основних симптомів за опитувальником GSRS серед обстежених хворих із СПК на початку спостереження залежно від клінічного фенотипу
Рис. 5. Показники основних симптомів за опитувальником GSRS серед обстежених хворих із СПК на початку спостереження залежно від клінічного фенотипу
Примітка: * достовірність відмінностей між групами (р<0,05).
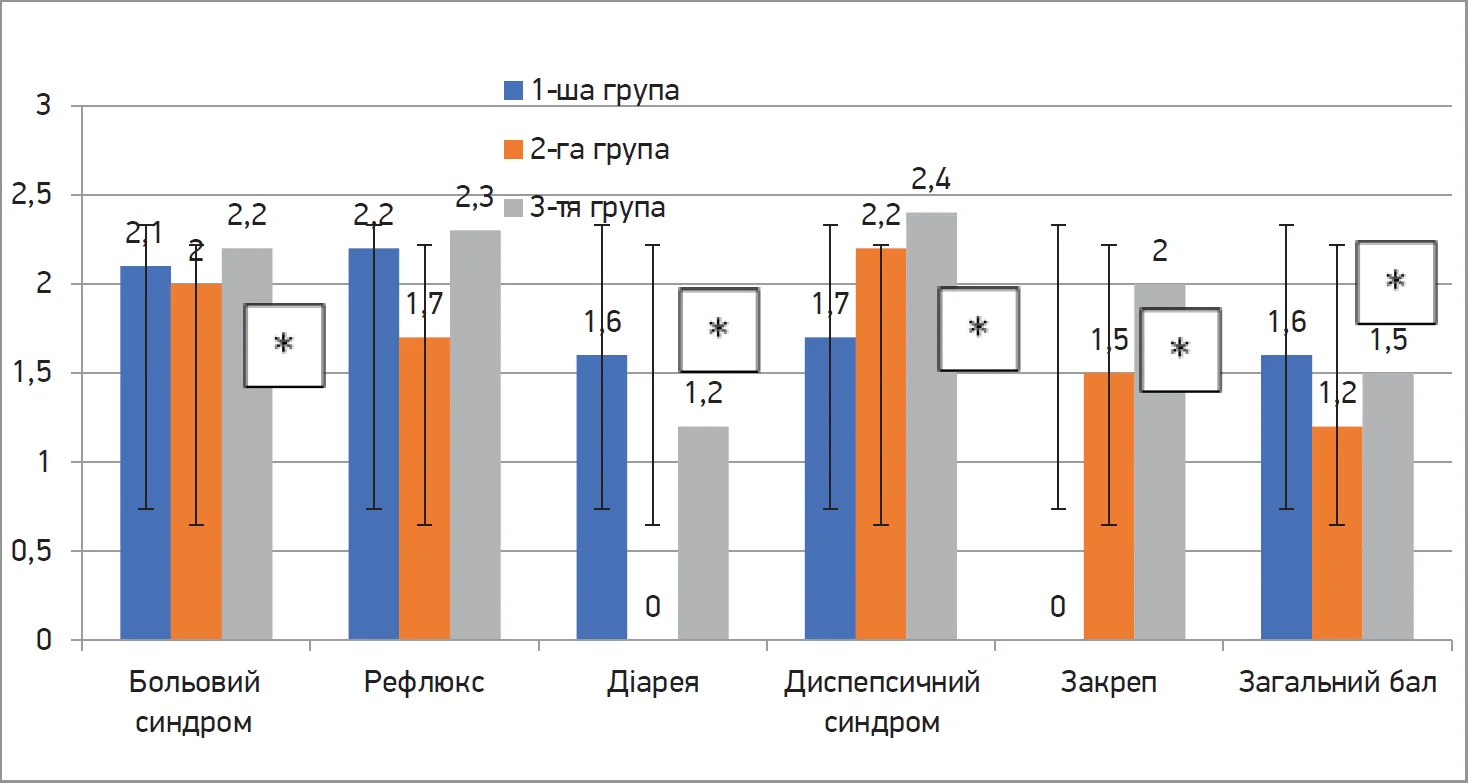
Рис. 6. Показники основних симптомів за опитувальником GSRS серед обстежених хворих із СПК наприкінці спостереження залежно від клінічного фенотипу
Примітка: * достовірність відмінностей між групами (р<0,05).
|
Таблиця 6. Динаміка показників ЯЖ за шкалами опитувальника SF‑36 у хворих із СПК на тлі лікування оригінальним препаратом мебеверину залежно від клінічного фенотипу |
||||||
|
Шкала опитувальника SF‑36 |
Група 1 – СПК із діареєю, n=26 |
Група 2 – СПК із закрепами, n=24 |
Група 3 – СПК змішаного варіанту, n=22 |
|||
|
|
на початку |
наприкінці |
на початку |
наприкінці |
на початку |
наприкінці |
|
Фізичне |
38 (32,3; 46,9) |
69,5* (41,6; 74,7) |
44,5 (36,7; 50,7) |
76 (55,8; 84,3)* |
38 (32,6; 49,4) |
69 (52,5; 78,3)* |
|
Рольове фізичне функціонування |
43 (33,9; 50,5) |
75* (62,6; 80,7) |
50 (39,8; 54,6) |
74 (48,7; 79,5)* |
39 (27,8; 46,8) |
72 (56,6; 77,8)* |
|
Інтенсивність болю |
71 (60,1; 76,7) |
29,5 (25,3; 34,4)* |
75 (63,6; 79,5) |
31,5 (28,3; 46,8)* |
71 (52,3; 78,3) |
30,5 (26,8; 42,4)* |
|
Загальне здоров’я |
38 (32,6; 44,7) |
78 (63,6; 86,3)* |
43 (32,5; 52,1) |
76 (45,4; 79,7)* |
36 (31,5; 40,6) |
78 (61,7; 78,8)* |
|
Життєздатність |
40,6 (36,2; 48,3) |
45 (38,6; 49,8) |
49 (35,6; 56,3) |
58 (42,8; 63,4) |
38 (21,3; 46,9) |
45 (31,6; 54,9) |
|
Соціальне |
38,3 (35,6; 54,9) |
62,4 (41,5; 74,8) * |
46,5 (34,4; 54,3) |
51,5 (38,8; 55,8) |
49,5 (31,6; 56,3) |
53,2 (38,5; 57,8) |
|
Рольове |
44,9 (32,7; 53,4) |
47 (35,2; 53,5) |
50 (40,8; 56,9) |
56,5 (44,6; 49,7) |
38 (32,7; 45,6) |
46 (34,7; 53,6) |
|
Психологічне здоров’я |
40,8 (34,3; 53,7) |
45,7 (32,9; 56,8) |
43 (37,9; 53,4) |
57 (52,6; 65,3)* |
38 (25,5; 46,7) |
62 (59,4; 72,0)* |
|
Примітка: * достовірність відмінностей (р<0,05). |
||||||
Отже, отримані результати демонструють, що терапія пацієнтів із включенням оригінального препарату мебеверину супроводжувалася достовірним зменшенням інтенсивності больового синдрому вже на 1-й день лікування з повним зникненням симптомів через 2 місяці незалежно від клінічного фенотипу СПК. Установлено достовірне поліпшення показників, що характеризують диспепсичний, астенічний синдроми та ЯЖ із найзначимішим результатом у пацієнтів із СПК із діареєю.
Висновки
- У пацієнтів із різними типами СПК на тлі комплексного лікування, яке включало оригінальний препарат мебеверину (Дуспаталін®), дієту відповідно до типу СПК, адсорбент діосмектит (у пацієнтів із діареєю) та лактулозу (у пацієнтів із закрепами), уже на 1-му тижні терапії спостерігали значне зменшення абдомінального болю, зменшення чи усунення закрепу чи діареї незалежно від типу СПК.
- Значне зменшення або зникнення болю та спазму в кишечнику спостерігали через 15 хвилин після прийому оригінального препарату мебеверину (Дуспаталін®).
- На тлі комплексного лікування встановлено достовірне зменшення частоти або зникнення абдомінального болю і диспепсичних скарг за опитувальниками SF‑16 та GSRS (p<0,05).
- Оригінальний препарат мебеверину (Дуспаталін®) продемонстрував сприятливий профіль безпеки під час лікування СПК упродовж 8 тижнів.
- Застосування оригінального препарату мебеверину (Дуспаталін®) може сприяти покращенню ЯЖ пацієнтів із СПК, зменшенню астенічного синдрому, тривоги та депресії.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 20 (582), 2024 р



 Коваленко О. Ю.
Коваленко О. Ю.
