30 листопада, 2023
Патогенетично-орієнтована терапія функціональних гастроінтестинальних розладів
 Функціональні гастроінтестинальні розлади (ФГІР) – група захворювань, які характеризуються хронічними симптомами з боку травного тракту (біль у животі, дисфагія, диспепсія, діарея, запор, здуття живота) за відсутності патологічних змін у результатах додаткових досліджень. Історично ФГІР вважали станами без жодного органічного підґрунтя, але покращення розуміння їхнього патогенезу дозволило з’ясувати, що в основі лежать зміни міжорганної комунікаційної осі «мозок – кишечник». У чинній класифікації (IV Римські критерії) ФГІР розподілено на 33 хвороби дорослих та 20 педіатричних; найпоширеніші з них – синдром подразненого кишечнику (СПК) і функціональна диспепсія (ФД) (Fikree A., Byrne P., 2021).
Функціональні гастроінтестинальні розлади (ФГІР) – група захворювань, які характеризуються хронічними симптомами з боку травного тракту (біль у животі, дисфагія, диспепсія, діарея, запор, здуття живота) за відсутності патологічних змін у результатах додаткових досліджень. Історично ФГІР вважали станами без жодного органічного підґрунтя, але покращення розуміння їхнього патогенезу дозволило з’ясувати, що в основі лежать зміни міжорганної комунікаційної осі «мозок – кишечник». У чинній класифікації (IV Римські критерії) ФГІР розподілено на 33 хвороби дорослих та 20 педіатричних; найпоширеніші з них – синдром подразненого кишечнику (СПК) і функціональна диспепсія (ФД) (Fikree A., Byrne P., 2021).
Світова поширеність ФГІР – у межах 40%; на частку цих хвороб припадає ≈12% робочого навантаження сімейного лікаря та 30% – навантаження амбулаторного гастроентеролога (Jones M. P. et al., 2007; Shivaji U. N., Ford A. C., 2014). ФГІР часто асоціюються із хронічним болем та іншими функціональними синдромами, наприклад синдромом хронічної втоми; у ⅔ пацієнтів розвиваються психопатологічні стани, в т. ч. тривожність та депресія (Petersen M. W. et al., 2020). За даними B. Spigel і співавт. (2009), якість життя осіб із ФГІР є гіршою, ніж хворих із серцевою недостатністю ІІІ ступеня чи ревматоїдним артритом.
Основними ланками патогенезу ФГІР є зміни моторної функції травної системи (як сповільнення, так і пришвидшення), вісцеральна гіперчутливість, зміни мікробіоти, підвищена проникність стінки кишечнику та зміни обробки сенсорних сигналів від травного тракту центральною нервовою системою (Black C. J. et al., 2020).
Підхід до діагностики ФГІР має передбачати ретельний збір анамнезу з особливим акцентом на червоних прапорцях – ознаках потенційно небезпечних патологічних станів. До цих ознак належать схуднення, сімейний анамнез ракових пухлин, виникнення симптомів у нічний час, розвиток анемії та наявність гастроінтестинальних кровотеч. Огляд хворого із ФГІР має передбачати пальпацію з метою виявлення новоутворень у абдомінальній ділянці та оцінки больового синдрому, а також ректальне пальцеве обстеження (Fikree A., Byrne P., 2021).
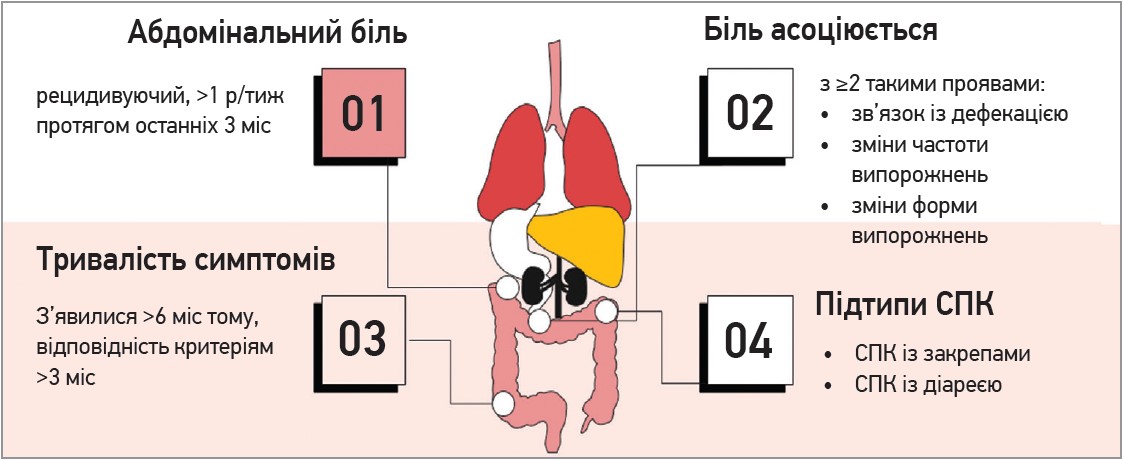
Діагностичні критерії одного з найпоширеніших ФГІР (СПК) представлено на рисунку. Під час діагностики СПК слід диференціювати з колоректальним раком, раком яєчників, мальабсорбцією жовчних солей, мікроскопічним колітом, целіакією, хворобою Крона. СПК також необхідно диференціювати з іншими ФГІР, зокрема ФД, функціональними біліарними розладами, функціональним запором, діареєю та здуттям живота. Разом з тим часто два або більше ФГІР можуть спостерігатися в одного пацієнта.
Рис. Діагностичні критерії СПК
Специфічні валідовані біомаркери СПК дотепер відсутні, продовжують вивчатися перспективні кандидати, включаючи антивінкулінові антитіла для постінфекційного варіанта СПК (Vasapolli R. et al., 2021). Всім пацієнтам із ФГІР необхідно зробити загальний аналіз крові (як скринінг анемії), визначити рівень С‑реактивного білка, сечовини та електролітів, пройти серологічні тести на визначення целіакії, здійснити оцінку функції щитоподібної залози, отримати дані щодо рівня фекального кальпротектину (за наявності діареї), а також встановити статус інфікування H. pylori (за наявності антигенів у калі чи за допомогою 13C‑сечовинного дихального тесту). Якщо в пацієнта спостерігаються типові симптоми СПК на тлі нормального рівня фекального кальпротектину, а симптоми червоних прапорців відсутні, ендоскопічне обстеження нижніх відділів травної системи не потрібно. Аналогічно, за негативного аналізу на H. pylori та в разі відсутності симптомів тривоги не проводиться ендоскопія верхніх відділів. Для скринінгу різних причин болю в животі доцільним може бути проведення ультразвукового обстеження (Fikree A., Byrne P., 2021).
Якщо встановлено діагноз ФГІР, важливо пояснити пацієнту, чим характеризується такий стан. Задля уникнення неправильних очікувань варто повідомити хворому, що повністю усунути симптоми навряд чи вийде, але збільшити контроль над ними абсолютно можливо. В разі ФГІР важливо скоригувати психосоціальні фактори, як-от харчування, вживання кофеїну, алкоголю та медикаментів, рівень фізичної активності, сон, рівень стресу, тривожність тощо (Fikree A., Byrne P., 2021).
Фармакотерапія ФГІР передбачає дві основні стратегії: патогенетичне лікування (наприклад, прийом нейромодуляторів із метою усунення вісцеральної гіперчутливості) та симптоматична терапія. Остання ґрунтується на домінувальних симптомах і зазвичай містить декілька ліній рекомендованих засобів. Так, першою лінією усунення абдомінального болю вже протягом декількох декад є спазмолітичні препарати з антихолінергічним механізмом дії та кальцієві блокатори зі спазмолітичним впливом. Ці препарати є відносно безпечними, але антихолінергічні засоби можуть зумовлювати специфічні побічні ефекти: закрепи, сухість у роті, розлади зору та затримку сечі (Fikree A., Byrne P., 2021; Colomier E. et al., 2020). Якщо призначений спазмолітик не забезпечив очікуваного результату, варто спробувати інший препарат цієї групи. Друга лінія представлена нейромодуляторами: антидепресантами (трициклічні антидепресанти та селективні інгібітори зворотного захоплення серотоніну) і габапентиноїдами (прегабалін, габапентин).
При СПК із проносами першою лінією є лоперамід, другою – ондансетрон, третьою – рифаксимін та елюксадолін; за варіанта із закрепами препарати першої лінії – осмотичні проносні засоби (поліетиленгліколь та лактулоза), другої – прукалоприд, третьої – ліки секретагогічної дії (лінаклотид, лубіпростон). На жаль, останні три препарати в Україні практично не доступні.
Відповідно до британських рекомендацій з лікування СПК (Irritable bowel syndrome in adults, Quality standard, NICE, 2016), алгоритм ведення пацієнтів із таким станом на первинній ланці медичної допомоги є досить простим. Важливе значення мають довірливі стосунки із хворим і надання рекомендацій щодо харчування та способу життя. Харчування пацієнта має бути регулярним і здоровим зі зменшенням вживання кофеїну, алкоголю, пряної / жирної їжі, збільшенням вживання розчинної клітковини (харчових волокон). Допомогти зменшити симптоматику може також дієта з низьким вмістом ферментованих оліго-, ди-, моносахаридів і поліолів (т. зв. дієта з обмеженням FODMAPs). Дієти з елімінацією певних продуктів і безглютенові дієти не рекомендовані, за виключенням випадків целіакії або встановленої харчової алергії. При СПК доцільно підвищити рівень та поліпшити регулярність фізичної активності. Що стосується фармакотерапії, то стартове лікування за наявності болю передбачає спазмолітики чи олію м’яти перцевої, у разі запору – проносні засоби, при діареї – лоперамід. При невдалому застосуванні препаратів першої лінії на рівні первинної медичної допомоги хворого рекомендують скеровувати до гастроентеролога (Vasant D. H. et al., 2021).
У випадку ФД призначаються інгібітори протонової помпи та ерадикаційна терапія, а в разі невдалого лікування – Н2-гістаміноблокатори і прокінетики. Третю лінію складають нейромодулятори (трициклічні антидепресанти, анксіолітики) (Fikree A., Byrne P., 2021).
Римські критерії IV перегляду виокремлюють такий ФГІР, як функціональне здуття та розтягнення живота (ФЗРЖ). ФЗРЖ характеризується суб’єктивними симптомами, як-от відчуття переповнення живота, тиск (розпирання) в черевній порожнині, відчуття роздування живота, що рецидивують. Ці симптоми можуть також свідчити про органічні захворювання, які слід своєчасно диференціювати від ФЗРЖ. До таких захворювань належать, зокрема, целіакія, непереносимість лактози, фруктози та інших вуглеводів, зовнішньосекреторна недостатність підшлункової залози, гастропарез, цукровий діабет, гіпотиреоз, склеродермія, синдром надмірного бактеріального росту в тонкому кишечнику, гострий гастроентерит, злоякісні пухлини шлунка, кишечнику та яєчників, асцит. У діагностичному процесі головне – виключити нефункціональні причини, а також з’ясувати наявність / відсутність симптомів тривоги. Пацієнтів із помірним ФЗРЖ слід переконати, що цей стан є доброякісним і не пов’язаний із життєзагрозливими хворобами.
Лікування ФЗРЖ передбачає різнопланову симптоматичну терапію залежно від домінуючих симптомів. Знизити інтенсивність болю та дискомфорту допомагають спазмолітики, а надмірне газоутворення, здуття і розтягнення живота дієво усуває симетикон. У низки інших засобів, як-от активоване вугілля, іберогаст і солі магнію, доказова база відсутня (Mari A. et al., 2019).
Отже, вагоме місце в лікуванні ФГІР посідає спазмолітична терапія. Із цією метою може застосовуватися Ентероспазміл Н – комбінована дієтична добавка, до складу якої входять селективний спазмолітик флороглюцинол (75 мг) та антифлатулент симетикон (130 мг), що впливають на два основні механізми появи симптомів – спазм гладеньких м’язів і надмірне газоутворення в кишечнику.
Варто зауважити, що комбіновані засоби дозволяють зменшити сумарну кількість препаратів для прийому, а це надзвичайно важливо для формування стійкої прихильності до лікування – ключового аспекту терапії хронічних хвороб, особливо схожих на ФГІР, тобто тих, при яких не так часто спостерігаються тривалі ремісії із повним зникненням симптомів.
Флороглюцинол – похідне фенолу з неспецифічним спазмолітичним ефектом, що діє безпосередньо на гладенькі м’язи. Флороглюцинол спричиняє релаксацію цих м’язів за рахунок пригнічення активності іонних кальцієвих каналів (Bueno L. et al., 1997; Lazaraki G. et al., 2014), через що не має вищезазначених антихолінергічних побічних ефектів, які асоціюються із застосуванням деяких інших підкласів спазмолітиків (Ford A. C. et al., 2008; Ruepert L. et al., 2011). Важливо, що флороглюцинол діє лише на спазмовані м’язи, водночас не впливаючи на м’язи у фізіологічному стані (Corvino A. et al., 2022). За допомогою проведення багатоцентрового відкритого рандомізованого порівняльного дослідження ІІІ фази виявлено, що застосування флороглюцинолу протягом 5-7 днів ефективно усуває біль та спазми, асоційовані з нирковою або жовчною колькою. За своєю ефективністю флороглюцинол не поступався декскетопрофену (у випадку ниркової кольки) та метамізолу і спазмолітику скополамінового ряду (за біліарної кольки) (Corvino A. et al., 2022).
У дослідженні S. Y. Shin і співавт. (2020) взяли участь пацієнти із СПК із діареєю, яких рандомізували до груп флороглюцинолу та плацебо. Прийом препарату тривав 2 тиж, після чого за учасниками спостерігали впродовж додаткового 1 тиж. Через 3 тиж помірне чи значне покращення стану достовірно частіше спостерігалося в групі флороглюцинолу, ніж у групі плацебо (61,6 проти 30,6%); частота побічних ефектів була однаковою. Флороглюцинол також сприяв покращенню якості життя: в пролікованих цим засобом пацієнтів наявність СПК стала менше перешкоджати щоденній активності, стурбованість власним станом здоров’я знизилася. Хворі також стали менше уникати певних продуктів, які були тригерами діареї. На думку авторів, флороглюцинол є безпечним і дієвим методом усунення симптомів СПК. Інше дослідження флороглюцинолу як препарату для лікування СПК показало, що застосування цього засобу в дозі 50 мг 3 р/добу протягом 2 міс достовірно зменшувало інтенсивність абдомінального болю, частоту випорожнень, відчуття потреби в негайній дефекації, виділення слизу з каловими масами, відчуття неповної дефекації та здуття живота (Jafri W. et al., 2006). Спостереження останніх років свідчать, що флороглюцинолу притаманні також антиоксидантні, антиапоптотичні, антибактерійні, протизапальні, протиалергійні, антитромботичні властивості (Park C. et al., 2023; Khan F. et al., 2022; Clara B. et al., 2020; Blanchard C. et al., 2018). Така плейотропна дія може стати додатковим обґрунтуванням для призначення флороглюцинолу.
Другий компонент Ентероспазмілу Н – симетикон – зменшує інтенсивність і частоту виникнення здуття живота та відчуття його розтягнення (Mari A. et al., 2019). Симетикон – інертна речовина силіконового походження, яка протидіє піноутворенню, зменшуючи здуття, біль і дискомфорт у животі за рахунок запобігання утворенню оточених слизом закритих газових «кишень» у травному тракті (Ebadi M., 2011). Симетикон уперше було схвалено Управлінням з контролю за якістю продуктів харчування та лікарських засобів США (FDA) у 1952 р. (Burta O. et al., 2018). Механізм дії симетикону полягає у несистемному сурфактантному впливі, за рахунок якого препарат зменшує поверхневий натяг бульбашок газу в травному тракті. Внаслідок зменшення поверхневого натягу бульбашки зливаються й утворюють великі пухирі газу, які легко відригуються або відходять через анальний отвір. Симетикон не впливає на вироблення газу в кишечнику, а лише сприяє полегшенню відходження вже утворених газів (Voepel-Lewis T.D. et al., 1998). Він також діє як топічний бар’єр, захищаючи слизову оболонку травної системи від таких подразників, як шлункова кислота, жовчні солі та фармакопрепарати (наприклад, ацетилсаліцилова кислота) (Meier R., Steuerwald M., 2007). Через відсутність системної абсорбції симетикону притаманний відмінний профіль безпеки: препарат дозволений для вживання вагітним і жінкам, які годують груддю (Drugs and Lactation Database, 2017; Hagemann T. M., 1998). Для досягнення потужного стійкого ефекту симетикон доцільно призначати не одноразово, а декілька днів регулярно за графіком (Ingold C. J., Akhondi H., 2023).
Різні автори вивчали застосування симетикону в лікуванні гелікобактерної інфекції, дитячих кольок та асоційованих із високими фізичними навантаженнями гастроінтестинальних симптомів у професійних спортсменів (Ingold C. J., Akhondi H., 2023). Метааналіз М. А. Martínez-Vázquez і співавт. (2012) показав, що додавання симетикону до спазмолітиків збільшує загальну ефективність лікування СПК.
Результати особисто проведеного порівняльного з мебеверином пілотного дослідження за участю пацієнтів із ФГІР демонструють, що Ентероспазміл Н є ефективним і безпечним при лікуванні функціонального біліарного болю та СПК, діагностованих за IV Римськими критеріями. Пацієнти, які відповідали критеріям включення у дослідження, повідомляли про наявність та динаміку симптомів ФГІР, заповнюючи спеціальний опитувальник для вивчення важкості функціональних проявів перед включенням у спостереження, на 7-й, 14-й, 21-й та 30-й день за бальною системою. Оцінка інтенсивності проявів ФГІР (біль, здуття тощо) проводилася за наведеною в таблиці градацією.
|
Таблиця. Оцінка інтенсивності проявів ФГІР |
|
• Максимальна важкість симптомів відповідає 500 балам |
|
• Легкі прояви ФГІР – від 75 до 175 балів |
|
• Прояви ФГІР середньої тяжкості – від 175 до 300 балів |
|
• Тяжкі прояви – 300-500 балів |
|
• Показник <75 балів відповідає ремісії ФГІР або групі контролю в порівняльних дослідженнях |
Через 1 міс лікування в усіх пацієнтів, котрі отримували Ентероспазміл Н, спостерігалася виразна позитивна динаміка симптомів ФГІР. Здуття живота достовірно послабилося в абсолютної більшості (83%) хворих. Натомість мебеверин продемонстрував зменшення здуття живота лише в половини хворих, які його приймали. Ремісії ФГІР вдалося досягти третині осіб, які протягом одного місяця отримували Ентероспазміл Н. Натомість ремісії не досяг жоден пацієнт, який протягом 30 днів приймав мебеверин. Ентероспазміл Н отримав дуже схвальні відгуки, наприклад, від пацієнта Н., 21 р.: «Мене повністю перестав турбувати біль, здуття було не сильне, але повністю зникло»; пацієнтка К., 29 р.: «Живіт болить значно менше, за винятком критичних днів; помітила погіршення, коли пропустила прийом».
Отже, через збільшення кількості та потужності психоемоційних стресів у наш час проблема ФГІР набуває усе більшої актуальності, а наявний потенціал лікування цих станів дотепер використовується не всіма спеціалістами. У веденні хворих із ФГІР ключове значення мають виявлення і корекція фонових психоемоційних станів, виключення «червоних прапорців» як ймовірних ознак органічних захворювань. На початку взаємодії з пацієнтом необхідно встановити довірчі відносини, аргументовано заспокоїти хворого, переконавши його в доброякісності патологічного стану, але водночас пояснити, що повне вилікування ФГІР може бути проблематичним, однак цілком реально досягти контролю над симптомами. Провідною стратегією лікування є комбінування оптимізації дієти із симптоматичною терапією, яку слід обирати на основі скарг пацієнта, що домінують. Застосування Ентероспазмілу Н – комплексної дієтичної добавки, яка містить спазмолітик флороглюцинол та антифлатулент симетикон, дозволяє ефективно і безпечно усунути симптоми ФГІР, досягти ремісії, покращити якість життя цих пацієнтів.
Подвійна дія Ентероспазмілу Н надає можливість за допомогою одного засобу усунути два провідні симптоми ФГІР: абдомінальний біль та відчуття переповнення, розтягнення чи здуття живота, що виникає за рахунок надмірного газоутворення. Обидва складники Ентероспазмілу Н добре вивчені в клінічних дослідженнях, а також мають прогнозований профіль ефективності та безпеки. Отриманий клінічний досвід застосування Ентероспазмілу Н у пілотному дослідженні демонструє хороші перспективи у досягненні ремісії ФГІР. Тому планується більш детальне вивчення цього питання у більшої кількості пацієнтів.
Медична газета «Здоров’я України 21 сторіччя» № 19/1 (556), 2023 р