5 березня, 2021
Рекомендації з ведення пацієнтів із хронічною ішемією нижніх кінцівок
Групою експертів Асоціації ангіологів та судинних хірургів України проведено адаптацію Глобальних рекомендацій щодо лікування хронічної ішемії, що загрожує кінцівкам (GLOBAL)1 та Рекомендацій щодо захворювань периферичних артерій Європейського товариства судинної медицини (ESVM)2.
Останні структуровані у вигляді таблиць з обов’язковим наведенням ступеня та рівня доказовості положень рекомендацій. Після положень рекомендацій надано додаткові матеріали (класифікації, алгоритми обстеження та лікування пацієнтів) та роз’яснення. Дані рекомендації можуть бути використані широким загалом медичних фахівців, у повсякденній практиці яких зустрічаються пацієнти із захворюваннями периферичних артерій.
Ключові слова: хронічна ішемія нижніх кінцівок, критична ішемія нижніх кінцівок, захворювання периферичних артерій, цукровий діабет, виразка стопи, ендоваскулярне втручання, аортокоронарне шунтування, практичний посібник, доказова медицина.
CFA – загальна стегнова артерія (ЗСА)
DFA – глибока стегнова артерія (ГСА)
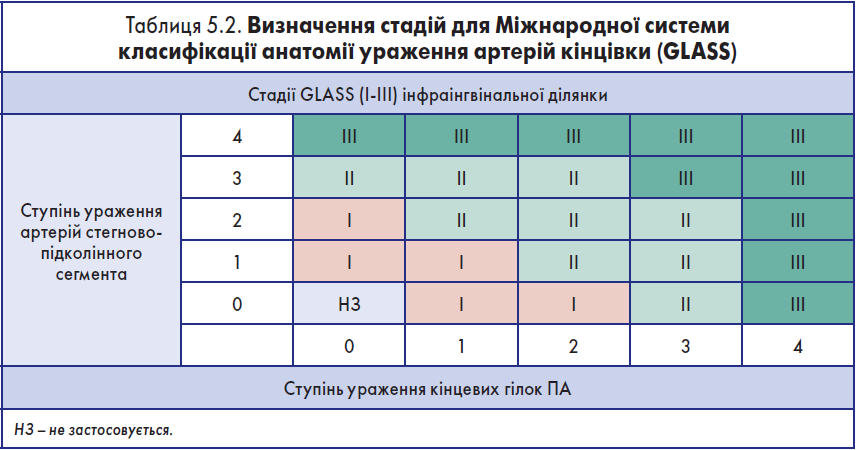
GLASS – Міжнародна система класифікації анатомії уражень артерій кінцівок
GRADE – Система класифікації, оцінки, розробки та експертизи рекомендацій
IDEAL – Ідея, розвиток, оцінка і довгострокові дослідження
IDSA – Американське товариство фахівців інфекційних хвороб
PaСО2 – парціальний тиск вуглекислого газу в артеріальній крові
PEDIS – перфузія, площа, глибина, інфекція і чутливість
Pop – підколінна артерія
PVR – плетизмографія
SFA – поверхнева стегнова артерія (ПСА)
SVS – Товариство судинних хірургів
TASC – Трансатлантичний консенсус
TcPO2 – транскутанна оксиметрія
WIfI – класифікація оцінки рани, ішемії та інфекції стопи
АВК – ампутація з виокремлення коліна
АК – аортоклубовий
ВПВ – велика підшкірна вена
ГБО – гіпербарична оксигенація
ГСА – глибока стегнова артерія
ДУС – дуплексне ультразвукове сканування
ЗПА – захворювання периферичних судин
ЗСА – загальна стегнова артерія
КГПА – кінцеві гілки підколінної артерії
КЖОСЗ – якість життя, зумовлена станом здоров’я
КІНК – критична ішемія нижніх кінцівок
КПІ – кісточково-плечовий індекс
КТ – тиск на рівні кісточки
КТА – комп’ютерна томографічна ангіографія
МРА – магнітно-резонансна ангіографія
МР-ангіографія – магнітно-резонансна ангіографія
НКА – надколінна ампутація
НОР – науково обґрунтована реваскуляризація
ОПЕ – об’єктивні показники ефективності
ПАТТ – подвійна антитромбоцитарна терапія
ПВВ – периферичне [ендо-]васкулярне втручання
ПВГА – передня великогомілкова артерія
ПК – прохідність кінцівок
ПКА – підколінна ампутація
ППІ – пальце-плечовий індекс
ППК – переміжна пневматична компресія
ПРСП – показники результативності, що повідомляються пацієнтами
ПС – поперекова симпатектомія
ПС – підколінний сегмент
ПСА – поверхнева стегнова артерія
ПСШК – пікова систолічна швидкість кровотоку
ПТ – тиск на рівні пальця;
РКД – рандомізовані контрольовані дослідження
СДС – синдром діабетичної стопи
СНССЯ – серйозні небажані серцево-судинні явища
ССЗР – синдром системної запальної реакції
ССМ – стимуляція спинного мозку
ТМ – трансметатарзальний
ТСХ – Товариство судинних хірургів
УСПС – ураження стегно-підколінного сегмента
ХІНК – хронічна ішемія нижніх кінцівок
ХТО – хронічна тотальна оклюзія
ЦД – цукровий діабет
ЦСА – цифрова субтракційна ангіографія
ШДЦА – шлях доступу до цільової артерії
Анотація
Хронічна ішемія нижніх кінцівок (ХІНК) може бути пов’язана з підвищеним ризиком виникнення гострих ішемічних подій як із боку нижніх кінцівок із подальшою необхідністю великої ампутації, так і з погіршенням якості життя хворого через судинні катастрофи в інших артеріальних басейнах (серце, головний мозок, нирки, артерії кишечника) із високим рівнем летальності. Рекомендації базуються на даних Світових рекомендацій із ведення пацієнтів із судинними захворюваннями (Global Vascular Guidelines), що сфокусовані на визначенні, оцінці й тактиці ведення пацієнтів із ХІНК із метою поліпшення їх науково обґрунтованого лікування. Термін «ХІНК» має ширше значення порівняно з терміном «критична ішемія кінцівок», оскільки останній передбачає порогові значення порушеної перфузії, а не їх діапазон. ХІНК – це клінічний синдром, який визначається наявністю захворювання периферичних артерій (ЗПА) у поєднанні з болем, що виникає у стані спокою, гангреною або виразкою нижніх кінцівок, які не загоюються впродовж більш ніж 2 тижнів. Венозна, травматична, емболічна й неатеросклеротична етіології виразок виключаються. Всі пацієнти з підозрою на ХІНК мають бути якнайшвидше направлені до фахівця із судинних захворювань. Важливим аспектом є оцінка ризику втрати кінцівки пацієнтом за допомогою класифікації WIfI (система класифікації Товариства судинних хірургів, що заснована на оцінці рани, ішемії та інфекції стопи). Для верифікації діагнозу ХІНК необхідне проведення об’єктивних гемодинамічних досліджень, включаючи визначення кісточково-плечового індексу у якості первинного методу діагностики. Науково обґрунтована реваскуляризація (НОР) визначається трьома незалежними факторами: ризик для пацієнта, тяжкість ураження кінцівки й анатомічна складність. Пацієнти середнього та високогоризику визначаються на підставі смертності під час процедури та дворічної смертності, що викликана будь-якими причинами.
Міжнародні рекомендації з ведення пацієнтів із судинними захворюваннями пропонують застосовувати нову Міжнародну систему – анатомічну класифікацію ураження артерій кінцівки (GLASS), яка включає визначення кращого шляху доступу до цільової артерії (ШДЦА), оцінку прохідності артерій нижніх кінцівок, на основі чого втручання поділяються за трьома ступенями складності. Оптимальна стратегія реваскуляризації також визначається наявністю аутовени для відкритого шунтування. Рекомендації для НОР засновані на найбільш достовірних наявних наукових даних, доказах першого рівня з поточних досліджень. Шунтування може бути рекомендоване у пацієнтів середнього ризику з вираженою загрозою кінцівки та високою складністю ураження, натомість як у пацієнтів із менш складною анатомією, середнім ризиком втрати кінцівки і групи високого ризику перевагу слід віддавати ендоваскулярним методикам. Усім пацієнтам із ХІНК має бути забезпечена найкраща, науково обгрунтована медикаментозна терапія, що включає антитромботичні, гіполіпідемічні, антигіпертензивні препарати, водночас слід рекомендувати відмову від куріння, дієту, фізичні вправи й профілактичний догляд за ногами. Дотримуючись НОР, рекомендується довгострокове спостереження за пацієнтами. Ефективність методів непрямої реваскуляризації (спінальна стимуляція, пневматична компресія, простаноїди, гіпербарична оксигенація) на теперішній час не було встановлено. Методи клітинної та генної терапії для лікування ХІНК мають бути обмежені для використання до проведення рандомізованих клінічних досліджень. Міжнародні рекомендації з ведення пацієнтів із судинними захворюваннями сприяють, у тому числі, стандартизації дизайнів і кінцевих точок, що застосовуються у клінічних дослідженнях у пацієнтів із ХІНК. Важливість наявності багатопрофільних бригад та центрів, що мають передовий досвід для запобігання ампутації, розглядається як ключове серед сучасних завдань системи охорони здоров’я.
Критична ішемія нижніх кінцівок
У 1982 році робоча група судинних хірургів визначила критичну ішемію нижніх кінцівок (КІНК) як ішемічний біль у стані спокою з тиском на рівні кісточки (КТ) <40 мм рт. ст. або некрозом тканини з КТ <60 мм рт. ст. у пацієнтів без цукрового діабету (ЦД). Пацієнти з ЦД були навмисно виключені з даного визначення через симптоми нейропатії та підвищену сприйнятливість до інфекцій, які ускладнюють інтерпретацію. Це визначення довго було предметом суперечок, оскільки воно не охоплювало велику групу пацієнтів, які потрапили до групи ризику ампутації з більш широкого діапазону видів ішемії. Щоб вирішити цю проблему, за останні п’ять десятиліть було розроблено та опубліковано безліч найрізноманітніших систем класифікації ішемії нижніх кінцівок і ран/синдрому діабетичної стопи (СДС), багато з яких залишаються актуальними й сьогодні. Ці та інші найбільш поширені класифікації та їхні відповідні компоненти й ступені тяжкості представлені у табл. 1. Серед судинних хірургів загальноприйнятими є класифікації Фонтейна і Резерфорда, а ортопеди, хірурги стопи, фахівці в галузі СДС традиційно застосовують систему класифікації Вагнера та класифікацію, розроблену в Техаському університеті. Хоча кожна із цих систем має свої переваги, використання великої кількості різних систем класифікації заважає розробці оптимальних алгоритмів лікування. Крім того, таке розмаїття класифікацій призвело до відсутності єдиного підходу до лікування пацієнтів із СДС, а також пацієнтів без ЦД по всьому спектру ХІНК.
Визначення, представлені в табл. 1, були розроблені переважно для опису пацієнтів із «чистою» ішемією, викликаною атеросклерозом. Це пояснюється тим, що в той час переважаючим фактором ризику розвитку захворювання було куріння, і глобальної епідемії ЦД ще не було. Таким чином, у цьому визначенні переважну загрозу для кінцівки становила саме ішемія. Однак, оскільки сьогодні пацієнти із ЦД складають більшість усіх пацієнтів із ХІНК, необхідно враховувати абсолютні параметри порушення перфузії за наявності нейропатії, характеристики виразки та наявність інфекції.
Консервативне лікування
ХІНК – це кінцева стадія прояву системного атеросклерозу. Вона часто супроводжується серцево-судинними захворюваннями, що призводить до надзвичайно високої смертності через інсульт та інфаркт міокарда. Якщо вчасно не виявити і не впливати на фактори ризику та супутні захворювання, то прогнози щодо ХІНК зазвичай невтішні: рівень смертності протягом 1 року після встановлення діагнозу становить від 20 до 26%. У дослідженні за участю 574 пацієнтів із ХІНК, яким не було проведено реваскуляризацію через 2 роки, 31,6% пацієнтів померли переважно від серцево-судинних захворювань, а 23% осіб було необхідне проведення великої ампутації.
Основне консервативне лікування полягає у моніторингу та управлінні факторами серцево-судинних ризиків, які призводять до атеротромбозу. Це включає регулярні фізичні навантаження, зниження ваги у пацієнтів із надмірною вагою, відмову від нікотину для курців, вживання антитромбоцитарних препаратів, а також лікування артеріальної гіпертензії, дисліпідемії та ЦД.
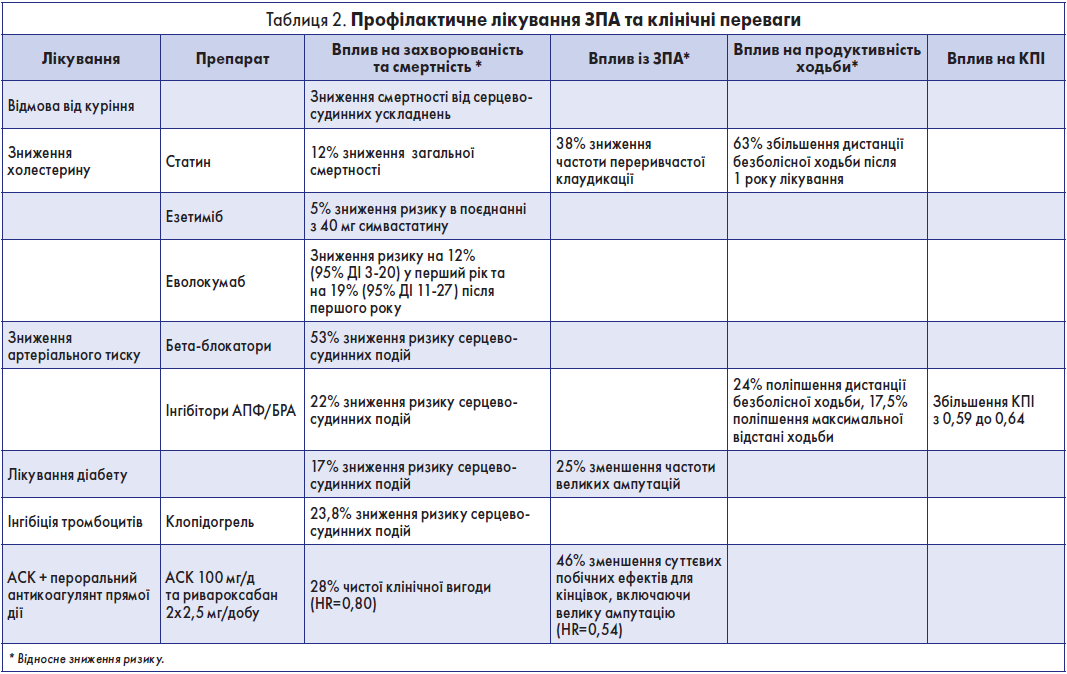
Цілі лікування ЗПА полягають у зниженні ризику майбутніх серцево-судинних подій (ЗПА усіх стадій за класифікацією Фонтейна) для поліпшення параметрів ходіння, мобільності та якості життя у хворих із ЗПА II стадії за класифікацією Фонтейна, а також збереження кінцівок, зменшення болю та покращення/підтримки рівня якості життя у хворих із ЗПА III та IV стадій за класифікацією Фонтейна (табл. 2).
Таким чином мета лікування пацієнтів із ХІНК полягає не тільки у збереженні функціональної кінцівки, а й у зниженні серцево-судинної захворюваності та смертності, що може бути досягнуто завдяки інтенсивній модифікації факторів ризику і застосуванню ефективного лікування. У той час як деякі фактори ризику, такі як вік і стать, модифікувати не представляється можливим, можна вплинути на інші фактори, такі як гіперліпідемія, гіпертензія, діабет, куріння і малорухливий спосіб життя.
Антитромбоцитарна терапія
Наполегливо рекомендується призначати антитромбоцитарні препарати всім пацієнтам із симптомами ЗПА для зниження ризику розвитку серйозних небажаних серцево-судинних явищ (СНССЯ). Робоча група дослідників антитромбоцитарних препаратів провела метааналіз досліджень антитромбоцитарних препаратів, виконаних до 1997 року. Він налічував 135 тис. пацієнтів із цереброваскулярними захворюваннями, ішемічною хворобою серця або ЗПА (ПК), які отримували лікування антитромбоцитарними препаратами, і 77 тис. пацієнтів у контрольній групі. У групі антитромбоцитарної терапії спостерігалося зниження СНССЯ на 22% і було показано, що прийом 75-150 мг АСК на день так само ефективний, як і прийом більш високих доз препарату, але при цьому знижується ризик виникнення кровотечі. У більш пізньому метааналізі вивчалася специфічна перевага АСК у 16 дослідженнях вторинної профілактики за участю 17 тис. паціентів. Результати досліджень підтвердили перевагу антитромбоцитарних препаратів: й у чоловіків, й у жінок частота СНССЯ знизилася на 18,2%. Дослідницька група профілактики критичної ішемії нижніх кінцівок (CLIPS) порівняла перевагу прийому 100 мг АСК на день із прийомом плацебо у 185 пацієнтів із симптомами ЗПА і КПІ <0,85 або ППІ <0,6; за результатами дослідження повідомлялося про зниження ризику судинних подій на 64% порівняно із 24% зниження ризику у групі плацебо.
Однак у літературі з’являється дедалі більше доказів того, що альтернативні АСК препарати, такі як тиклопідин, дипіридамол і клопідогрель, можуть бути більш ефективними. У дослідженні клопідогрелю проти АСК у пацієнтів із ризиком ішемічних подій (CAPRIE), незважаючи на те що воно не було спеціально сплановано для пацієнтів із ХІНК, порівняли застосування 75 мг клопідогрелю на день і 325 мг АСК на день у пацієнтів із ЗПА. Дослідники відзначили зниження виникнення СНССЯ на 8,7% у групі пацієнтів, які отримували клопідогрель, порівняно із групою пацієнтів, які приймали АСК. Значної різниці в ризику кровотечі між двома препаратами не спостерігалося.
Було також показано, що інші антитромбоцитарні препарати, такі як тікагрелор і ворапаксар, знижують СНССЯ у пацієнтів із ЗПА. Однак переваг цих препаратів перед клопідогрелем не було показано. У дослідженні застосування тікагрелору при захворюванні периферичних артерій (EUCLID) за участю 13 885 пацієнтів із симптомами ЗПА і КПІ ≤0,8 його порівняли із клопідогрелем. Хоча обидва препарати мають схожий профіль безпеки, перевага тікагрелору по відношенню до клопідогрелю не була доведена. У рамках дослідження з оцінки дії ворапаксару для профілактики інсультів та інфарктів у пацієнтів з атеросклерозом – тромболізис при інфаркті міокарда 50 (TRA 2°P-TIMI 50) досліджували дію ворапаксару, антагоніста рецептора 1, який активується протеазами, на вторинну профілактику ішемічних подій у пацієнтів зі стабільним перебігом атеросклерозу, у т.ч. симптомним ЗПА. Гостра ішемія нижніх кінцівок, заздалегідь задана кінцева точка дослідження, скоротилася на 41% у групі пацієнтів із ЗПА. Однак застосування ворапаксару пов’язувалося зі збільшенням частоти внутрішньочерепних крововиливів у пацієнтів, які перенесли інсульт або транзиторну ішемічну атаку. У рамках метааналізу прийом ворапаксару разом із АСК не показав великого впливу на зниження СНССЯ у пацієнтів з атеросклерозом і пов’язувався із незначним збільшенням числа внутрішньочерепних крововиливів.
Нарешті, за результатами метааналізу, в якому порівнювалася дія тікагрелору, тиклопідину, АСК, цилостазолу, пікотаміду, ворапаксару і клопідогрелю в якості монотерапії або у складі подвійної антитромбоцитарної терапії (ПАТТ) у пацієнтів із ЗПА, було виявлено, що монотерапія клопідогрелем має кращий профіль безпеки та ефективності (зниження СНССЯ).
Тривала ПАТТ або системна антикоагулянтна терапія з прийомом антагоністів вітаміну К не показана при ЗПА.
Антикоагулянти
З точки зору периферичних артерій, немає показань для повнодозової терапії пероральними антикоагулянтами за допомогою антагоністів вітаміну К у пацієнтів із ЗПА за відсутності гострих емболічних подій. Тим не менше було досліджено ефект низькодозової антитромботичної терапії з використанням перорального антикоагулянту в комбінації з АСК.
У результаті проведення багатоцентрового рандомізованого дослідження стратегій антитромботичної терапії (COMPASS) за участю 7470 пацієнтів зі стабільним ЗПА від легкого до помірного ступеня тяжкості було доведено, що комбінація ривароксабану у дозі 2,5 мг 2 рази на добу з АСК знижує ризики серцево-судинної смерті, інфаркту міокарда, інсульту та серйозних небажаних ішемічних подій із боку кінцівки порівняно із застосуванням тільки АСК. У дослідження включали пацієнтів, яким раніше було проведено реваскуляризацію на артеріях нижньої кінцівки, ампутацію, а також пацієнтів із ПК і показником КПІ <0,9, встановленим стенозом периферичних артерій >50% або стенозом сонної артерії >50%. Загалом, у 8,5% досліджуваних пацієнтів КПІ становив <0,7. У цій популяції відзначалося значне зниження ризиків розвитку великої ампутації, гострої та хронічної ішемії нижніх кінцівок порівняно з пацієнтами, які приймали тільки АСК. Комбінація препаратів була пов’язана з невеликим збільшенням частоти клінічно значущих кровотеч, проте ризики найбільш загрозливих типів кровотеч (фатальні, ВЧК, кровотеча у критичний орган) були зіставними у групах порівняння.
У дослідженні VOYAGER порівнювалося застосування ривароксабану в комбінації з АСК із монотерапією АСК у пацієнтів із ЗПА, яким було проведено реваскуляризацію. У дослідження було включено 6564 пацієнтів із симптомним ЗПА нижніх кінцівок, яким було проведено реваскуляризацію із приводу «переміжної» кульгавості (77% пацієнтів) та хронічної загрозливої ішемії кінцівки (23%). Пацієнти включалися в дослідження з 1-го по 10-й день після успішно проведеної процедури і досягнення гемостазу, спостереження тривало 30 міс. У 65% пацієнтів проводилася ендоваскулярна реваскуляризація (включаючи гібридну), у 35% – хірургічна. Близько 50% пацієнтів на момент рандомізації приймали клопідогрель, переважна більшість з яких приймала його протягом 1 міс. Пацієнти, які потребували тривалого прийому клопідогрелю (більше 6 міс) на момент рандомізації, у випробування не включалися.
Аналіз дослідження показав, що терапія ривароксабаном 2,5 мг 2 рази на добу разом із АСК 100 мг 1 раз на добу асоційована з достовірно нижчим ризиком сукупності подій гострої ішемії кінцівок, великої ампутації за судинними показаннями, інфаркту міокарда, ішемічного інсульту та смерті, спричиненої серцево-судинною патологією, на 15% порівняно з монотерапією АСК. У групі пацієнтів, у яких застосовували вазопротекторну дозу ривароксабану 2,5 мг 2 рази на добу разом із АСК 100 мг, ризик гострої ішемії кінцівок був нижчим на 33%, ризик незапланованих повторних реваскуляризацій – на 12%, ризик госпіталізацій унаслідок коронарних або периферичних тромботичних подій – на 22%.
Між групами не відзначалося статистично значущих відмінностей за частотою кровотеч зі смертельними наслідками, внутрішньочерепних крововиливів або кровотеч у життєво важливі органи. Слід зазначити, що показник абсолютної клінічної користі постійно збільшувався з часом протягом усього періоду дослідження, що тривало 30 міс. Безпека та відношення користь/ризик при застосуванні ривароксабану 2,5 мг 2 рази на добу разом із АСК 100 мг залишилися стабільними, незважаючи на супутній прийом клопідогрелю або його відсутність.
Використання комбінації ривароксабану у вазопротекторній дозі 2,5 мг два рази на добу разом із АСК 100 мг на добу суттєво покращує прогноз лікування пацієнтів із ЗПА щодо ішемічних подій із кінцівками та серцево-судинних подій. Саме тому доцільно розглянути тривале призначення такої схеми у всіх пацієнтів із ЗПА після проведення реваскуляризації з метою зменшення ризиків як серцево-судинних подій, так і рецидиву ішемії кінцівки, що може потребувати повторної реваскуляризації.
Інші засоби
Немає доказів того, що лікування вазоактивними препаратами ефективно покращує ефективність ходьби при переміжній кульгавості, а отже, вони не показані.
Систематичний огляд порівняння цилостазолу, нафтидрофурилу і пентоксифіліну при переміжній кульгавості проаналізовано загалом у 26 РКД та визначено, що нафтидрофурил є найбільш ефективним засобом. Пентоксифілін виявився найменш ефективним у плані покращення максимальної та безболісної дистанції ходьби. Максимальну відстань ходьби було збільшено на 60% (95% довірчий інтервал [ДІ] 20-114), 25% (95% ДІ 11-40) та 11% (95% ДІ 1-24) при застосуванні нафтидрофурилу, цилостазолу та пентоксифіліну відповідно, а дистанцію безболісної ходьби було збільшено на 49, 13 та 9% відповідно.
Статини можуть бути корисними для поліпшення відстані ходьби, але дослідження невеликі й, як уже зазначалося, потребують додаткового обґрунтування.
Простаноїди, пентоксифілін, L-аргінін, буфломедил та гінкго білоба не мають достатніх доказів для застосування у клінічній практиці у пацієнтів із переміжною кульгавістю. Те саме стосується ізоволемічної гемодилюції та інших альтернативних засобів лікування.
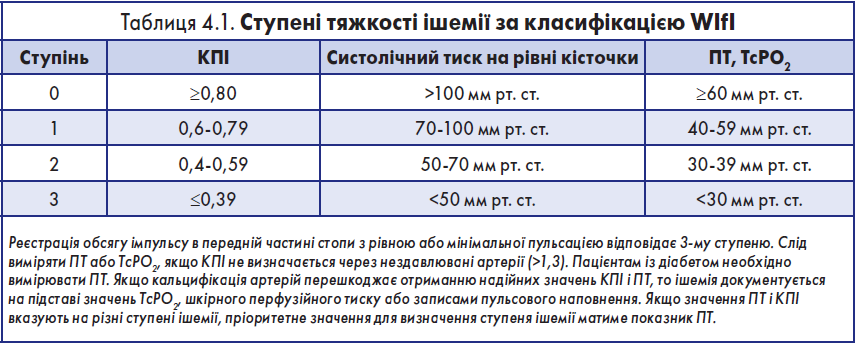
КПІ – кісточково-плечовий індекс; КТ – тиск на рівні кісточки; ППІ – пальце-плечовий індекс; TcPО2 – транскутанна оксиметрія; ПТ – тиск на рівні пальця.
Взято з Hirsch A.T., Haskal Z.J., Hertzer N.R., Bakal C.W., Creager M.A., Halperin J.L. et al. ACC/AHA 2005 Practice Guidelines for the management of patients with peripheral arterial disease (lower extremity, renal, mesenteric, and abdominal aortic): a collaborative report from the American Association for Vascular Surgery/Society for Vascular Surgery, Society for Cardiovascular Angiography and Interventions, Society for Vascular Medicine and Biology, Society of Interventional Radiology, and the ACC/AHA Task Force on Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Peripheral Arterial Disease): endorsed by the American Association of Cardiovascular and Pulmonary Rehabilitation; National Heart, Lung, and Blood Institute; Society for Vascular Nursing; TransAtlantic Inter-Society Consensus; and Vascular Disease Foundation. (Практичні рекомендації щодо ведення пацієнтів із захворюванням периферичних артерій (артерії нижніх кінцівок, нирок, брижові артерії і черевна аорта): спільний звіт Американської асоціації судинних хірургів / Товариства судинних хірургів, Товариства серцево-судинної ангіографії і втручань, Товариства судинної медицини і біології, Товариства інтервенційної радіології та Цільової групи ACC/AHA з розробки практичних посібників (Комітет з написання рекомендацій щодо ведення пацієнтів із захворюванням периферичних артерій): затверджено Американською асоціацією серцево-судинної і легеневої реабілітації; Національним інститутом серця, легень і крові; Товариством з ведення пацієнтів із захворюваннями судин; Трансатлантичним консенсусом; і Фондом із судинних захворювань.)
Міжнародна система класифікації анатомії уражень артерій кінцівок (GLASS)
Обґрунтування. Точна оцінка загрози втрати кінцівки і стратифікація анатомічної моделі захворювання покладено в основу НОР. Це стосується не лише звичайної медичної практики, а й клінічних результатів, оцінок і досліджень. Автори пропонують нову, клінічно орієнтовану концепцію класифікації моделей ураження артерій у пацієнтів із ХІНК. Система класифікації GLASS базується на принциповому уникненні застосування існуючих підходів класифікації ЗПА і є більш прихильною до аналогу системи SYNTAX, розробленої для оцінки ішемічної хвороби серця.
Існуючі на даний момент системи класифікації анатомії уражень ЗПА або описують локалізацію і ступінь тяжкості окремих уражень артерій, або дають кількісну оцінку тяжкості й характеру захворювання. Системи класифікації, засновані на описі ураження або сегмента, корисні для порівняння ефективності ендоваскулярних пристроїв у чітко визначених клінічних ситуаціях. Однак такі системи не допоможуть у визначенні стратегій НОР для лікування пацієнтів із ХІНК, особливо з огляду на складні, багаторівневі моделі захворювань та дедалі більшу кількість периферичних моделей захворювань, які спостерігаються в сучасній клінічній практиці.
Успішна реваскуляризація при ХІНК, особливо у пацієнтів із некрозом тканини, майже завжди вимагає відновлення пульсуючого кровотоку до стопи. Оскільки окремі схеми класифікації, засновані на типі ураження, погано співвідносяться з ефективною реваскуляризацією при ХІНК, фахівці із судинних захворювань повинні інтегрувати підходи щодо сегментів артерій у тактику лікування, що зачіпає сегменти всієї кінцівки. Фактори, що визначають успішний анатомічний результат, значно відрізняються для шунтування та ендоваскулярного втручання. Для проведення шунтування необхідний належний приплив і відтік крові й, вірогідно, найголовніше – відповідна аутовена. Порівняно із цим успіх ендоваскулярного втручання переважно визначається виразністю атеросклерозу в передбачуваному шляху доступу до цільової артерії (ШДЦА), який забезпечить кровотік до стопи. Якщо у ШДЦА виявляється безліч вогнищ уражень, то технічний успіх і стабільна прохідність судин кінцівки в цілому оцінюються як функція кожного відновленого ураження.
Система GLASS ґрунтується на визначенні ШДЦА у кожного пацієнта шляхом візуалізації високої якості і потребує обрання кращої зони підколінної артерії та її гілки. ШДЦА зазвичай вибирають з урахуванням найменш ураженої артерії стегна, через яку здійснюється приплив крові до стопи. ШДЦА також можна вибрати на підставі інших відповідних факторів, таких як ангіосомальна концепція або уникнення судини, на якій раніше вже проводилися втручання. Оскільки відношення між моделлю ураження, спричиненого оклюзією, прохідністю при обраному методі втручання та клінічним успіхом лікування ХІНК досить складні, використання узагальненої системи класифікації анатомії уражень, такої як GLASS, допомагає встановити цей взаємозв’язок. Бажаний ШДЦА для ендоваскулярного втручання і бажана цільова артерія для шунтування не завжди збігаються; таким чином, клінічне рішення має бути засноване на порівняльній оцінці ризику й успіху обох методик. Як і SYNTAX, система GLASS розроблена передусім з урахуванням можливого результату ендоваскулярного втручання. Тому в систему було включено такі фактори, як якість венозного шунта або відтік крові з дистальних відділів, що більше стосується шунтування.
Відносно кальцинозу судин у GLASS прийнята дихотомна шкала суб’єктивної оцінки, за якою тяжкий ступінь кальцинозу (наприклад, >50% по колу, дифузні, масивні бляшки або ураження за типом «коралового рифу») підвищується в одному сегменті на один рівень. Це є суб’єктивним визначенням, яке зробив лікар про те, що ступінь кальцинозу технічно ускладнює ендоваскулярне втручання (й очікуваний показник технічної неефективності). Були запропоновані альтернативні підходи для оцінки ступеня кальцинозу артерій при ЗПА, але вони більш складні й жоден із запропонованих підходів не був валідований з урахуванням відмінностей у клінічних результатах. Що стосується уражень артерій стопи, то в системі GLASS прийнято трирівневу класифікацію уражень для опису стану артерій, які перетинають кісточку (у т.ч. термінальні гілки малогомілкової артерії) та дугу стопи. На даний момент система класифікації уражень артерій стопи для первинної оцінки стану кінцівки в системі GLASS не розглядається, враховуючи те, що відсутні переконливі докази того, як така оцінка впливає на результати лікування. Однак цю класифікацію рекомендовано застосовувати в подальших дослідженнях, щоб краще визначати, яким чином включити ураження, пов’язане з відтоком крові від стопи, до системи класифікації анатомії уражень при ХІНК.
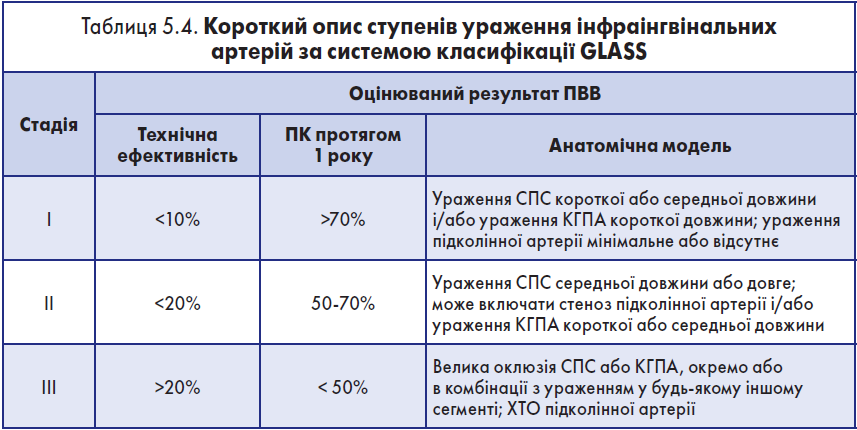
Після вибору ШДЦА ступені ураження стегново-підколінного сегмента та кінцевих гілок підколінної артерії визначаються на підставі ангіограм високої якості. Комбінація ступеня ураження стегново-підколінного сегмента та кінцевих гілок підколінної артерії, визначає загальний ступінь ураження за класифікацією GLASS від I до III ступеня, яка пов’язана з технічною складністю реваскуляризації (низька, середня, висока).
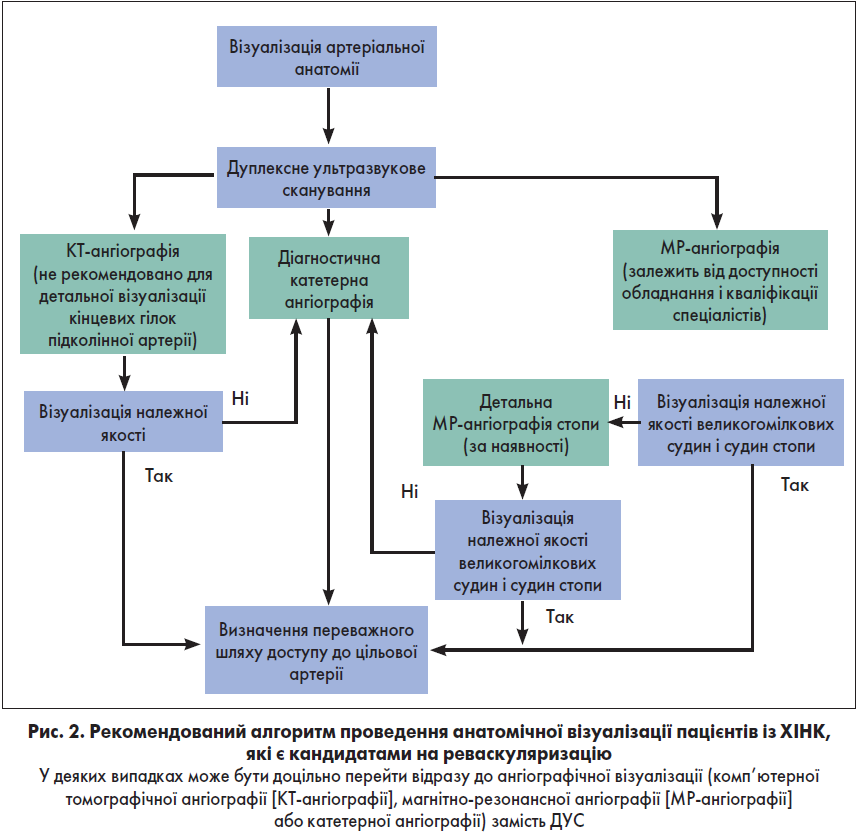
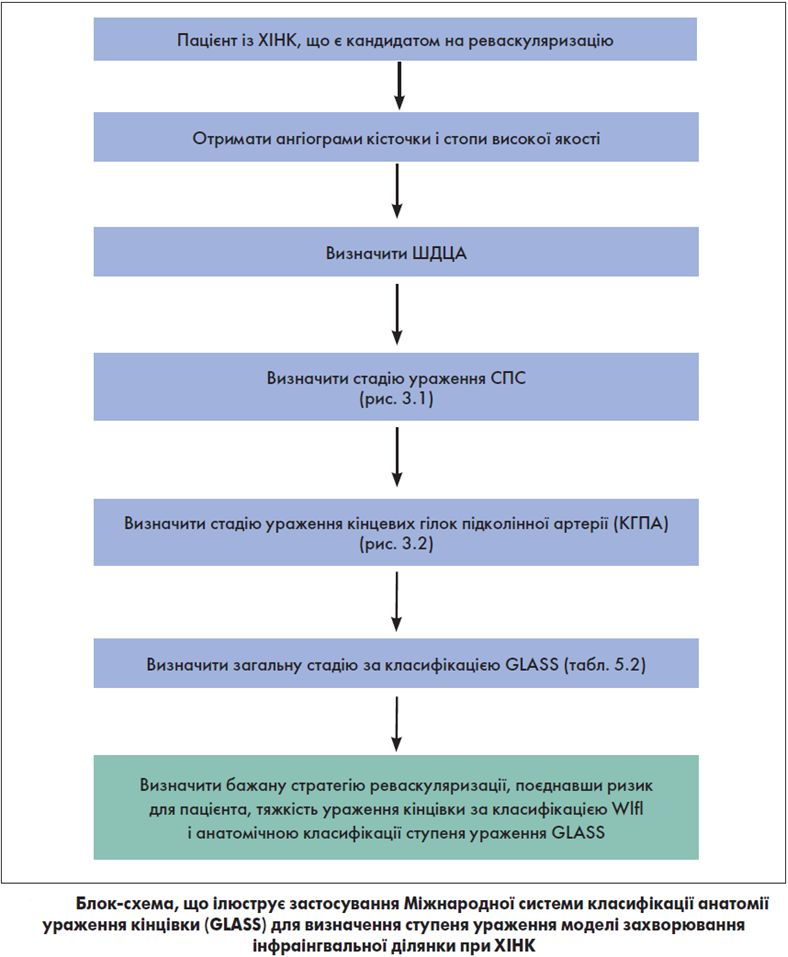
Лікування ХІНК із використанням системи GLASS. Використання системи GLASS включає в себе виконання наступних кроків (див. блок-схему):
- Отримання ангіограм кісточки і стопи високої якості.
- Визначення ШДЦА.
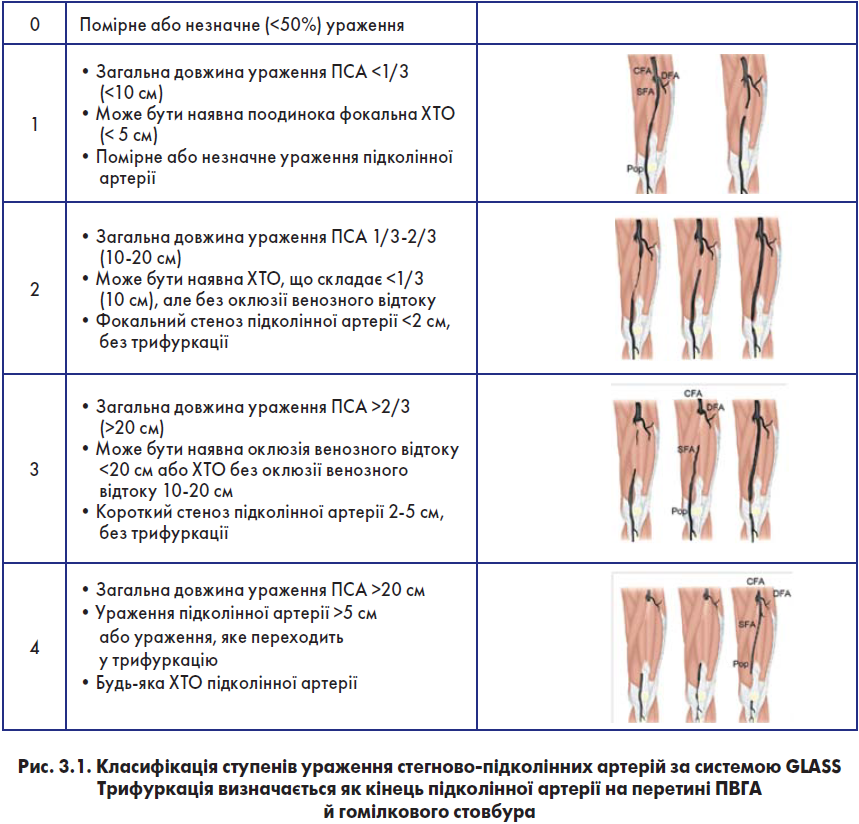
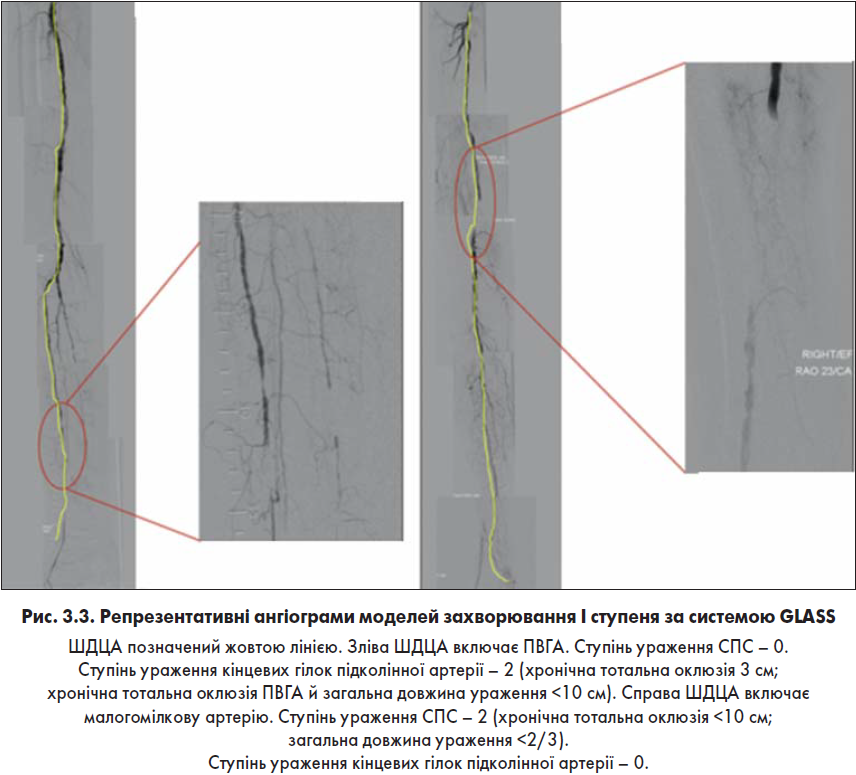
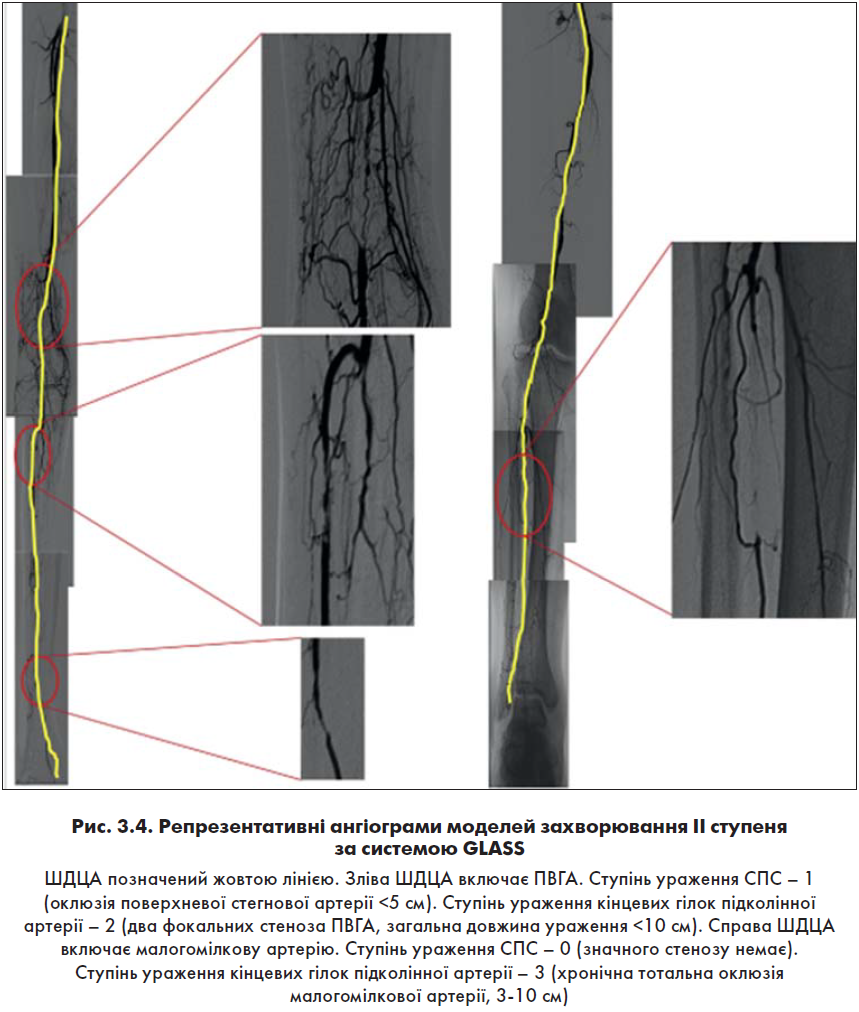
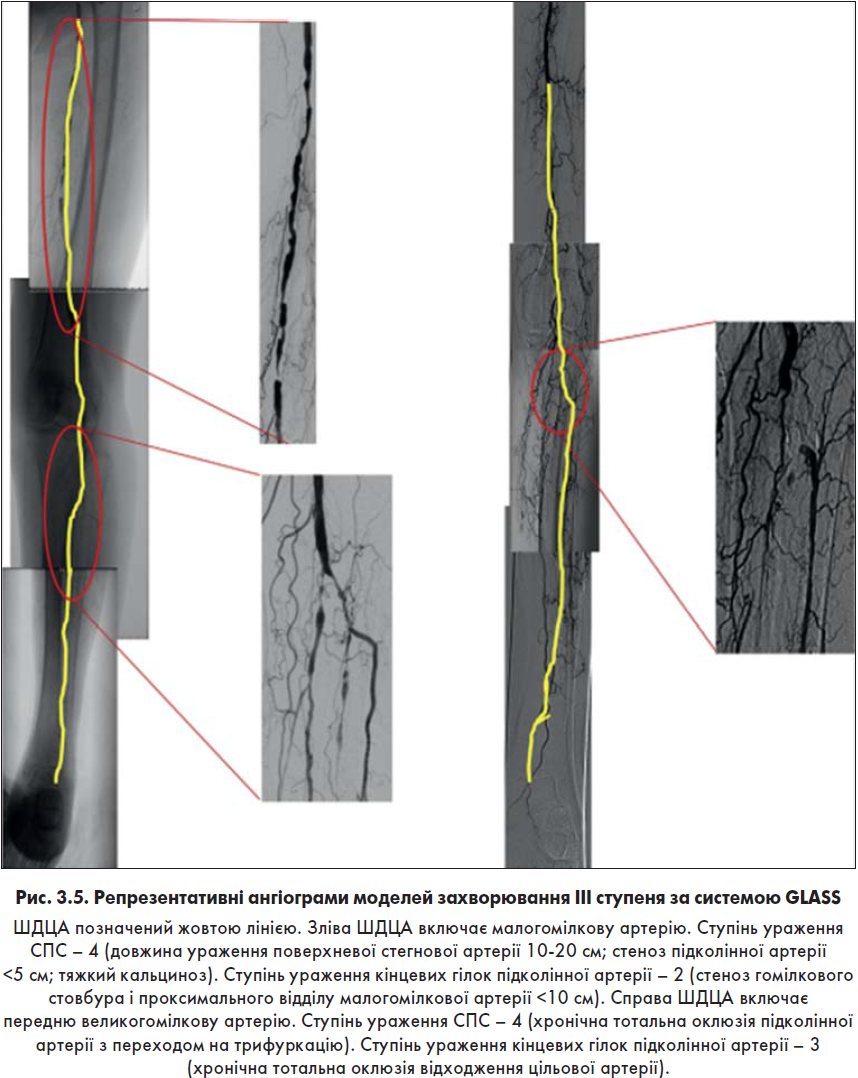
- Визначення ступеня ураження артерій стегново-підколінного сегмента за системою GLASS (0-4, рис. 3.1).
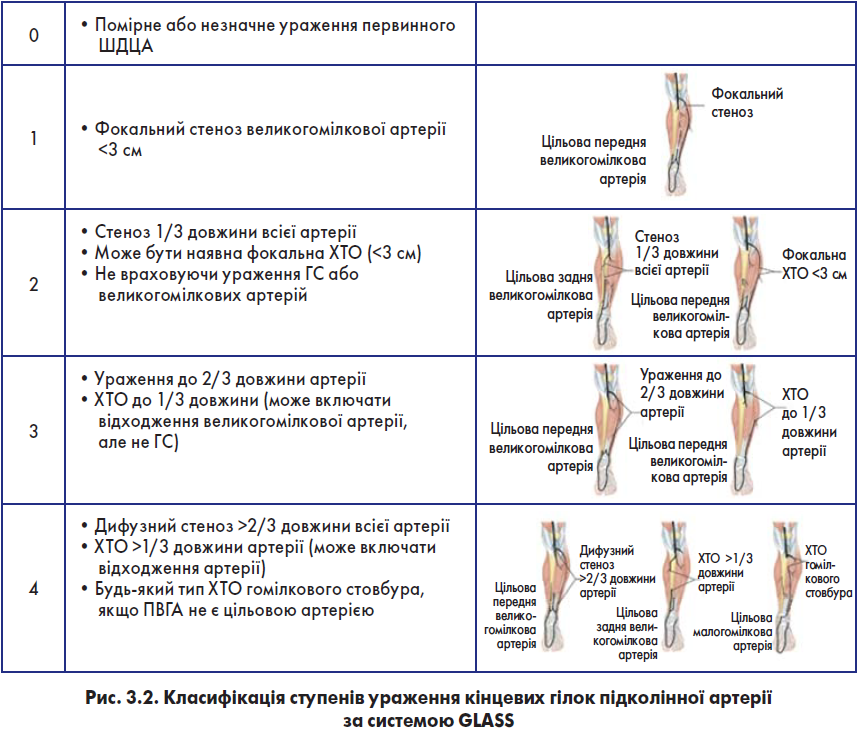
- Визначення ступеня ураження кінцевих гілок підколінної артерії за системою GLASS (0-4, рис. 3.2).
- Визначення наявності вираженого кальцинозу (наприклад, >50% по колу, дифузні, масивні бляшки або ураження за типом «коралового рифу», швидше за все, негативно вплинуть на результат ендоваскулярного втручання) у стегново-підколінному сегменті та кінцевих гілках підколінної артерії обраного ШДЦА. Якщо кальциноз присутній, збільшити ступінь ураження сегмента на одиницю.
- Об’єднати ступені стегново-підколінного сегменту і сегменту кінцевих гілок підколінної артерії, щоб визначити загальний ступінь GLASS (табл. 5.2).
- Використовувати модифікатор артерій стопи (P0, P1 або P2) для опису стану артерій нижче кісточки.
Для окремого пацієнта із ХІНК стратегія НОР ґрунтується на повній інтеграції наступних аспектів:
- оцінюваний ризик для пацієнта і довгострокова виживаність;
- ступінь загрози втрати кінцівки (наприклад, за класифікацією WIfI);
- анатомічна модель і тяжкість ураження кінцівки (наприклад, за системою GLASS).
За редакцією д. мед. н. П.І. Нікульнікова, д. мед. н. І.М. Ґудза, д. мед. н. Ю.Г. Орла, к. мед. н. А.В. Ратушнюка
Список літератури знаходиться в редакції.