5 травня, 2022
Пронтосан – новий підхід до лікування хронічних ран
Ефективне лікування ран, що важко загоюються, є важливою хірургічною проблемою. Недостатня увага до них або невчасне застосування консервативного лікування може викликати серйозні ускладнення, усунення яких, зрештою, потребує радикальних хірургічних методів. Представляємо огляд літератури щодо ефективності та безпечності застосування місцевого антисептика полігексаніду та поверхнево-активної речовини бетаїну для лікування хронічних ран.
Ключові слова: хронічна рана, синдром діабетичної стопи, трофічна виразка, антисептик, полігексанід, бетаїн, Пронтосан.
Хронічні рани – глобальна проблема сучасності, яка негативно впливає на економіку країн, оскільки вимагає великих фінансових витрат на довготривале лікування й часто призводить до стійкої втрати працездатності пацієнтів [1]. Цьому сприяє загальна тенденція до старіння населення, малорухливий спосіб життя й, як наслідок, поширеність неінфекційних захворювань, таких як ожиріння, цукровий діабет 2 типу, гіпертонічна хвороба, хронічна венозна недостатність нижніх кінцівок [2]. Саме у цій категорії хворих найчастіше утворюються трофічні виразки в ділянці гомілки та/або стопи.
Хронічні рани – це патологічний стан, який характеризується наявністю глибоких дефектів покривних тканин, що відрізняються поганою тенденцією до загоєння та схильністю до рецидивування. Хронічна рана потребує тривалого лікування (від 4-6 міс і більше) і характеризується високою частотою рецидиву.
До хронічних ран належать:
- ураження шкіри та м’яких тканин при синдромі діабетичної стопи;
- трофічні виразки внаслідок порушення кровообігу у судинах нижніх кінцівок при наступних станах:
– хронічна венозна недостатність;
– атеросклероз артерій нижніх кінцівок;
– облітеруючий ендоартеріїт;
– артеріальна гіпертензія (виразка Марторелла);
- пролежні;
- опіки II-IV ступенів.
У світі 370 млн пацієнтів живуть із діагнозом «цукровий діабет». Очікується, що до 2030 року кількість таких хворих зросте до 552 млн [3]. У 5-7% пацієнтів із цукровим діабетом має місце синдром діабетичної стопи, основою патогенезу якого є діабетичні мікро- й макроангіопатії, периферична нейропатія нижніх кінцівок та остеоартропатія. Більш ніж у половини пацієнтів, які відвідують спеціалізовані кабінети діабетичної стопи, відзначаються інфекційні ускладнення [4]. Річний показник ампутацій серед пацієнтів із цукровим діабетом у Європі становить 0,5-0,8%, в Україні – 0,9% [5].
Згідно зі статистикою, 1% населення світу страждає на трофічні виразки, пов’язані з порушенням венозного та артеріального кровообігу нижніх кінцівок [6]. За даними дослідження, проведеного у Великобританії, венозні трофічні виразки виявляли із частотою 0,76 на 100 чоловіків та 1,42 на 100 жінок віком >65 років (Lindsey E., 2010). В останні роки відмічається зростання частоти трофічних виразок змішаного генезу. Так, відповідно до результатів обстеження пацієнтів із венозними виразками нижніх кінцівок, у 15-30% із них виявляли ознаки артеріальної недостатності (Mosti G. et al., 2012).
Лише у 50% пацієнтів трофічні виразки загоюються протягом 4 міс, у 20% – рана не загоюється протягом 2 років, а у 8% – навіть через 5 років лікування, тоді як частота рецидивів складає 6-15% [7]. Тому, незважаючи на велику кількість запропонованих методів системного та місцевого лікування, проблема не втрачає актуальності й потребує пошуку нових, більш дієвих способів вирішення.
Вибір антисептика для лікування та профілактики інфекційних ускладнень хронічних ран
Патогенез переходу ран від гострих до хронічних та таких, що погано загоюються, залишається недостатньо вивченим, однак, імовірно, однією із його складових є погана регуляція перебігу місцевого запального процесу [1]. Приєднання інфекції є ускладнюючим фактором, що призводить до погіршення загального стану пацієнтів, а також до збільшення тривалості та зниження ефективності лікування й, зрештою, до збільшення фінансових витрат [8].
Забезпечення умов повної стерильності для хронічних ран є майже нереальним, адже більшість ранових інфекцій походять від власного мікробіому пацієнта [9]. Умовно-патогенні мікроорганізми колонізують ранові поверхні, утворюють біоплівки, які обмежують бактеріальний кліренс шляхом фагоцитозу, стимулюють вироблення прозапальних цитокінів і знижують чутливість бактерій до антибіотиків. Усе це значно сповільнює процес загоєння ран [10, 11].
Хронічні рани, особливо такі, що містять некротизовані тканини, несуть більший ризик інфікування, а отже, потребують особливого лікування для зменшення бактеріальної контамінації. Більше того, багато пацієнтів із хронічними ранами, як правило, мають коморбідну патологію, у результаті чого їхня імунна система може бути ослабленою й недостатньо ефективно реагуватиме на бактеріальну контамінацію та колонізацію. Таким пацієнтам необхідний більш ретельний нагляд для профілактики інфекційних ускладнень, ніж пацієнтам із гострими ранами та меншою кількістю системних захворювань.
Обов’язковою умовою ефективного лікування ран, особливо таких, що важко загоюються, є повноцінна хірургічна обробка/санація рани. Метою обробки/санації рани є видалення гною та нежиттєздатних тканин, що усуває бактеріальні колонії й сприяє зменшенню мікробної контамінації рани. Завершенням санації є обробка рани антисептиками.
Згідно з останнім оновленням Консенсусу щодо ранових антисептиків (2018) [10], полігексанід є рекомендованим міжнародними експертами антисептиком першого вибору для лікування критично колонізованих ран, ран із ризиком інфікування, опіків та профілактики інфекційних ускладнень хірургічної рани.
У засобі комплексної дії для промивання, очищення та зволоження ран Пронтосан антибактеріальний компонент представлений 0,1% водним розчином полігексаніду, який має бактерицидний ефект широкого спектра дії проти бактерій і грибів, включаючи такі збудники, як метицилін-резистентний золотистий стафілокок, ентерококи, синьогнійна паличка, бактерії групи кишкової палички та інші мікроорганізми зі стійкою резистентністю до лікування.
Поверхнево-активна речовина (ПАР) засобу Пронтосан представлена ундециленамідопропіл-бетаїном. За рахунок гідрофільної частини молекули та низького поверхневого натягу рідини бетаїн проникає у всі важкодоступні місця рани, розм’якшуючи, розпушуючи й зрештою видаляючи фібринові нальоти та біоплівки з ранової поверхні. За рахунок гідрофобної частини молекули бетаїн поглинає нерозчинні у воді компоненти та біоплівки (солюбілізація), мобілізуючи їх у вигляді дрібнодисперсної суспензії, що видаляється з поверхні рани новим надходженням розчину для іригації ран Пронтосан при промиванні та очищенні рани. Таким чином досягається запобігання повторному осаду контамінованих дрібних часток рани та повторній контамінації ранової поверхні.
Пронтосан забезпечує й зберігає зволоження ранової поверхні, сприяє переходу процесу загоєння ран у фази регенерації та епітелізації, добре переноситься пацієнтами, адже аплікація препарату є безболісною. Засіб є сумісним із будь-яким типом перев’язувального матеріалу та сучасних ранових покриттів (пов’язок).
Засіб Пронтосан, завдяки полігексаніду, що входить до його складу, відповідає всім сучасним вимогам до місцевих антисептиків:
- потужна бактерицидна дія;
- низька токсичність;
- слабка резорбція;
- відсутність резистентності та алергічних реакцій;
- безболісність при нанесенні на рану.
Комбінація ПАР бетаїну та антибактеріального компоненту полігексаніду сприяє відмінному очищенню рани, що значно пришвидшує її загоєння.
Пронтосан представлений у формі розчину для іригації ран, а також у формі гелю для ран.
Застосування Пронтосану у формі розчину має найбільше значення в лікуванні ран за відсутності значних місцевих і системних порушень метаболізму тканин та прогнозованої тривалості лікування від 1 до 6 тижнів. При довгому загоєнні рани першочерговим завданням є не разове зменшення числа колонієутворюючих одиниць (кількість мікроорганізмів, культивованих в 1 мл поживного середовища), а тривале пригнічення їх росту. Найбільш ефективним у цьому випадку буде застосування Пронтосану у формі гелю. Завдяки довгому знаходженню у рані й більш тривалій дії гелеві форми випуску Пронтосану запобігають її вторинному інфікуванню, появі антибіотикорезистентної флори, дозволяють знизити частоту перев’язок і, таким чином, зменшити навантаження на медперсонал (Подпрятов С.Є., 2021).
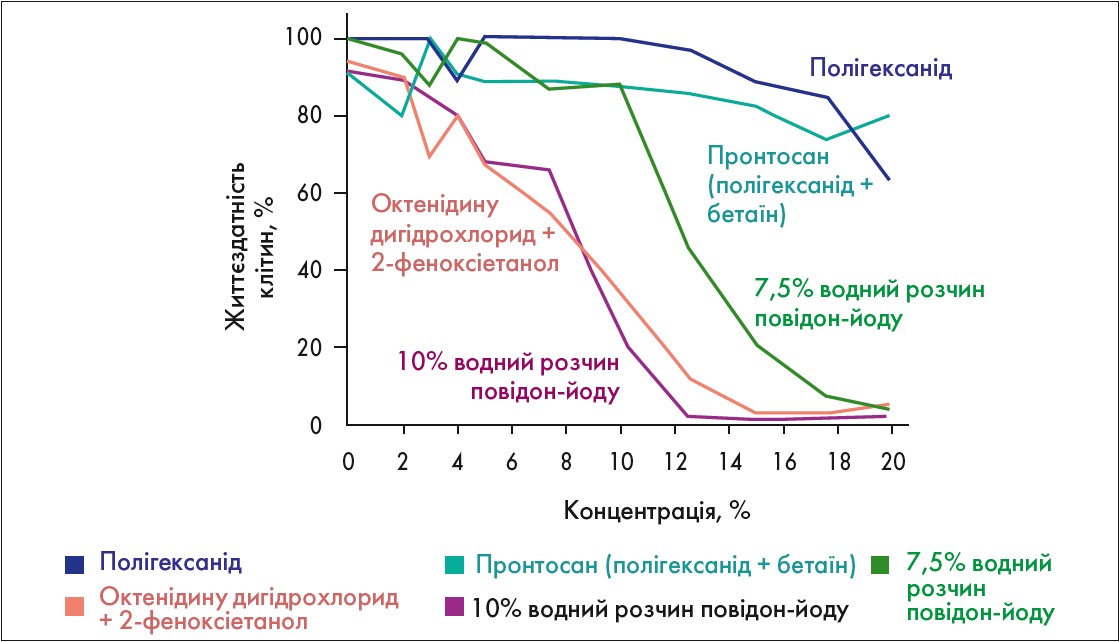
Окрім антибактеріальної ефективності однією з важливих характеристик сучасних антисептичних засобів є ступінь цитотоксичності. Цитотоксичні ефекти речовин, з якими накладають пов’язки, здатні пригнічувати життєздатність, проліферацію та міграцію клітин, що беруть участь у процесі загоювання рани, і, таким чином, сповільнювати його (Wiegand C. et al., 2019). Німецькими науковцями було проведено порівняльне дослідження цитотоксичної дії п’яти найчастіше використовуваних ранових антисептиків та Пронтосану при титруванні концентрації їх розчинів у бік збільшення на клітини шкірних покривів: первинні кератиноцити, фібробласти та культивовані людські кератиноцити [13]. За результатами роботи зазначено, що засоби, які містили полігексанід або полігексанід у комбінації з бетаїном (Пронтосан), продемонстрували мінімальну цитотоксичність по відношенню до кератиноцитів та фібробластів порівняно з іншими досліджуваними антисептиками (рисунок).
Рис. Цитотоксичний вплив антисептиків на клітини шкіри (Hirsch T. et al., 2010)
Світовий досвід застосування Пронтосану
L. Atkin et al. (2020) у своєму дослідженні вивчали вплив комбінованої терапії розчином та гелем, які містять полігексанід та бетаїн (Пронтосан), на загоєння хронічних важковиліковних ран із тривалістю хвороби до 20 років та періодом спостереження більше одного місяця [12]. У всіх хворих відзначалось поліпшення стану рани та зменшення розмірів ранового дефекту, які спостерігались уже на третій день від початку комбінованої терапії Пронтосаном розчином та Пронтосаном гелем. У понад половини пацієнтів, які отримували вищезазначене місцеве комбіноване лікування більше місяця, спостерігалось повне загоєння рани. Про поліпшення стану ранового ложа було повідомлено вже через два дні після початку лікування, при цьому у ряді випадків повідомлялося про зменшення кількості ексудату, вираженості болю та неприємного запаху. Крім того, автори дослідження зазначили, що використання комбінованої терапії Пронтосаном дозволило зменшити вдвічі частоту зміни пов’язок.
Отримані результати підтверджують дані іншого великого ретроспективного дослідження за участю 953 пацієнтів, у якому вдалося досягти загоєння/повного закриття 80% хронічних ран при застосуванні комбінованої терапії Пронтосаном у вигляді розчину та гелю: промивання Пронтосаном Розчином для іригації ран при кожній первинній хірургічній обробці/санації рани або при зміні пов’язки та наступне додаткове нанесення Пронтосану Гелю для ран перед накладанням ранового покриття у випадку повної відсутності або наявності помірної ексудації рани [14].
Американські дослідники A. Oropallo et al. (2021) також встановили, що Пронтосан при застосуванні в комбінації Пронтосан розчин + Пронтосан гель ефективний у лікуванні хронічних/важкозагоюваних ран нижніх кінцівок, зокрема автори вказували на покращення зовнішнього вигляду рани та зменшення її розмірів після 4 тижнів застосування даної комбінації. Пацієнти відмічали добру переносимість і покращення якості життя на фоні застосування обох форм випуску Пронтосану [15].
Отже, засіб для промивання, очищення та зволоження ран Пронтосан, що містить у своєму складі антисептик полігексанід та поверхнево-активну речовину бетаїн, демонструє високу ефективність і безпечність при лікуванні хронічних ран, що було підтверджено численними дослідженнями. Засіб ефективний проти більшості мікроорганізмів зі стійкою резистентністю до лікування, сприяє більш швидкому переходу процесу загоєння ран у фази регенерації та епітелізації, добре переноситься пацієнтами й може тривало, протягом 8 тижнів, використовуватися після відкриття флакона.
Література
- Brown H.L., Clayton A., Stephens P. The role of bacterial extracellular vesicles in chronic wound infections: Current knowledge and future challenges. Wound Repair Regen. 2021 Nov; 29(6): 864-880. DOI: 10.1111/wrr.12949.
- Yenilmez M.I. Economic and Social Consequences of Population Aging the Dilemmas and Opportunities in the Twenty-First Century. Applied Research in Quality of Life. 2015; 10: 735-752. DOI: 10.1007/s11482-014-9334-2.
- Bakker K., Apelqvist J., Schaper N. International Working Group on Diabetic Foot Editorial Board: Practical guidelines on the management and prevention of the diabetic foot 2011. Diabetes Metab Res Rev. 2012; 28 (Suppl 1): 225-231. DOI: 10.1002/dmrr.2253.
- Hinchcliffe R.J., Andros G., Apelqvist J. et al. A systematic review of the effectiveness of revascularization of the ulcerated foot in patients with diabetes and peripheral arterial disease. Diabetes Metab Res Rev. 2012 Feb; 28 (Suppl 1): 179-217. DOI: 10.1002/dmrr.2249.
Повний список літератури знаходиться в редакції.
Підготувала Єлизавета Лисицька