4 червня, 2024
Антибіотикорезистентність у клінічній практиці: зміна парадигми
 Присвячена Всесвітньому дню нирки конференція, яка відбулася 24-25 квітня, зібрала в лавах слухачів багатьох нефрологів, терапевтів і сімейних лікарів України. Помітно зацікавила аудиторію доповідь Флоріана Вагенленера (директор клініки урології, дитячої урології та андрології, м. Гіссен, Німеччина), який привернув увагу учасників до проблеми антибіотикорезистентності (АБР).
Присвячена Всесвітньому дню нирки конференція, яка відбулася 24-25 квітня, зібрала в лавах слухачів багатьох нефрологів, терапевтів і сімейних лікарів України. Помітно зацікавила аудиторію доповідь Флоріана Вагенленера (директор клініки урології, дитячої урології та андрології, м. Гіссен, Німеччина), який привернув увагу учасників до проблеми антибіотикорезистентності (АБР).
За прогнозами експертів, у 2050 р. АБР спричинить 10 млн смертей. Однак і зараз дані є невтішними: вже у 2019 р. 4,9 млн осіб померли внаслідок інфекцій, обумовлених антибіотикорезистентними патогенами. Серед провідних патогенів у списку причин смерті є і поширені етіологічні збудники урологічних інфекцій, наприклад Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, Enterococcus faecium (Antimicrobial Resistance Collaborators Consortium, 2022).
На мікроорганізми постійно діє селекційний тиск, який обумовлює адаптивні генетичні мутації, у т. ч. розвиток АБР, насамперед у разі неправильного або надмірного застосування антибіотиків (АБ) у медицині, ветеринарії та сільському господарстві. АБР дає бактеріям та іншим мікробам не лише здатність виживати у середовищі, насиченому АБ та антисептиками, а й здатність передавати адаптаційні генетичні елементи по горизонталі, поширюючи АБР серед інших бактерій-сусідів. АБР ускладнює лікування багатьох хвороб, провокує їх тривалий затяжний перебіг, підвищує ризик розповсюдження захворювань, подовжує стаціонарне лікування, збільшує витрати на фармакотерапію та підвищує показники смертності (Ahmed S. K. et al., 2024).
Вагомим фактором поширення АБР є війна. За даними S.J.C. Pallett і співавт. (2023), резистентність бактерій чітко асоціюється з воєнними діями. Таке спостерігалося в Сирії, Афганістані та зараз – в Україні. Порівняно з довоєнним часом зареєстровано збільшення резистентності Klebsiella pneumoniae до карбанепенему на 11%, до аміноглікозидів – на 7%, до фторхінолонів – на 16%. Механізми таких несприятливих змін є багатогранними. Насамперед в умовах війни медики не завжди дотримуються протоколу профілактики АБР.
На прикладі Німеччини протягом останніх років можна відстежити різке зростання відсоткової частки ентеробактерій, які продукують карбапенемази. Також значно почастішали випадки резистентності Escherichia coli та Klebsiella pneumoniae до АБ резерву та їхньої омнірезистентності, а в такому випадку залишається дуже мало опцій для боротьби з інфекцією. Звісно, паралельно до наростання АБР відбувається і процес створення нових АБ, проте з 1990-х рр. було синтезовано лише декілька молекул. На щастя, розроблено інноваційні препарати, здатні впливати на резистентні ентеробактерії та синьогнійну паличку: цефтолозан/тазобактам, цефтазидим/авібактам, цефепім/енметазобактам, цефепім/таніборбактам, іміпенем/релебактам, меропенем/ваборбактам, цефідерокол, фінафлоксацин, плазоміцин, гепотидацин. Однак із цими АБ слід бути обережними, оскільки в разі їхнього неконтрольованого використання до них теж невдовзі може виникнути резистентність. Загалом збільшення споживання АБ корелює із наростанням АБР: це природний еволюційний процес. Саме тому доцільно зменшувати загальне споживання АБ, насамперед за поширених інфекцій – наприклад, при неускладнених інфекціях сечовивідних шляхів (ІСШ).
На найпоширенішу ІСШ – гострий цистит – щороку страждає ≈10% жінок світу, а в постменопаузальній популяції цей показник є ще вищим і становить >20%. Відповідно до рекомендацій Європейської асоціації урології, при неускладнених ІСШ слід застосовувати т. зв. нішеві АБ, тобто препарати, які застосовуються лише за цього показання. До цієї групи належать фосфоміцину трометамол, нітрофурантоїн і півмецилінам, а в деяких регіонах (це залежить від рівня резистентності) – триметоприм та триметоприм/сульфаметоксазол. Натомість фторхінолони за таких інфекцій не показані. Якщо перша лінія терапії виявилася неефективною, застосовують цефалоспорини (наприклад, цефадроксил).
Однак кожен АБ (навіть вузького спектра, як-от фосфоміцину трометамол або нітрофурантоїн) чинить вплив на мікробіом. У дослідженні A. Gessner і співавт. (2020) порівняли вплив різних препаратів (фосфоміцину трометамолу, нітрофурантоїну та фітопрепарату BNO 1045, що в Україні представлений препаратом Канефрон® Н) на мікробіом кишечнику щурів. Виявилося, що навіть нішеві АБ значно змінюють співвідношення різних бактерійних родин у складі мікробіому; натомість ефект Канефрону Н приблизно відповідає ефекту води, тобто Канефрон® Н не чинить жодного несприятливого впливу.
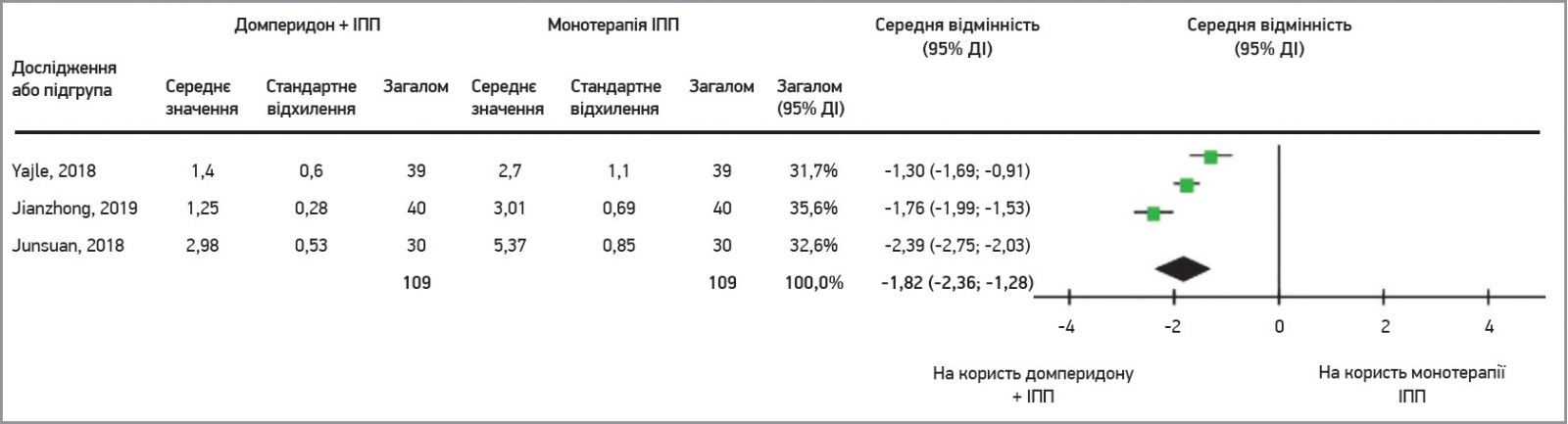
У рандомізованому подвійному сліпому плацебо-контрольованому авторському дослідженні Ф. Вагенленера та співавт. (2018) взяли участь >600 пацієнтів із неускладненим циститом, яких було рандомізовано в групи Канефрону Н 3 р/добу 7 днів та одноразового прийому 3 г фосфоміцину трометамолу. Наприкінці періоду дослідження не було виявлено статистично достовірної різниці між групами за показником частки успішного лікування. 83,5% пацієнтів групи Канефрону Н і 89,8% хворих групи фосфоміцину трометамолу не потребували додаткової антибіотикотерапії (АБТ) (різниця недостовірна; р=0,0014) (рис. 1).
Рис. 1. Частка пацієнтів груп Канефрону Н та фосфоміцину трометамолу, які не потребували додаткової АБТ
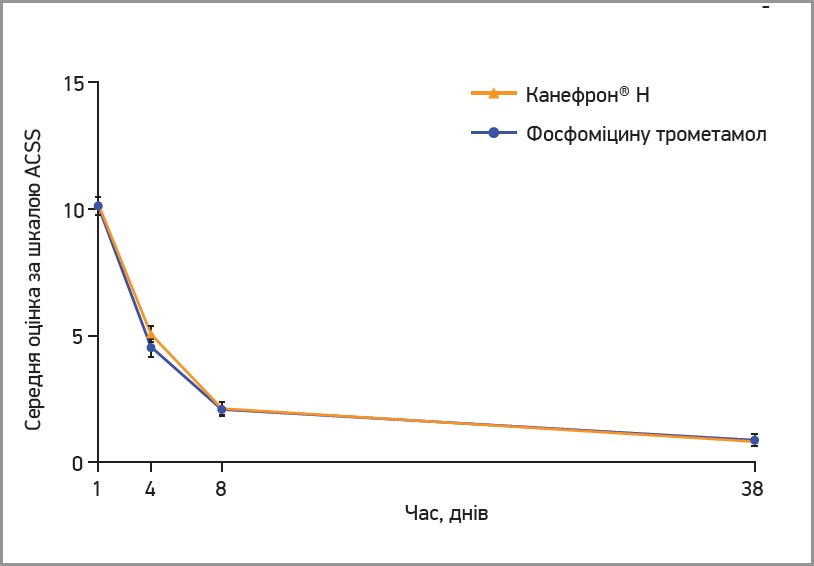
Також протягом усього періоду лікування та через 38 днів від початку дослідження не було зафіксовано міжгрупової різниці за шкалою оцінки симптомів гострого циститу (ACSS), тобто динаміка покращення виявилася аналогічною (рис. 2).
Рис. 2. Динаміка середньої оцінки за шкалою ACSS для Канефрону Н та фосфоміцину трометамолу
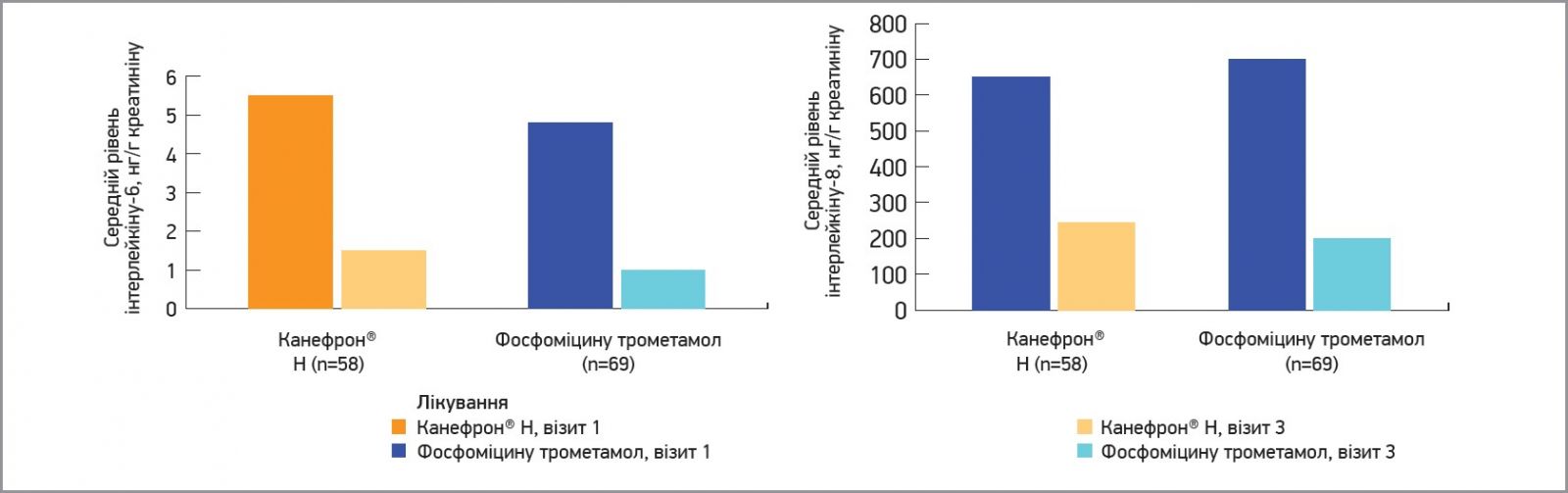
Крім оцінки клінічної ефективності Канефрону® Н та фосфоміцину трометамолу, вивчався також їхній вплив на рівні цитокінів у сечі. Канефрон® Н забезпечував аналогічне фосфоміцину трометамолу зниження вмісту прозапальних інтерлейкінів 6 та 8 у сечі пацієнтів з ІСШ (рис. 3) (Butler D. et al., 2023).
Рис. 3. Зниження вмісту прозапальних інтерлейкінів 6 та 8 у групах Канефрону Н та фосфоміцину трометамолу
Цікаво, що Канефрон® Н також протидіє рецидивам ІСШ. Порівняно з АБ Канефрон® Н зменшував імовірність повторного встановлення діагнозу ІСШ упродовж 30-365 днів після курсу лікування. Цей протирецидивний ефект спостерігався і в загальній групі пацієнтів, і в окремих підгрупах (жінки/чоловіки, особи віком <40/41-60/>60 років) (Holler M. et al., 2021). Отже, для лікування гострих спорадичних випадків неускладненого циститу доцільно використовувати не АБТ, а Канефрон® Н, який не лише усуває поточну проблему, а й запобігає її повторному виникненню.
Загалом, за даними метааналізу Y. Kausner і співавт. (2022), у >60% пацієнтів з ІСШ можна уникнути застосування АБ за допомогою різних стратегій дії – наприклад, використання фітопрепаратів (Канефрону Н).
Висновки
1. Проблема АБР продовжує наростати в усьому світі, а розроблення АБ неспроможне забезпечити людству достатню кількість нових діючих речовин.
2. Поширеність АБР напряму залежить від глобального споживання АБ, тому стратегії обмеження їх призначення є надзвичайно важливими.
3. При неускладнених ІСШ для запобігання АБР доцільно застосовувати фітопрепарати (Канефрон® Н).
Підготувала Лариса Стрільчук