26 квітня, 2026
Ревматологія у фокусі: факти, тренди й оновлення 2025 року
 Ревматологія сьогодні перебуває у стані динамічного розвитку, коли наукові відкриття, клінічні дослідження та оновлені рекомендації формують сучасні стандарти ведення пацієнтів. Минулий рік став особливо багатим на ключові події, які визначають майбутнє спеціальності: від появи нових терапевтичних стратегій та біологічних препаратів до перегляду класифікаційних критеріїв і впровадження інноваційних технологій у діагностику та лікування. Під час заходу «Ревматологічний калейдоскоп 2025» провідні експертки Єлизавета Давидівна Єгудіна, д.мед.н., професорка, керівниця навчального центру Інституту ревматології, лікарка-ревматологиня Клініки сучасної ревматології (м. Київ), та Світлана Анатоліївна Трипілка, к.мед.н., доцентка, ревматологиня вищої кваліфікаційної категорії Медичного центру здоров’я (м. Харків), розглянули головні новини у цій галузі, зосередившись на змінах, що відбулися протягом останнього року, та проаналізували їх окремо для кожної нозології з позицій сучасних рекомендацій і результатів актуальних досліджень.
Ревматологія сьогодні перебуває у стані динамічного розвитку, коли наукові відкриття, клінічні дослідження та оновлені рекомендації формують сучасні стандарти ведення пацієнтів. Минулий рік став особливо багатим на ключові події, які визначають майбутнє спеціальності: від появи нових терапевтичних стратегій та біологічних препаратів до перегляду класифікаційних критеріїв і впровадження інноваційних технологій у діагностику та лікування. Під час заходу «Ревматологічний калейдоскоп 2025» провідні експертки Єлизавета Давидівна Єгудіна, д.мед.н., професорка, керівниця навчального центру Інституту ревматології, лікарка-ревматологиня Клініки сучасної ревматології (м. Київ), та Світлана Анатоліївна Трипілка, к.мед.н., доцентка, ревматологиня вищої кваліфікаційної категорії Медичного центру здоров’я (м. Харків), розглянули головні новини у цій галузі, зосередившись на змінах, що відбулися протягом останнього року, та проаналізували їх окремо для кожної нозології з позицій сучасних рекомендацій і результатів актуальних досліджень.
Остеоартрит
Сучасні підходи до лікування остеоартриту (ОА) поступово змінюються: від традиційного контролю симптомів до пошуку нових терапевтичних стратегій, що враховують метаболічні фактори, своєчасність втручань та інноваційні методи. У дослідженні за участю 9464 пацієнтів було встановлено, що високий індекс вісцерального ожиріння значно підвищує ризик розвитку ОА, – це підкреслює важливість контролю метаболічних факторів для профілактики (Wang et al., 2025).
Єдиним препаратом із доведеною ефективністю при ОА у пацієнтів з ожирінням наразі є семаглутид. У 68-тижневому рандомізованому випробуванні він забезпечував значне зменшення маси тіла, виразне полегшення болю та поліпшення фізичної функції, що підтвердило його потенціал як терапевтичної опції у комплексному лікуванні (Bliddal et al., 2024). Водночас у когортному дослідженні було показано, що внутрішньосуглобові ін’єкції глюкокортикоїдів (ГК) зменшували потребу в тривалому застосуванні анальгетиків, але могли негативно впливати на прогресування хвороби (Hawley et al., 2025). Це підтверджує дані, отримані іншими науковцями, відповідно до яких ін’єкції ГК асоціювалися із виразнішим прогресуванням ОА, тоді як гіалуронова кислота, навпаки, знижувала темпи структурних змін; обидва методи забезпечували зменшення болю (Bhardwaj et al., 2025).
Важливим немедикаментозним компонентом є фізична терапія. Її ранній старт після встановлення діагнозу та достатня кількість занять (понад 12) пов’язані зі значно нижчим ризиком майбутньої потреби у застосуванні внутрішньосуглобових ін’єкцій (Neogi et al., 2025).
Що ж до інноваційних підходів, то одноразове введення мезенхімальних стромальних клітин із жирової тканини не показало клінічно значущих переваг над плацебо, хоча терапія мала сприятливий профіль безпеки. Це свідчить про необхідність подальших досліджень для уточнення ролі клітинної терапії при ОА (Pers et al., 2025).
Подагра
Останні роки характеризуються суттєвими змінами у підходах до лікування подагри – від оптимізації уратознижувальної терапії до врахування метаболічних факторів та супутніх станів. У ретроспективному аналізі CARES було показано, що частка пацієнтів у ремісії поступово зростала з 37% на першому році до понад 63% – на шостому, із початковою перевагою фебуксостату над алопуринолом у перші два роки (White et al., 2018). Водночас проспективне когортне дослідження із залученням 527 чоловіків засвідчило, що ефективність фебуксостату значно знижувалася при ожирінні, що підкреслювало важливість контролю маси тіла (Cheng et al., 2025).
Додатковий терапевтичний потенціал мають препарати для лікування дисліпідемії. Так, аторвастатин і розувастатин не лише знижують рівень сечової кислоти, але й модулюють запальні механізми через інтерлейкін (IL)-37, пригнічуючи продукцію IL‑1β (Akbari et al., 2024; Ridker et al., 2023). Фенофібрат проявляє урикозуричний ефект завдяки інгібуванню URAT1 та достовірно знижує рівень сечової кислоти, зокрема у пацієнтів із цукровим діабетом 2-го типу (Liu et al., 2025).
У сфері діагностики в сучасних рекомендаціях Американської колегії ревматологів (ACR, 2025) наголошено, що діагноз подагри у більшості випадків можна встановити на основі клінічної картини, результатів лабораторних показників та рентгенографії. Підтвердження наявності кристалів моноурату натрію є бажаним, але не завжди обов’язковим. Методи візуалізації, зокрема ультразвукове дослідження та спектральна комп’ютерна томографія, особливо корисні у міжнападовому періоді. Ультразвук має чутливість близько 76% і специфічність 84%, що робить його цінним доповненням до клінічної оцінки (Pivlenskse et al., 2024; Gessl et al., 2024).
Ревматоїдний артрит
Сучасна стратегія ведення пацієнтів із ревматоїдним артритом (РА) поступово трансформується – акцент робиться на ранньому виявленні осіб із підвищеним ризиком розвитку хвороби для пошуку рішень, що дозволяють мінімізувати фармакологічне навантаження. Клінічно підозріла артралгія розглядається як стан, що може передувати розвитку РА. Концепція, запропонована Європейським альянсом асоціацій ревматологів (EULAR) і ACR (2025) щодо клінічно-підозрілої артралгії базується на поєднанні клінічних ознак, серологічних маркерів та даних візуалізації, зокрема магнітно-резонансної томографії, що дозволяє виявити субклінічне запалення й ідентифікувати пацієнтів із підвищеним ризиком прогресування до РА (van Steenbergen et al., 2025).
Що стосується терапії, за результатами ретроспективного когортного дослідження, поступове зниження дози метотрексату в стабільних пацієнтів не супроводжувалося суттєвим підвищенням ризику загострень за умови ретельного моніторингу (Haider et al., 2025).
Інший напрям – раннє застосування біологічних препаратів. Так, індукційна терапія інгібіторами фактора некрозу пухлини (TNF) в осіб із раннім РА асоціювалася з нижчим ризиком тяжко контрольованого перебігу хвороби та більшою ймовірністю ремісії без лікування у довгостроковій перспективі порівняно зі стандартною стратегією, як-от синтетичні хворобомодифікувальні антиревматичні препарати (Toyoda et al., 2025).
Важливим залишається питання використання ГК. Дослідження показало, що парентеральне введення ГК під час міст-терапії корелювало із більш раннім припиненням їх застосування, тоді як потреба у біологічних чи таргетних препаратах не залежала від способу введення. Це узгоджується із сучасними настановами, в яких рекомендовано обмежувати тривалість терапії ГК через ризик побічних ефектів (Fernаndez-Codina et al., 2023).
Спондилоартрит та псоріатичний артрит
Зміни у веденні пацієнтів зі спондилоартритом (СпА) та псоріатичним артритом (ПсА) стосуються як уточнення класифікаційних критеріїв, так і оптимізації терапевтичних стратегій, що дозволяє індивідуалізувати лікування та поліпшувати довгострокові результати. Згідно із даними Міжнародного товариства з оцінки спондилоартриту (ASAS), термінологія СпА передбачає поділ на аксіальний і периферичний СпА, що дає змогу точніше враховувати стадію та форму захворювання (van der Heijde et al., 2024). Переглянуті критерії ASAS-SPARTAN (2025) для аксіального СпА поєднують клінічні ознаки, лабораторні маркери та сучасні методи візуалізації, забезпечуючи точнішу стратифікацію пацієнтів і сприяючи ранньому виявленню хвороби (Smolen et al., 2025).
У реальній практиці важливим є вибір стартової біологічної терапії. За даними конгресу ACR Convergence 2025, початкова терапія TNF-інгібіторами асоційована із нижчим ризиком неприхильності до лікування та кращою довгостроковою ефективністю порівняно з інгібіторами IL‑17 та янус-кіназ (JAK) (Magrey et al., 2025).
Що стосується ПсА, після неефективності першого TNF-iнгібітора перехід на упадацитиніб (JAK-інгібітор) забезпечував кращі результати, ніж повторне застосування іншого інгібітора TNF чи IL‑17. Це підтверджує ефективність зміни механізму дії терапії та підкреслює важливість індивідуалізованого підходу (Mease et al., 2023).
Таким чином, сучасні дані демонструють, що у менеджменті осіб із СпА та ПсА ключовими є рання діагностика, правильна стратифікація пацієнтів та обґрунтований вибір стартової терапії. За неефективності лікування першої лінії призначення засобу з іншим механізмом дії може бути дієвішою стратегією, ніж зміна препаратів у межах однієї групи.
Васкуліти
У сучасній практиці лікування системних васкулітів відбувається суттєва трансформація: замість традиційного використання ГК дедалі ширше застосовуються таргетні препарати, а також удосконалюється підхід до дозування вже відомих ліків. Так, упадацитиніб був схвалений для лікування гігантоклітинного артеріїту. У фазі 3 дослідження SELECT-GCA він продемонстрував значно вищу частоту стійкої ремісії порівняно із плацебо (46,4 vs 29%; p=0,002), а також кращі показники за вторинними кінцевими точками, включно із меншою кумулятивною дозою ГК. Профіль безпеки був подібним до плацебо, без серйозних несприятливих серцево-судинних подій, що особливо важливо для JAK-інгібіторів (Blockmans et al., 2025).
Інший напрям стосується васкулітів, асоційованих з антинейтрофільними цитоплазматичними антитілами. Дослідження показало, що ультранизькі дози ритуксимабу (200 мг що шість місяців) забезпечують таку ж підтримку ремісії, як і стандартні низькі дози (500 мг), без зростання ризику інфекцій чи гіпогаммаглобулінемії. Це відкриває можливість безпечнішої та економічно вигідної стратегії підтримувальної терапії (Fernаndez-Codina et al., 2025).
Отже, останні дані свідчать про нові можливості у лікуванні васкулітів – застосування JAK-інгібіторів при гігантоклітинному артеріїті та використання ультранизьких доз ритуксимабу при васкулітах, асоційованих з антинейтрофільними цитоплазматичними антитілами, що дозволяє зменшити медикаментозне навантаження та оптимізувати безпеку лікування.
Автоімунні міозити
У сфері автоімунних міозитів дедалі більше уваги приділяється стандартизації термінології та перегляду класифікаційних підходів. Це важливо не лише для точнішої діагностики, але й для узгодженості результатів досліджень та оптимізації терапії.
У сучасних рекомендаціях наголошується на відмові від термінів «дерматополіміозит», «ідіопатична запальна міопатія» та «ідіопатичний міозит», які створюють плутанину та не відповідають сучасним концепціям. Натомість пропонується використовувати уніфіковані визначення – «міозит» або «поліміозит», що забезпечує єдність у науковій та клінічній практиці (Giannini et al., 2025).
Отже, впровадження узгодженої термінології сприяє точнішій стратифікації пацієнтів, поліпшує комунікацію між лікарями та дослідниками й відкриває шлях до більш індивідуалізованих стратегій терапії.
Вагітність і лактація
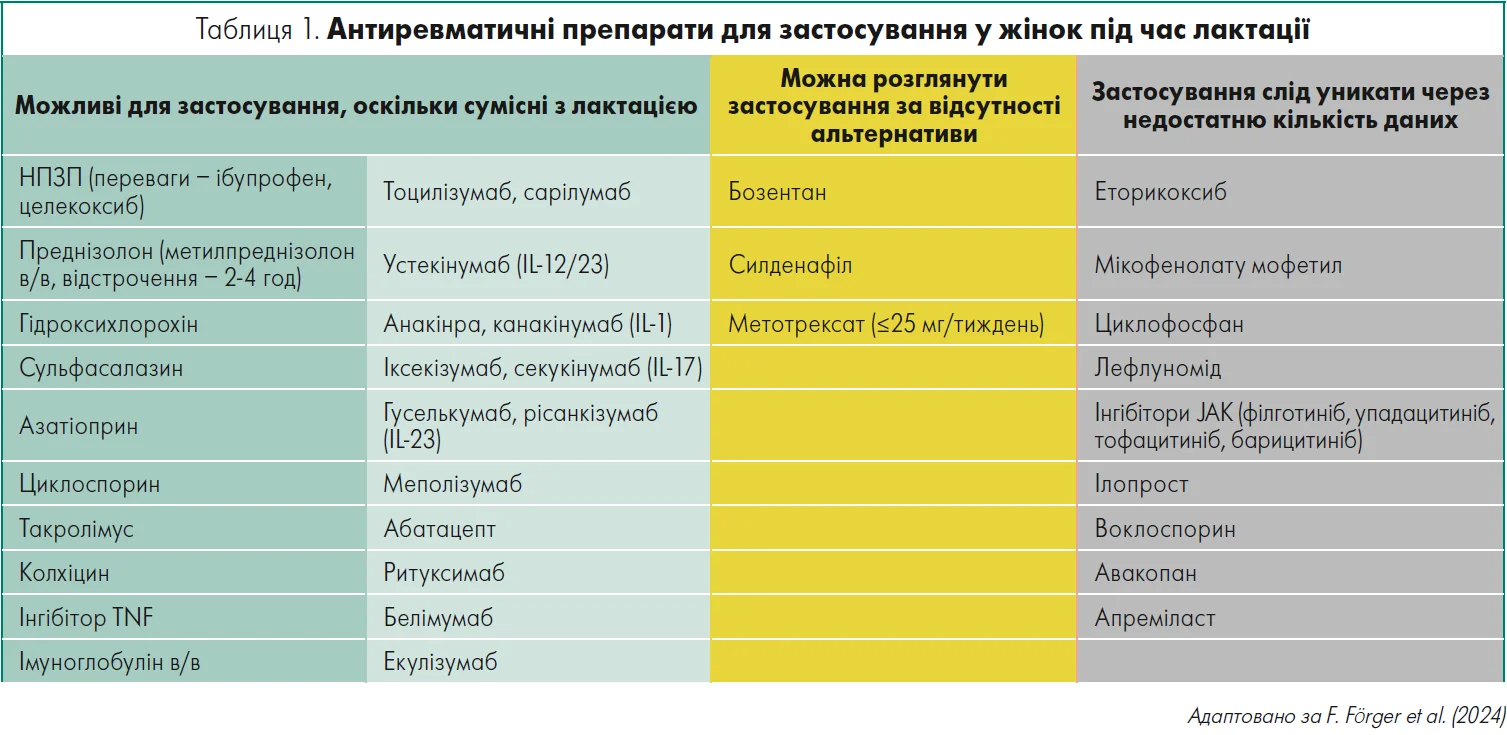
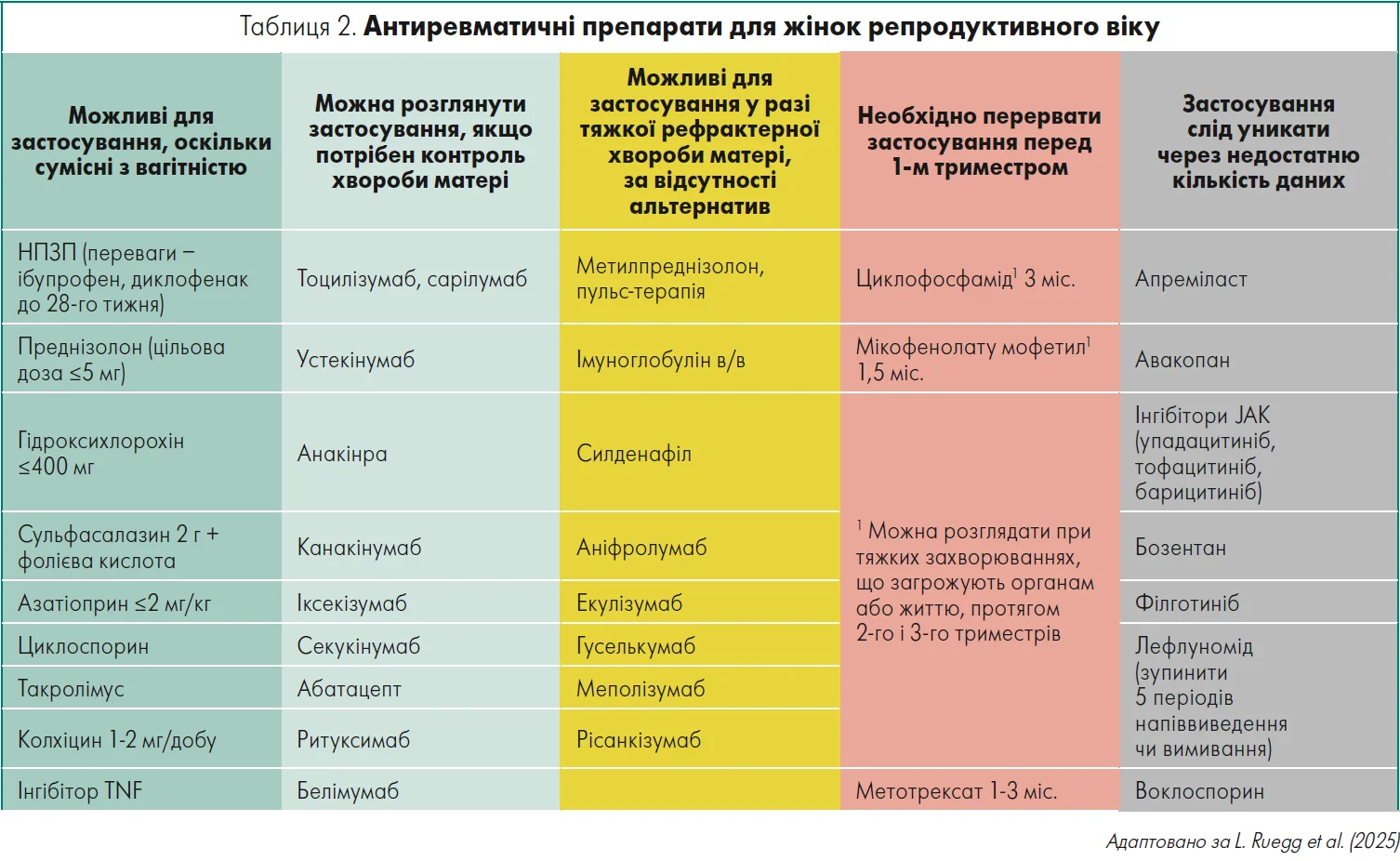
Окремо експертки зупинилися на змінах щодо безпеки застосування препаратів, які використовуються для лікування ревматичних захворювань під час вагітності й лактації, адже це критично важливо для здоров’я матері та дитини (табл. 1 і 2). Так, станом на 2025 р. накопичено нові дані щодо застосування гідроксихлорохіну (ГХХ). Метааналіз даних жінок з антифосфоліпідним синдромом показав, що додавання ГХХ до стандартної терапії асоційоване із вищим показником живонароджень (Berman et al., 2025). У когортному дослідженні серед пацієнток із системним червоним вовчаком встановлено, що приймання ГХХ знижує ризик прееклампсії, що має ключове значення для збереження здоров’я матері та плода (Nguyen et al., 2025).
Окрім того, аналіз безпеки підтвердив, що використання ГХХ у першому триместрі не підвищує ризик вроджених вад розвитку (Alle et al., 2025).
Знеболення при ревматологічних захворюваннях: сучасні можливості
Фахівці наголошують, що адекватний контроль болю є ключовим компонентом ведення пацієнтів із ревматологічними захворюваннями. Суглобовий біль не лише знижує якість життя, але й обмежує функціональність, тому сучасні стратегії лікування включають використання технологічно удосконалених форм нестероїдних протизапальних препаратів (НПЗП).
Диклоберл® Ретард – капсули диклофенаку натрію по 100 мг, створені за технологією мікрогранул. Така форма забезпечує контрольоване вивільнення діючої речовини у дванадцятипалій кишці, поступове надходження повної дози протягом тривалого часу та зниження ризику побічних ефектів із боку шлунково-кишкового тракту. Це дозволяє поєднувати ефективність, стабільність і безпеку при тривалій протизапальній терапії.
Диклоберл® N 75 – ін’єкційна форма диклофенаку натрію із доведеною ефективністю у післяопераційному періоді. У клінічному дослідженні показано, що внутрішньом’язове введення препарату забезпечує значне зменшення інтенсивності болю у перші 4‑12 год після гінекологічних втручань порівняно із внутрішньовенним введенням парацетамолу (Shah et al., 2016). Це підтверджує його перевагу як засобу для швидкого та ефективного контролю післяопераційного болю.
Отже, сучасна ревматологія демонструє перехід до більш персоналізованого підходу, що поєднує ранню діагностику, стратифікацію ризиків та раціональний вибір терапії з урахуванням механізму дії препаратів. Оновлені клінічні рекомендації та результати досліджень відкривають нові можливості для підвищення ефективності й безпеки лікування, зокрема у складних клінічних ситуаціях. Водночас оптимальний контроль симптомів, зокрема болю, залишається невід’ємною складовою поліпшення якості життя пацієнтів.
Підготувала Людмила Суржко
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 1 (76) 2026 р.