26 квітня, 2026
Антидепресанти та ризик постуральної гіпотензії
Одним із побічних ефектів при застосуванні антидепресантів є постуральна гіпотензія (ПГ). Хоча ПГ за такої антидепресивної терапії є досить рідкісною, вона може бути пов’язана із серйозними ускладненнями в осіб похилого віку, наприклад, падіннями, інсультом та когнітивною дисфункцією. При проведенні рандомізованих контрольованих досліджень (РКД), присвячених впливу антидепресантів, популяція літніх пацієнтів часто виключається, а на оцінюванні несприятливих явищ не сфокусовано належну увагу. C. Bhanu et al. проаналізували ризик виникнення ПГ на тлі використання антидепресантів у дорослих хворих віком ≥60 років в умовах первинної медичної допомоги. Отримані результати розміщені в онлайн-публікації «Antidepressants and risk of postural hypotension: a self-controlled case series study in UK primary care» (British Journal of General Practice, 2025; https://doi.org/10.3399/BJGP.2024.0429).
ПГ визначається як зниження систолічного артеріального тиску (АТ) на ≥20 мм рт. ст. або діастолічного АТ на ≥10 мм рт. ст. протягом 3 хв після прийняття вертикального положення (або положення із піднятою головою під час тесту із нахилом ортостатичного столу щонайменше під кутом 60°) (Freeman et al., 2011). ПГ є поширеним явищем, яке вражає приблизно третину осіб похилого віку (McDonagh et al., 2021). Серйозні ускладнення у цієї категорії пацієнтів включають підвищений ризик падінь, інфаркту міокарда, інсульту, фібриляції передсердь, деменції та смерті через церебральну й серцеву гіпоперфузію (Saedon et al., 2020; Clark et al., 2018).
ПГ описувалася як побічний ефект антидепресантів у раніше проведених дослідженнях, але на практиці вона розпізнається рідко (Rivasi et al., 2020). ПГ не визнається несприятливим явищем трициклічних антидепресантів (ТЦА) і згадується як нечаста побічна дія селективних інгібіторів зворотного захоплення серотоніну (СІЗЗС) у Британському національному формулярі (BNF, 2025). Слід зауважити, що понад 87% літніх осіб із депресією отримують антидепресанти, і цей показник продовжує зростати (Giovannini et al., 2020). Крім того, ТЦА широко використовуються із приводу болю та проблем зі сном. Здебільшого такі випадки зустрічаються у загальній клінічній практиці, де ПГ погано виявляється (Bhanu et al., 2023). До того ж рекомендацій щодо лікування ПГ, викликаної препаратами, наразі бракує. Більшість доказів із цього питання були отримані у невеликих перехресних дослідженнях або РКД, в яких чи то не були включені літні особи, чи то недостатньо оцінювалися побічні реакції на ліки як вторинний результат терапії (Florisson et al., 2021; Junqueira et al., 2021).
У цьому контексті C. Bhanu et al. (2025) прагнули оцінити ризик виникнення ПГ, пов’язаної з лікуванням антидепресантами, у дорослих хворих віком ≥60 років в умовах первинної медичної допомоги, використавши рутинно зібрані відомості з бази даних медичних досліджень IQVIA (IMRD) у Великій Британії.
Матеріали й методи дослідження
Дизайн та критерії включення
Було здійснене дослідження серії випадків із самоконтролем (SCCS), що включало дані загальної клінічної практики, взяті з електронних медичних записів IMRD із 1 січня 2000 р. по 31 грудня 2018 р. Науковці оцінювали зв’язок між впливом антидепресантів та ПГ (Blak et al., 2011).
Аналіз SCCS слугує для вивчення кореляції між ефектом, що змінюється з часом, та результатом. Це метод, альтернативний когортним дослідженням та дослідженням типу «випадок-контроль», що спершу був розроблений для оцінювання зв’язку між вакцинацією та небажаними явищами (Petersen et al., 2016). Відтоді цей інструмент широко застосовується у фармакоепідеміології, зокрема у багатьох дослідженнях, присвячених вивченню серйозних побічних ефектів окремих препаратів (Chui et al., 2023; Mansfield et al., 2018).
При застосуванні методу SCCS аналізуються лише окремі випадки. Тому ймовірність несприятливих результатів оцінюється у певні часові межі впливу препарату (період ризику) порівняно із часовим діапазоном поза цими вікнами ризику (референтний період), щоб визначити, чи є вищим ризик негативних наслідків під час застосування медикаменту.
Ключові переваги такого підходу полягають у тому, що окремі пацієнти самі контролюють процес, до того ж ризик аналізується індивідуально. Завдяки цьому незмінні загальні фактори, як-то стать, етнічна належність, соціальна депривація та генетичні чинники, не заважають оцінюванню (Ikuta et al.,. 2022). На додаток, метод SCCS дозволяє оцінити побічні ефекти лікарських засобів у тяжких хворих похилого віку із супутніми патологіями та поліпрагмазією, що більше підходить для менеджменту пацієнтів у реальній клінічній практиці, які за інших умов були б виключені з РКД.
Критеріям включення відповідали пацієнти, які отримали рецепт на антидепресант та мали випадок ПГ упродовж дослідження. Для учасників період спостереження розпочався не пізніше ніж: 1 січня 2000 р., дати їхньої реєстрації, дати запису даних на прийнятному рівні якості та звітності про смертність або досягнення віку 60 років плюс 12 місяців безперервної реєстрації в IMRD. Кінець періоду спостереження для кожної особи припадав на найбільш ранню із таких дат, як: 31 грудня 2018 р., дата останнього збору даних, досягнення віку 100 років або смерть.
Оцінювані препарати
Відомості про призначувані антидепресанти у базі даних IMRD були згруповані відповідно до підрозділів BNF (Hardoon et al., 2013):
- ТЦА та інші подібні за структурою чи дією антидепресанти (наприклад, амітриптилін);
- СІЗЗС (наприклад, сертралін);
- інші антидепресанти (наприклад, міртазапін).
Інші антидепресанти включали агомелатин, дулоксетин, флупентиксол, міртазапін, нефазодон, окситриптан, ребоксетин, триптофан, венлафаксин та вортіоксетин.
Рецепт вважався прийнятним, якщо це був перший призначений пацієнтові антидепресант, і це сталося протягом дослідження. Період застосування препарату вважався безперервним, якщо між послідовними призначеннями була перерва ≤90 днів. Цей метод використовувався у попередніх дослідженнях, присвячених вивченню антидепресантів (Jeffery et al., 2023). Дати початку та завершення впливу антидепресанту визначалися для кожного учасника лише на основі першого безперервного періоду використання ліків. Кінець ефекту препарату визначався як дата останнього призначення в межах безперервного періоду плюс 30 днів, щоб врахувати остаточну тривалість його приймання (Ikuta et al., 2022).
Період ризику до початку дії препарату. За методом SCCS, виникнення ПГ не має суттєво впливати на подальше застосування антидепресантів. У такому разі через встановлений діагноз ПГ може зменшитися ймовірність призначення препарату клініцистом згодом, що потенційно призведе до викривлення оцінок (Petersen et al., 2016). Тому автори включили 90-денний період до початку приймання антидепресанту, щоб врахувати цей момент.
Період ризику за ініціації терапії (дні 1‑28 та 29‑56). Стартовий період приймання антидепресанту визначався із 1-го по 28-й день від першого призначення препарату. Цей часовий інтервал вважався таким, що найімовірніше відображав розвиток ПГ на тлі лікування, а не через інші причини. Дослідники включили додатковий стартовий період приймання препарату із 29-го по 56-й день, що становив більше вікно для звернення пацієнтів до сімейного лікаря із приводу побічних ефектів або для перегляду терапії.
Період ризику при продовженні лікування (день ≥57). Період продовження впливу антидепресанту визначався як час від 57-го дня до кінця терапії (різний для кожного учасника). Кінець періоду використання препарату визначався як дата останнього приймання плюс 30 днів (для врахування остаточного ефекту).
Референтний період. Референтними вважалися періоди поза межами описаних вище вікон ризику, без впливу антидепресанту.
Аналізовані результати
Результат визначався як перший зареєстрований в учасника діагноз ПГ протягом періоду спостереження. ПГ було ідентифіковано за допомогою визначень, що мають спеціальні коди, як-то: показник АТ під час фізикального огляду – постуральне падіння (медичний код 2468.00), ортостатична гіпотензія (G870.00), постуральна гіпотензія (G870.11), паркінсонізм з ортостатичною гіпотензією (F130300) (Bhanu et al., 2023).
Статистичний аналіз
Для розрахунку відносної частоти подій (ВЧП), за допомогою яких порівнювалася ймовірність розвитку ПГ у періоди ризику впливу препарату та поза ними, було використано умовну регресію Пуассона. Також проводилося коригування за віком у 5-річних вікових діапазонах: 60‑64, 65‑69, 70‑74, 75‑79, 80‑84, 85‑89, 90‑94 та 95‑99 років.
Результати дослідження
У базі даних IMRD загалом ідентифікували 41 005 (2%) осіб віком ≥60 років із вперше зареєстрованим діагнозом ПГ упродовж періоду спостереження; 19 979 (49%) були чоловіками та 21 026 (51%) – жінками. З-поміж відібраних пацієнтів із ПГ 8313 (20%) мали вперше виписаний рецепт на ТЦА, 8899 (22%) – на СІЗЗС та 4656 (11%) – на інший антидепресант протягом періоду дослідження.
До основних медикаментів групи СІЗЗС, на які були виписані рецепти, належали циталопрам (35%), сертралін (17%) та флуоксетин (20%). При застосуванні СІЗЗС спостерігався більший ризик розвитку ПГ упродовж 1‑28 днів (ВЧП 4,22; 95% довірчий інтервал [ДІ] 3,76‑4,74), що залишався підвищеним, але меншою мірою, протягом 29‑56 днів (ВЧП 2,52; 95% ДІ 2,15‑2,94) та від 57-го дня – до кінця терапії (ВЧП 1,62; 95% ДІ 1,50‑1,77) (таблиця, рисунок). Також вищу ймовірність ПГ було виявлено протягом 90-денного періоду до початку впливу препарату (ВЧП 2,10; 95% ДІ 1,89‑2,29).
|
Таблиця. Відносна частота ПГ, пов’язаної з ТЦА, СІЗЗС та іншими антидепресантами |
|||
|
Референтний період |
Події, n |
Загальна кількість людино-років |
ВЧП (95% ДІ) |
|
ТЦА, n=8313 90-денний період до початку лікування Дні 1‑28 Дні 29‑56 День 57 – кінець лікування |
7356 223 141 81 6303 |
90 318 2014 658 582 72 132 |
1,11 (0,97‑1,27) 2,12 (1,79‑2,50) 1,39 (1,11‑1,73) 1,27 (1,13‑1,43) |
|
СІЗЗС, n=8899 90-денний період до початку лікування Дні 1‑28 Дні 29‑56 День 57 – кінець лікування |
6861 453 302 161 1156 |
87 880 2159 701 632 8367 |
2,10 (1,89‑2,29) 4,22 (3,76‑4,74) 2,52 (2,15‑2,94) 1,62 (1,50‑1,77) |
|
Інший антидепресант, n=4656 90-денний період до початку лікування Дні 1‑28 Дні 29‑56 День 57 – кінець лікування |
3782 258 92 46 478 |
46 941 1137 365 326 4687 |
1,99 (1,75‑2,26) 2,17 (1,76‑2,68) 1,23 (0,92‑1,64) 0,91 (0,81‑1,03) |
Адаптовано за C. Bhanu et al. (2025)
Серед ТЦА більшість призначень (81%) припадало на амітриптилін. Автори відзначили більшу ймовірність розвитку ПГ при використанні ТЦА протягом 1‑28 днів (ВЧП 2,12; 95% ДІ 1,79‑2,50), що залишалася підвищеною, але меншою мірою, протягом 29‑56 днів (ВЧП 1,39; 95% ДІ 1,11‑1,73) та 57 днів – до кінця лікування (ВЧП 1,27; 95% ДІ 1,13‑1,43). Упродовж 90-денного періоду до початку впливу препарату підвищеного ризику виявлено не було (ВЧП 1,11; 95% ДІ 0,97‑1,27) (див. табл. та рис.).
У групі інших антидепресантів більшість призначень припадало на такі препарати, як міртазапін (64%), дулоксетин (12%) та венлафаксин (12%). Протягом 1‑28 днів спостерігався підвищений ризик розвитку ПГ, пов’язаний із даними ліками (ВЧП 2,17; 95% ДІ 1,76‑2,68). Значного збільшення ймовірності ПГ після цього періоду не спостерігалося. Підвищений ризик також був виявлений протягом 90-денного періоду до початку впливу препарату (ВЧП 1,99; 95% ДІ 1,75‑2,26) (див. табл. та рис.).
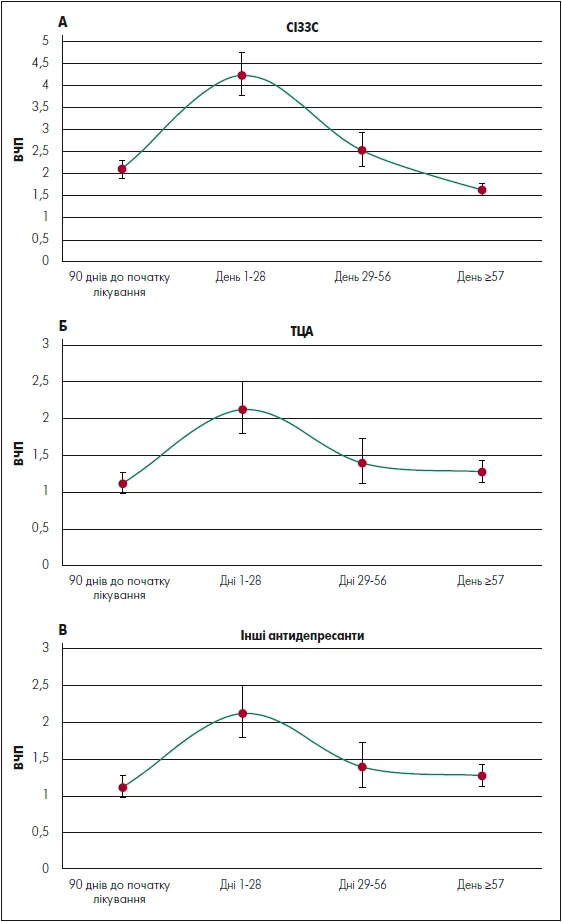 Рисунок. Графіки ВЧП і 95% ДІ у періодах ризику на тлі застосування СІЗЗС (А), ТЦА (Б) та інших антидепресантів (В) для ілюстрації схожих часових тенденцій щодо розвитку ПГ (пік у період ризику із 1-го по 28-й день)
Рисунок. Графіки ВЧП і 95% ДІ у періодах ризику на тлі застосування СІЗЗС (А), ТЦА (Б) та інших антидепресантів (В) для ілюстрації схожих часових тенденцій щодо розвитку ПГ (пік у період ризику із 1-го по 28-й день)
Адаптовано за C. Bhanu et al. (2025)
Обговорення
Підсумки
Аналіз SCCS, присвячений впливу антидепресантів та розвитку ПГ, що охоплював >41 тис. осіб похилого віку (реальна популяція, яка зазвичай не входить цілком до РКД), показав статистично значуще підвищений ризик ПГ протягом перших 28 днів після початку застосування будь-яких антидепресантів. Досліджувані групи включали: ТЦА, СІЗЗС та інші антидепресанти (міртазапін, дулоксетин і венлафаксин). Загалом імовірність розвитку ПГ була найбільшою при використанні СІЗЗС, далі йшли інші антидепресанти та ТЦА. Ризик розвитку ПГ знижувався із 28-го дня в усіх групах. Окрім того, автори виявили статистично значуще зростання ймовірності виникнення ПГ протягом 90-денного періоду до початку приймання СІЗЗС та інших антидепресантів, чого не спостерігалося на тлі лікування ТЦА.
Сильні сторони та обмеження
C. Bhanu et al. (2025) стверджують, що це було перше дослідження, в якому вивчали антидепресанти та ПГ із використанням великої бази даних первинної медичної допомоги, включно зі складною популяцією літніх осіб. Варто відзначити низку суттєвих переваг цього випробування. Так, при аналізі бази даних IMRD стали доступними адекватний розмір вибірки пацієнтів із ПГ та майже повні дані про призначення ліків. Окрім того, РКД зазвичай фокусуються на оцінюванні ефективності, а не побічних явищ препаратів, що потребує набагато більшої кількості учасників. Отже, у багатьох дослідженнях небажані ефекти вивчаються недостатнім чином, зокрема випадки ПГ часто не враховуються або не оцінюються послідовно (Junqueira et al., 2021; Bhanu et al., 2024). До того ж із РКД нерідко виключаються особи похилого віку з поліморбідністю та поліпрагмазією, а також ті, хто отримують низький рівень медичних послуг, тому дані щодо побічних реакцій та потенційної шкоди від лікування можуть бути занижені (Ruiter et al., 2019). Завдяки аналізу SCCS був запропонований дієвий спосіб ретельно вивчити ризик ПГ при застосуванні антидепресантів протягом певних періодів їх впливу в популяції літніх хворих з урахуванням усіх похибок, незмінних із часом.
Були і певні обмеження. Наприклад, у дослідженні не було достатньо великої вибірки для вивчення впливу окремих препаратів чи доз, тому автори оцінювали ефекти за категоріями ліків вищого рівня (підрозділи BNF). Окрім того, деякі рецепти, виписані у закладах первинної медичної допомоги, можуть ніколи не використовуватися. Тож у цьому дослідженні могли бути пацієнти, яким призначили ліки, але вони їх не приймали. Таким чином, оцінка ефекту могла бути дещо неповною. На додаток, частина рецептів могла бути виписана у закладах вторинної медичної допомоги, наприклад, у психіатричних клініках, тож вони не були враховані у базі даних первинної медичної допомоги.
Крім того, дослідники не могли контролювати виникнення нових клінічних станів, зміни тяжкості основного захворювання або вплив інших ліків, незалежно пов’язаних із ПГ. Також було неможливо достеменно встановити, що саме впливало на підвищення ризику розвитку ПГ: показання до лікування (основне захворювання) чи сам препарат. Варто відзначити, що C. Bhanu et al. (2025) спостерігали цікаву закономірність підвищеного ризику ПГ протягом 90-денного періоду до початку застосування СІЗЗС та інших антидепресантів, але не ТЦА. Цей так званий фоновий ризик міг асоціюватися з депресією, що часто незалежно пов’язана із ПГ (Calvi et al., 2021). Своєю чергою поширеними показаннями для призначення ТЦА у Великій Британії є не депресія, а нейропатичний біль, безсоння та мігрень (які не пов’язані незалежно із ПГ) (Coupland et al., 2011).
Точність аналізу SCCS залежить від своєчасної реєстрації гострих подій (Whitaker et al., 2006). Однак у цьому дослідженні міг бути певний часовий проміжок між тим, коли у пацієнта виникла ПГ, та записом у медичну карту про неї сімейного лікаря. Також може існувати певна упередженість, пов’язана із тим, що хворі часто пояснюють симптоми ПГ як побічні явища препарату на початку його приймання, але насправді симптоми виникають пізніше, що було відзначено експертною групою.
Порівняння із наявними даними літератури
C. Bhanu et al. (2025) дійшли несподіваного висновку про те, що приймання СІЗЗС корелювало із найвищою ймовірністю розвитку ПГ, про що свідчило чотириразове зростання ризику ПГ протягом періоду їх впливу із 1-го по 28-й день. СІЗЗС є препаратами першої лінії для лікування депресії в осіб похилого віку і загалом вважаються безпечними та найчастіше призначуваними літнім пацієнтам антидепресантами (Giovannini et al., 2020; Calvi et al., 2021). Нещодавній систематичний огляд РКД показав, що СІЗЗС не були пов’язані з ПГ (Bhanu et al., 2021). Однак ці докази були отримані у випробуваннях із залученням молодшої популяції порівняно з учасниками дослідження, що розглядається (середній вік – 57 та 71 рік відповідно).
R. Briggs et al. (2018) отримали більш узгоджені з роботою C. Bhanu et al. (2025) результати, згідно з якими спостерігався подвоєний ризик ПГ на тлі застосування СІЗЗС. Останні мають механізми дії, які можуть впливати на постуральний АТ, як-то інгібування кальцієвих каналів та вазоконстрикція, а також зниження частоти серцевих скорочень, що інколи посилюються у старших когортах хворих (Lavan et al., 2016).
Є повідомлення, що СІЗЗС викликають ПГ рідше, ніж ТЦА (Rivasi et al, 2020). Проте це може бути пов’язано з тим, що ТЦА зазвичай призначають у вищих дозах для лікування депресії (наразі є менш поширеним у клінічній практиці), а не в нижчих дозах із приводу безсоння та болю (Coupland et al., 2011).
На додачу, чіткою тенденцією для всіх груп антидепресантів у цьому дослідженні стало те, що ризик ПГ був найвищим упродовж перших 1‑28 днів лікування. Це нагадує «феномен першої дози», що вперше був задокументований для блокатора α-адренорецепторів празозину R. M. Graham et al. (1976). Він характеризується тяжкою симптоматичною ПГ, яка зазвичай виникає протягом 90 хв після приймання першої дози. Результати нещодавнього дослідження SCCS, присвяченого вивченню впливу тамсулозину та ПГ, також продемонстрували, що перші вісім тижнів після старту терапії були періодом високого ризику, подібно до представлених у цій статті даних (Bird et al., 2013).
ПГ, спричинена антидепресантами, асоційована із дією кількох нейромедіаторних систем на регуляцію АТ (Calvi et al., 2021). Побічні ефекти антидепресантів зазвичай виникають протягом 2‑4-тижневого «вікна» після початку їх застосування (Kelly et al., 2008). ПГ, зумовлена використанням ліків, також частіше проявляється в осіб похилого віку через відмінності у фармакокінетиці. Метаболічні зміни, пов’язані зі старінням, наприклад, зміни маси печінки та функції нирок, можуть впливати на метаболізм препарату, що призводить до підвищення концентрації у крові. Фармакодинамічна чутливість також інколи зростає у літніх пацієнтів (Gutsmiedl et al., 2020; Berger et al., 2011).
Значення для майбутніх досліджень та клінічної практики
ПГ не зазначена як побічний ефект у BNF та інструкціях із застосування ТЦА або інших антидепресантів і згадується як рідкісне несприятливе явище при лікуванні СІЗЗС (NICE, 2025). C. Bhanu et al. (2025) вважають, що ПГ має бути вказана у застереженнях для літніх осіб та як побічна реакція на ТЦА у фармацевтичних формулярах.
Депресія у похилому віці є поширеним явищем, і часто рішення про призначення антидепресанту приймається ретельно, з урахуванням балансу між ризиком і користю для літнього пацієнта (Frost et al., 2019; Giovannini et al., 2020). Результати представленого дослідження підтверджують безпечне використання антидепресантів за показаннями. Однак автори вважають, що лікарі мають бути добре обізнані про підвищений ризик ПГ до початку лікування антидепресантами, особливо СІЗЗС, у хворих похилого віку. Наприклад, можна розглянути моніторинг ПГ у пацієнтів із високим ризиком, зокрема таких, у кого відзначається значна ймовірність падінь або ризик ПГ з інших причин, як-то супутній цукровий діабет чи хвороба Паркінсона.
У майбутніх клінічних випробуваннях антидепресантів доцільно проводити оцінювання ПГ як частини профілів побічних ефектів. Необхідні подальші дослідження з метою встановити, чи є відмінності в медикаментозно-індукованій ПГ у межах класу препаратів залежно від дози та супутніх захворювань.
Підготувала Олена Коробка
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 1 (76) 2026 р.



