13 січня, 2021
Шлях до біосимілярів при рідкісних захворюваннях – урок на прикладі хвороби Гоше
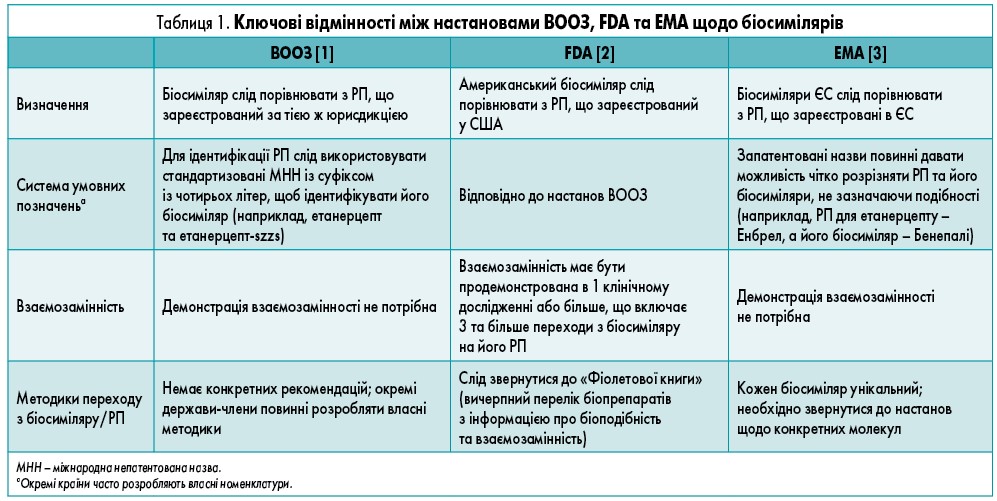
Біосиміляр – це біотерапевтичний засіб, подібний до зареєстрованого референтного препарату (РП) за якістю, безпекою та ефективністю (табл. 1). Термін «біосиміляр» був введений в ужиток для біологічних препаратів, оскільки їх складність унеможливлює виготовлення ідентичної копії. На противагу цьому генерик – це точна копія низькомолекулярного препарату з відомою хімічною структурою та сталою кількістю атомів. Враховуючи те, що термін дії патенту біопрепаратів закінчується, за допомогою біосимілярів можна розширити доступ до лікування та зменшити витрати.
Крім настанов, опублікованих Всесвітньою організацією охорони здоров’я (ВООЗ) [1] у 2009 р., розроблення біоподібних засобів жорстко регулюється Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) [2] та Європейським агентством з лікарських засобів (EMA) [3]. Ці організації вимагають, щоби подібність до РП була продемонстрована шляхом проведення всебічних досліджень порівнянності, у яких підтверджувалися б фармацевтична якість, біологічна активність, безпека (включаючи імуногенність) та ефективність.
У регіонах із ретельним регуляторним наглядом, таких як Європейський Союз (ЄС), США, а нещодавно і в Японії, Канаді та Австралії, розроблення настанов щодо виробництва біосимілярів сприяло збільшенню використання цих препаратів серед співробітників галузі охорони здоров’я. Однак впровадження таких настанов у Латинській Америці, Азії та країнах, що не входять до ЄС, залишається повільним. Історична відсутність регуляторного контролю в цих регіонах призвела до суперечливого схвалення так званих непорівнюваних біотерапевтичних препаратів (НБП), які не відповідають встановленим стандартам для затвердження біосимілярів. У цій статті ми представляємо досвід впровадження НБП у сферу лікування рідкісних захворювань, зокрема хвороби Гоше (ХГ), та розглядаємо більш широке їх значення в лікуванні рідкісних захворювань.
Непорівнювані біотерапевтичні препарати не є біосимілярами
Біосиміляри та НБП можуть відрізнятися від РП за різними важливими структурними й функціональними параметрами, включаючи профіль глікозилювання та чистоту. Однак, на відміну від біосимілярів, затвердження НБП (також відомих як біомімікричні засоби, або призначені копії) зазвичай відбувається за скороченими нормативними шляхами реєстрації, при цьому враховуються обмежені клінічні дані та дані про порівняння з РП. У такій ситуації ці відмінності можуть мати важливі наслідки для ефективності лікарських засобів і безпеки пацієнтів [4]. Наприклад, НБП рекомбінантних еритропоетинів були пов’язані з несприятливими імунологічними ефектами, що призводять до істинної еритроцитарної аплазії [5]. Крім того, тоді як настанови ВООЗ, FDA та EMA щодо біосимілярів вимагають використання унікальної системи іменування, яка дозволяє лікарям розрізняти біосиміляр та його РП (табл. 1), скорочені нормативні шляхи реєстрації НБП можуть дозволити використовувати ту саму міжнародну непатентовану назву (МНН) для НБП та його РП. Це може спричинити плутанину щодо того, які саме лікарські засоби призначають співробітники галузі охорони здоров’я, і призвести до ненавмисної заміни препаратів та неточностей у повідомленнях про небажані явища. Фахівці зі сфери охорони здоров’я та пацієнти, особливо ті, що мають хронічні, прогресуючі захворювання з незворотними ускладненнями, такими як рідкісні генетичні захворювання, повинні знати, що НБП не слід розглядати як біосиміляри РП, якими вони лікуються.
Хвороба Гоше – приклад рідкісного захворювання
Хвороба Гоше – це рідкісна спадкова лізосомна хвороба накопичення, яка уражає 1 людину із 40 000-60 000 (залежно від етнічної належності) [6]. Причиною захворювання є біалельні мутації гена, що кодує лізосомну глюкоцереброзидазу (GBA). ХГ характеризується накопиченням глюкозилцераміду в макрофагах печінки, селезінки та кісткового мозку, що призводить до численних проявів, включаючи гепатоспленомегалію, анемію, тромбоцитопенію, затримку росту та патологію скелета. Існує три типи ХГ; 2 та 3 типи ХГ можна відрізнити від 1 типу за наявністю ураження ЦНС. Хвороба Гоше – прогресуюче захворювання, яке зумовлює віддалені ускладнення, такі як остеонекроз і злоякісні новоутворення. Клінічні та рентгенологічні докази про різноманітні ураження кісток фіксують у більшості пацієнтів навіть за відсутності значних гематологічних і вісцеральних аномалій, що підкреслює гетерогенність проявів ХГ та необхідність тривалого моніторингу.
Хвороба Гоше 1 типу була першим захворюванням, яке успішно почали лікувати за допомогою ферментозамісної терапії (ФЗТ). Спочатку, в 1991 р., – за допомогою глюкоцереброзидази, отриманої з плаценти (алглюцераза, Ceredase®, виробництва компанії «Джензайм Корпорейшн», США), а з 1994 р. – за допомогою рекомбінантної глюкоцереброзидази (іміглюцераза, Церезим® 400 ОД, виробництва компанії «Джензайм Корпорейшн», США1). Окрім препарату Церезим® 400 ОД, на сьогодні доступні два інших препарати ФЗТ для лікування ХГ в США та/або в Європі: ВПРІВ2 (велаглюцераза альфа, виробництва компанії «Шайєр Фармасьютикалз Айленд Лтд», Ірландія, США) та Елелісо3 (таліглюцераза альфа, виробництва компанії «Пфайзер Ейч.Сі.Пі. Корпорейшн», США). Наявні також два низькомолекулярні препарати субстрат-редукуючої терапії: Cerdelga® (еліглюстат, виробництва «Джензайм Корпорейшн», США) та Zaveska® (міглустат, виробництва компанії Actelion Pharmaceuticals, США).
Для ефективності ФЗТ при ХГ потрібен селективний, опосередкований манозними рецепторами ендоцитоз ферменту клітинами-мішенями. Таке селективне поглинання правильними клітинами залежить від вуглеводного профілю ферменту. Глюкоцереброзидаза – це глікопротеїн, що має чотири ковалентно зв’язані олігосахаридні ланцюги, приєднані до бічних амінокислотних ланцюгів, з яких один олігосахарид є олігоманозою. Терапевтичне таргетування рекомбінантної GBA на наповнені глюкозилцерамідом макрофаги залежить від рецептор-опосередкованого ендоцитозу через ці термінальні залишки манози. Однак GBA має й інші термінальні вуглеводні залишки, які розпізнають рецептори на інших типах клітин. Отже, з терапевтичної точки зору, відносний вміст термінальних залишків манози є важливою характеристикою якості ферменту, що визначає зв’язок між його структурою та функцією, а також потенційно модулює ефективність ФЗТ. На профіль глікозилювання рекомбінантних білків можуть впливати аспекти виробничого процесу (наприклад, клітинна лінія, в якій виробляється білок), деякі з яких призначені для модифікації таргетної доставки білка і тому є запатентованими [7]. Це враховується для затвердження біосимілярів, однак не враховується для затвердження НБП.
Окрім наявних нині препаратів ФЗТ для лікування ХГ ще три препарати ФЗТ були затверджені за межами США/ЄС із МНН іміглюцераза:
- Abcertin® (виробництва компанії ISU Abxis, Південна Корея) на сьогодні зареєстрований для використання в таких країнах, як Південна Корея, Іран, Болівія та Казахстан на основі регуляторних шляхів реєстрації, що не відповідають вимогам ВООЗ щодо розроблення/затвердження біосиміляру (табл. 2);
- Asbroder™ затверджений як засіб для лікування орфанних захворювань у Мексиці. Про препарат Asbroder™ немає жодних публікацій у науковій літературі, як і інформації про клінічні дослідження, однак діюча речовина як для препарату Asbroder™, так і для препарату Abcertin® виробляється компанією ISU Abxis. Незважаючи на використання однакової з препаратом Церезим® 400 ОД МНН, Asbroder™ не відповідає визначенню біосиміляру згідно з ВООЗ [8];
- Glurazyme® (виробництва компанії Generium Pharmaceutical, РФ) нещодавно був затверджений у Росії відповідно до місцевих положень щодо біосимілярів і тому вважається взаємозамінним із його РП в РФ. Однак дані щодо цього продукту не опубліковано та не представлено.
Abcertin® був спочатку затверджений у Південній Кореї в 2012 р. згідно з національним регуляторним шляхом реєстрації, який дозволяв подавати дані III фази вже після затвердження, а також не відповідав шляхам затвердження біосимілярів та інших засобів для лікування орфанних захворювань. Препарат було затверджено на основі результатів трьох клінічних досліджень: 5-денного подвійного сліпого плацебо-контрольованого дослідження з підвищенням дози I фази за участю 24 здорових добровольців (NCT01881633); 24-тижневого проспективного відкритого дослідження з переходом (switch-over study) II фази за участю одного дорослого і чотирьох дітей/підлітків з підтвердженою ХГ 1 типу, які раніше отримували лікарський засіб Церезим® 400 ОД; і 24-тижневого постреєстраційного дослідження III фази за участю 7 дітей, які раніше не отримували лікування, з ХГ 1 типу. Дослідження, що забезпечують пряме порівняння з РП – препаратом Церезим® 400 ОД – фізико-хімічні, імунологічні або структурні дані, не представлені. Дослідження III фази, у яких би прямо порівнювали препарати Abcertin® і Церезим® 400 ОД (NCT01161914), було скасовано ще до набору добровольців.
Автори дослідження II фази спочатку називали Abcertin® біосиміляром для лікарського засобу Церезим® 400 ОД [9]. Хоча відтоді вони змінили позиціонування препарату в поправці до своєї першої публікації, плутанина щодо точної природи препарату Abcertin® може зберігатися [10]. Це частково спричинене тим, що інструкція для медичного застосування цього засобу містить дані з безпеки й ефективності клінічних досліджень лікарського засобу Церезим® 400 ОД. У ній не вказано, що досвід не базується на клінічному застосуванні препарату Abcertin®, і частково тому, що виробник прийняв МНН іміглюцераза без дотримання настанов ВООЗ щодо іменування.
Як результат – працівники галузі охорони здоров’я та пацієнти можуть бути введені в оману, вважаючи, що різні препарати ФЗТ, які мають однакову МНН (в цьому випадку – іміглюцераза), є однаковими або біоподібними, такими, що характеризуються еквівалентними ефективністю та безпекою, а також що вони взаємозамінні. Потенційні наслідки можуть включати ненавмисний перехід і заміну одного препарату іншим, що спричиняє труднощі при оцінюванні профілю безпеки та створює ризик неточностей у повідомленнях про небажані явища для кожного препарату. Крім того, з огляду на прогресуючий характер захворювання, потенційні відмінності в клінічній користі для пацієнта можуть бути помітні лише після тривалого періоду лікування, особливо при ураженнях кісток.
Обговорення та заклик до дії
Недавній досвід затвердження для лікування ХГ НБП, які використовують ту саму МНН, спонукає до міркувань, які слід враховувати під час розроблення, отримання дозволу на реєстрацію та використання біосимілярів для лікування рідкісних захворювань (табл. 2). По-перше, існує невелика кількість генотипово та фенотипово відмінних пацієнтів, що мають такі рідкісні захворювання, як ХГ. Отже, клінічні дослідження повинні бути ретельно сплановані, щоб надати достатньо порівнянних даних для біосиміляру та його РП відповідно до настанов EMA, FDA або ВООЗ. По-друге, як і багато рідкісних захворювань, ХГ є хронічним прогресуючим захворюванням, яке може призвести до низки віддалених незворотних ускладнень, якщо не лікувати його оптимальним чином. Систематичний тривалий збір реальних доказів, який проводиться на основі Реєстру пацієнтів з хворобою Гоше Міжнародної об’єднаної групи з питань хвороби Гоше (ICGG), продовжує висвітлювати природний перебіг цієї хвороби. Реєстр також покращив розуміння віддаленої ефективності терапії. Тривалий збір реальних даних має бути обов’язковим для будь-якого лікарського засобу, розробленого для лікування рідкісних захворювань. По-третє, профілі глікозилювання повинні бути повністю охарактеризовані для всіх біопрепаратів, оскільки це може впливати на їхню імуногенність, ефективність, специфічну активність та біорозподіл [7]. Додатковим критичним фактором є використання унікального ідентифікатора іменування, який дає змогу розрізняти біологічні продукти для забезпечення відстежуваності, щоб уникнути плутанини на рівні призначення та відпуску, а також серед пацієнтів.
Існує нагальна потреба в удосконаленні навчання та підвищенні рівня обізнаності працівників галузі охорони здоров’я, котрі займаються лікуванням рідкісних захворювань, і пацієнтів із рідкісними захворюваннями щодо відмінностей між РП, біосимілярами та НБП, включаючи нормативні вимоги, термінологію та вимоги щодо тривалого моніторингу. Відповідальність за це лежить на промисловості, медичних товариствах/установах і групах захисту прав пацієнтів. Лікарі повинні пильно стежити за джерелами інформації про лікарські засоби та забезпечувати відповідність методів лікування пацієнтів світовим стандартам. Усі зацікавлені сторони, включаючи постачальників медичних послуг, пацієнтів, регуляторні органи та промисловість, мають надавати інформацію щодо встановлення та перегляду державної політики стосовно біосимілярів.
Регуляторні органи повинні наполягати на використанні прозорого маркування продукції та унікальної номенклатури для біопрепаратів, а також впроваджувати тривалий моніторинг ефективності та звітування з безпеки через бази даних спостережень і фармаконагляду. Виробники біосимілярів несуть відповідальність за надання та публікацію високоякісних даних, які демонструють схожість між пропонованим біосиміляром і його РП, а також забезпечують тривалий збір даних про реальну безпеку та ефективність. Без цього нагляду подальше впровадження НБП та/або використання тієї самої МНН може призвести до ризику інвалідизації, погіршення якості життя та, зрештою, збільшення витрат на лікування вразливих груп пацієнтів, у тому числі з прогресуючими рідкісними захворюваннями.
Таким чином, послідовне прийняття глобальних регуляторних стандартів (ВООЗ, FDA або EMA), включаючи унікальне найменування, терміново необхідне в усіх країнах для всіх без винятку біопрепаратів. Це потрібно для того, щоб усі НБП насправді були біосимілярами. Специфіка рідкісних захворювань та унікальні проблеми, пов’язані з розробленням біологічних засобів для лікування орфанних захворювань, можуть свідчити про необхідність створення конкретних настанов для біосимілярів щодо лікування рідкісних захворювань.
Література
- World Health Organization. Regulatory Expectations and Risk Assessment for Biotherapeutic Products 2014. https://www.who.int/biologicals/WHO_Risk_Assessment_for_Biotherapeutics_1st_PC_24_Jan_2014.pdf. Accessed June 2019.
- United States Food and Drug Administration. Scientific Considerations in Demonstrating Biosimilarity to a Reference Product Guidance for Industry 2015. https://www.fda.gov/media/82647/download. Accessed June 2019.
- European Medicines Agency Committee for Medicinal Products for Human Use (CHMP).CHMP/437/04 Rev 1. Guideline on similar biological medicinal products 2014. https://www.ema.europa.eu/en/documents/scientific-guideline/guideline-similar-biological-medicinal-products-rev1_en.pdf. Accessed June 2019.
- International Federation of Pharmaceutical Manufacturers & Associations. IFPMA policy statement on non-comparable biotherapeutic products 2014. https://www.ifpma.org/wp-content/uploads/2016/02/Non-comparable_Biotherapeutic_Products__English__02.pdf. Accessed June 2019.
- Ebbers H.C., Crow S.A., Vulto A.G., Schellekens H. Interchangeability, immunogenicity and biosimilars. Nat Biotechnol. 2012; 30: 1186-1190.
- Valle D., Beaudet A.L., Vogelstein B. et al. The Online Metabolic and Molecular Bases of Inherited Disease. New York: McGraw Hill Companies Inc; 2018: 146.
- Sola R.J., Griebenow K. Glycosylation of therapeutic proteins: an effective strategy to optimize efficacy. BioDrugs. 2010; 24: 9-21.
- Castaneda-Hernandez G., Carbajal-Rodriguez L., Ceron-Rodriguez M. et al. Are there biosimilar orphan drugs for Gaucher disease? An overview in Mexico. GaBiJ. 2019; 8: 1-5.
- Lee B.H., Abdalla A.F., Choi J.H. et al. A multicenter, open-label, phase III study of Abcertin in Gaucher disease. Medicine. 2017; 96: e8492.
- Choi J.H., Lee B.H., Ko J.M. et al. Erratum: A phase 2 multi-center, open-label, switch-over trial to evaluate the safety and efficacy of Abcertin® in patients with type 1 Gaucher disease. JKorean MedSci. 2015; 30: 1373.
- Drelichman G. et al. The road to biosimilars in rare diseases – ongoing lessons from Gaucher disease. Am J Hematol, 2019;1-5.Wileyonlinelibrary.com/journal/ajh.
https://doi.org/10.1002/ajh.25701.
1Лікарський засіб Церезим® 400 ОД, порошок для приготування концентрату для розчину для інфузій по 400 ОД, зареєстрований в Україні. Р.П. № UA/8659/01/02. Наказ МОЗ № 2205 від 31.10.2019.
2Лікарський засіб ВПРІВ, порошок для розчину для інфузій по 400 ОД, зареєстрований в Україні. Р.П. UA/15706/01/01. Наказ МОЗ № 1194 від 29.05.2019.
3Лікарський засіб Елелісо, порошок ліофілізований для розчину для інфузій по 200 ОД, зареєстрований в Україні. Р.П. UA/14379/01/01. Наказ МОЗ № 91 від 17.01.2020.
Стаття надрукована за підтримки ТОВ «Санофі-Авентіс Україна».
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (67) 2020 р.