30 травня, 2021
Гормоночутливий рак грудної залози у молодих жінок – тактика лікування

Рак грудної залози (РГЗ) є найпоширенішим онкологічним захворюванням у жінок у світі. Зокрема, за 2018 р. було виявлено 2,1 млн нових випадків РГЗ. Естроген-рецепторпозитивний (ER+) люмінальний РГЗ є другою за частотою причиною смерті молодих жінок від онкологічних захворювань (GLOBOCAN, 2019). Поширеність РГЗ у жінок віком до 40 років сягає 6,5%, тоді як у молодших 30 років – 0,6%. Оскільки ризик розвитку РГЗ у жінок молодого віку є занадто низьким для того, щоб запроваджувати програми скринінгу в цій віковій групі, часто РГЗ виявляють вже на пізніх стадіях (W. Han et al., 2010). Особливостями РГЗ у молодих жінок є високий ризик і швидкий розвиток місцевого рецидиву, високий ризик смерті після локального рецидиву, розвитку раку другої молочної залози та складний взаємозв’язок між ендокринною й імунною системами. Крім цього, молоді жінки більшою мірою страждають не лише фізично, а й емоційно, рідше дотримуються режиму ендокринної терапії. Під час лікування РГЗ у молодих жінок необхідно враховувати їх спосіб життя та потенційні проблеми із фертильністю.
 У рамках вебінару, присвяченого гормоночутливому РГЗ у молодих жінок, експерт МОЗ України за спеціальністю «Онкологія», завідувач кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктор медичних наук, професор Олексій Олексійович Ковальов розповів про сучасні можливості лікування пацієнток з ER+/HER2- РГЗ у пременопаузі.
У рамках вебінару, присвяченого гормоночутливому РГЗ у молодих жінок, експерт МОЗ України за спеціальністю «Онкологія», завідувач кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктор медичних наук, професор Олексій Олексійович Ковальов розповів про сучасні можливості лікування пацієнток з ER+/HER2- РГЗ у пременопаузі.
– ER+ РГЗ є хронічним рецидивуючим захворюванням із найбільшим ризиком розвитку рецидиву у перші 5 років, який, втім, в окремих пацієнток зберігається і впродовж 20 років. Імовірність рецидиву та в подальшому смерті складає приблизно 5-10% у хворих із І стадією, 15‑20% – ІІ стадією та 50% – із ІІІ стадією раку. У 5-10% повторно діагностованих випадків метастатичного РГЗ (мРГЗ) має місце захворювання de novo.
Відомою є імуногістохімічна гетерогенність РГЗ. Зокрема, найчастіше, а саме у 80% випадків, зустрічається ER+ РГЗ, у 60% випадків – ER+ та прогестеронпозитивний (PG+), у 13% – ER+/PG-, а близько 2% становить ER-/PG+ РГЗ, хоча існування такої комбінації є суперечливим та потребує додаткового вивчення.
РГЗ – гетерогенна пухлина з молекулярно-генетичної точки зору, що було продемонстровано Charles M. Perou та співавт., які у 2000 р. запропонували першу молекулярно-генетичну класифікацію РГЗ. Окрім цього, у ході прогресування ER+ РГЗ може змінювати свої біологічні характеристики.
Клінічний випадок
Пацієнтка 59 років. Діагноз: ER+/HER2- рак грудної залози.
Через 2 роки після встановлення діагнозу було виявлено новоутворення в лівій легені. Обстеження дало змогу визначити такі характеристики пухлини: ER-/HER2-/хромогранін +. Встановлено діагноз карциноїд. Ще через 1 рік виявлено множинне ураження печінки метастазами РГЗ, при цьому тканина пухлини мала такі характеристики: ER-/хромогранін -/HER2+++ (T. Foukalis et al., 2012).
Отже, нестабільність рецепторів РГЗ при його прогресуванні потребує проведення повторних біопсій пухлини та унеможливлює використання архівних матеріалів для прийняття клінічних рішень.
Актуальною проблемою залишається розвиток гормонорезистентності у пацієнток з РГЗ. Виділяють первинну (прогресування впродовж перших 2 років ад’ювантної гормонотерапії (АГ) або впродовж перших 6 міс гормонотерапії 1-ї лінії з приводу мРГЗ) та вторинну (прогресування через 2 роки після АГ або після 12 міс гормонотерапії 1-ї лінії з приводу мРГЗ) резистентність ER+ РГЗ (F. Cardoso et al., 2020).
Причини гормонорезистентності ER+ РГЗ є різними. Важливо розрізняти резистентність до окремого препарату (може розвиватися при розладах метаболізму естрогену, модифікації стероїдних рецепторів, порушенні фосфорилювання та низькій експресії ER тощо) від істинної резистентності, яка виникає при порушенні регуляції клітинного циклу.
У нормі клітина має обмежену кількість клітинних циклів. Порушення ліміту поділу (ліміту Хейфліка) є однією з 10 ознак ракової клітини (D. Hanahan, R.A. Weinberg, 2011). Ключову роль в управлінні поділом клітини відіграє особливий клас білків – цикліни. Цикліни активуються факторами росту й естрогенами, утворюють комплекси з циклінзалежними кіназами (CDK4 і CDK6) та активують їх. Активований комплекс циклін D1/CDK 4/6 фосфорилює білок Rb (супресор), що стимулює прогресію клітинного циклу та перехід клітини із фази G1 у фазу S. Висока експресія генів циклінів характерна для багатьох видів раку (L. Hartwell, T. Hunt, P. Nurse, 2001). Мутації або ампліфікації «стартового» гена призводять до надмірної експресії білка цикліну D1, що прискорює прогресію клітинного циклу та поділ клітини. Тому цикліни стали мішенню для протипухлинної терапії (C. Bai et al., 1994). Так, механізм дії інгібіторів CDK 4/6 (іCDK 4/6) полягає у зупинці клітини у фазі G1, інгібуванні Rb, епітеліально-мезенхімального переходу та проліферації, модуляції імунної системи (за рахунок продукції інтерферону ІІІ, зниження проліферації Treg та стимуляції проліферації NK), а також синергічній протипухлинній активності з інгібіторами фосфоінозитид 3-кінази (РІ3К; D. Fry, P. Toogood, 2014).
Історично для лікування мРГЗ ER+/HER2- використовували антиестрогени й інгібітори ароматази, а медіана виживаності таких пацієнтів у ХХ столітті становила від 16 до 20 міс. Поворотним моментом у лікуванні мРГЗ стало впровадження інгібіторів CDK 4/6 та mTOR, яке різко збільшило виживаність хворих і зумовило необхідність перегляду алгоритмів лікування ER+ РГЗ.
У дослідженні MONALEESA‑2, яке включало 668 раніше не лікованих пацієнток у постменопаузі із ER+/HER2- РГЗ, порівнювали застосування комбінації рибоциклібу у дозі 600 мг/добу та летрозолу у дозі 2,5 мг/добу із монотерапією летрозолом 2,5 мг/добу (летрозол + плацебо). Згідно з отриманими результатами, додавання рибоциклібу дозволило збільшити виживаність без прогресування (ВБП) до 25,3 міс, в той час як у контрольній групі цей показник дорівнював 16 міс (рис. 1; G.N. Hortobagyi et al., 2018). Медіана загальної виживаності (ЗВ) сягала 33 міс у групі плацебо + летрозол, а у групі рибоциклібу досягнута не була. Варто зауважити, що ефективність рибоциклібу не залежала від локалізації метастазів і віку хворих (рис. 2А, Б; G.S. Sonke et al., 2018).
 Рис. 1. Розрахунок ВБП за оцінкою дослідника за методом Каплана – Маєра
Рис. 1. Розрахунок ВБП за оцінкою дослідника за методом Каплана – Маєра
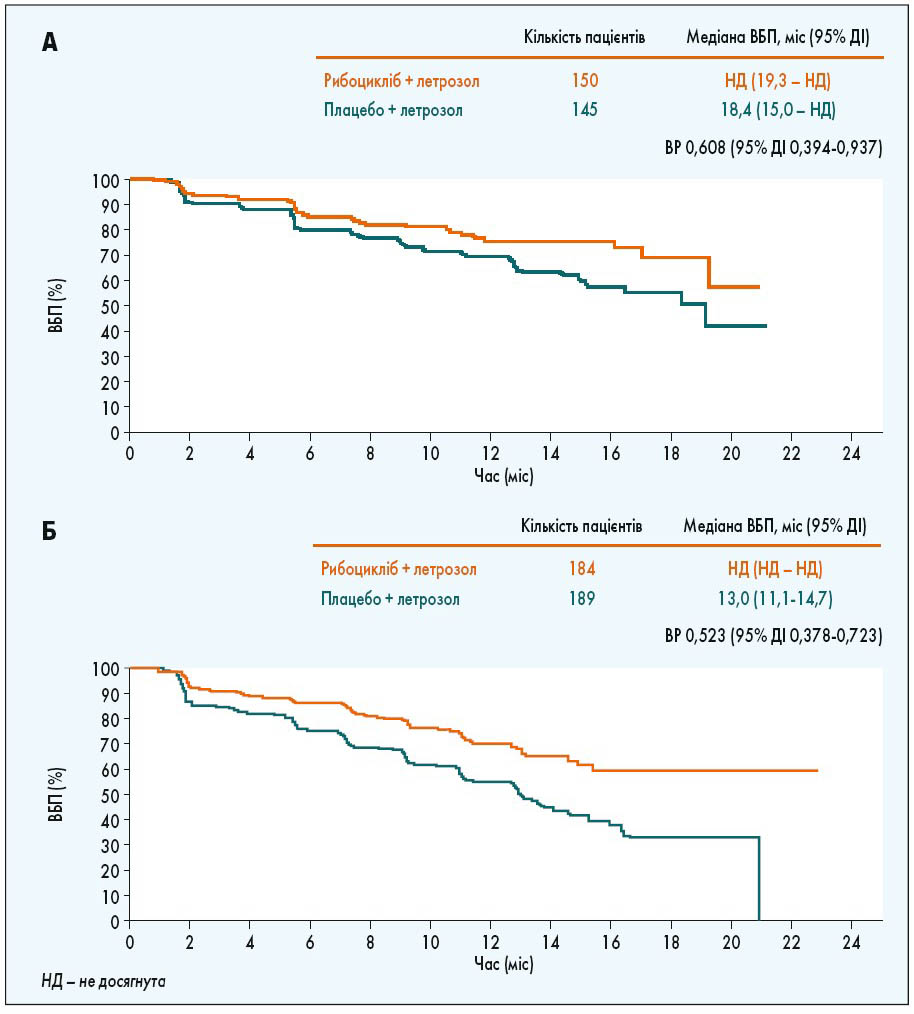 Рис. 2. Розрахунок ВБП за методом Каплана – Маєра у групах хворих віком ≥65 років (А) та ≤65 років (Б)
Рис. 2. Розрахунок ВБП за методом Каплана – Маєра у групах хворих віком ≥65 років (А) та ≤65 років (Б)
Наступним стало дослідження ІІІ фази MONALEESA‑3. У ньому оцінювали ефективність рибоциклібу 600 мг/добу у поєднанні з фулвестрантом 500 мг у жінок у постменопаузі та чоловіків із ER+/HER2- РГЗ, які раніше не отримували або пройшли не більше одного курсу ендокринної терапії (ЕТ). Першу лінію лікування призначали пацієнтам із рецидивом через >12 міс після завершення ад’ювантної ендокринної терапії (АЕТ) або із РГЗ IV стадії без попередньої ЕТ, а 2-гу – особам із рецидивом через >12 міс після завершення АЕТ, або із рецидивом через >12 міс після АЕТ із наступною 1-ю лінією ЕТ з приводу поширеної стадії, або РГЗ IV стадії з прогресуванням після 1-ї лінії ЕТ (антиестрогени/інгібітори ароматази). Загалом було включено та рандомізовано на 2 групи (у співвідношенні 2:1) 726 пацієнтів. Особливістю цього дослідження було включення жінок у пременопаузі та чоловіків (вік хворих варіював від 31 до 89 років).
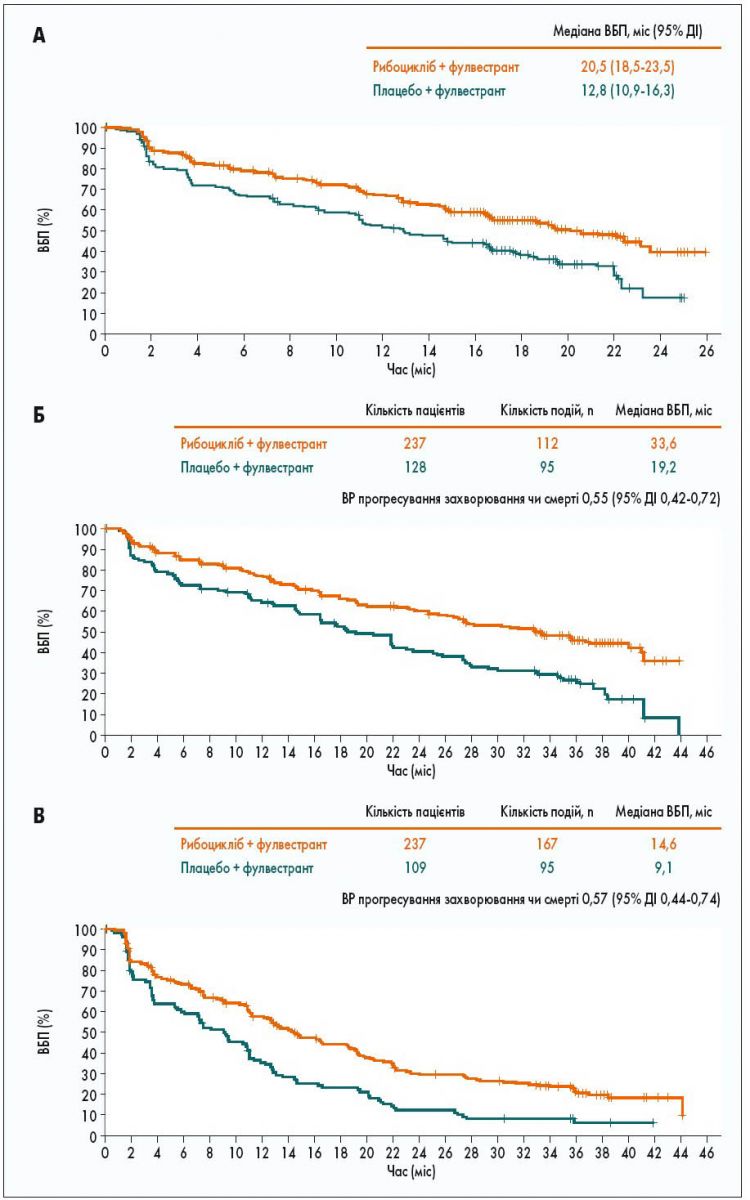
Згідно з отриманими результатами, ВБП значно покращилась у пацієнтів, які отримували рибоцикліб з фулвестрантом, порівняно з контрольною групою: медіана ВБП склала 20,5 та 12,8 міс відповідно (відносний ризик – ВР – 0,593; 95% довірчий інтервал – ДІ – 0,480-0,732; p<0,001; рис. 3А). Аналогічні результати отримані при оцінюванні ефективності терапії у підгрупах. Так, у пацієнтів, яким проводили 1-шу лінію терапії, медіана ВБП становила 33,6 міс (95% ДІ 27,1-41,3) у групі рибоциклібу та 19,2 міс (95% ДІ 14,9-23,6) у групі плацебо (рис. 3Б). Покращення ВБП вдалося досягти й у хворих із раннім рецидивом та тих, які отримували 2-гу лінію лікування (рис. 3В; D.J. Slamon et al., 2019).
Рис. 3. Розрахунок ВБП за методом Каплана – Маєра: за оцінкою дослідника (А); у групі хворих, які отримували 1-шу лінію терапії (Б); у групі пацієнтів із раннім рецидивом або тих, які отримували 2-гу лінію терапії (В)
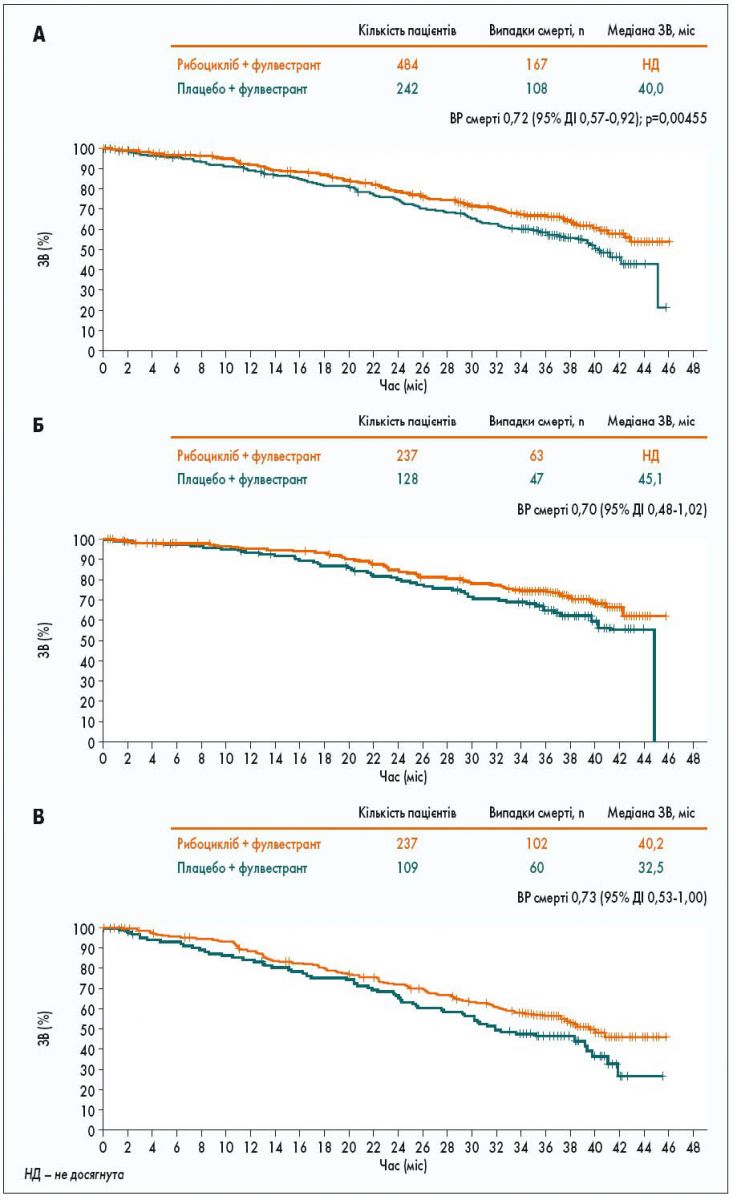
Застосування рибоциклібу з фулвестрантом дозволило збільшити ЗВ пацієнтів, про що свідчило зменшення ризику смерті на 28% (ВР 0,72; 95% ДІ 0,57-0,92; p=0,00455) порівняно з контрольною групою. ЗВ через 42 міс становила 57,8% (95% ДІ 52,0-63,2) у групі рибоциклібу та 45,9% (95% ДІ 36,9-54,5) у групі плацебо (рис. 4А). ЗВ при застосуванні рибоциклібу у 1-й лінії терапії досягнута не була, у 2-й сягала 40,2 міс, тоді як у групі плацебо медіана ЗВ складала 45,1 та 32,5 міс відповідно (рис. 4Б, В).
Рис. 4. Розрахунок ЗВ за методом Каплана – Маєра: загальний показник (А); у групі пацієнтів, які отримували 1-шу лінію терапії (Б); у групі пацієнтів, які отримували 2-гу лінію терапії (В)
При оцінюванні профілю безпеки найчастішими побічними реакціями 3-4 ступеня при застосуванні рибоциклібу були нейтропенія, подовження інтервалу Q-T та гепатотоксичність. Враховуючи можливий розвиток подовження інтервалу Q-T при призначенні рибоциклібу, було запропоновано забезпечувати пацієнтів портативними апаратами ЕКГ для можливості самостійного його моніторингу. Варто зауважити, що ефективність рибоциклібу не знижувалась при редукції дози.
Згідно з рекомендаціями Національної онкологічної мережі США (2020), комбінація рибоциклібу з інгібіторами ароматази та рибоциклібу з фулвестрантом є пріоритетними режимами 1-ї лінії лікування ER+/HER2- мРГЗ.
Отже, завдяки покращенню ЗВ, ВБП і якості життя хворих, іCDK 4/6 у поєднанні з ЕТ є стандартом лікування пацієнтів з ER+/HER2- РГЗ. Інгібітори CDK 4/6 у комбінації з інгібіторами ароматази/фулвестрантом застосовують при мРГЗ de novo, первинній чи вторинній резистентності, у жінок у постменопаузі, а також у жінок у пременопаузі та чоловіків у поєднанні з агоністами лютеїнізуючого гормону. Більшість експертів надає перевагу призначенню інгібіторів CDK 4/6 у 1-й лінії, проте існує невелика група пацієнтів із обмеженим метастатичним навантаженням та менш агресивною біологією пухлини, у яких можна використовувати лише ЕТ (F. Cardoso et al., 2020).
Загалом застосування іCDK 4/6 в 1-й лінії має переваги у всіх групах пацієнтів з ER+/HER2- РГЗ, крім рибоциклібу, ефективність якого не залежить від локалізації метастазів; дещо гірший прогноз спостерігається у пацієнтів із метастазами в печінці. Прогноз також може бути гіршим у пацієнтів із низькодиференційованою пухлиною (G3), PG- РГЗ та при короткому інтервалі до розвитку рецидиву. За наявності лише кісткових метастазів при високому рівні ECOG та тривалому безрецидивному періоді прогноз є сприятливішим.
Коли краще використовувати іCDK 4/6 – в 1-й чи 2-й лінії лікування? Якою є оптимальна комбінація іCDK 4/6? Ці питання наразі залишаються не вирішеними. Також на сьогодні не існує біомаркерів, що дозволили б ідентифікувати пацієнтів, для яких лікування було б найбільш ефективним, адже валідність наявних предиктивних маркерів не доведена. Окрім цього, актуальною залишається проблема резистентності до іCDK 4/6. Щодо застосування іCDK 4/6 у поєднанні з ЕТ як підтримуючої терапії після хіміотерапії, то даних, які підтвердили б ефективність такої комбінації, немає, тому з цією метою рекомендовано проводити лише ЕТ. Можливість використання іCDK 4/6 в (нео)ад’ювантному режимі поки вивчається.
Кіскалі (рибоцикліб) – єдиний іCDK 4/6, що забезпечує доведене збільшення тривалості життя пацієнток із ER+/HER2- мРГЗ. Клінічна ефективність препарату Кіскалі (рибоциклібу) в пацієнток у пре- та менопаузі в комбінації із різними гормональними препаратами при гормоночутливому та гормонорезистентному РГЗ була доведена у трьох рандомізованих дослідженнях. Кіскалі (рибоцикліб) значно покращив ЗВ у двох дослідженнях ІІІ фази, знижуючи ризик смерті приблизно на 30%. Терапія препаратом Кіскалі (рибоциклібом) дозволяла відкласти початок хіміотерапії, а також покращувала або зберігала якість життя пацієнтів (D.J. Slamon et al., 2019; S.A. Im et al., 2019).
Підготувала Ольга Нестеровська
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 2 (69) 2021 р.