24 липня, 2020
Лапатиніб та терапія після лапатинібу у пацієнтів, які отримували лікування з приводу HER2-позитивного метастатичного раку молочної залози

Результати багатоцентрового ретроспективного дослідження
Лапатиніб застосовується у лікуванні HER2-позитивного метастатичного раку молочної залози (МРМЗ). Ампліфікація експресії HER2 відбувається у 20-25% хворих на рак молочної залози та асоційована з поганим прогнозом [1]. Комбінація трастузумабу з лапатинібом (HL) характеризується вираженим синергічним впливом препаратів [2, 3], що дозволяє досягти кращого клінічного ефекту, ніж при монотерапії лапатинібом [4]. Результатами досліджень було встановлено, що продовження терапії трастузумабом після прогресування захворювання супроводжувалося вищою ефективністю лікування. Цей ефект пояснювався антитілозалежною клітинно-опосередкованою цитотоксичністю трастузумабу [5, 6]. Лапатиніб має інший механізм дії, для нього не характерна антитілозалежна клітинно-опосередкована цитотоксичність. Виникає запитання: чи буде ефективним продовження лікування лапатинібом? Доказова база щодо терапії лапатинібом після прогресування захворювання все ще відсутня.
Метою дослідження було визначити ефективність та безпеку комбінації лапатинібу з капецитабіном (LX) та HL з хіміотерапією (HLC) у хворих, які раніше отримували лікування трастузумабом і таксанами, а також окреслити план лікування пацієнтів з прогресуванням захворювання після терапії лапатинібом у клінічній практиці.
Матеріали та методи. Ретроспективно проаналізовано дані пацієнтів з HER2‑позитивним МРМЗ, які отримували лікування у п’яти лікарнях Китаю протягом 2015‑2019 рр. Попереднє лікування включало таксани та трастузумаб. Хворі отримували лапатиніб (1250 мг/добу) з капецитабіном (2000 мг/м2 площі поверхні тіла) або лапатиніб (750‑1250 мг/добу) з трастузумабом (6 мг/кг після навантажувальної дози 8 мг/кг) та з одним із режимів хіміотерапії (капецитабін, препарати платини тощо). Основним критерієм оцінювання результату була виживаність без прогресування. Оцінювали також загальну виживаність, безпеку, ефективність лікування після прогресування захворювання.
Результати. Загалом у дослідження включено дані 242 хворих. Терапія за схемою LX проведена у 164 (68%) пацієнтів, HLC – у 78 (32%). Більшість хворих отримували хірургічне лікування; встановлена de novo IV стадія була у 15% випадків. Гістологічно у 85% пацієнток була протокова карцинома, у 10% – часточкова карцинома, у 5% – інший гістотип пухлини. Вісцеральне метастатичне ураження спостерігалось у 72% хворих групи LX та 73% групи HLC. Рефрактерність до трастузумабу була більш характерною, ніж резистентність. Загалом групи LX та HLC істотно не відрізнялися за базовими характеристиками хворих (вік, тривалість безрецидивного періоду, статус естрогенових рецепторів, наявність вісцерального метастатичного ураження, резистентність до трастузумабу).
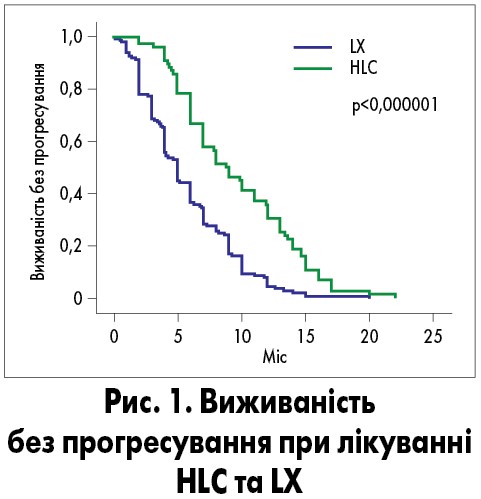 Ефективність лікування. Медіана спостереження становила 21 міс. Комбінація HLC забезпечувала статистично значуще покращення виживаності без прогресування порівняно з LX (відносний ризик – ВР – 0,44; 95% довірчий інтервал – ДІ – 0,33-0,59; р<0,0000001; рис. 1). Медіана виживаності без прогресування становила 5 міс у групі LX та 8,8 міс у групі HLC. Медіана загальної виживаності на момент аналізу не була досягнута.
Ефективність лікування. Медіана спостереження становила 21 міс. Комбінація HLC забезпечувала статистично значуще покращення виживаності без прогресування порівняно з LX (відносний ризик – ВР – 0,44; 95% довірчий інтервал – ДІ – 0,33-0,59; р<0,0000001; рис. 1). Медіана виживаності без прогресування становила 5 міс у групі LX та 8,8 міс у групі HLC. Медіана загальної виживаності на момент аналізу не була досягнута.
За наявності резистентності до трастузумабу медіана виживаності без прогресування становила 4 міс у групі LX та 11 міс у групі HLC (ВР 0,26; 95% ДІ 0,12-0,54; р=0,00032). Аналогічні показники у хворих із рефрактерністю до трастузумабу становили 5 і 8 міс відповідно (ВР 0,51; 95% ДІ 0,36-0,71; р=0,000056; рис. 2).
При аналізі даних підгруп було виявлено, що перевага схеми HLC над LX спостерігалась майже у всіх випадках, за винятком групи пацієнток віком старше 60 років, у яких ефективність обох схем лікування була майже однаковою. Відповідні показники медіани виживаності без прогресування становили 6 і 7 міс (р=0,11).
 Рис. 2. Виживаність без прогресування при лікуванні HLC та LX хворих із резистентністю до трастузумабу (А) та рефрактерністю до трастузумабу (Б)
Рис. 2. Виживаність без прогресування при лікуванні HLC та LX хворих із резистентністю до трастузумабу (А) та рефрактерністю до трастузумабу (Б)
За результатами однофакторного аналізу, терапія HLC (ВР 0,44; 95% ДІ 0,33-0,59; р<0,0000001) та попередня кількість ліній терапії МРМЗ <3 (ВР 0,65; 95% ДІ 0,49-0,89; р=0,005) були предикторами більш тривалого безрецидивного періоду. Багатофакторний аналіз дав змогу виявити, що ці самі позиції (ВР 0,42; 95% ДІ 0,31-0,57; р<0,0000001; ВР 0,6; 95% ДІ 0,44-0,81; р=0,001) є незалежними прогностичними факторами зниження ризику прогресування захворювання.
Безпека. Загалом як схема терапії HLC, так і LX добре переносились пацієнтами. Частота побічних явищ 3 і 4 ступенів тяжкості становила 16,5% у групі LX та 21,8% у групі HLC (р=0,57). При лікуванні за схемою LX виникали такі небажані явища, як діарея (5,5%), нейтропенія (6,7%), лейкопенія (6,1%), пальмарно-плантарний синдром еритродизестезії (3%). Відповідні дані у групі HLC були такими: нейтропенія (11,5%), лейкопенія (11,5%), діарея (7,7%), блювання (3,8%). Жодного летального випадку внаслідок ускладнень не зафіксовано.
Терапія після прогресування захворювання. Аналіз даних проведено за 175 випадками прогресування після лікування із включенням лапатинібу. 34,8% (n=61) пацієнток отримували терапію трастузумабом, 19,4% (n=27) – піротинібом, 12% (n=21) – лапатинібом, 8% (n=14) – трастузумабом і лапатинібом, 24% (n=42) – не продовжували анти-HER2 терапію. Продовження лікування із застосуванням лапатинібу забезпечило кращу медіану виживаності без прогресування порівняно з відсутністю анти-HER2 терапії (4 та 2 міс відповідно; ВР 0,59; 95% ДІ 0,37-0,94; р=0,01) та аналогічну ефективність при зміні на інше анти-HER2 лікування (4 міс; ВР 0,97; 95% ДІ 0,70-1,36; р=0,88). Продовження анти-HER2 терапії було більш ефективним, ніж припинення (4 та 2 міс відповідно; ВР 0,58; 95% ДІ 0,41-0,83; р=0,001). Відповідні криві виживаності наведені на рис. 3.
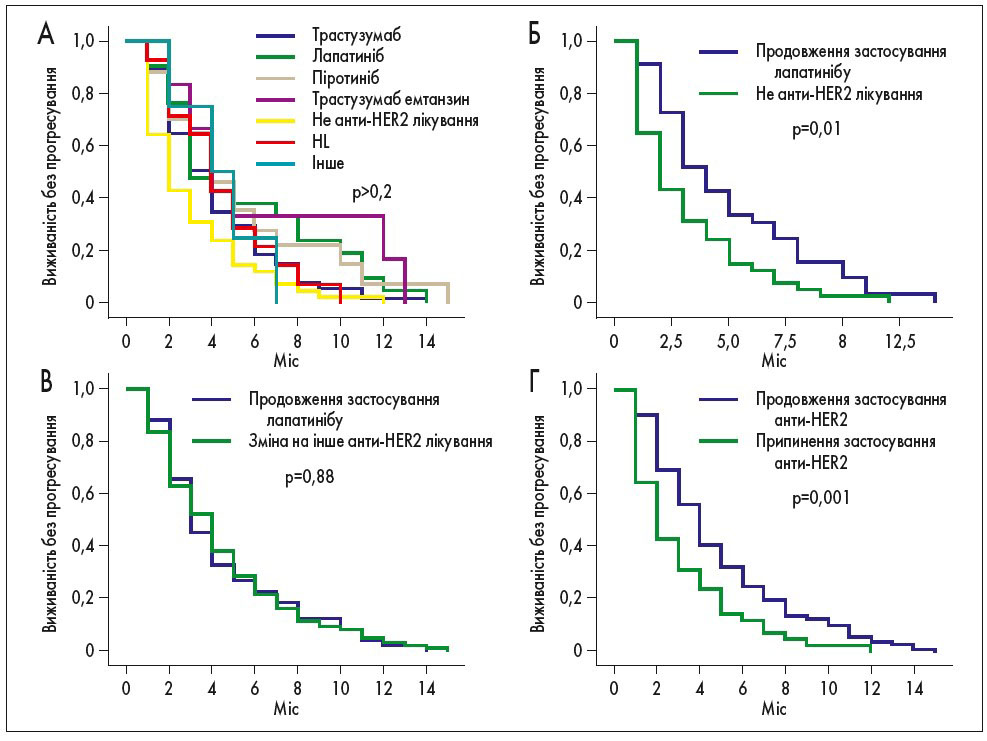 Рис. 3. Виживаність без прогресування у пацієнтів з рецидивом після терапії лапатинібом: A – всі види лікування; Б – продовження терапії лапатинібом у порівнянні з припиненням анти-HER2 терапії; В – продовження терапії лапатинібом у порівнянні зі зміною на іншу анти-HER2 терапію; Г – продовження анти-HER2 терапії у порівнянні з припиненням анти-HER2 терапії
Рис. 3. Виживаність без прогресування у пацієнтів з рецидивом після терапії лапатинібом: A – всі види лікування; Б – продовження терапії лапатинібом у порівнянні з припиненням анти-HER2 терапії; В – продовження терапії лапатинібом у порівнянні зі зміною на іншу анти-HER2 терапію; Г – продовження анти-HER2 терапії у порівнянні з припиненням анти-HER2 терапії
Обговорення. За результатами проведеного дослідження в клінічній практиці для лікування HER2-позитивного МРМЗ частіше застосовувалась комбінація LX (68%). Причиною цього могла бути вища вартість лікування з використанням HLC та менша доказова база щодо доцільності для не першої, а наступних ліній системного протипухлинного лікування.
За даними дослідження, виконаного у Німеччині з залученням 451 пацієнтки з HER2-позитивним МРМЗ, у 53% випадків для лікування був призначений трастузумаб, у 52% – трастузумаб з пертузумабом, у 19% – лапатиніб, у 28% – трастузумаб емтанзин (Т‑DM1) [7]. Проте це дослідження стосувалося першої лінії терапії. У світовій літературі відсутні дані щодо особливостей призначення та ефективності наступних ліній анти-HER2 терапії.
Результати рандомізованого дослідження EGF100151 із включенням 399 хворих з HER2-позитивним МРМЗ показали, що комбінація лапатинібу з капецитабіном є більш ефективною, ніж монотерапія капецитабіном. Це виражалося більш тривалим безрецидивним періодом, хоча статистично достовірних відмінностей щодо загальної виживаності між групами не було [8]. Саме результати дослідження EGF100151 стали підґрунтям для рекомендації схеми LX до застосування у клінічній практиці.
У трайлі CEREBEL порівнювали комбінацію LX та трастузумабу з капецитабіном при HER2-позитивному МРМЗ. Автори дійшли висновку, що обидва режими системного протипухлинного лікування мають зіставну ефективність [9].
У рандомізованому дослідженні EMILIA, що включало 991 хвору, яка отримувала лікування з приводу HER2-позитивного МРМЗ, порівнювали ефективність LX та Т-DM1. Виживаність без прогресування була вищою при терапії Т-DM1 (9,6 проти 6,4 міс; p<0,01). Слід зазначити, що частина пацієнтів з цього дослідження отримувала першу лінію терапії, що може впливати на отриманий результат [10].
Комбінація лапатинібу з трастузумабом за результатами доклінічних досліджень характеризується вищою ефективністю. У дослідженні ІІІ фази EGF104900 було продемонстровано, що призначення трастузумабу з лапатинібом порівняно з монотерапією лапатинібом характеризується більш тривалим безрецидивним періодом, хоч і не впливає на загальну виживаність пацієнток з HER2-позитивним МРМЗ, які отримали численні лінії системного протипухлинного лікування [4].
У рандомізованому дослідженні ALTERNATIVE (n=355; HER2-позитивний гормоночутливий МРМЗ) було показано, що комбінація трастузумабу з лапатинібом та інгібіторами ароматази є більш ефективною, ніж терапія трастузумабом з інгібіторами ароматази. Медіана виживаності без прогресування становила 11,0 та 5,7 міс відповідно (р=0,0064). У цьому дослідженні встановлено ефективність та безпеку подвійної анти-HER2 терапії у комбінації з ендокринною терапією [11].
Висновки. Лікування за схемою HLC (порівняно з LX) дозволяє подовжити тривалість безрецидивного періоду з прийнятним рівнем побічних явищ у хворих з HER2-позитивним МРМЗ. Продовження лікування з використанням лапатинібу чи іншого анти-HER2 препарату супроводжується вищою виживаністю без прогресування, якщо порівнювати з відмовою від анти-HER2 терапії.
Список літератури знаходиться в редакції.
Xie Y. et al. Real-world data of lapatinib and treatment after lapatinib in patients with previously treated HER2- positive metastatic breast cancer: A multicenter, retrospective study. Cancer Med. 2020; 9: 2981-2988. https://doi.org/10.1002/cam4.2943.
Реферативний переклад з англ. Олени Поступаленко
Більше матеріалів тут: https://health-ua.com/actual-theme/oncology/42118-aktualna-tema-nova-era-v-lkuvann-raku-grudno-zalozi?utm_source=qr-code&utm_medium=AT_oncology_42118-aktualna-tema-nova-era-v-lkuvann-raku-grudno-zalozi&utm_campaign=Novartis
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 3 (64) 2020 р.




