30 березня, 2021
Атезолізумаб проти доцетакселу у попередньо лікованих пацієнтів з недрібноклітинним раком легені
Кінцеві результати рандомізованих клінічних досліджень II фази POPLAR та III фази OAK
До активного клінічного застосування імунотерапії у пацієнтів із прогресуючим або метастатичним недрібноклітинним раком легені (НДРЛ) прогноз і результати терапії доцетакселом були поганими. Застосування імунотерапії, наприклад атезолізумабом, пембролізумабом та ніволумабом, спрямоване на ліганд програмованої смерті 1 (PD-L1) або білок програмованої смерті клітин 1 (PD‑1), змінило підхід до лікування пацієнтів з прогресуванням захворювання після першої лінії лікування, надаючи додаткові можливості таким пацієнтам.
Ефективність і безпеку імунотерапії анти-PD-L1 препаратом атезолізумабом у пацієнтів із попередньо лікованим НДРЛ вивчали спочатку у дослідженні II фази POPLAR, а згодом у дослідженні III фази OAK. Перші результати цих досліджень виявили значне покращення виживаності з прийнятним профілем безпеки імунотерапії порівняно з доцетакселом. Первинний аналіз досліджень POPLAR та OAK показав більшу загальну виживаність (ЗВ) у разі використання атезолізумабу порівняно з доцетакселом (незалежно від експресії PD-L1) у пацієнтів із прогресуванням захворювання після попередньої терапії препаратами платини та найбільші переваги у пацієнтів з найвищою експресією PD-L1.
У дослідженнях, присвячених імунотерапії, клінічна користь для пацієнтів зазвичай відзначається протягом певного періоду. Однак такі показники, як виживаність і виживаність без прогресування (ВБП), не можуть дати повного уявлення про користь імунотерапії. Таким чином, для оцінювання користі для пацієнтів цього методу лікування необхідний аналіз тривалої виживаності та інших показників. Опорні дослідження, OAK та POPLAR, підтримують позитивну оцінку тривалих переваг атезолізумабу у попередньо лікованих пацієнтів, враховуючи подібність у методології та структурі цих досліджень.
Матеріали та методи
Дизайн і характеристику досліджень POPLAR та OAK опубліковано раніше. POPLAR – рандомізоване відкрите дослідження II фази (NCT01903993), проведене в Європі, Азії та Північній Америці. OAK – рандомізоване відкрите дослідження III фази (NCT02008227), проведене в Європі, Азії, Північній і Південній Америці та Новій Зеландії. В обох дослідженнях брали участь дорослі (≥18 років) із вимірюваними вогнищами відповідно до критеріїв оцінки відповіді солідних пухлин (RECIST, версія 1.1) та показником за шкалою Східної об’єднаної онкологічної групи (ECOG) 0 або 1. Учасники цих досліджень раніше отримували від одного до двох режимів цитотоксичної хіміотерапії (≥1 комбінована терапія на основі препарату платини) з приводу НДРЛ IIIB або IV стадії. Крім того, пацієнти з мутацією EGFR або онкогеном ALK приймали інгібітор тирозинкінази.
Пацієнти були стратифіковані за рівнем експресії PD‑L1, кількістю попередніх ліній хіміотерапії та гістологічним варіантом пухлини (плоскоклітинний порівняно з неплоскоклітинним). Групи експресії PD-L1 на пухлинних клітинах (ПК) та імунних клітинах (IК), що інфільтрують пухлину, були такими: менш ніж 1% – на ПК0 та IК0; 1% чи більше – на ПК1/2/3 або ІК1/2/3; 50% або більше – на ПК3 та 10% чи більше – у IК3. Експресію PD-L1 оцінювали централізовано за допомогою імуногістохімічного аналізу VENTANA SP142 (Ventana Medical Systems, Tucson, AZ).
Учасників дослідження рандомізували у співвідношенні 1:1 на дві групи для лікування атезолізумабом (фіксована доза 1200 мг) або доцетакселом (75 мг/м2 площі поверхні тіла) через кожні 3 тижні. Пацієнти отримували атезолізумаб або доцетаксел до настання значної токсичності або прогресування захворювання за оцінкою дослідника. Лікування атезолізумабом можна було продовжувати і після прогресування захворювання, якщо, на думку дослідника, пацієнт отримував клінічну користь. Зміна лікування з доцетакселу на атезолізумаб була дозволена лише після того, як первинний аналіз даних OAK виявив клінічну користь атезолізумабу.
Основними кінцевими точками POPLAR та OAK були ЗВ у групі атезолізумаб vs доцетаксел та підгрупах за експресією PD-L1. Для оцінювання медіани ЗВ використовували метод Каплана – Меєра.
Аналіз безпеки проводили у всіх пацієнтів, які отримували будь-яку дозу препарату протягом періоду дослідження, причому пацієнтів групували залежно від того, чи приймали вони атезолізумаб.
Аналіз безпеки небажаних явищ (НЯ) проводили у пацієнтів з періодом спостереження ≥1 рік, який визначали як час від першого застосування атезолізумабу до 3 міс спостереження після введення останньої дози або останньої відомої дати спостереження.
Результати дослідження
Характеристики пацієнтів
У дослідженні POPLAR 287 пацієнтів рандомізовано у групи атезолізумабу (n=144) або доцетакселу (n=143), всі вони були включені в популяцію ITT (Intention-to-treat analysis). У дослідженні OAK 1225 пацієнтів рандомізовано для введення атезолізумабу (n=613) або доцетакселу (n=612), усіх їх було визначено як популяцію вторинного аналізу (ITT1225 або ITT). У цьому остаточному аналізі медіана спостереження становила 48,6 міс для POPLAR (точка відсікання даних 31 серпня 2018 р.) та 47,7 міс для ОАК (точка відсікання даних 9 січня 2019 р.). У дослідженні POPLAR було зафіксовано 121 (84,0%) випадок смерті у групі атезолізумабу та 120 (83,9%) в групі доцетакселу. У дослідженні OAK зареєстровано 486 (79,3%) випадків смерті у групі атезолізумабу та 496 (81,0%) у групі доцетакселу.
Загальна виживаність
Медіана ЗВ та відповідні показники відношення ризиків (ВР) після тривалого спостереження були подібними до таких у попередніх аналізах при більшій ЗВ у пацієнтів, які отримували атезолізумаб порівняно з доцетакселом: у POPLAR медіана ЗВ дорівнювала 12,6 проти 9,7 міс (ВР 0,76; 95% довірчий інтервал – ДІ – 0,58-1,00; рис. 1А), в OAK медіана ЗВ становила 13,3 проти 9,8 міс (ВР 0,78; 95% ДІ 0,68-0,89; рис. 1Б). Трирічна ЗВ у дослідженні POPLAR становила 18,7% (95% ДІ 12,1-25,3) та 10,0% (95% ДІ 4,7-15,2), а у дослідженні ОАК – 21,0% (95% ДІ 17,7-24,4) та 12,4% (95% ДІ 9,6-15,2) для пацієнтів, які отримували атезолізумаб або доцетаксел відповідно (рис. 1). Чотирирічна ЗВ у дослідженні POPLAR дорівнювала 14,8% (95% ДІ 8,7-20,8) та 8,1% (95% ДІ 3,2-13,0), а у дослідженні ОАК – 15,5% (95% ДІ 12,4-18,7) та 8,7% (95% ДІ 6,2-11,3) для пацієнтів, які отримували атезолізумаб або доцетаксел відповідно (рис. 1).
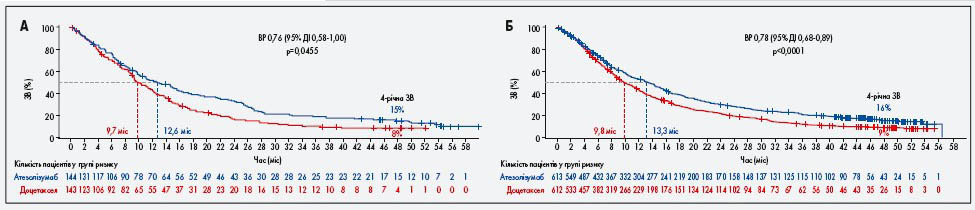 Рис. 1. ЗВ у групах ITT POPLAR та OAK. A – група ІТТ дослідження POPLAR (31 серпня 2018 р .; медіана спостереження 48,6 міс). Б – група ITT дослідження OAK (ITT1225, 9 січня 2019 р .; медіана спостереження 47,7 міс)
Рис. 1. ЗВ у групах ITT POPLAR та OAK. A – група ІТТ дослідження POPLAR (31 серпня 2018 р .; медіана спостереження 48,6 міс). Б – група ITT дослідження OAK (ITT1225, 9 січня 2019 р .; медіана спостереження 47,7 міс)
Медіана ЗВ була найдовшою у групах з найвищою експресією PD-L1 (експресія на ≥50% ПК3 або на 10% ІК3; рис. 2А і Б). Медіана ЗВ була довшою у пацієнтів підгрупи з експресією менше 1% на ПК0 та ІК0 порівняно з тими, хто отримував доцетаксел в OAK, а медіана ЗВ у пацієнтів у підгрупах ПК0 та IК0 була такою ж, як у тих учасників дослідження POPLAR, що приймали атезолізумаб і доцетаксел (рис. 2В та Г).
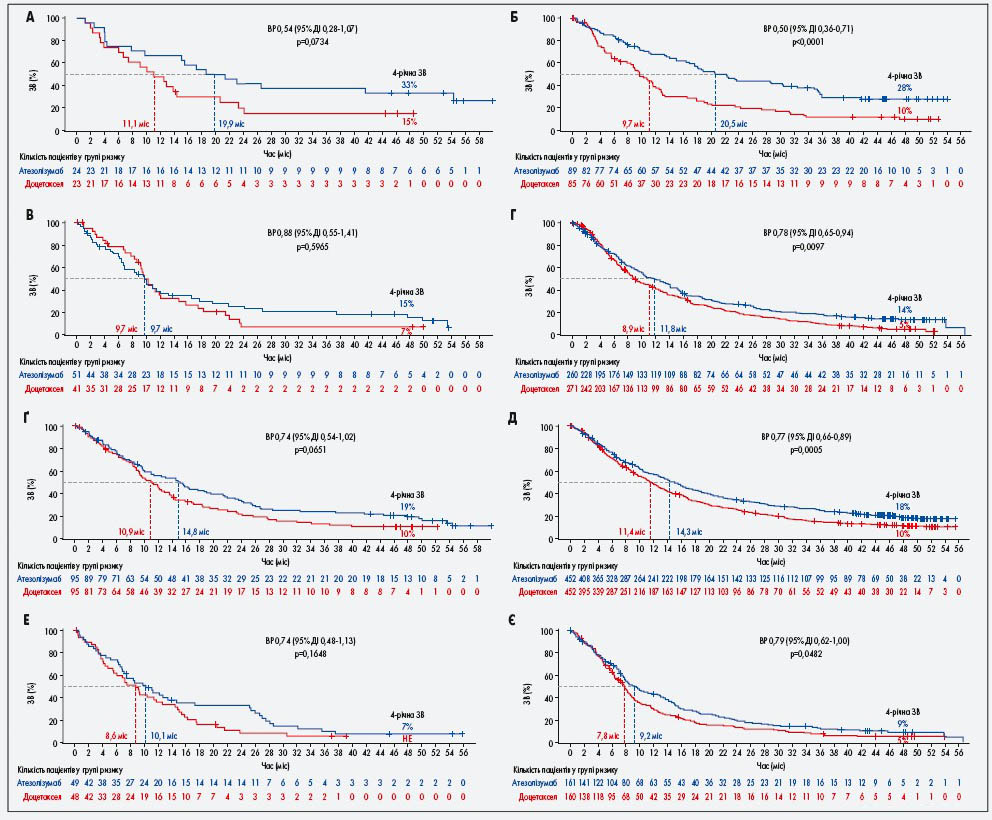 Рис. 2. ЗВ в учасників досліджень POPLAR та OAK за підгрупами залежно від експресії PD-L1 та гістологічного типу пухлини. А – при найвищій експресії PD-L1 (на >50% ПК3 або 10% ІК3) в дослідженні POPLAR. Б – при найвищій експресії PD-L1 на ПК3 та ІК3 в учасників дослідження OAK. В – при PD-L1-негативному статусі (експресії на <1% ПК0 та ІК0) у дослідженні POPLAR. Г – при PD-L1-негативному статусі у дослідженні OAK. Ґ – при неплоскоклітинному типі у дослідженні POPLAR. Д – при неплоскоклітинному типі у дослідженні OAK. Е – при плоскоклітинному типі у дослідженні POPLAR. Є – при плоскоклітинному типі у дослідженні OAK
Рис. 2. ЗВ в учасників досліджень POPLAR та OAK за підгрупами залежно від експресії PD-L1 та гістологічного типу пухлини. А – при найвищій експресії PD-L1 (на >50% ПК3 або 10% ІК3) в дослідженні POPLAR. Б – при найвищій експресії PD-L1 на ПК3 та ІК3 в учасників дослідження OAK. В – при PD-L1-негативному статусі (експресії на <1% ПК0 та ІК0) у дослідженні POPLAR. Г – при PD-L1-негативному статусі у дослідженні OAK. Ґ – при неплоскоклітинному типі у дослідженні POPLAR. Д – при неплоскоклітинному типі у дослідженні OAK. Е – при плоскоклітинному типі у дослідженні POPLAR. Є – при плоскоклітинному типі у дослідженні OAK
Пацієнти, які отримували атезолізумаб, мали вищу 3- та 4-річну ЗВ ніж ті, хто отримував доцетаксел у підгрупах експресії PD-L1. Так, у пацієнтів підгруп ПК3 або IК3, які приймали атезолізумаб або доцетаксел відповідно, 4-річна ЗВ у дослідженні POPLAR становила 33,3% (95% ДІ 14,5-52,2) та 14,9% (95% ДІ 0-30,1), а в дослідженні OAK – 27,8% (95% ДІ 18,1-37,5) та 9,8% (95% ДІ 2,8‑16,7; рис. 2А, Б). У пацієнтів підгруп ПК0 та IК0 4-річна ЗВ у дослідженні POPLAR становила 15,2% (95% ДІ 4,4-26,0) та 6,8% (95% ДІ 0-15,8), а в дослідженні OAK – 13,9% (95% ДІ 9,30-18,45) та 5,1% (95% ДІ 2,2-8,1; рис. 2В та Г).
Довша медіана ЗВ і вища 3- та 4-річна ЗВ спостерігались у пацієнтів як з неплоскоклітинною, так і з плоскоклітинною гістологічною формою пухлин, що приймали атезолізумаб (рис. 2Ґ, Є). У пацієнтів з неплоскоклітинною карциномою, які отримували атезолізумаб або доцетаксел відповідно, 4-річна ЗВ у дослідженні POPLAR становила 18,6% (95% ДІ 10,5-26,7) та 10,0% (95% ДІ 3,5-16,4), а в дослідженні OAK – 17,9% (95% ДІ 14,0-21,7) та 10,1% (95% ДІ 7,0-13,3; рис. 2Ґ, Д). У дослідженні POPLAR 4-річна ЗВ становила 7,0% (95% ДІ 0-14,7) у пацієнтів із плоскоклітинною карциномою, які отримували атезолізумаб; її не можна було оцінити (НЕ) у групі доцетакселу через невеликий обсяг вибірки, тоді як 3-річна ЗВ у підгрупах атезолізумабу та доцетакселу дорівнювала 9,4% (95% ДІ 0,70-18,06) та 5,2% (95% ДІ 0-12,0) відповідно. У дослідженні OAK 4-річна ЗВ становила 8,5% (95% ДІ 3,6-13,5) та 4,8% (95% ДІ 1,2-8,4) відповідно.
Пацієнти, які прожили 4 роки і довше
Загалом 19 пацієнтів у дослідженні POPLAR та 69 пацієнтів у дослідженні OAK були живими на 4-му році дослідження (48 міс), з них 15 і 4 у POPLAR та 43 і 26 в OAK були відповідно в групах атезолізумабу та доцетакселу. Порівняно з популяцією ITT у групі атезолізумабу більша кількість пацієнтів прожила 4 роки та мала неплоскоклітинну гістологічну форму (POPLAR – 87%; OAK – 88%) і оцінку 0 за шкалою ECOG (POPLAR – 73%; OAK – 56%). Крім того, ці пацієнти належали до підгрупи ПК3 або IК3 експресії PD-L1 (POPLAR – 40%; OAK – 23%); також були пацієнти підгруп ПК0 та IК0 (POPLAR – 33%; OAK – 37%). Серед пацієнтів з 4-річною виживаністю у групі атезолізумабу (з відомим статусом KRAS) – 2 з 5 в дослідженні POPLAR та 3 з 17 в дослідженні ОАК – мали мутації KRAS; 1 з 8 в POPLAR і 4 з 38 в ОАК мали мутацію EGFR; жоден в POPLAR і 2 з 28 в OAK мали мутації EML4-ALK.
Приблизно половина пацієнтів, що прожили 4 роки, мали клінічну відповідь на лікування. У дослідженні POPLAR у пацієнтів, що прожили 4 роки і довше, ВБП становила 13,3% (95% ДІ 0-30,5) у групі атезолізумабу та не оцінена у групі доцетакселу. У дослідженні OAK у пацієнтів, що прожили 4 роки, ВБП дорівнювала 34,6% (95% ДІ 19,6-49,6) у групі атезолізумабу та 19,2% (95% ДІ 2,4‑36,0) у групі доцетакселу.
Приблизно половина пацієнтів, що прожили 4 роки і довше, отримували атезолізумаб після прогресування захворювання.
Безпека
Середня тривалість лікування у загальній популяції групи атезолізумабу становила 3,7 міс (діапазон 0-51 міс) та 3,4 міс (діапазон 0-55 міс) у дослідженнях POPLAR та OAK відповідно. Побічні ефекти, що спостерігались через 4 роки в обох групах лікування, відповідали відомим профілям безпеки атезолізумабу та доцетакселу.
Середня тривалість лікування у пацієнтів групи атезолізумабу, які прожили 4 роки і довше, становила 26,5 міс (діапазон 3,7-50,6 міс) та 35,2 міс (діапазон 0,0-54,6 міс) у дослідженнях POPLAR та OAK відповідно. НЯ 3 або 4 ступеня, пов’язані з лікуванням, спостерігались у 27 та 16% пацієнтів, що отримували атезолізумаб і прожили 4 роки. НЯ, що призвели до переривання лікування, мали місце у 40 та 51% пацієнтів; НЯ, що зумовили відміну лікування, зареєстровано у 13 і 16% пацієнтів відповідно в дослідженнях POPLAR та OAK. У пацієнтів, що отримували атезолізумаб з принаймні 1 роком спостереження за безпекою, більшість НЯ мали місце протягом першого року (POPLAR – 97,7%; OAK – 98,1%).
Обговорення
Підсумковий аналіз досліджень POPLAR та OAK виявив послідовну та стійку перевагу ЗВ у групі атезолізумабу порівняно з доцетакселом у пацієнтів з раніше лікованим НДРЛ з експресією PD-L1 та за гістологічними підгрупами. Хоча найбільша користь спостерігалась у підгрупі найвищої експресії PD-L1 (експресія на ≥50% ПК3 або 10% IК3), пацієнти з PD-L1-негативними пухлинами (експресія на <1% ПК0 та IК0) також мали перевагу щодо виживаності при застосуванні атезолізумабу протягом 3 та 4 років лікування.
Пацієнти, які прожили 4 роки і довше, мали неплоскоклітинний рак і кращий статус за шкалою ECOG порівняно із загальною популяцією досліджень. Лише у незначної частини хворих були мутації EGFR, KRAS або EML4-ALK. У групі атезолізумабу 4-річної виживаності досягнули пацієнти з усіх підгруп за експресією PD-L1. Приблизно половина пацієнтів у кожній групі, які прожили 4 роки і довше, мали клінічну відповідь на лікування, проте у групі атезолізумабу тривалість відповіді була більша. Один пацієнт із 3 (POPLAR) та 6 з 11 (OAK), які прожили 4 роки і більше та мали клінічну відповідь на лікування, надалі отримували імунотерапію.
Тривале лікування атезолізумабом характеризується керованим профілем безпеки, що відповідає попереднім повідомленням із цих досліджень. У всіх пацієнтів атезолізумаб переносився добре, з меншим співвідношенням НЯ 3 або 4 ступеня, ніж у групі доцетакселу. Менше половини випадків припинення лікування було пов’язано з НЯ в групі атезолізумабу порівняно з групою доцетакселу.
На закінчення слід зазначити, що тривале спостереження за цими двома рандомізованими клінічними дослідженнями II та III фази свідчить про стабільно більшу перевагу виживаності у разі застосування атезолізумабу порівняно з доцетакселом у пацієнтів із раніше лікованим НДРЛ незалежно від рівня експресії PD-L1 або гістологічної форми пухлини. Встановлено, що атезолізумаб має послідовний і керований профіль безпеки з меншою кількістю пов’язаних із лікуванням НЯ та меншою кількістю випадків припинення лікування з приводу НЯ порівняно з доцетакселом. Більшість пацієнтів продовжували отримувати атезолізумаб або імунотерапію після прогресування захворювання, що свідчить про клінічну перевагу цих методів лікування у тривалій перспективі.
За матеріалами Mazieres J., Rittmeyer A., Gadgeel Sh. et al. Atezolizumab Versus Docetaxel in Pretreated Patients With NSCLC: Final Results From the Randomized Phase 2 POPLAR and Phase 3 OAK Clinical Trials. Journal of Thoracic Oncology. September 2020.
Підготував Назар Лукавецький
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 1 (68) 2021 р.



