24 жовтня, 2022
Бронхіальна астма у дітей: особливості лікування в умовах психоемоційного стресу
Війна в Україні стала без перебільшення найтяжчим випробуванням за всю історію незалежного існування нашої країни. Бойові дії, свідком яких є сьогодні кожен українець, внесли значні корективи у життя кожного і стали причиною значної перебудови у суспільстві. Це в першу чергу стосується вимушеної міграції населення. Так, з початком повномасштабного вторгнення мільйони людей в Україні покинули свої домівки. Деякі переїжджали в межах країни, інші виїхали за кордон. Хтось вже повернувся до місця постійного проживання, а для когось питання виїзду може постати згодом.
Дефіцит медикаментів, матеріалів, відсутність доступу до медичної допомоги, у тому числі й невідкладної, відсутність транспорту, документів – це лише частина проблем, з якими українці зіткнулися з початком війни. У більшості людей, особливо дітей, війна викликає значний стрес. Так, внутрішнє навантаження на людину через війну часто перевищує можливості людського організму, руйнуючи звичну поведінку, та може спричинити небезпечні наслідки для здоров’я. Дані минулих війн свідчать, що воєнні події призводять у людей до значного стресу та асоціюються із загостренням хронічних захворювань [3].
Посттравматичний стресовий розлад (ПТСР) у дітей є однією з ключових проблем у часи війн та епідемій, що реєструється у 16% випадків. Сучасні дані свідчать, що на окупованих з 2014 р. територіях частота інфекційних захворювань, хвороб органів дихання та бронхіальної астми зросла порівняно із загальнодержавними показниками. Результати нещодавнього опитування серед містян 18-64 років, які мають дітей до 18 років, показали, що 75% дітей демонструють ті чи інші симптоми травматизації психіки. При цьому найрозповсюдженішим симптомом визнані так звані «емоційні гойдалки», коли настрій швидко і без зовнішніх причин коливається від дуже гарного до надзвичайно поганого і навпаки.
Вплив стресу на перебіг бронхіальної астми
Бронхіальна астма (БА) – поширене неінфекційне захворювання, яке вражає як дорослих, так і дітей. Відповідно до сучасного визначення Глобальної ініціативи з астми (The Global Initiative for Asthma, GINA), БА є гетерогенним захворюванням, що характеризується хронічним запаленням дихальних шляхів. Визначається як наявність в анамнезі респіраторних симптомів, таких як хрипи, задишка, стиснення у грудях і кашель [5]. Відповідно до статистичних даних, на БА хворіють від 1 до 18% населення у кожній країні світу. За різними оцінками, від цієї патології страждають від 4 до 8% дітей. Сьогодні БА є найбільш поширеним хронічним захворюванням серед дітей в усьому світі, що негативно впливає на якість життя та створює значне навантаження на систему охорони здоров’я [6-7].
Протягом останніх двох десятиліть зростає кількість даних стосовно того, що хронічний стрес чинить негативний вплив на перебіг БА.
Деякі дослідження довели, що стрес може погіршити контроль БА та її перебігу через вплив на зниження відповіді на β2-агоністи короткої дії (SABA) та глюкокортикостероїди (ГКС) [11]. J.M. Brehm та співавт. (2015) продемонстрували, що діти з хронічним стресом мали нижчу бронходилататорну реакцію порівняно з дітьми з меншим рівнем хронічного стресу [12]. Цікаво, що розрахунковий вплив хронічного стресу на зниження бронходилататорної реакції посилювався, коли і діти, і їхні матері відчували сильний стрес.
Дані літератури підтверджують, що стрес як прямо, так і опосередковано може впливати на перебіг хронічних захворювань, у тому числі БА. Прямий вплив пов’язаний з негативною дією на функцію імунної системи, від чого посилюється вироблення прозапальних медіаторів. Встановлено, що наявність психологічного стресу перед інфікуванням істотно підвищує ризик розвитку респіраторної інфекції, на що вказують не лише симптоми інфекції, а й підвищений рівень специфічних антитіл [13]. J.P. Wisnivesky та співавт. (2010) визначили, що стрес в осіб із БА асоціюється з погіршенням контролю над БА та зниженням прихильності до лікування [14].
Сучасні дані також підтверджують асоціацію між ПТСР та БА. Так, у дослідженні R.D. Goodwin та співавт. (2007), проведеному з використанням реєстру близнюків Vietnam Era Twin Registry, продемонстровано, що ПТСР асоціюється з удвічі вищим ризиком розвитку БА у майбутньому [15]. Після терористичного нападу на Всесвітній торговий центр у Нью-Йорку 11 вересня 2001 р. велике 9-річне дослідження рятувальників показало, що загальна частота БА та ПТСР становила 27,6 і 31,9% відповідно [16]. Таким чином, наявні дані підтверджують причинно-наслідковий зв’язок між стресом і БА [17].
Війна, окрім того, що вона є окремим чинником стресу, несе з собою й інші фактори, асоційовані з ускладненим перебігом пульмонологічної та алергологічної патології: психологічні, екологічні тощо. Психологічні чинники включають високий рівень тривоги, ПТСР, у дітей часто наявний так званий синдром емоційної відстороненості, у дорослих – «вигорання». Окрім психологічних факторів, українці також стикаються з факторами війни, які включають додатковий контакт з алергенами (гриби, домашні тварини, хімічні сполуки, віруси і бактерії) у місцях перебування (бомбосховища, станції метро, місця збору людей для евакуації, транспорт для переїзду тощо).
Особливості медичної допомоги пацієнтам в умовах військових дій:
- обмеженість доступу до медичної допомоги, у тому числі невідкладної, та аптечної мережі;
- обмеженість очних консультацій з лікарем;
- дефіцит кваліфікованих медичних працівників, у тому числі алергологів/пульмонологів;
- відсутність доступу до специфічної алергодіагностики (шкірні, лабораторні тести з алергенами), функціональних методів діагностики (спірометрія).
Окрім того, пацієнти стикаються із додатковими тригерними факторами (застуда, віруси, бактерії, дим, продукти згоряння та інші отруйні речовини). Порушення режиму дієтичного/гіпоалергенного харчування, вживання продуктів, багатих на харчові алергени, прийом лікарських засобів з гуманітарної допомоги (в яких інший склад додаткових речовин, інструкції для використання іноземною мовою), порушення імунітету, а також порушення або зміни раніше відпрацьованих маршрутів пацієнтів. Ці та інші фактори чинять значний негативний вплив, асоціюються з високим ризиком розвитку гострої та загостренням хронічної патології, а також втрати контролю над захворюванням.
МІсце антилейкотрієнових препаратів у лікуванні БА
Безумовно, війна та пов’язані з нею фактори визначають потребу у новому підході до лікування БА. Наразі більшість фахівців згодні з думкою, що основні підходи до терапії повинні включати: продовження терапії, контроль симптомів загострення, знання маршруту дій при загостренні хвороби та контакт із лікарем.
Сучасна фармакотерапія БА включає дві групи препаратів: засоби контролю – базисну терапію, та засоби полегшення – препарати невідкладної допомоги (табл.) [20].
Якщо проаналізувати ступінчатий підхід GINA, привертає увагу той факт, що на усіх стадіях терапії БА застосовують препарати класу АЛТ. Препарати цієї групи довели свою ефективність та безпеку, у тому числі й у дітей раннього віку, та вигідно відрізняються від ІГКС більш високим рівнем комплаєнсу з боку батьків. Ключовими нішами застосування АЛТ у педіатричних пацієнтів є препаратконтролер, тобто базисна терапія БА, спрямована на контроль захворювання [21]. Незважаючи на значну роль психоемоційного стресу в перебігу БА, центральне місце в її патогенезі посідають запалення дихальних шляхів і гіперактивність бронхів. Так, порушення бронхіальної прохідності характеризується звуженням просвіту та спазмом гладкої мускулатури бронхів, супроводжується підвищеною продукцією слизу, набряком слизової оболонки, ушкодженням її епітелію та запальною інфільтрацією, що призводить до зворотньої обструкції бронхів і бронхіальної гіперактивності.
Сучасні дані свідчать, що ключову роль у розвитку БА відіграють IgE-опосередковані алергічні реакції, які характеризуються змінами структурнофункціональних властивостей біомембран, відповідальних за алергічне запалення клітин (опасистих клітин, базофілів, нейтрофілів, еозинофілів, Т-лімфоцитів, тромбоцитів), активацією синтезу і секрецією медіаторів алергічних реакцій. Доведено участь медіаторів ліпідного походження, з яких на особливу увагу заслуговують продукти метаболізму арахідонової кислоти.
Дані літератури свідчать, що при БА має місце активація синтезу ендогенних ейкозаноїдів, представниками яких є лейкотрієни (ЛТ).
 Лейкотрієни, включаючи цистеїнілові (LTC4, LTD4, LTE4) і LTB4, являють собою прозапальні медіатори, утворені з арахідонової кислоти за участю ферменту 5-ліпоксигенази та білка, який його активує (FLAP; рис. 1). Механізм дії лейкотрієнів пов’язаний із впливом на специфічні рецептори. Відомо 2 типи рецепторів: один – переважно чутливий до LTC4 та LTD4 і менш чутливий до LTE4, виявлений у бронхах людини, другий тип лейкотрієнових рецепторів знайдений у легеневих венах людини.
Лейкотрієни, включаючи цистеїнілові (LTC4, LTD4, LTE4) і LTB4, являють собою прозапальні медіатори, утворені з арахідонової кислоти за участю ферменту 5-ліпоксигенази та білка, який його активує (FLAP; рис. 1). Механізм дії лейкотрієнів пов’язаний із впливом на специфічні рецептори. Відомо 2 типи рецепторів: один – переважно чутливий до LTC4 та LTD4 і менш чутливий до LTE4, виявлений у бронхах людини, другий тип лейкотрієнових рецепторів знайдений у легеневих венах людини.
Лейкотрієни відносять до медіаторів ранньої фази алергічної реакції негайного типу, що опосередковують бронхоконстрикцію, гіперсекрецію слизу, підвищення судинної проникності, погіршення мукоциліарного кліренсу, хемотаксис еозинофілів у дихальні шляхи, проліферацію м’язових клітин бронхів. Крім того, лейкотрієни стимулюють диференціювання міофібробластів, що сприяє розвитку субепітеліального фіброзу.
Враховуючи ключову роль лейкотрієнів у патогенезі БА, з середини 1980-х років розпочато вивчення можливості використання антилейкотрієнових препаратів. Сьогодні відомі 2 класи препаратів цієї групи – інгібітори 5-ліпоксигенази та антагоністи лейкотрієнових рецепторів (АЛТ).
Механізм дії модифікаторів активності лейкотрієнів базується на протидії ефектам лейкотрієнів на рівні їх рецепторів. Лікарські препарати, що селективно впливають на лейкотрієнові патофізіологічні механізми, прийнято називати антилейкотрієновими. Сьогодні існують 3 групи препаратів, здатних впливати на синтез лейкотрієнів:
- інгібітори активності 5-ліпоксигенази;
- інгібітори 5-ліпоксигеназактивуючого протеїну (FLAP);
- антагоністи лейкотрієнових рецепторів (рис. 2).
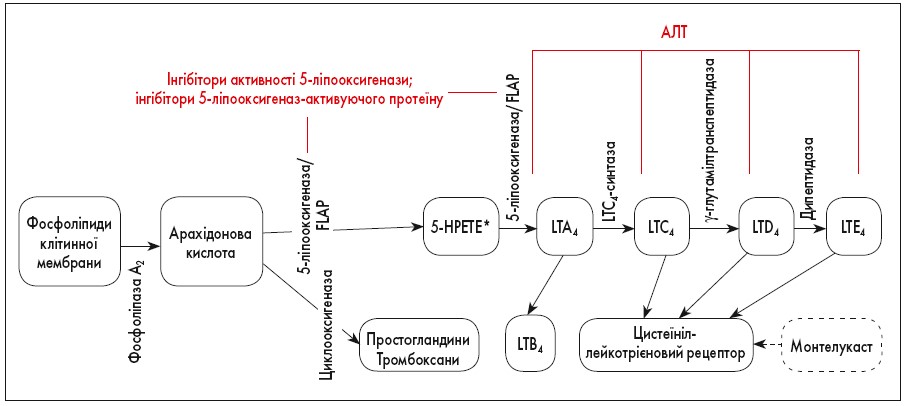 Рис. 2. Метаболізм арахідонової кислоти та механізм дії модифікаторів активності лейкотрієнів [19]
Рис. 2. Метаболізм арахідонової кислоти та механізм дії модифікаторів активності лейкотрієнів [19]
* 5-HPETE – 5-гідропероксиейкозатетранова кислота.
Роль монтелукасту в лікуванні БА
Завдяки впливу на лейкотрієновий шлях розвитку запалення АЛТ допомагають зменшити набряк, гіперсекрецію та бронхоспазм при БА.
Відомим представником АЛТ-препаратів є монтелукаст – цистеїніловий АЛТ, що використовується для підтримувального лікування БА та полегшення симптомів сезонної алергії [23]. Механізм його дії пов’язаний із блокуванням лейкотрієну D4 (і вторинних лігандів, лейкотрієнів C4 та E4) на рецептор цистеїнілового лейкотрієну CysLT1 у легенях і бронхах шляхом зв’язування з ним. Це зумовлює бронхоконстрикцію, спричинену лейкотрієном, і призводить до зменшення запалення. Механізм його дії зумовлює ефективність препарату для лікування гострих астматичних нападів [24].
Цистеїніл-лейкотрієни (LTC4, LTD4 і LTE4) є кінцевими продуктами шляху арахідонової кислоти і потужними медіаторами антиген-індукованих скорочень гладкої мускулатури дихальних шляхів [25]. Монтелукаст діє, антагонізуючи ці сполуки на їхньому рецепторі, таким чином захищаючи від бронхоконстрикції.
Терапія монтелукастом пригнічує бронхоспазм як на ранній, так і на пізній стадіях, знижує реакцію дихальних шляхів на антигени, зменшує кількість еозинофілів у периферичній крові та мокротинні у дорослих і дітей, покращує клінічний контроль БА.
Сьогодні монтелукаст включений до міжнародних рекомендацій та українських протоколів лікування БА як додаткова протизапальна терапія та як альтернатива ІГКС, має добру переносимість та нечасто викликає побічні ефекти [26].
Згідно з оновленими рекомендаціями GINA 2022 р., застосування АЛТ сьогодні розглядають як складову базисної терапії БА (рис. 3). Монтелукаст викликає бронходилатацію упродовж 2 год після перорального прийому. При цьому призначення препарату разом із SABA не тільки забезпечує підсилення бронходилатаційного ефекту, а й допомагає пришвидшити його.
 Рис. 3. Лікування дітей із БА віком <5 років
Рис. 3. Лікування дітей із БА віком <5 років
При менеджменті дітей із БА завжди існувала проблема стероїдофобії у батьків, яка пов’язана зі зменшенням прихильності до лікування та асоціюється з недостатнім контролем захворювання. Сучасні дані підтверджують, що у дітей із легкою формою БА монтелукаст є альтернативою низьким дозам ІГКС завдяки співставній ефективності та зручності застосування. Крім того, за недостатньої ефективності низької дози ІГКС додавання монтелукасту є альтернативою збільшенню дози ІГКС. Результати мультицентрового дослідження за участю 689 дітей із БА віком від 2 до 5 років продемонстрували, що, на відміну від плацебо, монтелукаст у дозі 4 мг/добу сприяв значному досягненню контролю симптомів і знижував потребу у використанні ІГКС [27].
Сьогодні на фармацевтичному ринку України увагу привертає генеричний препарат монтелукасту Глемонт (фармацевтична компанія «Гленмарк»), ключовою перевагою якого є доведена біоеквівалентність оригінальному монтелукасту. Виробництво цього лікарського засобу відповідає стандартам Управління з контролю за продуктами харчування та лікарськими засобами CША (FDA), що також підтверджує його високу якість. Препарат Глемонт випускається у формі таблеток 10 мг, вкритих оболонкою, жувальних таблеток 4 і 5 мг, що дозволяє підібрати найбільш оптимальну для пацієнта дозу та форму.
Рекомендовані дози для дітей:
у віці 2-5 років – 4 мг 1 р/добу;
6-14 років – 5 мг 1 р/добу;
≥15 років – 10 мг 1 р/добу.
Таким чином, сучасні дані підтверджують, що ризик розвитку та прогресування БА має пряму асоціацію зі стресом. Відповідно, контроль БА є ключовим моментом менеджменту педіатричних пацієнтів під час війни. Глемонт зарекомендував себе як ефективний та безпечний базисний препарат для лікування БА, застосування якого дозволяє досягти адекватного контролю над симптомами захворювання.
Список літератури знаходиться в редакції.
Підготувала Анна Хиць
Тематичний номер «Педіатрія»№ 3 (64)-4 (65) 2022 р.



