25 жовтня, 2022
Раціональне застосування мукоактивних препаратів для лікування захворювань дихальних шляхів у дітей
Гострі респіраторні захворювання (ГРІ) є найпоширенішим типом захворювань у дітей, їх частка складає близько 90% усієї інфекційної патології дитячого віку [1]. Щороку ГРІ накладають величезний тягар як на систему охорони здоров’я, що пов’язано з частими зверненнями по медичну допомогу, госпіталізацією та призначенням антибактеріальних препаратів, так і на суспільство в цілому. Останній факт пов’язаний із частим невиходом одного з батьків на роботу та втратою продуктивності [1, 2]. Проблема ГРІ у педіатричних пацієнтів ускладнюється ще й тим, що сьогодні ГРІ визначається як одна з ключових причин дитячої смертності. У 2016 р. з 68 млн епізодів понад 652 тис. дітей віком <5 років померли через ГРІ [3, 4]. Це свідчить про те, що ГРІ є вкрай серйозною проблемою, яка потребує вирішення, зокрема пошуку ефективних підходів до лікування патології у дітей.
ГРІ у структурі захворювань дитячого віку
ГРІ визначається як будь-яка гостра інфекційна хвороба верхніх або нижніх дихальних шляхів, що супроводжується розвитком респіраторного синдрому та загальноінтоксикаційними проявами різного ступеня вираженості. В етіологічній структурі ГРІ найбільша частка належить вірусам. На сьогодні відома значна кількість збудників гострих респіраторних вірусних інфекцій (ГРВІ), які переважно належать до 9 різних груп вірусів – грип, парагрип, аденовірус, респіраторно-синцитіальний вірус, пікорна-, корона-, рео-, ентеро- та герпесвіруси [5]. Саме ГРВІ за питомою часткою посідають провідне місце у структурі інфекційної патології людини, на них припадає близько 90% випадків. І лише в 10% захворювання викликано бактеріальною інфекцією, найпоширенішими представниками якої є Streptococcus pneumoniae, β-гемолітичний стрептокок групи А, Haemophilus influenzaе, Mycoplasma pneumoniae, Chlamidophila pneumoniae та Moraxella catarrhalis.
Для різних вірусних збудників характерним є ураження певних відділів дихальних шляхів: риновіруси та коронавіруси уражують переважно слизову оболонку носа, реовіруси – носа та глотки, парагрипозні віруси – гортані, вірус грипу – трахеї, РС-вірус – бронхів та бронхіол, аденовіруси – лімфоїдну тканину глотки і кон’юнктиви. Важливо розуміти, що вірусні агенти загалом зумовлюють запалення в усіх відділах дихальних шляхів, однак різною мірою, що і відрізняє їх за клінічною симптоматикою.
Проблема кашлю у дітей
Кашель є одним з ключових симптомів ураження дихальних шляхів при ГРІ. Залежно від тривалості розрізняють гострий кашель (триває <3 тижнів), затяжний (від 3 до 8 тижнів) та хронічний (зберігається >8 тижнів) [6]. Відповідно до результатів дослідження A.D. Hay та співавт. (2003), на 10-й день від початку ГРВІ кашель персистує у 40%, а на 25-й день – у 10% дітей [7]. Результати інших досліджень, які базувалися на аналізі скарг батьків дітей, демонстрували, що кашель є поширеним ізольованим симптомом, епізоди якого без видимих ознак ГРВІ відзначалися у 28% хлопчиків та у 30% дівчат [8, 9]. Статистичні дані в Україні свідчать, що кашель становить 30-50% усіх амбулаторних звернень до сімейного лікаря та педіатра, а >80% дітей із хронічним кашлем звертаються до лікаря амбулаторно >5 разів до моменту встановлення остаточного діагнозу і призначення ефективної терапії [10].
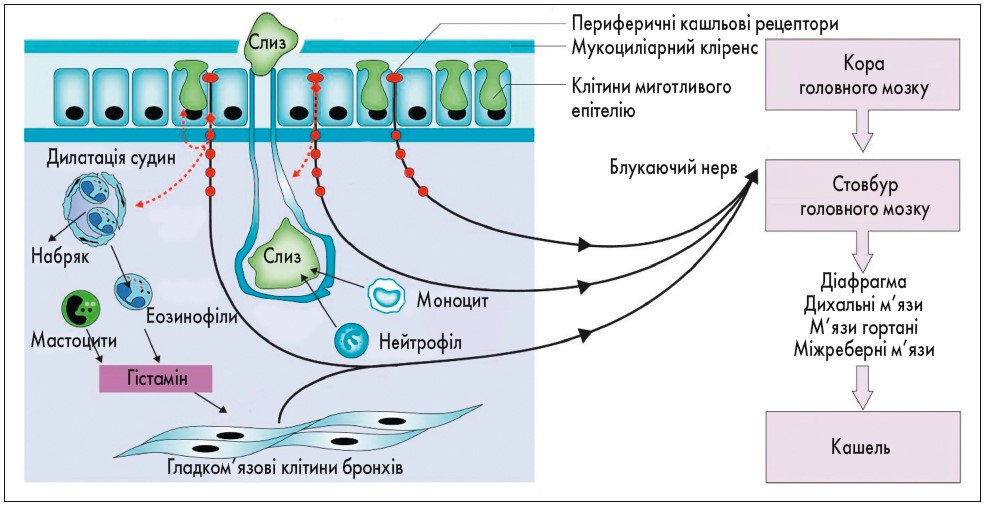
Кашель – рефлекторний акт, що виникає у відповідь на подразнення чутливих рецепторів nervus vagus, розташованих в органах дихання. Нейрорефлекторна дуга кашльового рефлексу складається з п’яти компонентів: кашльових рецепторів, аферентних волокон блукаючого та верхнього гортанного нервів, кашльового центру, який локалізується в довгастому мозку, еферентних пучків блукаючого і діафрагмального нервів, що проводять імпульси до мускулатури грудної клітки, діафрагми, а також черевного пресу (рис. 1).
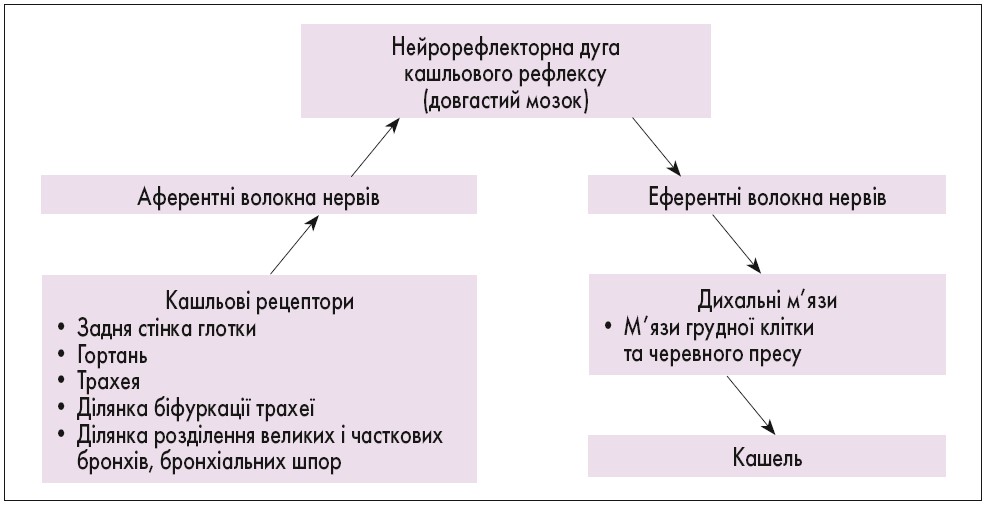 Рис. 1. Нейрорефлекторна дуга кашльового рефлексу
Рис. 1. Нейрорефлекторна дуга кашльового рефлексу
Кашель разом із мукоциліарним кліренсом миготливого епітелію є неспецифічним захисним механізмом, що допомагає звільнити просвіт дихальних шляхів від надлишку слизу та сторонніх часток, які осідають на ньому. Ключовими причинами розвитку кашлю є подразнення так званих кашльових зон, які представлені задньою стінкою глотки, голосовою щілиною та біфуркацією трахеї. Під час ГРІ кашель є основним захисним механізмом, що сприяє елімінації збудника та видаленню підвищеної кількості секрету з дихальних шляхів. Його роль є вкрай важливою, оскільки перебіг процесу запалення в респіраторній системі характеризується залученням іншого неспецифічного захисного механізму – гіперпродукції слизу (рис. 2). Відповідно, гіперсекреція слизу призводить до переповнення просвіту бронхів слизом, що може проявлятися бронхообструктивним синдромом та виникненням ателектазів.
У патогенезі продуктивного кашлю важливим моментом є також розуміння властивостей і складу бронхіального секрету, що, як відомо, складається з двох фаз: нерозчинної у воді (гель), представленої в основному муцинами, та розчинної (золь), до складу якої входять електроліти, білки та ферменти. У нормі співвідношення гелю до золю становить 1:1, але при ГРІ воно може зміщуватися у бік збільшення гелю, що призводить до порушень мукоциліарного транспорту і кліренсу, та, відповідно, стимулюватиме кашель. Розуміння змін бронхіального секрету при ГРІ особливо важливо при менеджменті дітей із кашлем, оскільки вони мають свої фізіологічні особливості будови дихальних шляхів. Так, через гіперкринію з переважанням гелю над золем бронхіальний секрет у дітей характеризується більшою в’язкістю, що у поєднанні з фізіологічно вузькими бронхами, слабкістю дихальної мускулатури та підвищеною гідрофільністю тканин зумовлює вищий ризик розвитку бактеріально-асоційованих проявів ГРІ [12].
Місце мукоактивних препаратів у терапії кашлю у дітей
У зв’язку з тим, що кашель – важливий механізм евакуації мокротиння з дихальних шляхів, підхід до лікування має бути зваженим. Відповідно до міжнародних гайдлайнів, медикаментозна терапія кашлю у дітей показана тільки в тих випадках, коли він погіршує якість життя, самопочуття і стан як самої дитини, так і її батьків. За сучасними даними, кашель при ГРІ заважає повсякденній активності у 76% дітей, порушує сон у 88% дітей та 72% батьків [13]. Для вибору ефективного лікування кашлю у дітей важливо не лише діагностувати захворювання, яке є першопричиною кашлю, а й оцінити продуктивність, давність та інтенсивність самого кашлю. Окрім того, важливо оцінити характер бронхіального секрету та встановити наявність/відсутність бронхообструктивного синдрому.
Сьогодні для лікування кашлю використовуються дві основні групи препаратів: протикашльові, які блокують різні ланки кашльового рефлексу, та мукоактивні, які модулюють фізико-хімічні властивості бронхіального секрету. Необхідність призначення протикашльової терапії визначається перш за все наявністю у хворого непродуктивного, сухого, надсадного, виснажуючого кашлю. Мукоактивні засоби сприяють відновленню реологічних властивостей мокротиння та поліпшують дренажну функцію бронхів, тому їх призначають при вологому кашлі.
Карбоцистеїн при лікуванні ГРІ у дітей у світлі доказової медицини
Сучасні дані свідчать, що карбоцистеїн є одним із мукоактивних препаратів, які призначають найчастіше [18]. У дослідженні Y.C. Duijvestijn та співавт. (2009), в якому загалом брали участь 497 дітей із ГРІ верхніх і нижніх дихальних шляхів без хронічної бронхолегеневої патології, була доведена ефективність застосування карбоцистеїну та ацетилцистеїну у дітей від 2 років порівняно із плацебо [19]. Результати попередніх досліджень також підтвердили, що карбоцистеїн має антиадгезивну дію проти вірусів і бактерій. Зокрема, карбоцистеїн здатний пригнічувати респіраторно-синцитіальну вірусну інфекцію шляхом зниження мембранної експресії рецепторів вірусів (ICAM-1) [20], вірус грипу та риновірус, а також зменшувати адгезію деяких бактерій (Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis) [21-23].
M. Chalumeau і Y.C.M. Duijvestijn (2013) у своєму дослідженні визначили, що застосування перорального ацетилцистеїну та перорального карбоцистеїну зменшувало прояви кашлю на 6-7-ий день у дітей із ГРІ верхніх і нижніх дихальних шляхів, порівняно із плацебо [26, 27]. Таким чином, ефективність застосування карбоцистеїну продемонстрована в низці клінічних досліджень, а також підтверджена десятиріччям застосування в клінічній практиці як у дітей, так і у дорослих із захворюваннями, що супроводжуються порушенням бронхіальної секреції.
Для педіатрів дуже важливим є вивчення безпеки препаратів, які застосовуються для лікування дітей. Дослідження минулих років підтвердили, що карбоцистеїн має високий профіль безпеки у зарубіжних та вітчизняних дослідженнях. Зокрема, за даними Кокранівського систематичного огляду 6 рандомізованих контрольованих клінічних досліджень продемонстровано, що карбоцистеїн має високий профіль безпеки при застосуванні у дітей віком старше 2 років із гострими захворюваннями верхніх і нижніх дихальних шляхів [19].
В Україні карбоцистеїн зареєстрований під назвою Флюдітек і випускається у формі сиропу, що містить 5 або 2% карбоцистеїну, по 125 мл у флаконі (для дорослих та дітей). Флюдітек сироп 2% призначають дітям від 2 років для лікування симптомів порушень бронхіальної секреції та виведення мокротиння, особливо при гострих бронхолегеневих захворюваннях, наприклад при гострому бронхіті, при загостреннях хронічних захворювань дихальної системи (табл.).
Додатковими ефектами карбоцистеїну (Флюдітек) є його протизапальна та антиоксидантна дії. Доведено, що карбоцистеїн зменшує інфільтрацію нейтрофілами та міграцію прозапальних клітин у дихальні шляхи, а також зменшує продукцію прозапальних цитокінів. Антиоксидантна дія карбоцистеїну пов’язана з його здатністю за рахунок активації трансмембранного транспорту стимулювати внутрішньоклітинний потік хлоридів і глутатіону, які є дієвим буфером, що перешкоджає розвитку оксидативного стресу або послаблює його негативні наслідки [29].
Дані літератури повідомляють, що більше 50% дітей віком до 6 років мають труднощі з дотриманням лікарських призначень [30], що зазвичай пов’язано з такими якостями препарату, як смак і аромат [31-33]. Так, смакова привабливість лікарських засобів для дітей може вплинути на дотримання режиму лікування, а також суттєво впливає на кінцевий терапевтичний результат [34]. Відповідно, краща смакова привабливість фармацевтичних засобів відіграє ключову роль у покращенні дотримання режиму лікування педіатричними пацієнтами [35].Так, результати нещодавнього дослідження Peng Y. та співавт. (2022) продемонстрували, що пероральний розчин карбоцистеїну зі смаком фруктів є більш привабливим, оскільки краще сприймається дітьми [36]. Препарат Флюдітек для дітей випускається у формі сиропу зі смаком і запахом банану, що покращує комплаєнс та забезпечує більш ефективне лікування ГРІ.
Таким чином, завдяки своїм властивостям та високому профілю безпеки, карбоцистеїн (Флюдітек) може застосовуватись при симптомах порушень бронхіальної секреції та виведення мокротиння, в тому числі і в педіатричних пацієнтів.
Список літератури знаходиться в редакції.
Підготувала Анна Хиць
Тематичний номер «Педіатрія»№ 3 (64)-4 (65) 2022 р.