10 лютого, 2023
Геріатричні синдроми в клінічній практиці
 Специфікою нинішнього етапу глобального постаріння, поряд зі збільшенням кількості літніх людей, є драматичне збільшення в популяції частки осіб віком від 80 років [38].
Специфікою нинішнього етапу глобального постаріння, поряд зі збільшенням кількості літніх людей, є драматичне збільшення в популяції частки осіб віком від 80 років [38].
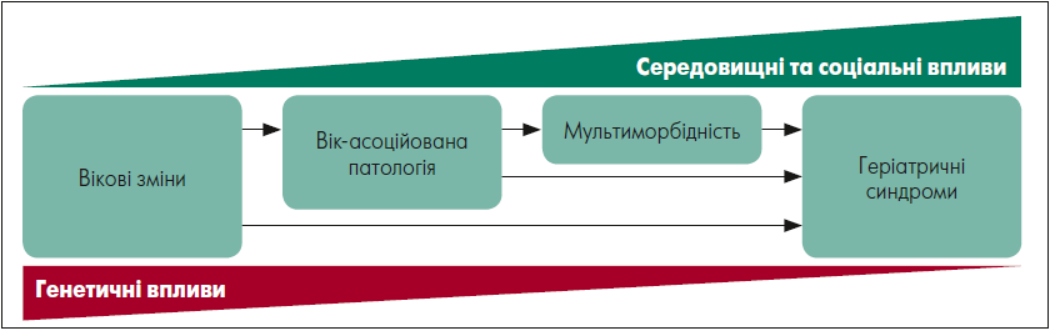
З огляду на це закономірним вбачається не тільки зростання вік-асоційованих хронічних захворювань і мультиморбідності, а й так званих геріатричних синдромів (ГС) (рис.).
Що таке геріатричний синдром?
Вікові зміни – морфологічні, функціональні, метаболічні – призводять до численних дефіцитів в органах і системах організму й одночасно є підґрунтям розвитку вік-асоційованих захворювань. У сукупності це порушує функціональний резерв організму такою мірою, що навіть незначні, безпечні для молодших осіб, стресові впливи можуть призвести до декомпенсації і несприятливих наслідків [41]. Діагностика симптомів, які віддзеркалюють порушення, тривожні щодо наслідків, і подальший цілеспрямований менеджмент є невід’ємним складником всебічного геріатричного оцінювання (ВГО).
Геріатричний синдром – термін для дефініції хронічних порушень здоров’я у літніх осіб, не ідентичний поняттям «хвороба» і «синдром». 1995 року запроваджено визначення ГС як «мультифакторіальний стан здоров’я, що розвивається внаслідок акумуляції порушень у множинних органах і системах і визначає вразливість (літніх осіб) до ситуаційних впливів» [26].
Характеристиками ГС є: 1) багатофакторність; 2) асоціація з віком; 3) несприятливий прогноз щодо функціонального стану, якості життя, смерті, залежності від сторонньої допомоги, потреби в довготривалому нагляді, 4) оборотність.
Слід зауважити, що під функціональним станом розуміють ступінь автономії людини, її здатність до самообслуговування. Функціональне зниження може охоплювати щоденну базисну активність (зокрема, харчування, одягання, купання, переміщення по квартирі, контроль фізіологічних відправлень, що визначається за індексом активностей повсякденного життя Катц) або, в легших випадках, інструментальну (прибирання домівки, приготування їжі, приймання медикаментів, управління фінансами, користування телефоном тощо, яка визначається за шкалою оцінювання інструментальної активності Лоутона).
Зазвичай ГС маніфестують як єдиний прояв. Їхній розвиток і прогресування зумовлені не лише віковими і патологічними змінами, а й середовищними впливами, зокрема соціальними. ГС мають загальні чинники ризику, як-от оксидативний стрес, хронічне запалення, гормональний дисбаланс, порушена толерантність до глюкози, дефіцит мікронутриєнтів тощо. Часто чинником ГС є медикаменти. Так, седативні та снодійні препарати можуть спричиняти делірій, порушення ходьби, падіння, когнітивні розлади [56].
Співіснування декількох ГС зумовлене не тільки спільними чинниками ризику, а й взаємним впливом: наприклад, погіршення зору поєднується з порушеннями ходьби, диссомнія – із депресією і деменцією, стареча немічність – із погіршенням балансування і моторики, із депресією. Кожен ГС несе загрозу каскаду несприятливих подій: нетримання сечі на тлі порушення рівноваги може призвести до падінь; своєю чергою, падіння асоційовані з подальшим погіршенням мобільності, іммобілізацією, пролежнями, високим ризиком травматичної смерті [31, 37].
Якими є відомі геріатричні синдроми?
Нині нараховується близько 60 ГС: немічність, падіння, нетримання сечі й калу, порушення сну, делірій, деменція, депресія, запаморочення, саркопенія, остеопороз; порушення зору та слуху, ходьби й рівноваги, харчування (мальнутриція) тощо [18].
Сформувалася певна ієрархія з виокремленням «великих» ГС, зважаючи на частоту й наслідки. Особливе місце в цьому переліку посідає синдром немічності, або старечої астенії (англ. frailty) [10].
У Міжнародній класифікації хвороб 10-го перегляду (МКХ‑10) «старечій астенії», яку ототожнюють із frailty, відповідає код R54. Водночас цей синдром притаманний і хворим молодого й середнього віку з тяжкою патологією, як-от злоякісні пухлини, хронічна серцева недостатність. Кількість осіб із синдромом немічності та загалом із ГС збільшується в популяції не лише через старіння населення, а й через безпосередній вплив тяжких захворювань. Так, у ВІЛ-інфікованих пацієнтів, у яких завдяки антиретровірусній терапії тривалість життя суттєво подовжена, первинна патологія трансформується у хронічні захворювання, які, своєю чергою, призводять до розвитку ГС [17].
Як часто виникають геріатричні синдроми?
Загалом ГС поширені в популяції літніх осіб, але здебільшого вони залишаються недіагностованими. Опубліковані дані щодо частоти ГС кардинально різняться, що пояснюється гетерогенністю обстежених контингентів, рівнем і методами діагностування.
Як приклад, поширеність синдрому немічності серед літніх осіб, що не перебувають у спеціалізованих закладах, становить близько 11%, водночас розбіжності в частоті широко варіюють залежно від методу оцінювання – від 4 дo 59%; в осіб віком від 85 років – 26‑44% [32].
Найвищі значення частоти ГС надають спеціалізовані заклади: у дослідженні за участю пацієнтів геріатричної амбулаторії в Туреччині поліфармацію (приймання чотирьох і більше препаратів) встановлено у 54,5%, нетримання сечі – у 47,6%, мальнутрицію – у 9,6%, депресію – у 35,1%, деменцію – у 21,6%, падіння – у 33,6%, саркопенію – у 31,7%, немічність – у 28,3%. Стратифікація за віком продемонструвала виразне зростання ГС саме з віком: у 20% 60‑69-річних пацієнтів не спостерігалося ГС, водночас майже у 48% віком >80 років фіксували понад чотири ГС одночасно [5].
Однією з найуразливіших груп є госпіталізовані пацієнти, а також особи в постгоспітальному періоді: з погляду на це було введено термін «постгоспітальній синдром» для виокремлення небезпечного періоду після госпіталізацї за гострими показаннями і ризиком неповернення до вихідного рівня функціонування [58].
Що означають геріатричні синдроми для клінічної практики?
ГС мають несприятливий прогноз щодо тривалості життя, функціонального стану, якості життя [49, 63]. Так, когнітивні порушення в дослідженні DECOFIRH Study виступали предиктором погіршення функціонального стану після госпіталізації, саркопенія – підвищеної смертності за ургентних операцій [16, 57].
У дворічному спостереженні за 16 640 пацієнтами віком >50 років зниження функціональних можливостей і наявність ГС виявилися чутливішими предикторами погіршення здоров’я і смерті, ніж захворювання [49].
У проспективному дослідженні постгоспітальних синдромів наявність апатії, болю, мальнутриції, порушення рухливості та страху падінь у 4,35; 3,26; 3,4; 6,65 і 3,17 раза відповідно підвищували ризик функціонального зниження; водночас апатія, недоїдання, втома та ризик падіння асоціювалися з підвищеною смертністю [58].
Виявлення ГС означає суттєві, а іноді кардинальні зміни в тактиці та стратегії лікування / обслуговування осіб похилого і старечого віку [28, 29].
Діагностування ГС за різних нозологій у різних клінічних ситуаціях (оперативні втручання, госпіталізація тощо), реалізація сукупності геріатричних підходів, адекватний менеджмент, як-от передбачається ВГО, асоційоване з поліпшенням прогнозу [51, 63].
Як діагностують геріатричні синдроми?
Слід констатувати, що натепер, на жаль, не існує єдиних стандартів діагностування ГС, натомість для кожного з них запропоновано досить широкий спектр спеціальних досліджень.
Падіння і порушення ходьби
Падіння є головною причиною травматичної смертності осіб старечого віку, асоційованою з тяжкими пошкодженнями. Чинниками ризику падінь є м’язова слабкість, падіння в анамнезі, порушення балансу і ходьби, використання під час ходьби допоміжних девайсів, дефіцит зору, остеоартрит, когнітивні порушення, депресія, застосування деяких медикаментів, вік понад 80 років [22].
У Європі щорічні фінансові витрати через падіння перевищують 30 млрд євро [53].
Найпростішим методом виявлення ГС є спостереження за рухами пацієнта. Як спеціальний інструментарій для оцінювання ризику падінь використовують відповідний опитувальник Десмонда. Розроблено прості тести для визначення мобільності та балансування: швидкість звичайної ходьби, тест «підйом-ходьба», стояння за різних положень ніг, стабільність під час поворотів, стійкість за підштовхування тощо [21, 22].
На особливу увагу заслуговують пацієнти з повторними падіннями, для яких необхідний детальний аналіз вживаних медикаментів, ортостатичної гіпотензії, аритмій, епізодів гіпоглікемії, нейром’язових симптомів, порушень балансу, зниження мінеральної щільності кісток [44].
Саркопенія
Саркопенія – це атрофічні та дегенеративні зміни скелетної мускулатури і погіршення її функцій. Втрата м’язової маси становить у середньому 0,5‑1% щорічно у віці після 25‑30 років [62].
Зниження м’язової маси спостерігається у 4% чоловіків і 3% жінок віком 70–75 років і зростає відповідно до 16 і 13% в осіб старше 85 років.
Дані щодо поширеності саркопенії різняться залежно від методів діагностування: за результатами дослідження T. Yazar et al. (2018), у літніх осіб без значущої патології вона коливалася від 9,8 до 31,5% [62].
Саркопенія є чинником фізичної немічності літніх людей. Погіршення функціонування «швидких» м’язових волокон, відповідальних за збереження рівноваги, веде до підвищення ризику мимовільних падінь. Наприклад, за даними американського центру контролю захворюваності, саркопенія є одним із п’яти основних чинників захворюваності та смертності в осіб віком від 65 років [9].
Для скринінгу саркопенії запропоновано простий опитувальник для швидкої діагностики саркопенії (SARC-F).
Європейська (EWGSOP, 2010), а потім Азійська (AWGS, 2014) робочі групі із саркопенії у літніх осіб розробили алгоритм діагностування, оснований на вимірюванні швидкості ходьби, сили кистей рук, м’язової маси [12, 15].
Мальнутриція
У широкому розумінні мальнутриція поєднує як дефіцит (протеїнів, вітамінів), так і надлишок (метаболічний синдром, ожиріння) харчування.
Як ГС цей стан зазвичай означає зниження маси тіла. Порушення харчування – поширений розлад у геронтологічній популяціїі, який пов’язаний із розвитком численних захворювань, із погіршенням функціонального статусу і підвищеною смертністю.
Хоча втрата ваги може мати добровільний характер, будь-яке значуще зниження маси тіла потребує настороженості, оскільки сигналізує про соматичну / психічну патологію, або про соціальні / фінансові / функціональні обмеження. Визначають динаміку зміни ваги, окружність талії, індекс маси тіла, а для оцінювання якості харчування використовують такі інструменти, як Міні-опитувальник нутриційного статусу (Mini-Nutritional Assessment), Спрощений опитувальник для оцінювання харчування (Simplified Nutrition Assessment Questionnaire) [25, 61].
Порушення слуху
У старості у понад третини осіб (віком 65‑74 років – у 24%, >75 років – у 40%) знижується слух. Слуховий дефіцит поєднується з погіршенням когнітивних функцій, функціонального стану, зменшенням адаптації у соціумі. Хоча найпростіший підхід для розпізнання – запитати пацієнта, чи є у нього порушення слуху, часто хворі недооцінюють свій стан.
Рекомендовано спектр скринінгових методів: тест із шепотом, тест зі слуховим апаратом; відповідну анкету, створену в межах Національної програми перевірки здоров’я та харчування в США (NHANES) [6, 48].
Одним із найточніших методів діагностування цієї патології є аудіометрія, яка натепер доступна для самооцінки (є відповідний застосунок для смартфона).
Порушення зору
Порушення зору є одним із найчастіших сенсорних дефіцитів. Значущість порушення зору часто лишається в тіні інших ГС і недооцінюється щодо прогностичної точки зору.
Так, за даними національного репрезентативного когортного дослідження здоров’я пенсіонерів Health and Retirement Study у США, порушення зору було пов’язане з поганим станом здоров’я у 50% літніх осіб, із його погіршенням у наступні 2 роки – у 31%, а також асоціювалося з підвищеною смертністю [30].
З погляду на поширеність і несприятливі наслідки порушень зору (падіння, депресія, функціональне зниження) рекомендовано проходити огляд в офтальмолога раз на 1‑2 роки.
Нетримання сечі
Через сором’язливість або ж через сприйняття нетримання сечі як нормальної ознаки старіння геріатричні пацієнти можуть не виявляти скарг. Водночас це поширений феномен, особливо у жінок, часто асоційований з інфекціями сечовивідного тракту, порушеннями сну, падіннями, змінами психіки, пролежнями, підвищеною смертністю [27].
Поряд із віковими і патологічними змінами органів малого тазу в розвитку нетримання сечі суттєву роль відіграють певні лікарські препарати, супутні захворювання, хірургічні втручання, променева терапія, порушення когнітивного та/або фізичного функціонування, психологічні чинники.
Для скринінгу на нетримання сечі запропоновано ставити два запитання:
- Чи були протягом останнього року випадки ненавмисного сечовипускання або «промокання»?
- Чи було у вас нетримання сечі протягом шести окремих днів?
За ствердної відповіді варто поставити додаткове запитання «Чи турбує вас нетримання сечі такою мірою, що ви хотіли б дізнатися, чи можна його лікувати?», яке важливе щодо готовності пацієнта обстежитися і лікуватися.
Когнітивне зниження / деменція
Раннє виявлення когнітивних порушень важливе для ідентифікації курабельних причин, контролю чинників ризику, уповільнення прогресування. На деменції Альцгеймера і судинного / змішаного типу припадає понад 80% її випадків.
Когнітивні порушення асоційовані з ризиком функціональної неспроможності, делірію, падінь. Відображенням важливості когнітивного здоров’я є формування уявлень про «когнітивну немічність» за аналогією з фізичною.
Для скринінгу використовують короткі когнітивні тести Mini-cog, Монреальский (MoCA) і Гонконгський (HKBC), добре відому коротку шкалу для оцінювання психічного статусу (MMSE), тест для лікарів загальної практики GP-Cog, кроскультуральний тест RUDAS тощо [13, 52].
Кожен із них має свої переваги та недоліки. Для первинної ланки системи охорони здоров’я обґрунтованими перевагами є короткий когнітивний тест Mini-cog, який потребує всього 2 хв; він може бути застосований для багатонаціонального населення та осіб із низьким рівнем освіти; його можуть виконувати й оцінювати непрофесіонали без втрати інформативності [1, 11].
Негативні прогнози щодо катастрофічного зростання частоти деменції / когнітивних порушень спонукають до розроблення нових методів скринінгу і раннього діагностування. Так, було продемонстровано більшу чутливість нещодавно розробленого Гонконгського короткого когнітивного тесту порівняно з тестом MoCA [13].
Результати жодного скринінгового тесту не є підставою для встановлення / виключення діагнозу деменції. Високоосвічені особи можуть демонструвати досить високі оцінки, але мати дефіцит розуміння й судження, і навпаки, в осіб із низьким рівнем освіти можуть бути занижені оцінки.
Депресія
Афективні порушення, насамперед депресія, часто виникають в осіб літнього та старечого віку. У 5‑10% загальної популяції віком > 65 років виявляються депресивні синдроми, у 1% – велика депресія; за наявності соматичної / неврологічної патології частота реєстрації депресії перевищує 30%. Є чітка залежність між виразністю депресії та погіршенням фізичного здоров’я, смертністю [23]. Депресія має спільні симптоми, чинники ризику та наслідки з немічністю. Тісне поєднання фізичних і психоемоційних порушень свідчить, що низька фізична активність, втома, втрата ваги є критеріями як ГС немічності, так і депресії [32].
Літні особи зазвичай не характеризують свій стан як депресію; їхні скарги є нетиповими, зокрема, домінують такі як втомлюваність, втрата апетиту, зниження ваги, порушення сну. Для скринінгу застосовують опитувальник з депресії PHQ‑2, за позитивної відповіді пропонується опитувальник PHQ‑9.
Оскільки часто пацієнт літнього віку не в змозі самостійно заповнити анкету, широко використовують Геріатричну шкалу депресії (GDS; версії з 30, 15 і 5 запитаннями), анкетування виконує лікар. Згадана шкала уміщує п’ять запитань і потребує часу в 3‑6 разів менше (до хвилини), вона порівнянна з довшими версіями за чутливістю і специфічністю [40, 44].
Синдром немічності (frailty)
Синдром немічності характеризує асоційоване з віком зниження функціонального резерву, що призводить до вразливості під впливом зовнішніх і внутрішніх стресових чинників і несприятливих медико-соціальних наслідків [39].
Хоча цей синдром і є самостійним, його формування і прогресування тісно пов’язане з розвитком інших ГС, вік-асоційованих захворювань і станів. Закономірно, що частота його виявлення зростає з віком. У США за критеріями дослідження Cardiovascular Health Study (СНS) у популяції осіб віком ≥65 років його діагностують у 7–12% (частота збільшується з віком: із 3,9% у 65–74-річних до 25% у тих, кому 85 років і більше; частіше розвивається в жінок порівняно з чоловіками: 8 проти 5%) [20].
Як зазначалося, дані щодо поширеності суттєво різняться залежно від методів діагностування – від 4 дo 59% [14].
До сьогодні не існує загальноприйнятого стандарту діагностування синдрому немічності. В огляді 2018 р. наведено 89 методів його ідентифікації [55].
Підходи до визначення синдрому немічності різняться не лише методично, але й концептуально. Одні дослідники розглядають його як оцінку фізичного стану людини.
Найвідоміший і широко вживаний фенотип frailty містить п’ять критеріїв:
- втрата маси тіла;
- зниження сили м’язів кистей (за даними динамометрії);
- виразна втомлюваність (за самооцінюванням);
- уповільнення швидкості ходьби (за реєстрацією);
- значне зниження фізичної активності (розрахунок згідно з анкетуванням за Міннесотським опитувальником активності у вільний час [MLTAQ]).
У разі наявності 1–2 балів особу вважали пренемічною (prefrail), 3 і більше балів – немічною (frail) [20].
Спрощений підхід передбачає оцінювання фізичної неспроможності за анкетуванням.
Шкала FRAIL оцінює п’ять параметрів: Fatigue – втома «Чи почуваєте себе стомленим»; Resistance – витривалість «Чи можете піднятись на другий поверх сходами»; Ambulation – аеробна активність «Чи проходите ви пішки один квартал»; Illness – множинна патологія «Чи є у вас п’ять і більше хвороб»; Lost of weight – втрата ваги. Оцінювання результатів аналогічне до такого за фенотипом frailty [36].
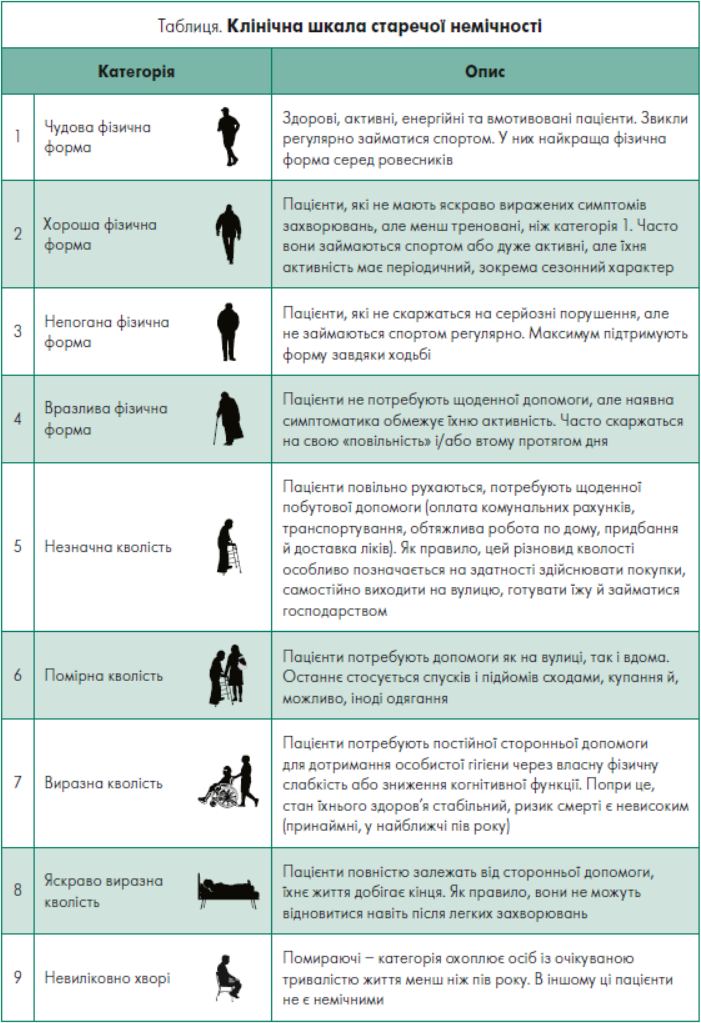
Візуальне оцінювання фізичного стану – найпростіший інструмент, і саме тому воно активно розробляється. Найвідомішою візуальна шкала Clinical Frailty Scale, розроблена 2007–2009 рр. в Університеті Далхаузі, Канада.
Шкала старечої немічності відображає стадії розвитку синдрому немічності: від відмінного стану фізичного здоров’я до пренемічності й різного ступеня немічності (табл.) [42].
Інший методологічний підхід для визначення немічності представлено моделлю накопичення дефіцитів, відомою як індекс Frailty.
Він охоплює сукупність різнопланових дефіцитів:
- тривожні симптоми, зокрема порушення сну, порушення пам’яті, поганий настрій;
- фізичні ознаки, як-от тремор і ослаблений пульс;
- результати лабораторних дослідження, як-от аномальні рівні креатиніну і кальцію в крові;
- супутні захворювання, наприклад діабет або хвороба Паркінсона;
- компоненти інвалідності, зокрема обмеження в повсякденному житті, як-от умивання, одягання, використання туалету і приймання їжі.
Залежно від результатів кожен пацієнт оцінюється як: «дуже здоровий; здоровий; добре контрольований; уразливий; із початковим, помірним або виразним постарінням» [34, 42].
У первинній моделі передбачалося визначення 70 клінічних дефіцитів; надалі модель спростили, і найкоротший варіант містить 30 параметрів [46].
Погляд на немічність як на інтегральну характеристику літньої людини віддзеркалюють й інші моделі, які, окрім фізичного здоров’я, оцінюють когнітивні, психоемоційні, соціальні складники. Edmonton Frail Scale (EFS) охоплює 10 доменів: когніція, баланс, мобільність, настрій, щоденне функціонування, приймання ліків, харчування, ставлення до здоров’я, соціальна підтримка і якість життя [43].
Анкета Tilburg Frailty Indicator (TFI) уміщує соціально-демографічні параметри, спосіб життя, множинні захворювання, життєві події та середовище проживання, фізичні, психологічні й соціальні показники [24].
Анкета Groningen Frailty Indicator (GFI) налічує 15 запитань щодо симптомів постаріння і обмежень щоденного функціонування в чотирьох сферах: фізичній, психологічній, когнітивній і соціальній [54].
Анкета Calgary Cardiac and Cognition Scale охоплює п’ять показників: когнітивні порушення, розлади настрою, порушення балансу, індекс маси тіла <21 або>30 кг/м2, самотнє проживання [19].
Різні методологічні й методичні підходи до виявлення синдрому немічності відображають відсутність єдиного погляду на нього. Частина дослідників розглядають його як вимір фізичного здоров’я і відокремлюють його від «психіко-емоційного» і «соціального» frailty, інші – як спільність порушень фізичного, психоемоційного і соціального здоров’я.
В Україні невизначеність щодо синдрому frailty поширюється і на термінологію: його визначають як старечу астенію; синдром немічності, крихкості, дряхлості, кволості; фрейлті.
Якою є ситуація з діагностуванням геріатричних синдромів за кордоном?
Навіть натепер у низці країн Європи геріатрична служба лишається недостатньо розвинутою. Ба більше, очевидним є прогалина між постійно зростаючою кількістю геріатричних пацієнтів і замалою кількістю геріатрів.
Аналіз, проведений Європейським геріатричним медичним товариством, засвідчив гетерогенність щодо різних аспектів геріатрії у країнах-членах: визнання як окремої спеціальності / субспеціальності, навчання, освітніх та професійних стандартів, академічного представництва, робочого контексту [50]. Системний аналіз баз даних MEDLINE, EMBASE і CINAHL (2010) продемонстрував, що навіть в економічно розвинених країнах лікарі загальної практики виконують когнітивні тести лише для половини геріатричних пацієнтів, а тести для оцінювання ризику падінь – для чверті [4].
Утім, за умов теперішнього глобального постаріння лікарі загальної практики не ознайомлені / недостатньо ознайомлені з ГС і їх наслідками. Попри реальні можливості поліпшити якість життя, знизити ризик захворюваності, госпіталізацій, смертності, питання ранньої діагностики лишаються поза увагою через поширену помилку, що ГС неможливо лікувати (і навіть стабілізувати процес) [47].
Водночас ГС як орієнтири для модифікації лікування пацієнтів із різними видами патології поступово входять до рутинної клінічної практики.
Як приклад можна навести американські (2017) і європейські (2018) рекомендації щодо артеріальної гіпертензії, де під час розгляду питань щодо цільових рівнів артеріального тиску, монотерапії на противагу комбінованій терапії критерієм виступає «frailty» [59, 60].
Діагностування ГС як складова ВГО набуло неабиякого розвитку в онкології, де розроблено скринінговий інструмент G‑8, орієнтований на онкохворих старшого віку [8].
Втім, імплементацію геріатричної діагностики суттєво гальмує її обтяжливість за часом. Саме тому нагальним завданням є розроблення простих методів, які не потребують участі лікаря, багато часу й додаткового обладнання.
Як приклад, коротке геріатричне оцінювання (Rapid Geriatric Assesment) уміщує анкету FRAIL для оцінювання немічності, SARC-F – саркопенії, SNAQ – мальнутриції, Rapid Cognitive Screen – когнітивної дисфункції, яка потребує близько 5 хв і виконується за участю навченої медсестри.
Крім того, для більшого спрощення процедури розроблено мобільний застосунок [33].
У РФ анкету із семи запитань регламентовано щорічно заповнювати особам віком від 60 років для виявлення тих, хто потребує спостереження сімейного лікаря або скерування до лікаря-геріатра для поглибленого дослідження [2].
У чому користь виявлення геріатричних синдромів?
Уже перше рандомізоване дослідження із ВГО L. Z. Rubenstein et al. (1984), складовою якої є діагностування ГС, продемонструвало позитивні результати. Так, очікуваним було поліпшення діагностування й функціонального статусу пацієнтів, зниження інституалізації до будинків для престарілих; неочікуваним – зменшення смертності, частоти повторних госпіталізацій, вартості лікування, а також поліпшення високої функціональної виживаності. Згодом це було підтверджено серією контрольованих досліджень в умовах лікарень, амбулаторій, відвідування вдома [45].
Спільність механізмів розвитку ГС свідчить про можливість одночасного позитивного впливу на них.
Це було підтверджено в проспективному дослідженні з лікування пацієнтів із м’якою-помірною деменцією: реалізація мультимодального впливу із залученням команди фахівців не лише сприяла гальмуванню очікуваного погіршення функціонального стану й когнітивних функцій, але і виявилася дієвою щодо профілактики таких ГС, як падіння, нетримання сечі, порушення харчування [31].
Якою є ситуація з геріатричними синдромами в Україні?
Попри безліч геріатричних діагностичних інструментів та їхню спрямованість на різні ланки медичної практики, у реальних умовах бракує системного скринінгу й поглибленого діагностування ГС в Україні.
Це прямо корелює з відсутністю в країні геріатричної служби і ставить питання про необхідність переосмислення й створення нової концептуальної моделі медичного обслуговування геріатричного контингенту, де одне із центральних місць має посісти раннє виявлення ГС.
Світова практика передбачає створення рекомендацій національними асоціаціями геріатрів щодо ВГО, у якому визначено конкретні валідизовані методи діагностування ГС. При цьому методи геріатричного діагностування мають бути стратифіковані залежно від глибини обстеження та рівня лікувального закладу [3, 7].
Висновки
ГС як хронічне порушення здоров’я має змістовне навантаження, що відрізняє його від таких звичних понять, як «хвороба» і «синдром». На відміну від більшості традиційних синдромів, де сукупність симптомів зазвичай виникає через єдиний етіологічний чинник, ГС мають поліетіологічну природу, але маніфестують у вигляді єдиної ознаки. Маючи загальні чинники ризику, вони співіснують і чинять взаємний вплив.
Кількість осіб із ГС збільшується не тільки через старіння населення, а й через підвищення виживаності пацієнтів із тяжкими захворюваннями. ГС мають прогностичну значущість щодо тривалості життя, функціонального стану та якості життя. Розвиток ГС можна не лише загальмувати, але й сприяти частковій / повній регресії. Спільність патогенетичних механізмів визначає можливість одночасного позитивного впливу на низку ГС.
Зокрема, ГС лежать в основі стратифікації геріатричних пацієнтів, що є невід’ємною складовою ВГО; слугують концептуальним і методичним підґрунтям організації медико-соціального забезпечення осіб літнього віку.
Насамкінець слід зазначити, що настав час для переосмислення наявної та створення нової моделі медичного обслуговування геріатричного контингенту, де центральне місце має посісти раннє виявлення ГС як невід’ємного компонента ВГО. За рекомендаціями Всесвітньої організації охорони здоров’я, не кожен літній пацієнт підлягає спостереженню лікаря-геріатра і потребує спеціалізованої геріатричної допомоги. Основою відокремлення уразливого геріатричного контингенту є скринінг на ГС, які найбільше обмежують життєдіяльність індивідуума.
Нині в Україні ГС лишаються terra incognita для широкого медичного загалу, практично немає геріатричної складової в підготовці лікарів і в післядипломній освіті, як і геріатрів загалом. Водночас ВГО з діагностуванням ГС є реальним інструментом для поліпшення якості життя, зниження частоти госпіталізації, інвалідизації та смертності.
Власне, брак «золотих» стандартів виявлення ГС порушує питання щодо розроблення саме національних стандартів геріатричного діагностування.
Список літератури знаходиться в редакції.
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 4 (63) 2022 р.