16 лютого, 2026
Лікування болю в пацієнтів із хронічними захворюваннями: вибір оптимального НПЗП
Приблизно 20% дорослих світу (еквівалентно >1,5 млрд осіб) страждають через хронічний біль [1, 2]. Ця цифра охоплює різні стани, включаючи розлади опорно-рухового апарату, нейропатичний біль та інші хронічні больові синдроми. Основними знеболювальними та водночас найзастосовуванішими засобами в світі [3] є нестероїдні протизапальні препарати (НПЗП). Наявність коморбідної патології потребує обережності при призначенні НПЗП, особливо серед пацієнтів старшого віку через наявність високого ризику розвитку серцево-судинних, ниркових ускладнень, захворювань печінки і шлунково-кишкового тракту (ШКТ).
У пацієнтів з остеоартритом (ОА), ревматоїдним артритом, анкілозивним спондилітом довготривале лікування неоптимальним НПЗП може мати негативні наслідки на перебіг основного захворювання, адже одним із довгострокових побічних ефектів НПЗП є негативний вплив на суглобовий хрящ.
Дослідження продемонстрували, що деякі НПЗП прискорюють рентгенографічне прогресування ОА. Саме масове використання НПЗП у пацієнтів з ОА протягом останніх 40 років є однією з основних причин швидкого зростання потреби в ендопротезуванні кульшового та колінного суглобів [4].
! На тлі терапії НПЗП важливим під час ведення пацієнтів із хронічним больовим синдромом є застосування стратегій профілактики ускладнень, що передбачає ідентифікацію факторів ризику та використання оптимальних терапевтичних доз НПЗП. Також варто зважати на те, що деякі НПЗП схвалені лише для короткочасного прийому (наприклад, кеторолак, німесулід).
Англійська дослідницька група LINK порівнювала швидкість рентгенологічного прогресування ОА колінного суглоба при застосуванні індометацину та плацебо. В дослідженні взяли участь 20 ревматологічних клінік Великої Британії. На 3-й рік у групі індометацину було удвічі більше пацієнтів, у яких спостерігалося прогресування [4].
Нідерландські дослідники вивчили >1600 осіб з ОА кульшового суглоба та 635 – з ОА колінного суглоба. Середній період спостереження становив 6,6 року. Виявлено, що тривале застосування диклофенаку пов’язувалося з більш ніж дворазовим збільшенням радіологічного прогресування ОА кульшового суглоба та триразовим – колінного суглоба. Було також показано, що використання ібупрофену пов’язано зі статистично значущим збільшенням прогресування ОА [4].
Раніше вважали, що селективність НПЗП регулює профіль серцево-судинної токсичності, проте останні результати свідчать, що серцево-судинний ризик може бути специфічним для препарату: рофекоксиб пов’язаний з підвищеним ризиком серцево-судинних подій, тоді як целекоксиб асоціюється з нижчою частотою інсульту порівняно з іншими НПЗП [5].
Під час проведення ретроспективного об’єднаного аналізу 21 РКД (9461 пацієнт віком ≥65 років з ОА, ревматоїдним артритом чи анкілозувальним спондилітом) виявлено, що побічні ефекти з боку ШКТ виникли в меншої кількості пацієнтів, котрі отримували целекоксиб (16,7%), ніж напроксен (29,4%), ібупрофен (26,5%) або диклофенак (21%) [5].
Через ризик розвитку ускладнень під час застосування НПЗП Європейське товариство клінічних та економічних аспектів остеопорозу, ОА і захворювань опорно-рухового апарату (ESCEO) рекомендувало використовувати НПЗП у найнижчій ефективній дозі протягом найкоротшого періоду часу, необхідного для контролю болю. Робоча група ESCEO вважає, що целекоксиб може бути кращим пероральним НПЗП через баланс між високою ефективністю при ОА в схвалених дозах і його меншою токсичністю, особливо на ШКТ [5].
Європейське агентство з лікарських засобів (EMA) підкреслює, що диклофенак, особливо у високих дозах (150 мг/добу), може асоціюватися з підвищеним ризиком артеріальних тромбозів (наприклад, інфаркту міокарда й інсульту). Що стосується целекоксибу, то його застосування з аспірином не зумовлює підвищення ризику кардіоваскулярних подій. У рекомендаціях Європейської мультидисциплінарної групи експертів щодо прийнятного використання НПЗП при ревматичних захворюваннях (2011) целекоксиб зазначено як один із найбезпечніших препаратів [6].
! Отже, НПЗП, якому варто віддати перевагу, можна вважати целекоксиб, котрому притаманні висока ефективність і низький потенціал токсичності, особливо щодо шлунково-кишкових і серцево-судинних побічних ефектів [7].
За результатами дослідження PRECISION, застосування целекоксибу супроводжувалося достовірно нижчим кардіоренальним ризиком, ніж використання ібупрофену; аналогічна тенденція виявлена під час порівняння з напроксеном (Obeid S. et al., 2022). В іншому клінічному дослідженні було показано достовірно нижчий ризик клінічно значущих подій із боку ШКТ при застосуванні целекоксибу порівняно з комбінацією диклофенак + омепразол (Chan F.K. et al., 2010). Відповідно до масштабного метааналізу F. Gregori та співавт. (2018), целекоксиб виявився єдиним НПЗП, прийом якого супроводжувався довгостроковим полегшенням болю. Автори також відзначили кращу гастроінтестинальну переносимість за тривалого застосування порівняно з неселективними НПЗП і відсутність зв’язку з підвищенням ризику кардіоваскулярних подій [7].
! Доказова база останніх років свідчить, що інгібітор ЦОГ‑2 целекоксиб може мати не лише аналгетичний і протизапальний, а й хворобомодифікувальний ефект.
Целекоксиб здатний стимулювати синтез протеогліканів і затримувати їх у хрящовій тканині. Нормалізація вмісту протеогліканів у хрящовій тканині свідчить про те, що раннє застосування цього препарату здатне сповільнити хондродеструкцію або навіть забезпечити її зворотний розвиток. Механізмами хондропротекторної дії целекоксибу можуть бути пригнічення вивільнення ПГ Е2, підтримання збалансованої дії протеолітичних ферментів у циклі деструкції й утворення хряща та зменшення вироблення оксиду азоту, який індукує апоптоз хондроцитів й активує руйнівні ферменти – матриксні металопротеїнази [7].
Під час проведення дослідження S. Cheleschi та співавт. (2021) in vitro виявлено, що глюкозаміну сульфат і целекоксиб чинять синергічну хондропротекторну, протизапальну, антиапоптичну й антиоксидантну дію (рис.).
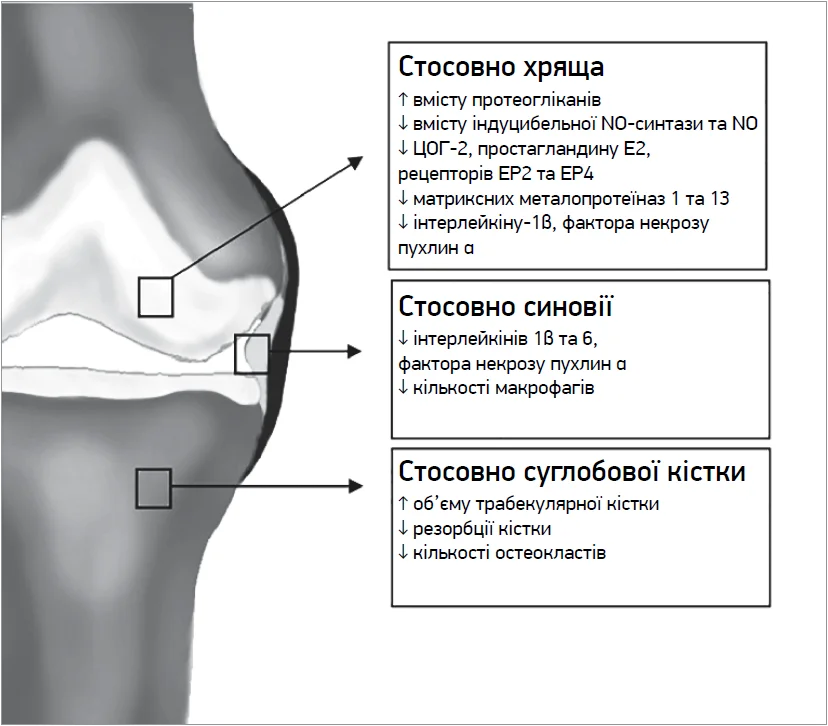 Рис. Ефекти целекоксибу in vivo
Рис. Ефекти целекоксибу in vivo
Іншим ЦОГ‑2-селективним НПЗП є еторикоксиб. Утім, консультативний комітет із лікування артриту при Управлінні з контролю за якістю продуктів харчування та лікарських засобів США (FDA) проголосував проти схвалення еторикоксибу для лікування болю за ОА через занепокоєння щодо серцево-судинних ризиків і відсутність доказів значної переваги над іншими НПЗП. Дослідження препарату Arcoxia демонструють, що він може збільшувати ризик підвищення артеріального тиску та виникнення застійної серцевої недостатності [8].
Целекоксиб (оригінальний препарат – Целебрекс®) є першим специфічним інгібітором ЦОГ‑2, дозволеним для використання при ОА та ревматоїдному артриті; рекомендований ESCEO як НПЗП першого вибору в разі ОА. Целекоксиб значно полегшує біль і запалення під час лікування протягом 24 тиж. Дослідження демонструють, що целекоксиб має таку саму ефективність, як і неселективні НПЗП, щодо полегшення болю та покращення функціонального стану, але пов’язаний з меншою частотою виразки верхніх відділів ШКТ. Сприятливий профіль безпеки разом із тривалим полегшенням симптомів робить целекоксиб оптимальним для довготривалого лікування, особливо в пацієнтів із високим ризиком розвитку шлунково-кишкових ускладнень [9].
Список літератури знаходиться в редакції.
Підготувала Олена Костюк
UKR-CELE-2025-00024
Медична газета «Здоров’я України 21 сторіччя» № 23-24 (610-611), 2025 р



