3 грудня, 2019
Результати 5-річного застосування дабрафенібу і траметинібу при метастатичній меланомі

Ще донедавна метастатична меланома асоціювалася з поганим прогнозом, проте після впровадження BRAF- і MEK‑таргетних агентів та інгібіторів контрольних точок результати лікування пацієнтів із цим захворюванням значно покращилися. Ці препарати, включно з блокаторами білка програмованої клітинної смерті 1 (PD‑1) й інгібіторами білка 4, асоційованого з цитотоксичними Т-лімфоцитами (CTLA‑4), здатні покращувати виживаність у певній підгрупі пацієнтів. Утім у багатьох хворих розвивається резистентність (первинна або набута), що зрештою призводить до смерті від меланоми. У дослідженнях ІІІ фази анти-PD‑1 препарати (пембролізумаб, ніволумаб), застосовані в 1-й лінії терапії, забезпечували виживаність без прогресування (ВБП) 27‑31% та загальну виживаність (ЗВ) 46% через 4 роки; у пацієнтів, які отримували пембролізумаб, 5-річна ЗВ становила 43%. У хворих, лікованих комбінацією ніволумабу й іпілімумабу, 4-річні ВБП та ЗВ дорівнювали 37 та 53% відповідно. Даних щодо 5-річної виживаності при застосуванні інших BRAF-таргетних препаратів у дослідженнях ІІІ фази поки що немає. Ці дані дозволять оцінити здатність терапії забезпечувати тривалий контроль хвороби (на підставі аналізу плато виживаності), а також вивчити фактори, які є прогностичними стосовно довгострокової виживаності.
У двох раніше оприлюднених рандомізованих дослідженнях ІІІ фази (COMBI-d та COMBI-v) оцінювали ефективність і безпеку комбінації дабрафеніб + траметиніб проти монотерапії інгібітором BRAF у пацієнтів з нерезектабельною чи метастатичною меланомою з мутаціями BRAF V600E або V600K. У попередньому об’єднаному аналізі даних пацієнтів, лікованих дабрафенібом і траметинібом, 3-річні ВБП та ЗВ становили 23% (95% довірчий інтервал – ДІ – 20-27) та 44% (95% ДІ 40-49) відповідно. Одномірний і багатомірний аналізи виявили статистично значимий взаємозв’язок між численними початковими параметрами (як-от функціональний статус за ECOG, стать, вік, кількість органів із метастазами, рівень лактатдегідрогенази – ЛДГ) та ВБП й ЗВ.
Метою цього дослідження було оцінити 5-річні результати лікування пацієнтів, які отримували дабрафеніб і траметиніб у дослідженнях COMBI-d та COMBI-v, зокрема ВБП та ЗВ, а також визначити потенційні фактори, асоційовані з довгостроковою користю від цієї терапії.
Методи
Був проведений аналіз об’єднаних даних ITT-популяції (від intention-to-treat – пацієнти, які отримали принаймні 1 дозу досліджуваного препарату) раніше не лікованих хворих на метастатичну меланому з мутаціями BRAF V600E або V600K у дослідженнях COMBI-d та COMBI-v. Вік учасників цих досліджень був у межах 22‑89 років та 18-91 року відповідно. Пацієнтів рандомізували для прийому комбінації дабрафеніб + траметиніб або контрольної терапії.
COMBI-d – подвійне сліпе рандомізоване дослідження ІІІ фази, в якому порівнювали дабрафеніб + траметиніб та дабрафеніб + плацебо. У відкритому рандомізованому дослідженні ІІІ фази COMBI-v оцінювали дабрафеніб + траметиніб порівняно з вемурафенібом. В обох дослідженнях пацієнтів стратифікували залежно від генотипу BRAF та початкового рівня ЛДГ, лікування продовжували до прогресування хвороби або розвитку неприйнятної токсичності.
Первинною кінцевою точкою у COMBI-d та COMBI-v були ВБП та ЗВ відповідно. Додатково оцінювали частоту і тривалість відповіді, безпеку та інші показники.
Результати
Загалом для лікування комбінацією дабрафеніб + траметиніб було рандомізовано 563 пацієнти – 211 у COMBI-d та 352 у COMBI-v. Із цих пацієнтів 363 (64%) мали меланому IV стадії M1c, рівень ЛДГ був підвищеним у 194 (34%) хворих.
Виживаність без прогресування
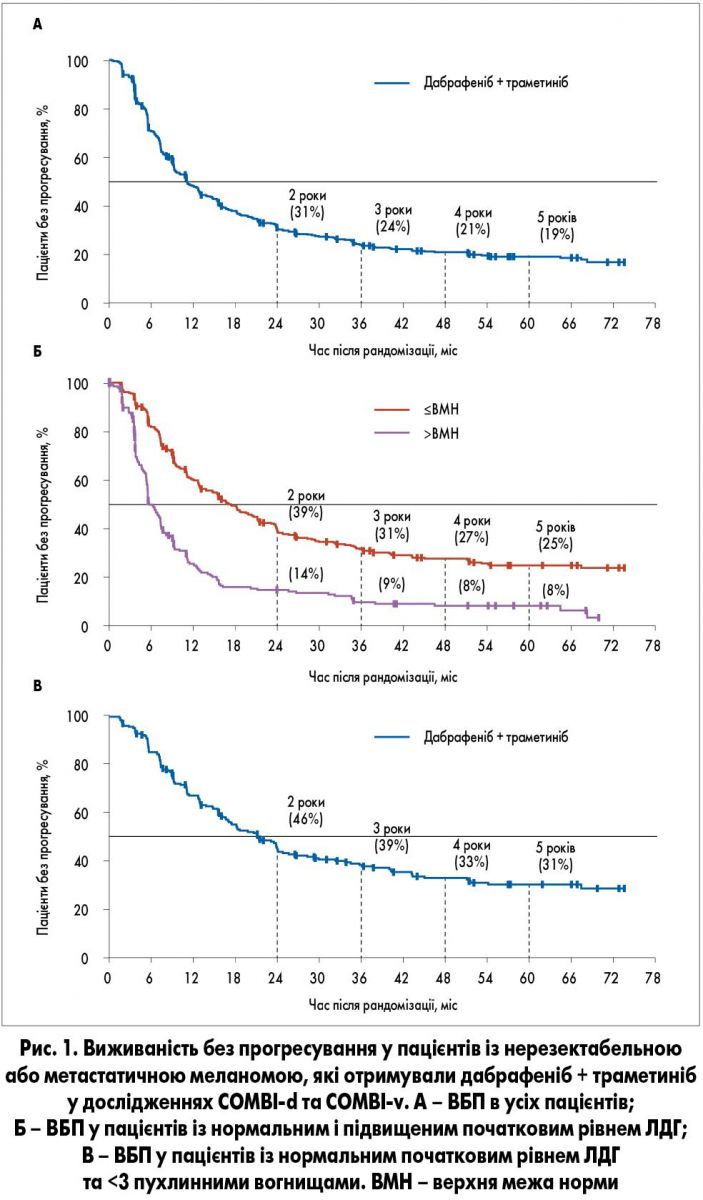
Прогресування хвороби або смерть зафіксовано в 417 (74%) з 563 пацієнтів. Медіана ВБП дорівнювала 11,1 міс (95% ДІ 9,5-12,8). ВБП становила 21% (95% ДІ 17‑24) через 4 роки та 19% (95% ДІ 15-22) через 5 років (рис. 1А). У пацієнтів з нормальним початковим рівнем ЛДГ 5-річна ВБП дорівнювала 25% (95% ДІ 20-30) проти 8% (95% ДІ 4-13) у хворих, у яких цей показник був підвищеним (рис. 1Б). Регресійний аналіз виявив підгрупу з 216 (38%) пацієнтів з особливо високою ВБП, яка характеризувалася нормальним початковим рівнем ЛДГ та наявністю <3 вогнищ хвороби до лікування. У цій підгрупі 5-річна ВБР склала 31% (95% ДІ 24-38; рис. 1В).
Із 59 пацієнтів, які залишилася у дослідженні та не мали прогресування через 5 років після рандомізації, 52 (88%) продовжували отримувати дабрафеніб та/або траметиніб. Багатомірний аналіз дозволив ідентифікувати низку факторів, які статистично значимо асоціювалися з подовженою ВБП (р<0,05): старший вік, жіноча стать, генотип BRAF V600E, кращий функціональний статус, нормальний рівень ЛДГ та <3 пухлинних вогнищ. Взаємозв’язок із ВБП був особливо помітним стосовно факторів, асоційованих зі специфікою кінетики пухлини та тяжкістю хвороби (функціональний статус, рівень ЛДГ, кількість пухлинних вогнищ).
Протипухлинне лікування після завершення терапії дабрафенібом і траметинібом
Після припинення прийому досліджуваних препаратів подальше протипухлинне лікування отримували 299 (53%) із 563 пацієнтів, рандомізованих на дабрафеніб і траметиніб. Найчастіше застосовували імунотерапію – у 196 (66%) з 299 хворих; зокрема 151 (51%) пацієнт отримував анти-CTLA‑4 терапію та 102 (34%) – анти-PD‑1 терапію.
Варто зауважити, що після припинення терапії досліджуваними препаратами не здійснювали оцінку відповіді за критеріями RECIST і не збирали дані щодо методу оцінки відповіді (клінічні критерії або RECIST), дозування або схеми лікування, а також причини відміни наступної терапії.
Загальна виживаність
На час цього аналізу помер 351 (62%) пацієнт із 563. Медіана ЗВ становила 25,9 міс (95% ДІ 22,6-31,5), 4- та 5-річна ЗВ – 37 (95% ДІ 33-42) та 34% (95% ДІ 30‑38) відповідно (рис. 2А). 5-річна ЗВ була вищою у пацієнтів з нормальним початковим рівнем ЛДГ (43%; 95% ДІ 38‑49), ніж у хворих із підвищеним рівнем (16%; 95% ДІ 11‑22; рис. 2Б). Серед пацієнтів із нормальним рівнем ЛДГ і кількістю метастатичних вогнищ <3 до лікування розрахована ЗВ становила 67% (95% ДІ 48‑61; рис. 2В). Вихідні фактори, які корелювали із ЗВ за результатами багатомірного аналізу, загалом відповідали факторам, що асоціювалися з ВБП.
Початкові характеристики пацієнтів, які залишалися живими через 5 років після рандомізації, були подібними до таких у хворих, котрі не мали прогресування. Серед 161 пацієнта, які продовжували участь у дослідженні, дабрафеніб та/або траметиніб отримували 69 (43%). Подальшу протипухлинну терапію застосовували в 72 (45%) зі 161 пацієнта; найчастіше це була імунотерапія анти-CTLA‑4 та/або анти-PD‑1 препаратами.
Частота відповіді
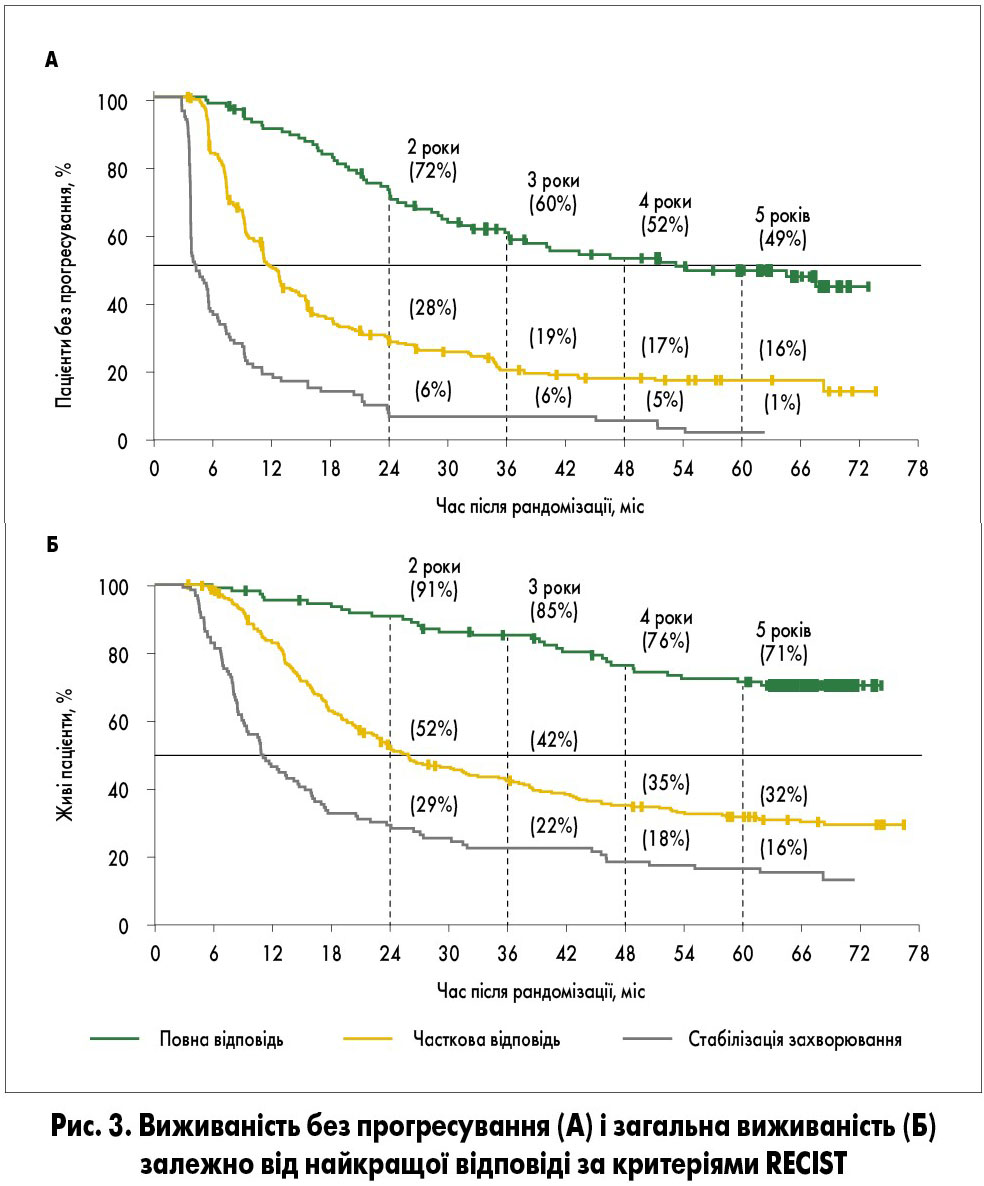
Об’єктивна відповідь на лікування комбінацією дабрафеніб + траметиніб була зафіксована у 383 (68%) із 563 пацієнтів, зокрема повна відповідь – у 109 (19%). У пацієнтів із повною відповіддю 5-річна ВБП становила 49% (95% ДІ 39-58) проти 16% (95% ДІ 12-22) у хворих із частковою відповіддю та 1% (95% ДІ 0-6) у пацієнтів зі стабілізацією захворювання (рис. 3А).
Із 59 пацієнтів, які не мали прогресування через 5 років після рандомізації, об’єктивна відповідь була підтверджена в 58 (98%; 95% ДІ 91-100), включно з 37 (63%) хворими із повною відповіддю. 5-річна ЗВ склала 71 (95% ДІ 62‑79), 32 (95% ДІ 26-37) та 16% (95% ДІ 10-24) у пацієнтів із повною відповіддю, частковою відповіддю та стабілізацією захворювання відповідно (рис. 3Б). Більшість хворих, які залишалися живими через 5 років після рандомізації, мали підтверджену об’єктивну відповідь (90%; 95% ДІ 84-94), включно з 72 (45%) пацієнтами з повною відповіддю. Медіана повної відповіді дорівнювала 36,7 міс (95% ДІ 24,1 – не досягнуто).
Початкові характеристики пацієнтів із повною відповіддю були подібними до таких у хворих без прогресування через 5 років. Пацієнти з повною відповіддю, які не мали прогресування захворювання (або вибули з дослідження до прогресування), та всі пацієнти з повною відповіддю за початковими характеристиками істотно не відрізнялися.
Із 383 пацієнтів із повною або частковою відповіддю 88 (23%) хворих припинили лікування препаратами, що вивчалися, до прогресування захворювання. Після цього 48 (55%) з них проходили додаткові візуалізаційні дослідження. Дані щодо прогресування, наявні для 15 хворих, свідчать, що медіана до прогресування становила 3,7 міс.
Небажані події
Небажані події (незалежно від причини) відбулися в 548 з 559 (98%) пацієнтів; жодних неочікуваних небажаних подій протягом подовженого періоду спостереження не було. У 99 (18%) хворих небажані події призвели до остаточного припинення лікування досліджуваними препаратами; найчастіше це були підвищення температури тіла (4%), зниження фракції викиду лівого шлуночка (4%) та підвищення активності аланінамінотрансферази (1%). Серед пацієнтів, які отримували дабрафеніб + траметиніб, не було жодного випадку смерті, потенційно пов’язаного із застосуванням цих препаратів.
Висновки
Аналіз об’єднаних даних досліджень COMBI-d та COMBI-v показав, що 1-ша лінія терапії комбінацією дабрафеніб + траметиніб забезпечує 5-річну виживаність приблизно у третини пацієнтів із нерезектабельною або метастатичною меланомою з мутаціями BRAF V600E або V600K. Повна відповідь на комбіноване лікування є сильним і раннім предиктором довгострокової користі. Біомаркерів, які б дозволяли визначати ризик прогресування після припинення терапії, на сьогодні не існує.
Список літератури знаходиться в редакції.
Стаття друкується у скороченні.
Robert C., Grob J.J., Stroyakovskiy D. et al. Five-Year Outcomes with Dabrafenib plus Trametinib in Metastatic Melanoma. N Engl J Med. 2019 Aug 15; 381(7): 626-636.
Переклав з англ. Олексій Терещенко
Коментарі експертів
 П.Д. Натан, Онкологічний центр Маунт-Вернон (Велика Британія)
П.Д. Натан, Онкологічний центр Маунт-Вернон (Велика Британія)
– Результати 5-річного спостереження за учасниками досліджень COMBI-d та COMBI-v, представлені на щорічному конгресі Американського товариства клінічної онкології (ASCO‑2019), показали виживаність без прогресування 19% та загальну виживаність 34% у цій популяції хворих [із нерезектабельною або метастатичною меланомою з мутаціями BRAF V600]. Примітно, що серед 19% пацієнтів, у яких було досягнуто повної відповіді на цю комбінацію [дабрафеніб + траметиніб], 49% не мали прогресування та 71% залишалися живими через 5 років. Отримані дані свідчать, що хворі на меланому з мутаціями BRAF V600 добре піддаються лікуванню інгібіторами BRAF/MEK. Пацієнти, котрі мають сприятливі початкові характеристики та рано досягають повної відповіді на лікування, імовірно отримують найбільшу користь від комбінованої терапії. З огляду на ці результати молекулярне тестування BRAF має стати стандартним дослідженням [у пацієнтів із нерезектабельною або метастатичною меланомою]. Таке тестування також є доцільним у пацієнтів із ІІІ стадією захворювання, які можуть отримувати користь від ад’ювантної терапії інгібіторами BRAF.
https://www.onclive.com/onclive-tv/dr-nathan-on-long-term-outcomes-with-dabrafenib-trametinib-in-braf-v600-mutant-melanoma
 К. Робер, Інститут Гюстава Руссі (Франція)
К. Робер, Інститут Гюстава Руссі (Франція)
– Наш аналіз показав, що застосування комбінації дабрафеніб + траметиніб як першої лінії терапії дозволяє досягти контролю над захворюванням протягом п’яти років у 1/5 пацієнтів і 5-річної виживаності приблизно у 1/3 пацієнтів. Хоча прогноз у хворих на метастатичну меланому завжди вважали несприятливим, сьогодні існує безліч причин не впадати у відчай. Отримані дані показали клінічно значимий позитивний вплив на виживаність пацієнтів. Ці результати свідчать, що таргетна терапія може забезпечити довгострокову виживаність і стійкий результат.
https://www.novartis.com/news/media-releases/long-term-survival-benefit-shown-metastatic-melanoma-patients-treated-novartis-tafinla-mekinist
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 3 (59), 2019 р.