4 червня, 2018
Дабрафениб и траметиниб в лечении пациентов с метастатической меланомой и мутацией BRAF V600E/K

До недавнего времени прогноз для пациентов с метастатической меланомой оставался неблагоприятным. Так, 5-летняя выживаемость составляла 6%, а медиана общей выживаемости (ОВ) – 7,5 мес. Значительный прогресс в лечении больных с метастатической формой меланомы связан с пониманием ее молекулярных механизмов, изучение которых позволило изменить подход к терапии. Новые терапевтические опции позволили значительно увеличить продолжительность жизни, следовательно актуальным аспектом стало качество жизни этих пациентов.
Первым препаратом, продемонстрировавшим долговременную клиническую эффективность у пациентов с меланомой на поздних стадиях независимо от молекулярного профиля, стало антитело, нацеленное на цитотоксический T-лимфоцитарный протеин (анти-CTLA‑4), – ипилимумаб. Применение комбинации ингибиторов BRAF и MEK (ингибиторы BRAF/MEK), а также режимов терапии на основе ингибиторов PD‑1 продемонстрировало значительное улучшение клинических исходов в исследованиях III фазы у пациентов с метастатической меланомой, однако длительность наблюдения в этих исследованиях была ограничена 2 годами. Предполагалось, что таргетная терапия будет связана с быстрым ухудшением состояния и смертью после развития вторичной резистентности, однако данные крупных долгосрочных рандомизированных исследований отсутствуют. В связи с расширением возможностей терапии BRAF V600-положительной меланомы актуальным является определение группы пациентов, для которой лечение будет наиболее эффективным.
Комбинация дабрафениба и траметиниба обеспечивала увеличение выживаемости без прогрессирования (ВБП) и ОВ по сравнению с монотерапией ингибиторами BRAF в рандомизированных исследованиях II и III фазы у пациентов с неоперабельной меланомой IIIC стадии или метастатической меланомой IV стадии и мутацией BRAF V600E/K. Комбинированная терапия была сопряжена со снижением частоты гиперпролиферативных поражений кожи (плоскоклеточный рак, кератоакантома) по сравнению с монотерапией ингибиторами BRAF, на фоне комбинированной терапии напротив чаще наблюдалось развитие пирексии.
Последний анализ рандомизированного исследования III фазы COMBI-d, в котором сравнивали эффективность комбинации дабрафениб + траметиниб и дабрафениба в сочетании с плацебо, дал такие результаты: медиана ВБП составила 11,0 и 8,8 мес (относительный риск – ОР – 0,67; 95% доверительный интервал – ДИ – 0,53-0,84; P 0,0004), медиана ОВ – 25,1 и 18,7 мес (ОР 0,71; 95% ДИ 0,55-0,92; P 0,0107), а 2-летняя ОВ – 51 и 42% соответственно. Эти результаты подтвердили данные первичного анализа COMBI-d и согласуются с результатами рандомизированного исследования III фазы COMBI-v.
Наиболее длительный период наблюдения (медиана 45,6 мес) был зарегистрирован в рандомизированном исследовании II фазы BRF113220 (часть C), в котором сравнивали эффективность применения дабрафениба в комбинации с траметинибом (n=54) и монотерапии дабрафенибом (n=54). У пациентов группы комбинированной терапии 2- и 3-летняя ВБП составила 25 и 21%, а 2- и 3-летняя ОВ – 51 и 38% соответственно.
 В настоящее время установлено, что эффективность лечения при метастатической меланоме может различаться в зависимости от исходных характеристик пациента.
В настоящее время установлено, что эффективность лечения при метастатической меланоме может различаться в зависимости от исходных характеристик пациента.
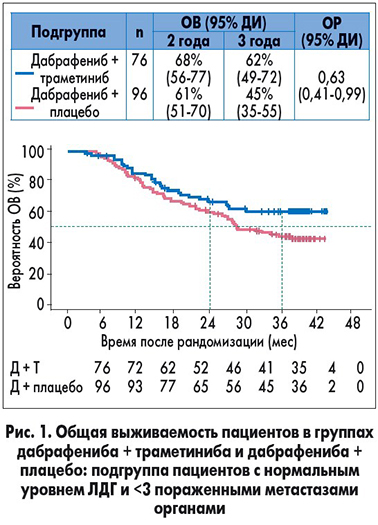
Объединенные данные этих исследований показали, что нормальный исходный уровень сывороточной лактатдегидрогеназы (ЛДГ) и поражение метастазами <3 органов являются благоприятными факторами. У пациентов с наличием этих факторов 2-летняя ВБП и ОВ достигали 46 и 75% соответственно. Текущий анализ исследования COMBI-d подтверждает это: самый высокий показатель 3-летней ОВ наблюдался у пациентов с нормальным значением ЛДГ и метастазами менее чем в 3 органах после комбинированной (у 62%) и монотерапии (у 45%; рис. 1). Таким образом, комбинированная терапия позволяет достичь большей выживаемости в случае наличия благоприятных прогностических факторов. Даже у пациентов с исходным уровнем ЛДГ выше порогового на фоне комбинированной терапии 3-летняя выживаемость была выше (25% против 14%; рис. 2).
Период наблюдения в исследовании COMBI-d (3 года) является наиболее продолжительным среди исследований III фазы по изучению комбинированной анти-BRAF/MEK терапии. Этапный анализ подтверждает долгосрочную клиническую эффективность и хорошую переносимость дабрафениба в комбинации с траметинибом у ранее нелеченных пациентов с BRAF V600E/K-положительной метастатической меланомой. Стоит отметить, что эти данные опровергают предположение о том, что у большинства пациентов, получавших ингибиторы протеинкиназы, быстро развивается вторичная резистентность. На 3-м году наблюдения комбинированная терапия продолжала демонстрировать значительное преимущество (ВБП – 22% против 12%, ОВ – 44% против 32%). В то время как многие пациенты, преодолевшие порог 3-летней выживаемости, продолжали получать дабрафениб и траметиниб, 12% пациентов, изначально получавших один лишь дабрафениб, перешли на комбинированное лечение [1].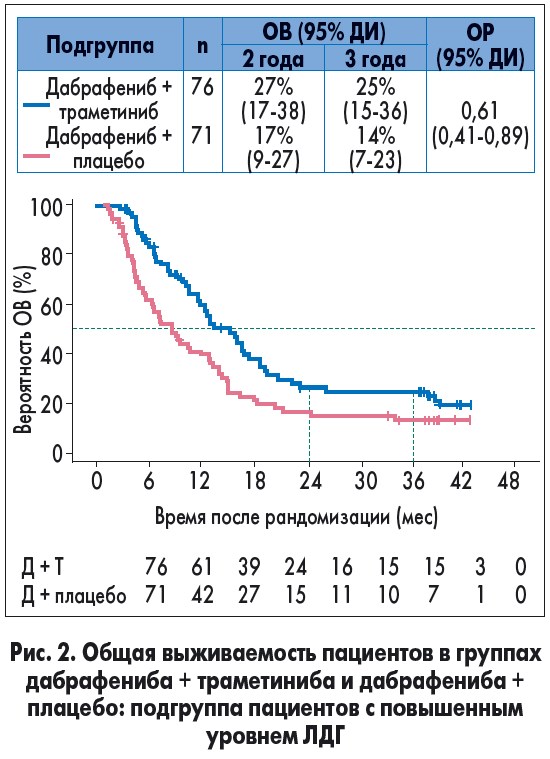
В этом исследовании 3-летняя ОВ на фоне комбинированной терапии (44%) подтверждает полученные ранее результаты (рандомизированное исследование II фазы BRF113220, 3-летняя ОВ – 38%). Двухлетняя ОВ (52%) сопоставима с таковой в рандомизированном исследовании COMBI-v (51%) и в объединенном анализе всех регистрационных исследований (53%) [2]. У пациентов, получивших любую системную терапию после прогрессирования заболевания, дальнейшее применение анти-PD‑1 было сходным в группах комбинированной и монотерапии, а частота последующей терапии ипилимумабом была выше в группе монотерапии. Таким образом, более высокая 3-летняя ОВ у пациентов, получавших дабрафениб и траметиниб, обусловлена именно комбинированным лечением.
Прямое сравнение показателей выживаемости, полученных при изучении доступных в настоящее время методов лечения, следует осуществлять с осторожностью из-за различий в исходных характеристиках исследуемых групп, включая наличие мутации BRAF V600E/K, а также время проведения исследования (например, какие методы лечения были доступны для последующей терапии). Хотя прямые сравнительные исследования по применению таргетной и иммунотерапии отсутствуют, тем не менее основные клинические исследования могут определить тенденции для каждого класса лекарственных препаратов. Важно сбалансировать преимущества иммунотерапии анти-PD‑1 (анти-CTLA‑4) и комбинированной терапии ингибиторами BRAF/MEK.
Продолжительность последующего наблюдения в ходе изучения эффективности анти-PD‑1 иммунотерапии несколько уступает таковой в исследованиях, посвященных таргетной терапии. Ориентировочный показатель 3-летней ОВ в настоящее время доступен только для исследований более ранней фазы. В исследовании I фазы, в котором оценивали монотерапию ниволумабом у 107 ранее леченных пациентов с меланомой независимо от мутационного статуса BRAF и повышенным уровнем ЛДГ у 36% больных, 2-, 3- и 5-летняя ОВ составила 48, 42 и 34% соответственно. В исследовании І фазы терапия ниволумабом в сочетании с ипилимумабом у 53 пациентов с распространенной меланомой независимо от ранее проведенного лечения способствовала увеличению 3-летней ОВ до 68%. Однако следует отметить, что эти результаты являются предварительными, а в соответствующих рандомизированных исследованиях выявлено, что 2-летняя выживаемость составила 64% – меньше, чем в исследовании I фазы. По мере того, как в более крупных исследованиях, посвященных оценке анти-PD‑1 терапии при метастатической меланоме, продолжается наблюдение, недавний метаанализ не продемонстрировал существенной разницы ОВ, обеспечиваемой ингибиторами BRAF/MEK и анти-PD‑1.
В целом данные о доступных в настоящее время методах лечения свидетельствуют, что не только иммунотерапия может увеличить продолжительность жизни пациентов с метастатической меланомой. Хотя первоначальная клиническая активность (например, частота ответов) между этими терапевтическими классами различается, доля пациентов, преодолевших порог 3-летней выживаемости, может быть сходной, что должно быть подтверждено дополнительным анализом иммунотерапии, особенно у пациентов с BRAF-мутацией.
Важно отметить, что плато выживаемости, полученное на фоне терапии ипилимумабом, еще не было достигнуто на фоне анти-PD‑1-терапии и остается потенциальной целью для комбинированной терапии ингибиторами BRAF/MEK.
Наиболее длительное наблюдение по оценке терапии ингибиторами BRAF/MEK среди исследований III фазы показало увеличение долгосрочной выживаемости на фоне терапии дабрафенибом в сочетании с траметинибом и ее хорошую переносимость у больных метастатической меланомой с мутацией BRAF V600. Эти результаты подтверждают эффективность продолжительного лечения дабрафенибом в сочетании с траметинибом в качестве первой линии терапии для пациентов с распространенной BRAF V600-положительной меланомой. Тем не менее есть необходимость в создании более полной модели, которая включала бы прогностические факторы, молекулярные и/или иммунные маркеры для дальнейшего принятия решений относительно этой популяции пациентов.
Последующее наблюдение в исследовании COMBI-d, запланированное на срок до 5 лет, обеспечит дальнейшее понимание преимуществ комбинированной терапии.
Данные по профилю безопасности дабрафениба в сочетании с траметинибом при длительном наблюдении были аналогичны полученным ранее; комбинированная терапия связана со снижением токсичности, связанной с парадоксальной активацией митогенактивированного протеинкиназного пути. Пирексия оставалась наиболее распространенным побочным эффектом комбинированной терапии, тем не менее она – управляемое нежелательное явление [3]. При последующем наблюдении частота ключевых нежелательных явлений, включая пирексию и вторичные злокачественные новообразования, изменилась незначительно. Это соответствует недавним сообщениям о том, что максимальное количество нежелательных явлений возникает в течение первых 6 мес лечения и в дальнейшем уменьшается.
В дополнение к таким клиническим показателям, как скорость прогрессирования, частота ответа и выживаемость, качество жизни, обусловленное состоянием здоровья (HRQoL), является важным фактором для пациентов с V600-положительной метастатической меланомой. В связи с этим в рамках исследования COMBI-d был проведен опрос (с использованием опросника QLQ-C30, разработанного Европейской организацией по изучению и лечению рака), касающийся HRQoL и выраженности симптомов заболевания у пациентов с меланомой и мутацией BRAF V600E или V600K, принимающих дабрафениб в сочетании с траметинибом и лишь один дабрафениб. Согласно его результатам, добавление траметиниба к дабрафенибу не приводило к ухудшению HRQoL пациентов.
Наоборот, отмечено улучшение качества жизни больных, получающих комбинированную терапию, по сравнению с таковым пациентов, принимавших один лишь дабрафениб. Это наряду с увеличением ВБП подтверждает преимущество комбинированной терапии.
В начале исследования наиболее выраженным симптомом была боль, статистически и клинически значимое снижение выраженности которой отмечалось у пациентов, получавших дабрафениб в комбинации с траметинибом в сравнении с одним лишь дабрафенибом. Эти результаты подтверждают пользу, которую комбинация может обеспечить пациентам для снижения уровня дистресса, связанного с болью при метастатической меланоме. Напротив, уменьшение выраженности осложнений со стороны желудочно-кишечного тракта чаще наблюдалось у пациентов, получавших дабрафениб в качестве монотерапии (например, диареи – 24% против 14%, рвоты – 20% против 14%). Как и сообщалось ранее, наиболее частым побочным эффектом при применении сочетания дабрафениб + траметиниб является пирексия, которая возникает примерно у половины пациентов (51% против 28%) [4].
Три клинических исследования III фазы продемонстрировали более высокую эффективность комбинированного ингибирования BRAF/MEK по сравнению с одним лишь ингибированием BRAF в отношении ОВ, ВБП и контроля роста опухоли. Проведенный анализ не только демонстрирует отсутствие значительного ухудшения HRQoL пациентов, получавших комбинированную терапию, но и свидетельствует об уменьшении выраженности нежелательных явлений по сравнению с таковыми у пациентов, получающих один лишь дабрафениб. Таким образом, комбинированная терапия более предпочтительна у пациентов с метастатической меланомой и мутацией BRAF V600, за исключением редких случаев, когда ингибитор MEK противопоказан.
Это первое исследование, в котором изучается влияние двух таргетных молекул на HRQoL у пациентов с распространенной или метастатической меланомой. Ранее проводился анализ HRQoL (с использованием опросника QLQ-C30) у пациентов с непереносимостью лечения или метастатической меланомой для трех новых терапевтических опций: ипилимумаба, дабрафениба и траметиниба в сравнении с химиотерапией. Результаты этих исследований показали умеренное снижение HRQoL у пациентов, получивших ипилимумаб в комбинации с дакарбазином или один лишь дакарбазин [5], тогда как дабрафениб и траметиниб в монорежиме напротив способствовали уменьшению выраженности симптомов, а значит – улучшению качества жизни [6].
Пациенты в рамках клинических исследований могут быть более мотивированны и, следовательно, более склонны сообщать о преимуществах терапии и переносить токсичность, связанную с лечением. Результаты этого анализа получены в ходе двойного слепого исследования, что обеспечивает более достоверную оценку ощущений пациентов. Исходные ответы пациентов были сопоставимы с эталоном Европейской организации по изучению и лечению рака QLQ-C30 для международной выборки пациентов со злокачественной меланомой III/IV стадии, т.е. популяция пациентов в этом исследовании может отражать характеристики популяции больных метастатической меланомой в целом.
Таким образом, применение комбинации траметиниба с дабрафенибом ассоциировано с более длительной выживаемостью пациентов с метастатической меланомой и мутацией V600. Преимуществами также являются улучшение качества жизни, связанное со здоровьем, и уменьшение выраженности боли на фоне терапии дабрафенибом в сочетании с траметинибом.
Литература
- Long G.V. et al. Dabrafenib plus trametinib versus dabrafenib monotherapy in patients with metastatic BRAF V600E/K-mutant melanoma: long-term survival and safety analysis of a phase 3 study. 2017.
- Long G.V., Weber J.S., Infante J.R. et al. Overall survival and durable responses in patients with BRAF V600-mutant metastatic melanoma receiving dabrafenib combined with trametinib. J Clin Oncol 2016.
- Grob J.J., Flaherty K., Long G.V. et al. Pooled analysis of safety over time and link between adverse events and efficacy across combination dabrafenib and trametinib (D+T) registration trials. J Clin Oncol 2016.
- Schadendorf D. et al. Health-related quality of life impact in a randomised phase III study of the combination of dabrafenib and trametinib versus dabrafenib monotherapy in patients with BRAF V600 metastatic melanoma. Eur J of Cancer 2015.
- Kotapati S., Francis S., Sherrill B.. Health related quality of life (HRQL) of patients receiving ipilimumab with dacarbazine as first-line treatment for unresectable stage III/IV melanoma. Pigment Cell Melanoma Res 2011.
- Grob J.J., Amonkar M.M., Martin-Algarra S. et al. Patient perception of the benefit of a BRAF inhibitor in metastatic melanoma: quality of life analyses of the BREAK‑3 study comparing dabrafenib with DTIC. Ann Oncol 2014.
Подготовила Екатерина Марушко
Тематичний номер «Онкологія» № 2 (53), травень 2018 р.




