19 серпня, 2025
Гепсидин – основний регулятор метаболізму заліза. Фізіологічна роль і клінічні кореляції
Залізо є надзвичайно важливим мікроелементом для функціонування всього організму. Залізо не тільки утворює активні центри молекул гемоглобіну та міоглобіну, що постачають кисень до тканин, а й входить до складу широкого спектра ферментів, які беруть участь в окисно-відновних реакціях, включаючи реакції дихального ланцюга. Однак надлишок вільного заліза може мати несприятливі наслідки, отже, незв’язане залізо ініціює утворення активних форм кисню, що зумовлює ушкодження тканин. Саме тому концентрація заліза в крові та насичення його внутрішньоклітинних запасів жорстко контролюються. Головним регулятором цих процесів є гепсидин.
Роль гепсидину в метаболізмі заліза
Гепсидин – це пептидний гормон, що складається із 25 амінокислот, кодується геном HAMP (19q13) і синтезується переважно в гепатоцитах. Гепсидин є основним регулятором метаболізму заліза в організмі людини. Він діє опосередковано, зв’язуючись із феропортином – унікальним мембранним білком, який функціонує як експортер двовалентного заліза в клітинах ретикулоендотеліальної системи, еритроцитах-попередниках червоного кісткового мозку, базолатеральній мембрані ентероцитів і меншою мірою – в гепатоцитах. Після зв’язування гепсидину із феропортином утворений комплекс інтерналізується; феропортин зазнає лізосомальної деградації. У результаті знижується відтік заліза із клітин на користь його внутрішньоклітинного зберігання.
Інший важливий ефект гепсидину – зниження абсорбції заліза з їжі в ентероцитах дванадцятипалої кишки та початкової ділянки порожньої кишки, що є результатом як блокування активності феропортину в ентероцитах, так і непрямого впливу гепсидину на транспортер двовалентних металів-1 (DMT1). DMT1 – це білок, розташований в апікальній мембрані ентероцитів, який відповідає серед іншого і за абсорбцію катіонів Fе 2+. Це надзвичайно важливо, оскільки в організмі людини більше немає механізмів, які могли б збільшити екскрецію заліза в разі його надлишку. Вплив гепсидину на ентероцити – єдиний механізм, який запобігає перевантаженню залізом.
Отже, гепсидин знижує рівень заліза в крові, пригнічуючи його абсорбцію в кишечнику та сприяючи його зберіганню в макрофагах, моноцитах, попередниках еритроцитів і гепатоцитах (рис.). Гепсидин запобігає надлишковій циркуляції заліза, незв’язаного із трансферином, отже, й виробленню шкідливих активних форм кисню.
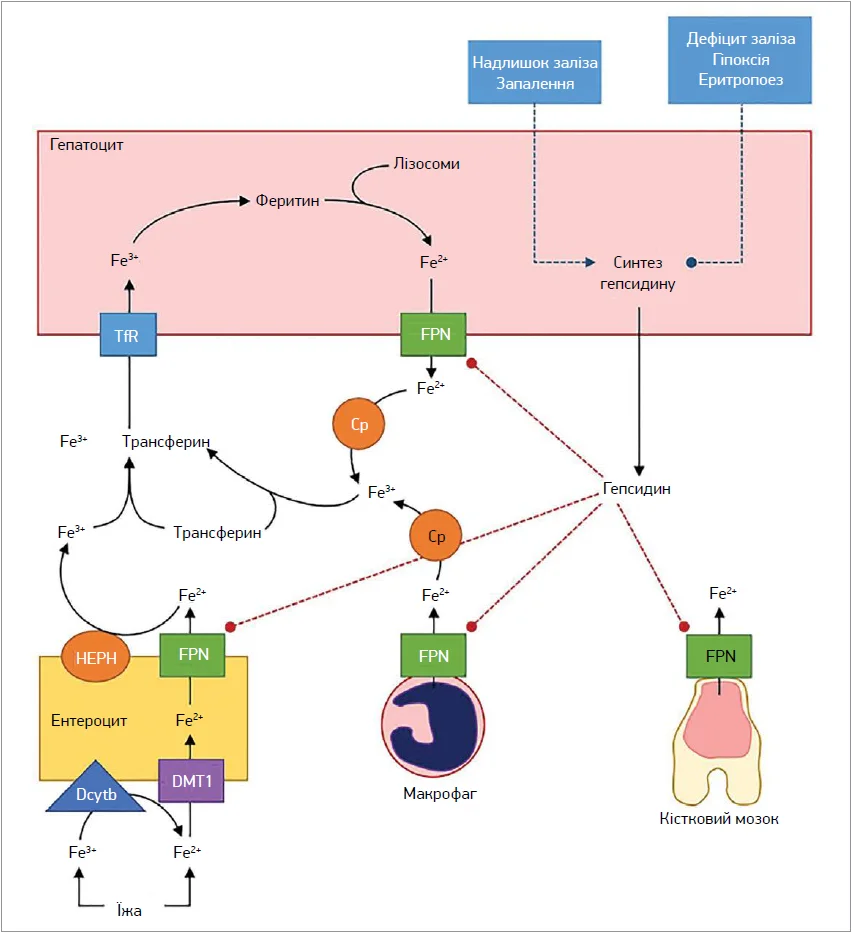 Рис. Роль гепсидину в метаболізмі заліза
Рис. Роль гепсидину в метаболізмі заліза
Примітки: стрілки з гострим кінцем вказують на стимуляцію процесу, штрихові стрілки із круглим кінцем – на пригнічення процесу або експресії білків; Cp – церулоплазмін; Dcytb – дуоденальний цитохром b; FPN – феропортин; HEPH – гефестин; TfR – рецептор трансферину.
Синтез гепсидину в печінці стимулюється надлишком заліза в крові. Своєю чергою, пригнічення його синтезу є результатом дефіциту заліза, гіпоксії та еритропоезу. Крім того, концентрація гепсидину значно зростає при запаленні, що пов’язано з його позитивним ефектом обмеження росту мікроорганізмів. Антимікробні властивості гепсидину тісно пов’язані з метаболізмом заліза, оскільки воно є одним із ключових факторів росту для численних мікроорганізмів. Індуковане гепсидином внутрішньоклітинне зв’язування заліза захищає організм людини від розвитку інфекцій або їхнього тяжчого перебігу, обмежуючи концентрацію заліза в кровообігу та тканинній рідині. Отже, гепсидин є білком гострої фази запалення, як і С-реактивний білок, фібриноген, феритин і прокальцитонін. Вважається, що інтерлейкін-6 (IL‑6), один з основних прозапальних цитокінів, є головним стимулятором синтезу гепсидину. Зв’язування IL‑6 зі специфічним рецептором (IL‑6R) активує сигнальний шлях JAK-STAT3, який індукує експресію гепсидину.
Гепсидин у патофізіології
Зміни рівня гепсидину спостерігаються при багатьох захворюваннях, особливо гематологічних і метаболічних.
Підвищення концентрації гепсидину у відповідь на запальний процес є одним із механізмів, що беруть участь у патогенезі анемії хронічних захворювань. Запалення стимулює експресію гепсидину, що зумовлює секвестрацію заліза в клітинах та обмежує його доступність для еритропоезу. Порушення еритропоезу та швидший розпад зрілих еритроцитів сприяють розвитку анемії, переважно нормоцитарної та нормохромної. Підвищена концентрація гепсидину супроводжується зниженням насичення трансферину та кількості заліза в крові, тоді як концентрація феритину, який також є білком гострої фази, збільшується. Схожий механізм може також спричиняти анемію в разі наявності онкологічних захворювань, особливо за множинної мієломи та лімфоми Ходжкіна.
Фізіологічно переважна більшість гепсидину фільтрується в первинну сечу та виводиться нирками. При хронічній хворобі нирок (ХХН) унаслідок втрати активних нефронів механізм виведення гепсидину стає неефективним. Високий рівень гепсидину в крові перешкоджає адекватному постачанню заліза для еритропоезу та є одним із механізмів розвитку анемії при ХХН. Важливо, що збільшення продукції гепсидину за ХХН потребує використання високих доз стимуляторів еритропоезу під час лікування анемії.
Гемохроматоз – це генетичне захворювання обміну заліза, яке незворотно спричиняє перевантаження залізом. Незалежно від конкретної генної мутації, яка визначає захворювання, надлишок заліза накопичується в організмі через дисфункцію або дефіцит гепсидину в результаті його аномальної структури, порушення передачі сигналів регуляторних механізмів або резистентності до феропортину. Дефіцит гепсидину, що належно функціонує, також впливає на імунну систему та підвищує сприйнятливість до інфекцій.
Крім того, встановлена роль гепсидину в патофізіології мієлодиспластичних синдромів (МДС), що супроводжуються неефективним еритропоезом. Порушення вироблення еритроцитів зумовлюють розвиток анемії, отже, й стимуляцію еритропоезу, що є сигналом для пригнічення синтезу гепсидину. Зниження секреції гепсидину сприяє підвищенню концентрації заліза в сироватці крові та перевантаженню його внутрішньоклітинних запасів. Дуже схожий механізм спостерігається також за β-таласемії – це генетичне захворювання, яке частково або повністю порушує синтез β-глобінових ланцюгів, що зумовлює неефективний еритропоез та утворення аномальних форм еритроцитів. Як і при МДС, симптоматичне лікування анемії за допомогою переливання еритроцитарної маси посилює дефіцит гепсидину.
Роль гепсидину під час вагітності
Підраховано, що для нормального перебігу вагітності необхідно 1040 мг заліза, тому системні запаси заліза в організмі вагітної, які оцінюються в 1 г, мають бути повністю виснажені. Однак цього не відбувається, оскільки щоразу більші потреби організму вагітної компенсуються підвищеним засвоєнням заліза та його більшим надходженням. Ці адаптаційні механізми регулює гепсидин. У міру збільшення терміну вагітності концентрація гепсидину в крові поступово знижується. В результаті збільшується кількість заліза, що транспортується з ентероцитів до кровотоку та тканин, отже, й кількість заліза, що абсорбується в кишечнику. Крім того, як материнський, так і фетальний гепсидин бере участь у регуляції перенесення заліза через плаценту. Отже, зниження експресії гепсидину у вагітних не лише визначає вище засвоєння заліза з їжі, а й збільшує кількість заліза, що надходить до плода з материнського кровообігу. Фізіологічно обидва механізми здатні забезпечити необхідну кількість заліза для належного росту плода. Однак слід пам’ятати, що за наявності дефіциту заліза в матері до вагітності, як-от при залізодефіцитній анемії, вищезазначені адаптаційні механізми можуть бути недостатніми.
Висновки
Гепсидин є основним регулятором метаболізму заліза. Сприяючи деградації феропортину, гепсидин зменшує відтік заліза із тканин і всмоктування заліза в кишечнику, отже, й концентрацію заліза в крові. Експресія гепсидину стимулюється зменшенням запасів системного заліза та запаленням, пригнічується в ситуаціях надлишку заліза або посилення еритропоезу, а також під час вагітності. Завдяки цій регуляції зміни концентрації гепсидину є компенсаторним механізмом, спрямованим на відновлення гомеостазу заліза в організмі, збільшення його постачання у відповідь на щоразу більші потреби під час вагітності або захист від патогенів. Однак при захворюваннях, пов’язаних з неінфекційною стимуляцією запальної реакції, підвищення продукції гепсидину є небажаним, оскільки зумовлює дефіцит заліза та його численні наслідки.
Джерело: Wojciechowska M., Wisniewski O.W., Kolodziejski P., Krauss H. Role of hepcidin in physiology and pathophysiology. Emerging experimental and clinical evidence. J. Physiol. Pharmacol. 2021 Feb; 72 (1). doi: 10.26402/jpp.2021.1.03.
Реферативний огляд підготував Ігор Петренко
Довідка «ЗУ»
Прикладом раціональної фармацевтичної технології для ефективного вирішення проблеми залізодефіцитної анемії є Сорбіфер Дурулес (Sorbifer® Durules®) виробництва ЗАТ «Фармацевтичний завод «ЕГІС» (Угорщина). Таблетки, вкриті оболонкою з модифікованим вивільненням, містять по 320 мг заліза сульфату безводного (що відповідає 100 мг двовалентного заліза) та 60 мг аскорбінової кислоти. Технологія виготовлення таблеток забезпечує безперервне вивільнення іонів заліза (II) з пористої матриці протягом 6 год. Повільне вивільнення запобігає небезпечно високим концентраціям заліза, завдяки чому можна уникнути подразнення кишкового епітелію. Вітамін С у складі препарату додатково підвищує абсорбцію заліза в кишковому тракті та бере участь в окисно-відновних процесах. Сорбіфер Дурулес показаний для профілактики та лікування залізодефіцитної анемії у дорослих та дітей віком >12 років. Для профілактики анемії призначають по 1 таблетці/добу. Для лікування анемії препарат слід приймати по 1 таблетці 2 р/добу. Протягом перших 6 місяців вагітності рекомендована доза препарату – 1 таблетка/добу; в останньому триместрі вагітності, а також у період годування грудьми – по 1 таблетці 2 р/добу. Тривалість лікування залежить від індивідуальних результатів перевірки вмісту заліза в плазмі крові. Після нормалізації рівня гемоглобіну введення препарату має тривати до повного насичення запасів заліза (близько 2 місяців).
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (599-600), 2025 р



