19 травня, 2021
Фармакокінетика і безпека біластину в дітей віком від 6 до 11 років з алергічним ринокон’юнктивітом або хронічною кропив’янкою
Біластин – це неседативний антигістамінний препарат (АГП) ІІ покоління, який не проникає крізь гематоенцефалічний бар’єр. В Європі цей засіб застосовують для лікування алергічного ринокон’юнктивіту (АРК) та хронічної кропив’янки (ХК) в дорослих і дітей віком від 6 років із масою тіла понад 20 кг. У Мексиці біластин нещодавно також був схвалений для лікування дітей віком від 2 років. Ефективність біластину порівнянна з такою інших пероральних H1-АГП ІІ покоління. Моделювання фармакокінетики (ФK) / фармакодинаміки (ФД) у здорових дорослих суб’єктів, доповнене некомпартментним аналізом, продемонструвало лінійну кінетику після перорального прийому біластину в діапазоні доз від 2,5 до 220 мг. Онтогенетична модель, створена на основі даних моделювання ФК/ФД у дорослих, підтвердила вибір дози біластину 10 мг/добу в педіатричній популяції віком від 2 до 11 років, що було підтверджено в клінічному фармакокінетичному дослідженні за участю дітей згаданої вікової групи, які хворіють на АРК або ХК.
Ключові слова: біластин, фармакокінетика, діти, алергічний ринокон’юнктивіт, хронічна кропив’янка, H1-АГП другого покоління
Оскільки біластин схвалений в Європі для лікування дітей віком ≥6 років, поточне дослідження повідомляє про результати двох ретроспективних аналізів ФК та даних щодо безпеки. Показники ФК, отримані Vozmediano та співавт., проаналізували з акцентом на дітей віком 6-11 років. Крім того, був проведений ретроспективний аналіз даних щодо безпеки в тій самій віковій групі. Дані було отримано під час ІІІ фази плацебо-контрольованого рандомізованого дослідження застосування біластину в дозі 10 мг/добу в терапії дітей, хворих на АРК або ХК.
Методи
Фармакокінетичні дані
Дані ФК були отримані з багатоцентрового міжнародного адаптивного відкритого дослідження з пероральним повторним застосуванням біластину в дозі 10 мг/добу в дітей віком від 4 до 11 років з АРК або ХК (дослідження BILA‑3009 / PED; Clinical Trials.gov Ідентифікатор: NCT01081574).
У попереднє моделювання ФК у педіатричній популяції було залучено суб’єктів віком 4-11 років [11, 12]. Цей ретроспективний аналіз зосереджується на дітях віком 6-11 років (n=24), відповідно до затверджених в Європі педіатричних показань.
Некомпартментний аналіз
Максимальна концентрація в плазмі (Cmax) і площа під кривою плазмової концентрації (AUC0-24) були розраховані за допомогою S-PLUS® (версія 8.2, програмне забезпечення TIBCO, Пало-Альто, Каліфорнія, США).
Порівняння показників НКА в дітей і дорослих
Системну експозицію після перорального прийому педіатричної дози біластину (10 мг/добу) дітьми порівнювали з дорослими (біластин перорально в дозі 20 мг/добу), використовуючи числові та графічні порівняння, зокрема форест-діаграми для візуальної оцінки неоднорідності досліджень. Для врахування різниці в часі забору зразків для педіатричних даних визначали концентрацію біластину в плазмі крові (Cp) з урахуванням часу після застосування дози.
Було розглянуто два альтернативні підходи до визначення референтних діапазонів AUC0-24 та Cmax у дорослих: популяційно-прогнозований 95% довірчий інтервал (ДІ), оснований на моделі ФК у популяції, розробленій на основі даних для дорослих, та більш консервативний 95% ДІ, що базується на основі отриманих значень НКА із 7 досліджень I фази (дослідження 459-02, 459-04 до 459-07, 459-10 та 459-11) у дорослих після прийому біластину в дозі 20 мг.
Дані з безпеки
Дані з безпеки були отримані у фазі III подвійного сліпого рандомізованого плацебо-контрольованого дослідження з паралельними групами за участю дітей віком 2-11 років з АРК або ХК, які впродовж 12 тиж лікувалися біластином у дозі 10 мг 1 раз на добу (n=260) або плацебо (n=249).
Біластин або плацебо застосовували перорально натще 1 раз на добу вранці. Було дозволене епізодичне використання препаратів «швидкої допомоги» – топічних деконгестантів короткої дії (очі/ніс), кортикостероїдів або АГП при ринокон’юнктивіті або топічних кортикостероїдів коротким курсом при кропив’янці.
Первинною кінцевою точкою була частка дітей у кожній групі лікування, в яких не спостерігалося будь-яких небажаних явищ у ході лікування (НЯХЛ; визначається як будь-який тип побічної реакції, яка мала місце впродовж усіх 4 міс дослідження, тобто 3-місячного періоду лікування та місячного періоду наступного спостереження), відповідно до керівництва Педіатричного комітету Європейської агенції лікарських засобів (PDCO).
Статистичний аналіз
Статистичну значущість оцінювали для двосторонніх критеріїв із граничним значенням альфа 0,05. Відсутні значення не враховували для статистичних розрахунків. Кількісні змінні характеризувалися кількістю суб’єктів, середнім значенням, стандартним відхиленням (СВ), максимальним, мінімальним та квартильним значенням. Якісні змінні характеризувалися за частотою та відсотком. Вторинні якісні змінні оцінювали за допомогою критерію узгодженості Пірсона або, якщо не були дотримані відповідні умови, точного критерію Фішера.
Результати
Фармакокінетичні дані
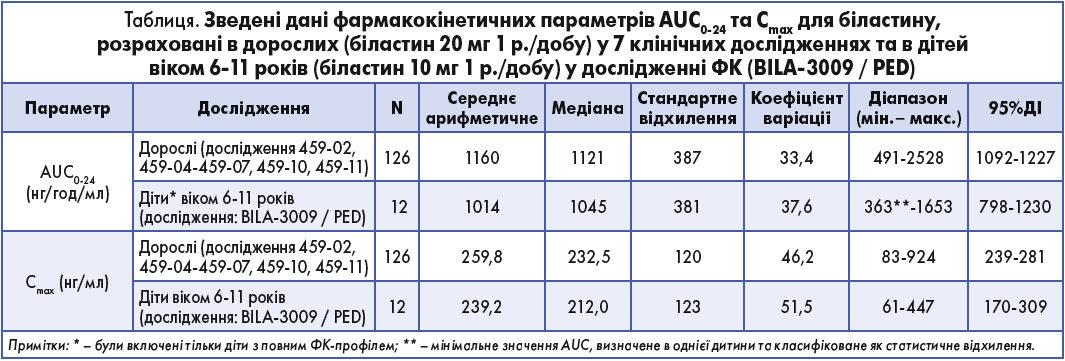
Усього було взято 88 зразків від 24 дітей віком від 6 до 11 років, що дало можливість охарактеризувати фази всмоктування, розподілу та елімінації профілю ФК у цій когорті. Експозиція та максимальна концентрація в плазмі крові в педіатричній популяції (n=12, що відповідає дітям із повним профілем ФК у цій розрідженій схемі відбору проб) після прийому біластину в дозі 10 мг/добу були подібними до тих, про які свідчили дані ФК у дорослих (n=126), отримані в ході 7 клінічних досліджень після застосування біластину в дозі 20 мг/добу (табл.).
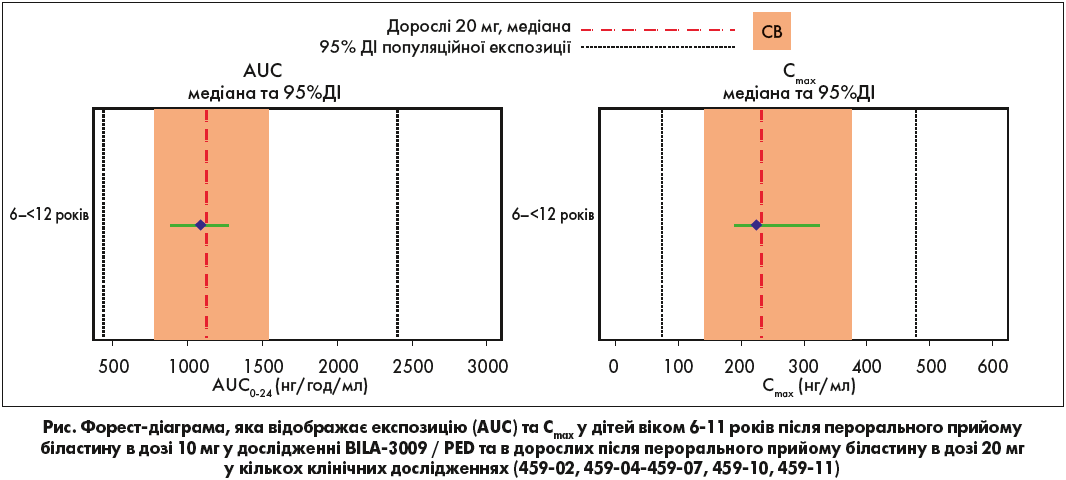
Медіана (СВ) AUC0-24 у педіатричній і дорослій популяціях становила 1045 (381) та 1121 (387) нг/год/мл відповідно, медіана Cmax – 212,0 (123) та 232,5 (120) нг/мл відповідно. Концентрація біластину в плазмі крові в дітей повністю збігалася з показниками, отриманими в дорослих учасників дослідження, була строго в рамках варіабельності дорослих та повторювала той самий часовий профіль ФК. Співвідношення медіан AUC0-24 і Cmax діти/дорослі становили 0,93 та 0,91 відповідно. Ба більше, системна експозиція та Cmax після перорального прийому біластину в дітей (10 мг/добу) була порівнянною з показниками, отриманими в дорослих (біластин перорально в дозі 20 мг/добу) за допомогою форест-діаграми (рис.), яка демонструє, що показники ФК педіатричної популяції були повністю в межах довірчих інтервалів дорослих.
Сині крапки на діаграмі представляють собою медіану, а зелені лінії – 95% ДІ у дітей. Червона лінія та помаранчева затінена ділянка – це медіана і одне СВ в дорослій популяції відповідно. Крім того, 95% ДІ популяційної експозиції, що базується на основі популяційної моделі ФК/ФД в дорослих після перорального прийому біластину в дозі 20 мг (435-2400 нг/год/мл, AUC, і 75-475 нг/мл, Cmax), позначений чорною пунктирною лінією.
Дані з безпеки
Оцінювали дані 393 осіб, які приймали досліджувані препарати та були рандомізовані у 2 групи: учасники першої (n=202) отримували біластин у дозі 10 мг, учасники другої (n=191) – плацебо. Медіана (СВ) віку груп біластину й плацебо становила 8,5 (1,6) та 8,5 (1,8) року відповідно. У групі біластину 105 (52%) учасників були віком 6-8 років і 97 (48%) – 9-11 років. Відповідна кількість за віком у групі плацебо становила 95 (49,7%) і 96 (50,3%). Суб’єкти в групах біластину та плацебо були переважно чоловічої статі (62,9 і 61,8% відповідно) та європеоїдної раси (93,1 і 92,7% відповідно). Середнє значення (СВ) індексу маси тіла в групах становило 18,0 (3,5) та 18,1 (3,5) кг/м2 відповідно. В учасників дослідження були діагностовані АРК (98,0 і 93,7%) або ХК (2,0 та 6,3%) із середнім часом з моменту встановлення діагнозу (СВ) 4,1 (2,5) та 4,0 (2,7) року відповідно.
Не було суттєвої різниці в частоті НЯХЛ між двома групами: повідомлено про 137 подій у 67,8% дітей, які отримували біластин, проти 129 подій у 67,5% досліджуваних, які отримували плацебо (р=0,952). Частка дітей із пов’язаними з лікуванням НЯХЛ у групах біластину та плацебо дорівнювала 5,4 і 7,9% відповідно (p=0,337); серйозні НЯХЛ виникали в 1,0 і 3,1% дітей відповідно (р=0,165), хоча жоден із побічних ефектів не вважався пов’язаним із лікуванням; відсоток дітей із НЯХЛ, що призвели до припинення лікування, становив 1,0 і 0,5% відповідно (p=1,0).
Найчастішими НЯХЛ (частота ≥5%) в обох групах були: головний біль (13,4 проти 12,6%), алергічний кон’юнктивіт (9,9 проти 9,4%), кашель (8,9 проти 7,9%), назофарингіт (7,9 проти 4,7%), фарингіт (7,4 проти 6,8%), алергічний риніт (6,4 проти 10,0%), підвищення температури тіла (5,0 проти 10,0%) та вірусна інфекція (4,5 проти 5,2%).
Обговорення
Результати ретроспективного дослідження ФК біластину в дітей віком 6-11 років з АРК або ХК зіставні з тими, що були отримані в педіатричній популяції з ширшим віковим діапазоном (2-11 років), що вказує на відсутність залежності ФК біластину від віку пацієнта. Поточний аналіз ФК обмежився даними дітей віком 6-11 років, що відповідає затвердженому в Європі показанню до застосування біластину в педіатрії: діти ≥6 років із масою тіла ≥20 кг. Педіатричні дані в повному наборі даних (у віці 4-11 років) найкраще описані за допомогою двокамерної моделі розподілу, метаболізму та виведення, яку використовують для опису ФК біластину в дорослих. Показники як AUC0-24, так і Cmax в дитячій (6-11 років) та дорослій групах виявилися дуже схожими, концентрація біластину в плазмі крові в дітей повністю збігалася з показниками дорослих, а співвідношення діти/дорослі для AUC0-24 та Cmax дорівнювали приблизно одиниці (0,93 та 0,91 відповідно). Ці результати свідчать на користь застосування біластину в дозі 10 мг в педіатричній популяції.
Дані щодо безпеки були отримані в результаті аналізу підмножини даних (у дітей віком 6-11 років) фази III плацебо-контрольованого рандомізованого дослідження біластину в дітей віком від 2 до 11 років з АРК або ХК. У цьому ретроспективному аналізі статистично значущої різниці в частоті НЯХЛ в дітей, які отримували біластин (10 мг) або плацебо, не спостерігали; найчастішою небажаною реакцією, про яку повідомлялося в обох групах, був головний біль (13,4 проти 12,6% відповідно). Ці результати підтверджують, що профіль безпеки та переносимості біластину в дозі 10 мг у дітей подібний до такого плацебо. У дорослих біластин у рекомендованій дозі 20 мг має високий профіль безпеки, виражений у хорошій переносимості та відсутності седативних або кардіотоксичних ефектів.
Отже, аналіз ФК та даних із безпеки в дітей віком 6-11 років свідчить на користь застосування біластину в педіатричній дозі 10 мг і підтверджує, що його профіль безпеки подібний до плацебо.
За матеріалами Rodriguez M., Vozmediano V., Bea A.G. et al. Pharmacokinetics and safety of bilastine in children aged 6 to 11 years with allergic rhinoconjunctivitis or chronic urticarial. European Journal of Pediatrics. 09.01.2020. https://doi.org/10.1007/s00431-019-03559-6
Підготувала Ганна Кирпач