28 лютого, 2023
Оцінка ефективності і безпеки біластину в дорослих пацієнтів з алергічним ринітом
Алергічний риніт (АР) – це IgE-опосередковане запалення слизової оболонки носа, що супроводжується виробленням імунних медіаторів, зокрема гістаміну, з яким і пов’язані всі симптоми АР [1].
Поширеність алергічних захворювань, у тому числі астми, риніту, анафілаксії або харчової та лікарської алергії, а також алергії на комах, зростає по всьому світу. На сьогодні на АР страждають понад 400 млн осіб, при цьому хвороба часто лишається недіагностованою, а пацієнти отримують недостатній обсяг лікування [2]. За статистичними даними, захворюваність на АР в західних країнах широко варіює і становить 1,4-39,7%, а, наприклад, в Індії коливається в межах 20-30% [3]. Дорослі частіше страждають на цілорічний АР (ЦАР), тоді як серед дітей частіше спостерігається сезонний АР (САР) [4].
Введення
Клінічно АР характеризується чотирма ключовими симптомами, а саме передньою або задньою ринореєю, чиханням, свербежем у носі і закладеністю носа. Ці симптоми значно знижують якість життя (QoL), призводячи до порушень сну, розвитку втоми і депресії, погіршення когнітивних здібностей, зниження працездатності та продуктивності [9].
Чинниками розвитку АР є цвіль, пилок рослин, пилові кліщі й епідермальні алергени, які осідають на слизовій оболонці носа, спричинюючи сенсибілізацію організму і розвиток алергічної реакції в разі подальшого контакту [10].
АР – це гетерогенне захворювання, яке часто лишається недіагностованим, оскільки пацієнти не усвідомлюють серйозність впливу симптомів АР на якість життя і дієздатність через пролонгованість симптомів, які не розпізнаються на початковій стадії. Як наслідок, по медичну допомогу звертаються пізно або не звертаються зовсім [11, 12].
Лікування АР полягає в зменшенні або усуненні його симптомів і охоплює низку фармакологічних груп препаратів, у тому числі інтраназальні кортикостероїди (КС), пероральні й інтраназальні антигістамінні препарати (АГП), протинабрякові засоби, інтраназальні кромони, інтраназальні антихолінергічні засоби та антагоністи лейкотрієнових рецепторів [13].
Багато з перелічених препаратів мають певні недоліки. Так, найпоширенішими побічними ефектами (ПЕ) інтраназальних КС є подразнення горла, носова кровотеча, поколювання, дискомфорт, печіння і сухість у носі [14, 15]. Пероральні АГП І покоління можуть виявляти седативний ефект із розвитком втоми і порушенням психічного стану. Інтраназальні АГП спричиняють гіркий присмак, головний біль, подразнення слизової носа, носові кровотечі та седацію [16]. Інтраназальні протинабрякові засоби часто асоційовані з чиханням і сухістю в носі, тому не рекомендуються до прийому впродовж більш як 3-5 днів через ризик розвитку медикаментозного риніту або рецидивної закладеності носа [10, 17]. Пероральні АГП допомагають значно полегшити симптоми АР і підвищити якість життя, утім препарати ІІ покоління мають кращий профіль безпеки, у тому числі й через відсутність седативних властивостей.
До загальновживаних АГП ІІ покоління належать: біластин, фексофенадин, цетиризин, левоцетиризин, лоратадин, дезлоратадин та ебастин [18].
Біластин – АГП ІІ покоління з швидким початком дії (30 хв – 1 год) і стійкою тривалістю дії (~26 год) [19-24]. Препарат застосовують перорально один раз на добу. Він швидко всмоктується після прийому всередину, досягаючи максимальної концентрації в плазмі крові через 1,0-1,5 год [15, 18, 25].
З огляду на те що біластин не метаболізується в печінці, будь-які лікарські взаємодії відсутні. Препарат не проникає крізь гематоенцефалічний бар’єр, а отже, не чинить седативну дію. Важливою перевагою біластину є те, що він має сприятливий профіль переносимості без седативного ефекту і впливу на психомоторну діяльність, а також навички водіння [26]. На відміну від цетиризину біластин не посилює дію алкоголю на центральну нервову систему (ЦНС) [27]. До того ж препарат не сприяє збільшенню ваги та немає антихолінергічних проявів або ПЕ з боку серцево-судинної системи [28].
Біластин має найбільшу кількість позитивних характеристик серед препаратів своєї групи відповідно до критеріїв і рекомендацій щодо АГП від EAACI (European Academy of Allergy & Clinical Immunology – Європейська академія алергії та клінічної імунології), GA2LEN (the Global Allergy and Asthma European Network – Глобальна європейська спілка алергії та астми), EDF (the European Dermatology Forum – Європейський дерматологічний форум) і WAO (World Allergy Organization – Всесвітня організація алергії) [29].
Рандомізоване дослідження, що оцінювало ефективність біластину в дозі 20 мг один раз на добу протягом 2 тиж у японських пацієнтів із ЦАР, показало, що препарат ефективний, добре переноситься і має швидкий початок дії [30]. Встановлено, що біластин перевершує плацебо, але порівнянний з іншими пероральними АГП за здатністю зменшувати вираженість симптомів риніту, назальних симптомів і поліпшувати якість життя. Зазначено, що сонливість на тлі прийому біластину була значно меншою проти інших АГП [31].
У поточному дослідженні оцінювали ряд клінічних параметрів АР, вплив на якість життя і безпеку застосування біластину в дозі 20 мг один раз на добу у формі таблеток протягом 4 тиж у пацієнтів з АР. Також через 2 год після прийому препарату оцінювали його седативний ефект.
Методи
Дизайн дослідження
Проспективне непорівняльне дослідження серед дорослих пацієнтів з АР, було проведено у 3 медичних центрах Індії з березня 2021 по лютий 2022 року. У дослідженні взяли участь 90 пацієнтів, які відповідали критеріям включення. Кожен із них для лікування АР отримував біластин у дозі 20 мг, по 1 таблетці на добу, протягом 4 тижнів.
Критерії включення
Пацієнти чоловічої і жіночої статі віком 18-60 років із клінічним анамнезом і симптомами АР, які раніше не отримували лікування, принаймні за 2 тиж до початку дослідження.
Критеріями виключення були: поліпи носа, викривлення носової перегородки або інші значні структурні вади розвитку носових шляхів; зловживання алкоголем, наркотиками, куріння; неалергічний риніт; інтраназальні або офтальмологічні операції за 3 міс до дослідження; прийом Н1- або Н2- АГП за 3-7 днів до початку дослідження; гострий або хронічний синусит за місяць до початку дослідження; підвищена чутливість до біластину або інших АГП, імідазолу, лактози; застосування КС, лоратадину або дезлоратадину впродовж останніх 10 днів, антилейкотрієнових препаратів або кетотифену протягом останніх 2 тиж, макролідів, імідазолу або протинабрякових засобів протягом останніх 3 днів або алерген-специфічної імунотерапії (АСІТ) впродовж 2 років (крім стабільної підтримувальної дози один раз на місяць); прийом будь-яких препаратів, що діють на ЦНС (антидепресанти, седативні засоби, анксіолітики, снодійні, опіоїди або нейролептики).
Кінцеві точки дослідження
Первинною кінцевою точкою була зміна TSS (total symptom score, шкала загальних симптомів), обчислена як сума назальних симптомів NSS (nasal symptom score) і неназальних симптомів (NNSS, non-nasal symptom score) від початкового рівня до 28-го дня дослідження.
Вторинними кінцевими точками були:
- частота TEAEs (treatment-emergent adverse events; ПЕ, асоційованих із лікуванням);
- зміни в перебігу ринокон’юнктивіту (оцінка за опитувальником якості життя (RQLQ, Rhinoconjunctivitis Quality of life Questionnaire) від вихідного рівня до 7-го і 28-го днів;
- зміна NSS і NNSS від вихідного рівня до 7-го дня;
- зміна показника SSS (Stanford Sleepiness Scale, стенфордська шкала сонливості) від вихідного рівня до 2-ї год після першої дози;
- зміни рівнів ферментів печінки, функції нирок і показників ехокардіограми від вихідного рівня до 28-го (27-го) дня.
Оцінка дослідження
Демографічні показники пацієнтів, дані анамнезу хвороби та загального медичного анамнезу, інформація щодо прийому ліків були задокументовані під час скринінгу. TSS розраховували як суму балів за 4 назальні симптоми (NSS: ринорея, закладеність носа, свербіж і чихання) і 3 неназальні симптоми (NNSS: сльозотеча, почервоніння і свербіж). Кожен симптом оцінювали на початковому етапі та під час ознайомчих візитів, при цьому 0 балів зараховували за відсутності симптомів, 1 бал – за наявності легких симптомів, які не порушують якість життя, 2 бали – за помірні, часті і дошкульні симптоми, 3 бали – за тяжкі, постійні симптоми, що заважають повсякденній діяльності або сну.
RQLQ складається з 28 питань у 7 розділах: обмеження активності; проблеми зі сном; носові симптоми; очні симптоми; симптоми, не пов’язані з носом/очима; практичні проблеми та емоційна функція. Пацієнтів просили згадати, наскільки їх турбував ринокон’юнктивіт протягом попереднього тижня, і відповісти на кожне питання за 7-бальною шкалою (від 0 – зовсім не страждає до 6 – серйозно страждає). SSS дає можливість респондентам вказати рівень сонливості за шкалою від 1 до 7 [32].
Протягом усього періоду дослідження реєстрували всі ПЕ і вели спостереження до їх розрішення. ПЕ визначали як будь-яку несподівану або несприятливу медичну подію, у тому числі будь-які ознаки, що виходять за звичні рамки (наприклад, зміни лабораторних даних або даних фізикального огляду), симптом або захворювання, тимчасово пов’язані з участю пацієнтів у дослідженні, незалежно від того, чи вважаються вони пов’язаними з участю в дослідженні, у тому числі супутні захворювання / травми і загострення раніше існуючих станів. Загальне та біохімічне дослідження крові на печінкові ферменти і функцію нирок, а також аналіз сечі виконували як до, так і після досліджуваного лікування.
Статистичний аналіз
Вибірка пацієнтів, яким було призначено лікування (ІТТ, intent-to-treat), охоплювала учасників, що отримали принаймні одну дозу досліджуваного лікування і пройшли принаймні одну оцінку після початкового дослідження. До вибірки, що виконала вимоги протоколу (PP, per protocol), увійшли пацієнти, які отримали принаймні одну дозу досліджуваного лікування і в яких не було будь-яких серйозних відхилень від протоколу. Вибірка для оцінки безпеки охоплювала пацієнтів, які отримали принаймні одну дозу досліджуваного лікування. Усі якісні змінні були підсумовані у вигляді частоти і відсотків. Усі неперервні змінні були підсумовані як n, середнє значення і стандартне відхилення (SD, standard deviation).
Зміни показників TSS, NSS, NNSS і RQLQ від вихідного рівня до 7-го або 28-го дня оцінювали за допомогою дисперсійного аналізу повторних вимірювань (ANOVA, ANalysis Of VAriance). Точкова оцінка змін була представлена разом із 95% довірчим інтервалом. Значення p базувалися на змішаній моделі для повторних вимірювань (MMRM, mixed model for repeated measures). Парний Т-тест використовували для аналізу зміни SSS до прийому препарату і через 2 год після першої дози.
Результати дослідження
Демографічні дані пацієнтів і початкові показники
Усі 90 обстежених пацієнтів відповідали критеріям включення, були зараховані до дослідження і зараховані до вибірки ІТТ. З них 84 пацієнти завершили дослідження. З 90 зареєстрованих пацієнтів 7 мали серйозні відхилення від протоколу і були виключені з вибірки РР. Середній вік (SD) пацієнтів становив 34,07 (10,06) року і 34,02 (10,31) року у вибірках ІТТ і РР відповідно.
Ефективність біластину через 4 тижні лікування
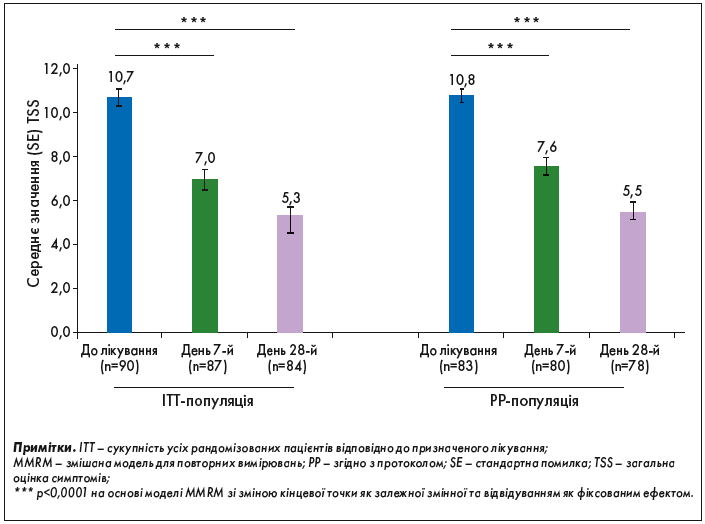
Динаміка TSS. Середнє значення (SD) TSS у популяції ITT знизилося з 10,7 (2,66) на початку дослідження до 7 (3,88) на 7-й день і до 5,3 (4) на 28-й день. Таким чином, середня зміна TSS від початкового рівня становила -3,7 (4,16) і -5,4 (5,83) на 7-й і 28-й дні відповідно. Під час обох візитів спостерігали статистично значуще зниження середньої оцінки TSS порівняно з вихідними даними (p<0,0001; рис. 1).
Рис. 1. Динаміка оцінки за TSS при АР від початку дослідження до 28-го дня
Середнє значення (SD) TSS у популяції PP знизилося з 10,8 (2,61) на початку дослідження до 7,6 (3,48) на 7-й день і до 5,5 (4,01) на 28-й день. Таким чином, середня зміна TSS від початкового рівня становила -3,3 (4,00) і -5,4 (5,94) на 7-й та 28-й дні відповідно.
Статистично значуще зниження середньої оцінки TSS порівняно з початковим рівнем (p<0,0001) спостерігали під час обох відвідувань.
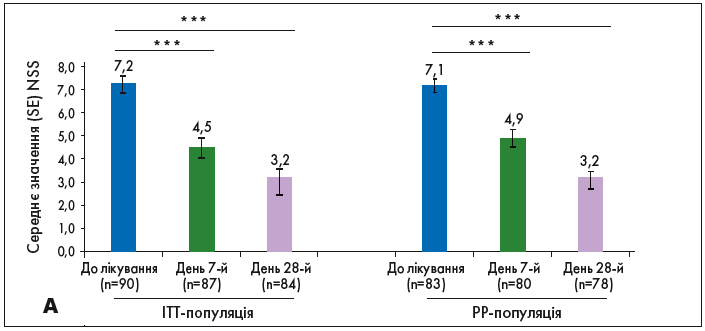
Динаміка NSS і NNSS. Середня оцінка (SD) за NSS у вибірці ITT знизилася із 7,2 (2,67) на початку дослідження до 4,5 (2,82) на 7-й день і до 3,2 (2,01) на 28-й день. Таким чином, середня зміна показника NSS від початкового рівня становила -2,7 (3,72) і -4,1 (4,36) на 7-й і 28-й дні відповідно. Під час обох візитів спостерігали статистично значуще зниження оцінки NSS порівняно з вихідними даними (p<0,0001; (рис. 2A).
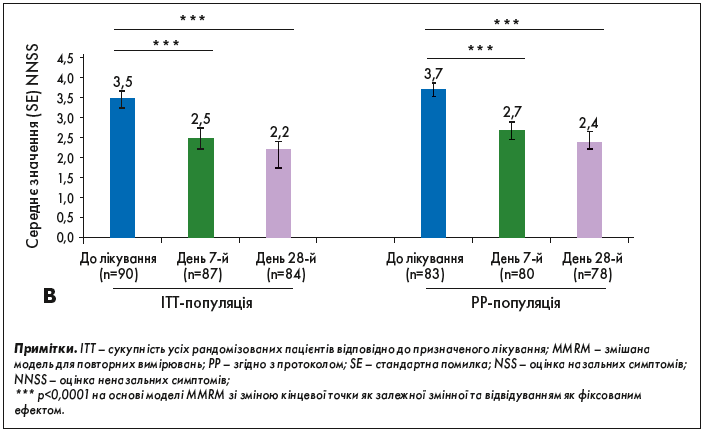
Середнє значення (SD) NNSS у вибірці ITT знизилося з 3,5 (1,60) на початковому рівні до 2,5 (1,85) на 7-й день, а потім незначно, до 2,2 (2,22), на 28-й день. Таким чином, середня зміна показника NNSS від початкового рівня становила -0,99 (1,33) і -1,3(1,91) на 7-й і 28-й дні відповідно. Під час обох візитів спостерігали статистично значуще зниження оцінки за NNSS порівняно з початковим рівнем (p<0,0001; рис. 2B).
Рис. 2. Динаміка показників NSS і NNSS при АР від початку лікування до 28-го дня
У групі PP середній показник (SD) NSS значно знизився (р<0,0001) із 7,1 (2,74) на початковому рівні до 4,9 (2,64) на 7-й день і до 3,2 (1,93) на 28-й день. Таким чином, середня зміна NNSS в порівнянні з вихідним рівнем становила - 2,3 (3,56) і -4,0 (4,42) на 7-й і 28-й дні відповідно. Під час обох візитів спостерігали статистично значуще зниження оцінки за NSS порівняно з початковим рівнем лінією (рис. 2A).
Аналогічним чином, середня оцінка (SD) за NNSS3,7 (1,45) на початковому рівні також значно (p<0,0001) знизилася до 2,7 (1,77) на 7-й день і до 2,4 (2,22) на 28-й день, при цьому середнє значення змінилося на -0,98 (1,33) і -1,4 (1,97) на 7-й і 28-й дні відповідно (рис. 2B).
Вплив біластину на якість життя
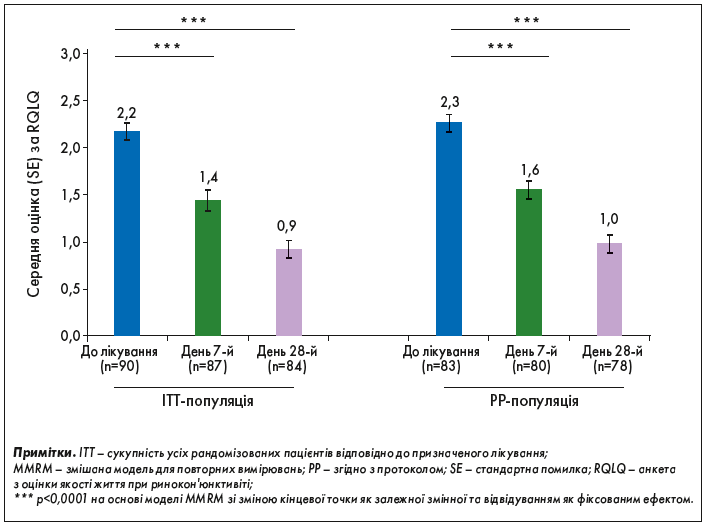
Середній бал за RQLQ (SD) групі ITT становив 2,17 (0,89) на початковому рівні і значно (р<0,0001) знизився: до 1,44 (1,01) на 7-й день і до 0,92 (0,88) на 28-й день.
Аналогічна зміна спостерігалася в групі PP, де середня базова оцінка (SD) за RQLQ становила 2,27 (0,86) і значно (р<0,0001) знизилася: до 1,56 (0,95) на 7-й день і до 0,98 (0,89) на 28-й день (рис. 3).
Рис. 3. Динаміка даних оцінки за RQLQ від початку лікування до 28-го дня
Седативний ефект біластину
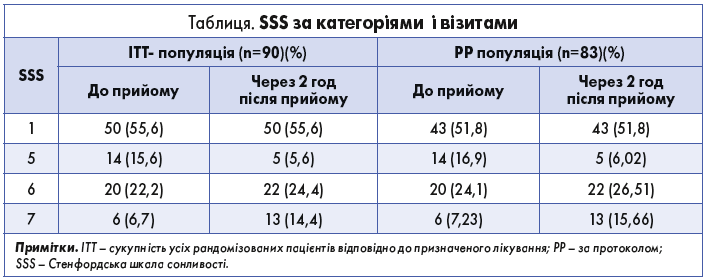
У групі ITT у 55,6% пацієнтів оцінка за SSS становила 1 (активний, пильний і не спить) на початку дослідження і залишалася такою через 2 год після введення 1-ї дози. У решти 44,4% пацієнтів вихідний бал за SSS становив ≥5 і залишився на такому рівні через 2 год після введення 1-ї дози (табл.). Більш того, медіана оцінки (діапазон) за SSS становила 1,0 (1,0-7,0) до і через 2 год після прийому препарату, що вказує на відсутність седативного ефекту і надалі. Подібні тенденції спостерігали і в групі РР.
Безпека біластину
Під час дослідження не було зареєстровано жодного ПЕ. Незначні зміни, що їх спостерігали при дослідженні печінкових ферментів та функції нирок, клінічно значущими визнані не були.
Обговорення
У цьому відкритому багатоцентровому дослідженні за участю пацієнтів з АР було продемонстровано значне зменшення вираженості симптомів АР на тлі застосування біластину в дозі 20 мг протягом 28 днів.
Статистично значуще зниження показників порівняно з базовим рівнем спостерігали за TSS (p<0,0001; первинна кінцева точка), NSS і NNSS через 7 і 28 днів після прийому препарату один раз на добу. Якість життя за RQLQ також значно покращилась, про що свідчить зниження оцінки за RQLQ після закінчення лікування (p<0,0001).
Результати поточного дослідження корелюють з данними ряду інших щодо ефективності і безпеки застосування біластину.
Систематичний огляд ефективності і безпеки перорального біластину в дозі 20 мг один раз на добу в дорослих і підлітків підтвердив його ефективність щодо усунення назальних і очних симптомів у пацієнтів з АР [27].
Дані 5 досліджень за участю 3329 пацієнтів показали, що ефективність біластину є порівняною з іншими АГП щодо TSS, NSS, NNS, оцінки дискомфорту при АР та якості життя і перевищує плацебо [27].
У поточному дослідженні не спостерігали суттєвих проблем із безпекою. Не повідомлялося про будь-які ПЕ або аномальні зміни лабораторних даних. Ці результати узгоджуються з попереднім дослідженням, яке підтверджує, що біластин безпечний і добре переноситься навіть після року безперервного лікування, і рекомендований як один з переважних для призначення препаратів в лікуванні АР. [24, 30]. У порівнянні з АГП І покоління, які були пов’язані зі значними ПЕ, передусім із седативним ефектом, біластин показав свої переваги і дав можливість уникнути небажаних ПЕ [31].
SSS використовували для оцінки психодинамічних ефектів 20 мг біластину через 2 год після застосування першої дози [28]. У метааналізі, проведеному Рандхавою та співавт., ефективність біластину була порівнянна з такою цетиризину, але було виявлено, що біластин виявляє значно менший седативний ефект [27].
В одиночному сліпому паралельному рандомізованому плацебо-контрольованому дослідженні, де учасники отримували разові дози 10, 20 і 50 мг (у 1-й частині) і добові дози 20 і 50 мг протягом 14 днів (у 2-й частині), була проведена оцінка за SSS на початку і через 2 і 24 год після застосування препарату в 1-й частині і на початку, через 2 і 24 год у 1-й, 8-й і на 14-й день у 2-й частині. Істотних відмінностей між біластином і плацебо виявлено не було, що вказує на відсутність у біластину седативного ефекту в разі тривалого застосування [18].
Перевагою цього дослідження стала оцінка впливу біластину в режимі реального часу на комплексні симптоми АР і на якість життя, у тому числі відсутність седативного ефекту в пацієнтів.
Висновки
У представленому багатоцентровому дослідженні в режимі реального часу було виявлено, що застосування біластину один раз на добу в дозі 20 мг протягом 28 днів значно полегшує симптоми АР відповідно до оцінок за TSS, NSS і NNSS, підвищує якість життя і забезпечує хороший профіль безпеки в пацієнтів з АР.
Список літератури – у редакції.
Реферативний огляд статті Bhargava S., Padmanabhan K., Ramappa C. Evaluation of efficacy and safety of bilastine 20 mg tablets in adult patients with allergic rhinitis. Int J Res Med Sci. 2022. Dec;10(12):2769-2775. https://doi.org/10.18203/2320-6012.ijrms20223077.
Підготувала Ірина Чумак.
Повну версію дивіться: www.msjonline.org
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (61) 2022 р.