1 грудня, 2024
Лікування алергічного ринокон’юнктивіту: в пошуках ідеального АГП
 Із приходом весняно-осіннього періоду декілька мільйонів людей у всьому світі стикаються з «черговою прикрою незручністю» – алергічним ринокон’юнктивітом (АРК). Досвідчений лікар навряд чи назве цю патологію «ніяковістю», адже АРК не лише негативно впливає на повсякденне життя та загальне самопочуття, значно знижуючи якість життя, але й асоційований зі значним економічним тягарем, особливо через непрямі витрати.
Із приходом весняно-осіннього періоду декілька мільйонів людей у всьому світі стикаються з «черговою прикрою незручністю» – алергічним ринокон’юнктивітом (АРК). Досвідчений лікар навряд чи назве цю патологію «ніяковістю», адже АРК не лише негативно впливає на повсякденне життя та загальне самопочуття, значно знижуючи якість життя, але й асоційований зі значним економічним тягарем, особливо через непрямі витрати.
Алергічний кон’юнктивіт не несе прямої загрози життю, тому йому зазвичай приділяють менше уваги, ніж іншим хронічним захворюванням із високою смертністю. Попри значну поширеність (приміром, у Північній Америці – приблизно 40% населення), майже третина випадків алергічного кон’юнктивіту залишається недодіагностованою та недолікованою. Перебіг алергічного кон’юнктивіту асоційований із високим ризиком розвитку іншої алергічної патології: алергічного риніту (АР), бронхіальної астми, еозинофільного езофагіту, атопічного дерматиту, харчової алергії (рис. 1). Лише 6% пацієнтів з алергією мають ізольовані очні симптоми, натомість 78% хворих на бронхіальну астму страждають на АР, а бронхіальну астму діагностують у 38% пацієнтів з АР. Алергічний кон’юнктивіт суттєво знижує якість життя, спричиняючи формування негативних емоцій (дратівливості, розчарування, гніву, збентеження), зниження продуктивності й концентрації, провокуючи виникнення втоми та зростання кількості діб непрацездатності.
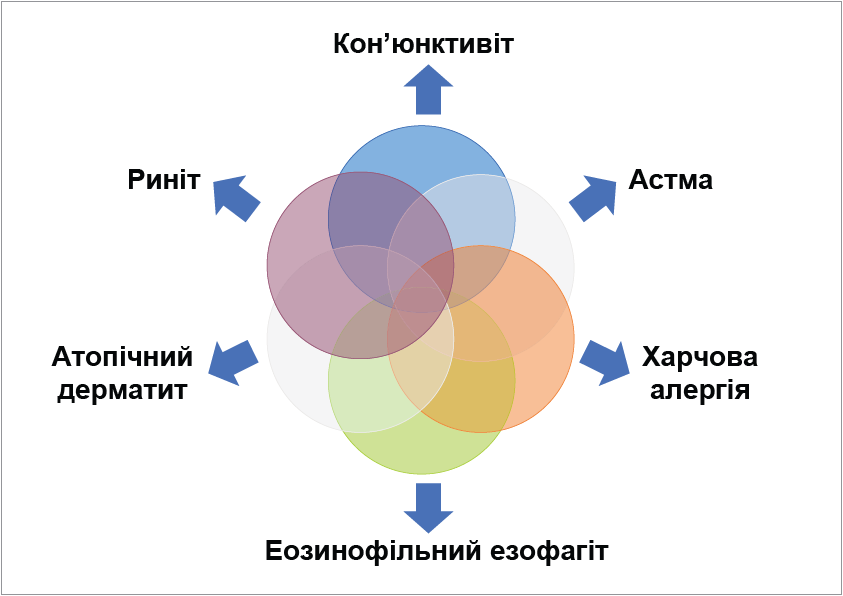 Рис. 1. Алергічні коморбідності (адаптовано за Dupuis P. et al., 2020)
Рис. 1. Алергічні коморбідності (адаптовано за Dupuis P. et al., 2020)
АРК: сучасні погляди
Чинна дефініція визначає АРК як алергічне захворювання носа й очей, що проявляється хронічним, переважно еозинофільним запаленням слизової оболонки носа та кон’юнктиви. Найчастішим збудником АРК є аероалергени, а саме амброзія, котра зумовлює та супроводжує перебіг АР. Рослинний пилок провокує виникнення більшої кількості очних симптомів, аніж інші форми аероалергенів. В Україні традиційно виділяють три періоди сплеску захворюваності на сезонний АР унаслідок алергічної реакції на пилок рослин. Вони відповідають трьом пікам цвітіння різних типів рослин. Перший пік – це весняний період, що зумовлений цвітінням рослин, які запилюються вітром (вільха, береза), другий пік припадає на літо, коли цвітуть злакові, третій (літньо-осінній) – на сезон цвітіння бур’янів. Щороку відзначають зростання кількості полісенсибілізованих пацієнтів: майже 80% хворих на АР відзначають реакцію на декілька алергенів; такі пацієнти мають вираженіші клінічні ознаки та вагоміше зниження якості життя.
Типовими клінічними ознаками АРК є закладеність носа, свербіж і почервоніння очей. Слід наголосити, що в пацієнтів з АР важливо відслідковувати очні симптоми, для цього корисною є візуальна аналогова шкала (ВАШ; рис. 2). Ураження очей спочатку характеризується молочно-/блідо-рожевим кольором кон’юнктиви із судинним застоєм, останній із часом може прогресувати до набряку кон’юнктиви (хемоз) (рис. 3). Очні симптоми негативно впливають на денну активність унаслідок погіршення зору (47,8%), скорочення щоденної активності (38,8%), зниження працездатності (25,8%), порушення сну (16,3%), збільшення кількості днів непрацездатності (12,9%). Підтвердження діагнозу АРК потребує призначення сучасної доказово обґрунтованої фармакотерапії, основою якої є антигістамінні препарати (АГП). Чинні сучасні рекомендації підкреслюють, що першою лінією терапії АР є АГП ІІ покоління, а вибір оптимального АГП залежить від багатьох чинників, зокрема безпеки й ефективності препарату, його впливу на психомоторні функції, наявності седативного ефекту. Результати клінічних досліджень свідчать, що біластин є найкращим вибором для лікування АР завдяки високій результативності та доброму профілю безпеки, можливості застосування в особливих групах пацієнтів і відсутності седативного ефекту.
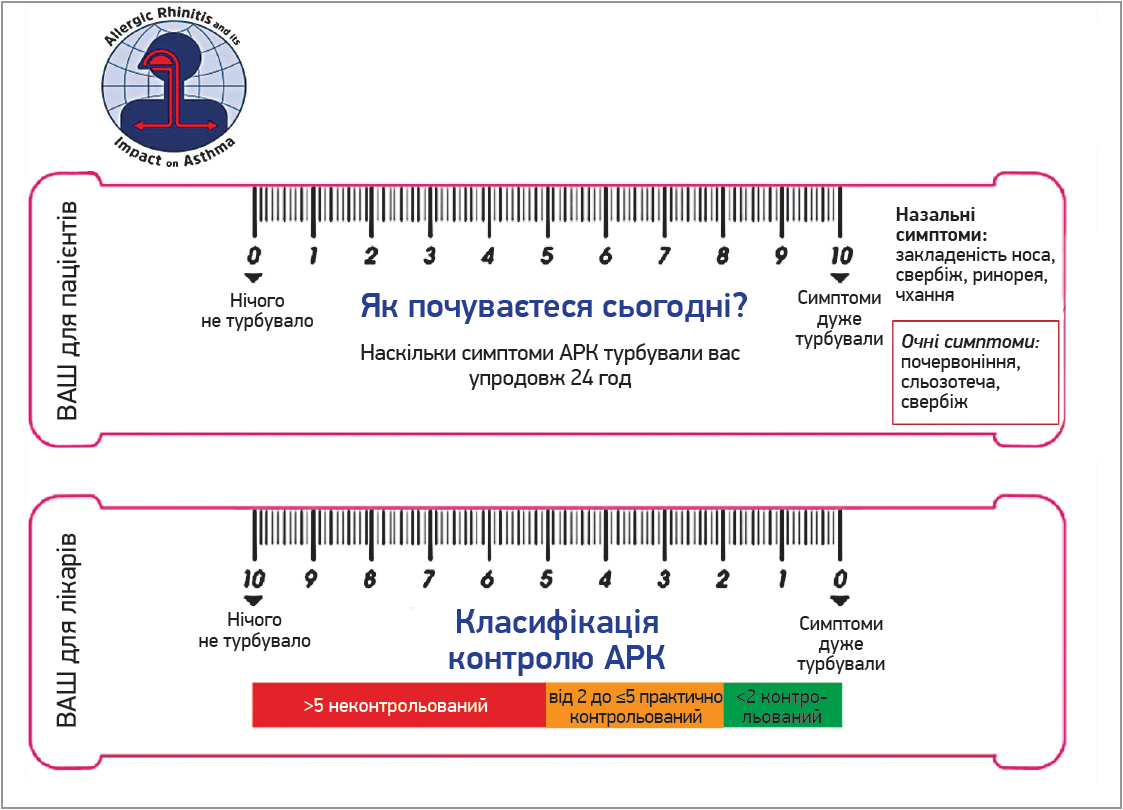 Рис. 2. Візуальна аналогова шкала (ВАШ) пацієнта та лікаря при лікуванні АР/АРК (адаптовано за Sybilski A.J., 2018)
Рис. 2. Візуальна аналогова шкала (ВАШ) пацієнта та лікаря при лікуванні АР/АРК (адаптовано за Sybilski A.J., 2018)
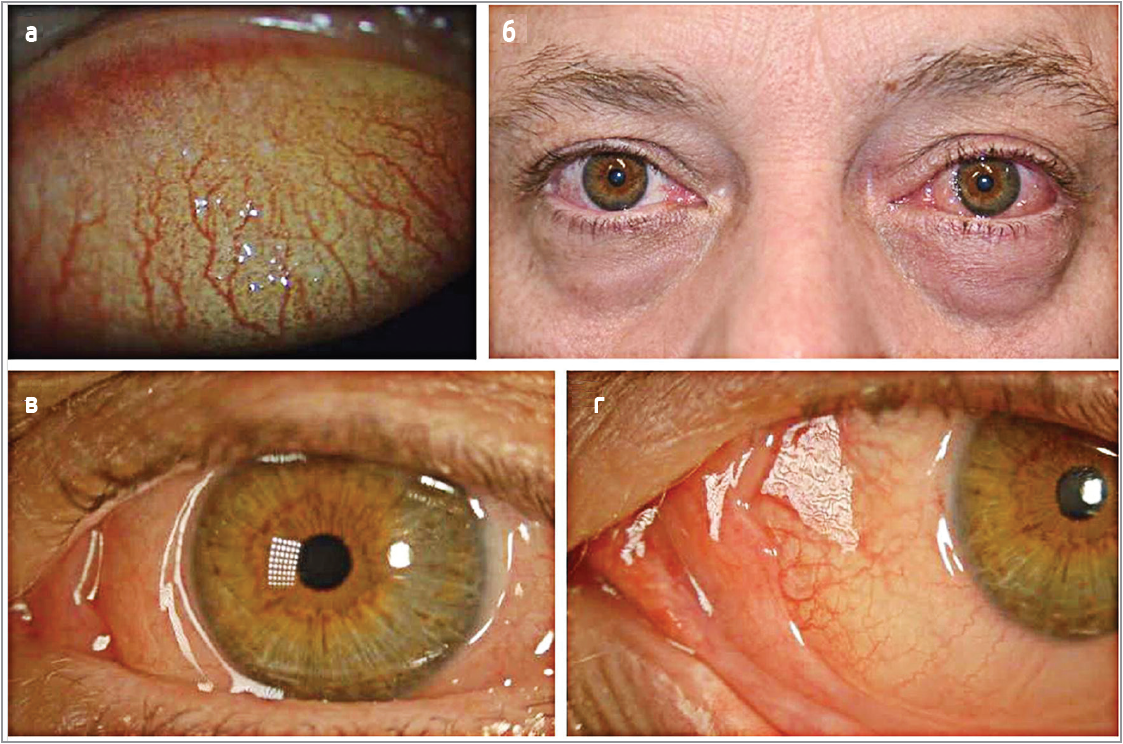
Рис. 3. Очні ознаки алергічного кон’юнктивіту: (a) хронічний цілорічний алергічний кон’юнктивіт, верхній тарзальний папілярний кон’юнктивіт; (б) гострий сезонний кон’юнктивіт – ліворуч (правий бік пацієнта) нормальне око, котре не зазнало впливу алергену, праворуч (лівий бік пацієнта) око, яке демонструє гостру алергічну реакцію протягом 20 хв після прямого контакту з алергеном пилку трави; (в) гострий алергічний кон’юнктивіт, інфекція та хімоз кон’юнктиви; (г) гострий алергічний кон’юнктивіт, сльозотеча (адаптовано за Prokopich C.L., Lee-Poyb M., Kimc H., 2018)
Клінічний випадок
У серпні на прийом до оториноларинголога звернулася пацієнтка Р., 30 років, зі скаргами на появу протягом останнього місяця ознак ринокон’юнктивіту, які посилюються вночі, а також виражену закладеність носа, що збільшується в серпні – вересні, епізоди кашлю та візингу (свистячого дихання) протягом серпня – вересня. Зазвичай для зменшення симптомів риніту пацієнтка застосовує АГП та/або інгаляційний кортикостероїд. З анамнезу хвороби відомо, що прояви АРК турбують пацієнтку вже протягом 4 років, від початку весни до осені. Хвора визначала наявність ознак орального алергічного синдрому при вживанні фруктів (яблук, персиків, дині, деяких видів горіхів); пацієнтка має домашніх улюбленців (кіт, собака). Під час проведення шкірних прик-тестів виявлено уртикарний дермографізм. Молекулярна алергодіагностика ALEX2 підтвердила раніше висловлене припущення щодо наявності полісенсибілізації до пилка різноманітних рослин, фруктів, шерсті котів. На підставі отриманих даних діагностовано персистивний АРК, поліноз, оральний алергічний синдром, полісенсибілізацію.
Крім елімінаційних заходів, корекції харчового раціону, пацієнтці призначено тривалий прийом біластину (Ніксар®, 20 мг), інгаляційний кортикостероїд, сольовий розчин, рекомендовано розглянути можливість проведення алергеноспецифічної імунотерапії з клінічно релевантними алергенами. Лікування забезпечило швидке нівелювання патологічних ознак АРК і досягнення доброго контролю над перебігом захворювання.
Обґрунтування рекомендованої терапії
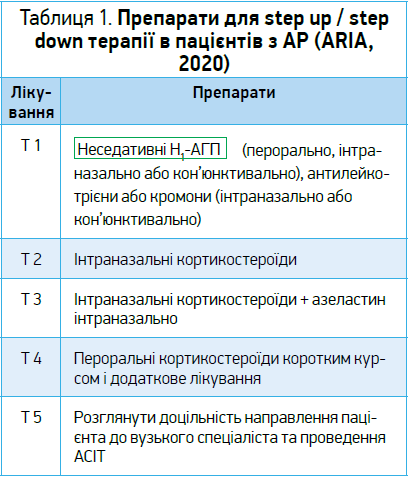
Призначаючи фармакотерапію нашій пацієнтці, ми керувалися положеннями сучасних настанов ARIA й EAACI/GA2LEN/EDF/WAO, котрі як терапію АРК першої лінії рекомендують використовувати АГП (табл. 1). Експерти віддають перевагу призначенню АГП ІІ окоління порівняно з представниками I покоління через краще співвідношення ефективність/безпека, сприятливу фармакокінетику та відсутність антихолінергічних і седативних побічних ефектів.
Аналізуючи інструкції до різних АГП ІІ покоління, можна виявити значні розбіжності в переліку показань для застосування. Такі представники цієї групи, як лоратадин, фексофенадин, дезлоратадин, левоцетиризин, рупатадин, офіційно рекомендовані для лікування АР та/або кропив’янки, тоді як пряме показання «терапія АРК» має лише один АГП ІІ покоління – біластин (Ніксар). Доведено, що біластин не лише полегшує чхання, виділення, свербіж і закладеність носа, але й зменшує свербіж очей, сльозотечу та почервоніння очей.
Високу ефективність біластину в лікуванні АРК пояснюють його сприятливими фармакологічними властивостями, котрі вигідно відрізняють його від інших АГП. По-перше, переважна більшість прийнятої дози біластину (95%) виводиться в незмінному вигляді (28,3% – із сечею, 66,5% – із фекаліями). По-друге, біластин не метаболізується печінковими CYP450, не індукує та не інгібує активність CYP450, унаслідок чого не провокує виникнення клінічно значущих лікарських взаємодій. Завдяки таким фармакологічним особливостям біластин може бути призначений хворим із порушенням функції печінки та нирок без корекції дозування. Клінічний ефект за прийому біластину розвивається відносно швидко (протягом першої години) та триває досить довго (протягом 24 год). Абсорбція препарату значно зменшується при одночасному прийомі з їжею, тому біластин варто приймати за 1 год до або через 2 год після їди.
Ще однією значущою характеристикою біластину є його висока спорідненість до H1-гістамінових рецепторів: вона в 5 і 3 рази перевищує таку фексофенадину та цетиризину відповідно. У межах рандомізованого подвійного сліпого перехресного одноцентрового дослідження, в якому порівнювали ефективність лікування АРК за допомогою одноразового прийому 20 мг біластину або 10 мг цетиризину, 120 мг фексофенадину, плацебо, було доведено, що біластин (n=74) протидіє виникненню назальних та очних симптомів АРК протягом 24 год, що значно перевищує тривалість дії фексофенадину (n=70) та плацебо (рис. 1).
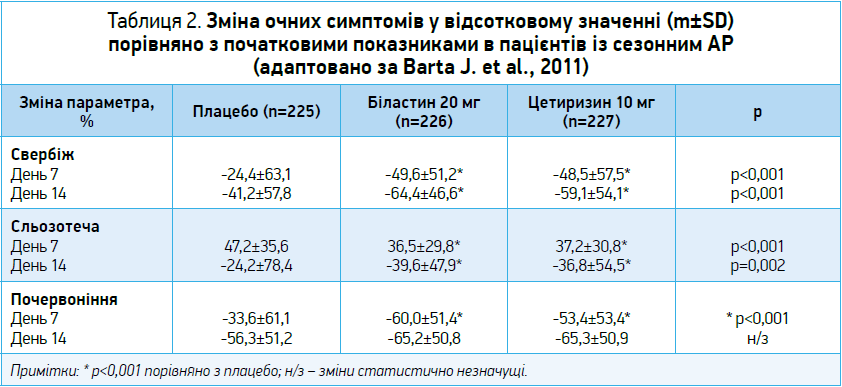
В іншому дослідженні продемонстровано, що 7- та 14-денна терапія 20 мг біластину (n=226) перевершує прийом 10 мг цетиризину (n=227) або плацебо (n=225) у нівелюванні почервоніння та свербежу очей, сльозотечі (табл. 2).
У дослідженні K. Okubo та співавт. (2017) 65 пацієнтів із сезонним АР та 55 – із цілорічним АР отримували біластин 20 мг/день протягом 12 або 52 тиж під час розповсюдження пилку сосни японської і кипарису в Токіо. Результати підтвердили ефективність і безпеку біластину за обох типів АР (рис. 4).
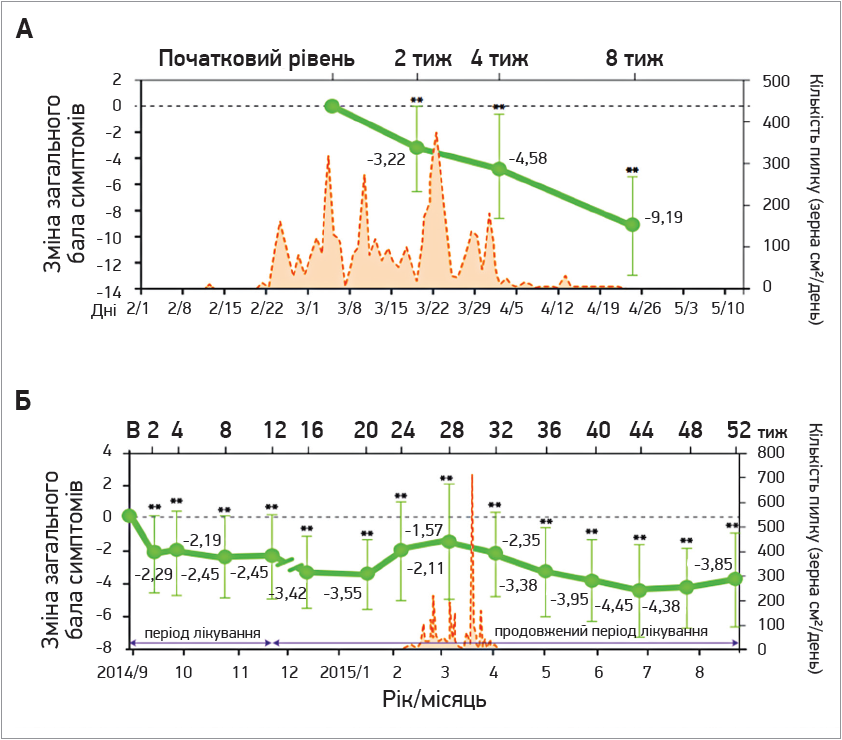 Рис. 4. Зміни загального бала симптомів (назальних та очних) за сезонного (А) та цілорічного (Б) АР (адаптовано за Okubo K. et al., 2017)
Рис. 4. Зміни загального бала симптомів (назальних та очних) за сезонного (А) та цілорічного (Б) АР (адаптовано за Okubo K. et al., 2017)
Важливою перевагою біластину є відсутність у нього седативного ефекту. Зазвичай пригнічення Н1-рецепторів у центральній нервовій системі (ЦНС) зумовлює виникнення сонливості, яка значно зменшує працездатність. Загальновідомим показником седативного потенціалу АГП є зайнятість H1-рецепторів ЦНС (H1RO), згідно з яким усі АГП розподіляють на неседативні (H1RO <20%), менш седативні (H1RO – 20-50%) і седативні (H1RO ≥50%). Здатність біластину зв’язуватися з Н1-рецепторами є найменшою порівняно з усіма іншими АГП ІІ покоління (рис. 5).
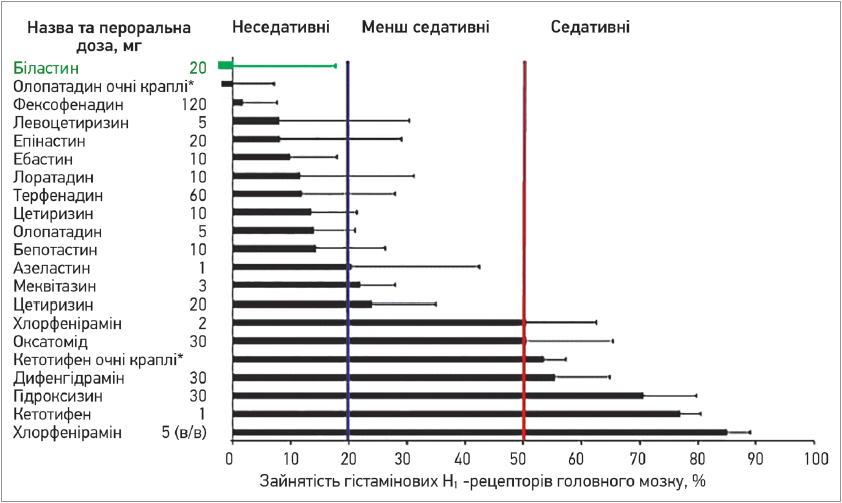 Рис. 5. Зайнятість гістамінових H1-рецепторів головного мозку (середній відсоток ± стандартне відхилення) антигістамінними препаратами (адаптовано за Kawauchi H. et al., 2019)
Рис. 5. Зайнятість гістамінових H1-рецепторів головного мозку (середній відсоток ± стандартне відхилення) антигістамінними препаратами (адаптовано за Kawauchi H. et al., 2019)
Більшість неседативних АГП є субстратами P-глікопротеїну, тому їх проникнення крізь гематоенцефалічний бар’єр (ГЕБ) обмежене. АГП ІІ покоління потрапляють до ЦНС через мозковий кровообіг і пасивно переносяться в ендотелій ГЕБ. Оскільки АГП є субстратами P-глікопротеїну, вони активно ретроградно транспортуються до мозкового кровообігу, і тільки їх мінімальна кількість зв’язується з Н1-рецепторами в головному мозку. Дослідження Н1RO неседативних, менш седативних і седативних АГП дало змогу встановити, що за умови зростання сироваткової концентрації лікарського засобу менш седативні та седативні АГП краще проникають у ЦНС і зумовлюють появу седативного ефекту; тоді як збільшення вмісту неседативних АГП у сироватці крові не супроводжується поліпшенням проникнення крізь ГЕБ і розвитком сонливості. Вважається, що H1RO неседативного АГП біластину (20 мг) становить майже 0%, тому цей препарат відносять до групи засобів, які не проникають у ЦНС.
Іншими важливими характеристиками, які опосередкують проникнення АГП у головний мозок, є їхні фізико-хімічні властивості. Доведено, що проникнення речовин крізь ГЕБ залежить від гідрофобності молекули, її молекулярної маси й електричного заряду. Деякі лікарські засоби з низькою молекулярною вагою (<400 Да) можуть проникати крізь ГЕБ за допомогою пасивної дифузії, але проникність препаратів із молекулярною масою 300-450 Да крізь ГЕБ зменшується в 100 разів. Доведено, що молекулярна маса біластину (463,6 кДа) значно перевершує таку дезлоратадину та левоцетиризину (відповідно, 310,8 та 388,9 кДа), що унеможливлює його перетин ГЕБ.
Клінічне дослідження здатності біластину (20 мг) провокувати виникнення сонливості або порушення/вповільнення когнітивних функцій проводили в чинних пілотів, штучно відтворюючи умови перебування на висоті 8000 м над рівнем моря за допомогою гіпобаричної барокамери. Доведено, що прийом біластину не впливав на пильність і здатність виконувати комплексні завдання порівняно з плацебо та гідроксизином (50 мг).
Відсутність седативного потенціалу дає змогу призначати біластин водіям та особам, які працюють із небезпечними механізмами під час лікування, що неможливо при використанні інших АГП ІІ покоління (в цьому випадку потрібно перевіряти реакцію на препарат перед застосуванням).
Висновки
Біластин (Ніксар®), сучасний неседативний АГП ІІ покоління, відповідає поточним рекомендаціям ARIA щодо застосовування АГП у лікуванні АР. Біластин (Ніксар®) використовується для симптоматичного лікування АРК, АР, кропив’янки; його прийом характеризується швидким початком (1 год) та тривалим періодом дії (24 год). Згідно з настановою ARIA біластин має особливі фармакологічні властивості, які унеможливлюють його перетин ГЕБ і виникнення седативного ефекту, забезпечують високу ефективність у лікуванні АРК, АР і добрий профіль безпеки; біластин (Ніксар®) відповідає критеріям EAACI/ARIA до оптимального лікарського засобу для лікування АР.
Медична газета «Здоров’я України 21 сторіччя» № 19/1 (581), 2024 р



 Гогунська І.В.
Гогунська І.В.
