15 грудня, 2020
Значення інтерферону в боротьбі з COVID‑19
 У грудні 2019 р. в Ухані, Китай, було зареєстровано спалах пневмонії в результаті зараження новим коронавірусом (CoV) важкого гострого респіраторного синдрому – SARS-CoV‑2. Це новий β-коронавірус, що має оболонку філогенетично схожу на SARS-CoV [1]. На відміну від коронавірусів HCoV‑229E, HCoV-OC43, HCoV-NL63 та HCoV-HKU, які є патогенними для людини та асоціюються зі слабкими клінічними симптомами, SARS-CoV‑2 нагадує як SARS-CoV, так і респіраторний синдром Близького Сходу (MERS), які можуть спричиняти важкі захворювання. Важливою відмінністю є те, що CoV, які уражають верхні дихальні шляхи, як правило, спричинюють легке захворювання, тоді як CoV, що уражають як верхні, так і нижні дихальні шляхи (наприклад, SARS-CoV‑2), можуть спричинювати важче захворювання [2].
У грудні 2019 р. в Ухані, Китай, було зареєстровано спалах пневмонії в результаті зараження новим коронавірусом (CoV) важкого гострого респіраторного синдрому – SARS-CoV‑2. Це новий β-коронавірус, що має оболонку філогенетично схожу на SARS-CoV [1]. На відміну від коронавірусів HCoV‑229E, HCoV-OC43, HCoV-NL63 та HCoV-HKU, які є патогенними для людини та асоціюються зі слабкими клінічними симптомами, SARS-CoV‑2 нагадує як SARS-CoV, так і респіраторний синдром Близького Сходу (MERS), які можуть спричиняти важкі захворювання. Важливою відмінністю є те, що CoV, які уражають верхні дихальні шляхи, як правило, спричинюють легке захворювання, тоді як CoV, що уражають як верхні, так і нижні дихальні шляхи (наприклад, SARS-CoV‑2), можуть спричинювати важче захворювання [2].
Не існує специфічного патогномонічного симптому на ранній стадії зараження COVID‑19. Інфіковані особи можуть скаржитися на слабкість, кашель, лихоманку або не мати жодних скарг і симптомів, та все ж вони вже є заразними. Точність ранньої діагностики на основі аналізу нуклеїнової кислоти може сягати 97%. Експіраторна задишка виникає на пізніх стадіях зараження, а респіраторний дистрес-синдром, гостра недостатність кровообігу або ниркова недостатність – у важких випадках.
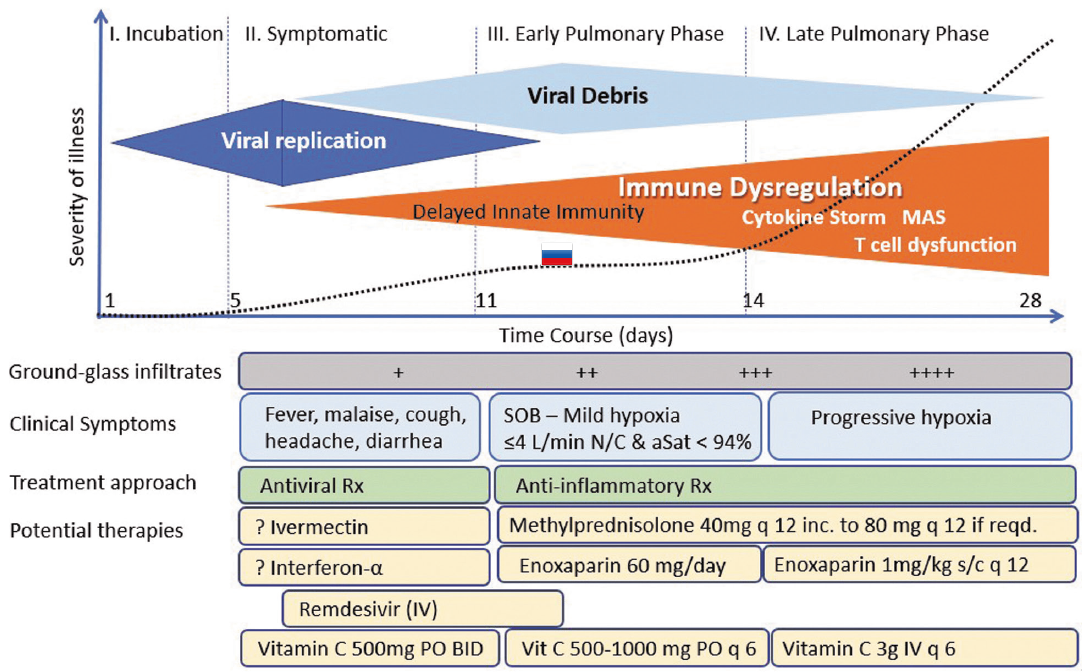
Ефективного терапевтичного протоколу для цього захворювання немає. Сучасні методи лікування є емпіричними, заснованими на симптомах і полягають у респіраторній підтримці, прийомі антибіотиків і противірусних препаратів, доповнених інфузією імуноглобуліну, гормональними засобами тощо (рис. 1) [3–5].
Рис. 1. Перебіг COVID-19 і загальний підхід до лікування [7]
SARS-CoV‑2 переважно передається через дихальні шляхи під час безпосереднього контакту. Повітряна та контактна ізоляція мають вирішальне значення для зменшення поширення вірусу. Саме тому пацієнтів з COVID‑19 та інфікованих SARS-CoV‑2 слід ізолювати в окремій кімнаті з постійною циркуляцією та дезінфекцією повітря і предметів навколишнього середовища [5]. Маска (N95) може на 95% заблокувати потрапляння вірусу в дихальні шляхи, а сувора гігієна рук може запобігти передачі вірусу контактним шляхом [6].
Нещодавно був розроблений фактично перший чіткий протокол профілактики та лікування COVID‑19 залежно від важкості стану пацієнта – EVMS Critical Care COVID-19 Management Protocol. Саме в ньому є дані щодо термінів призначення різних видів діагностичних тестів та лікування (рис. 2, 3) [7].
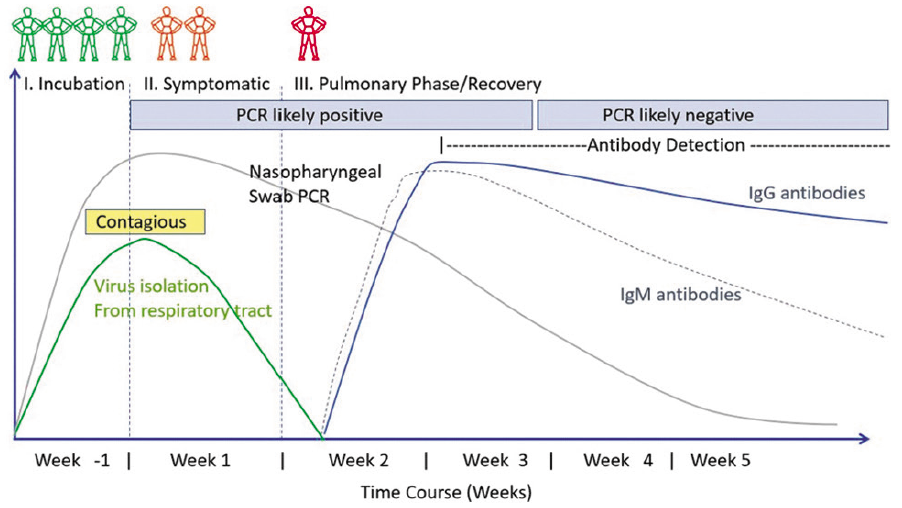 Рис. 2. Час проведення лабораторних досліджень на COVID-19
Рис. 2. Час проведення лабораторних досліджень на COVID-19
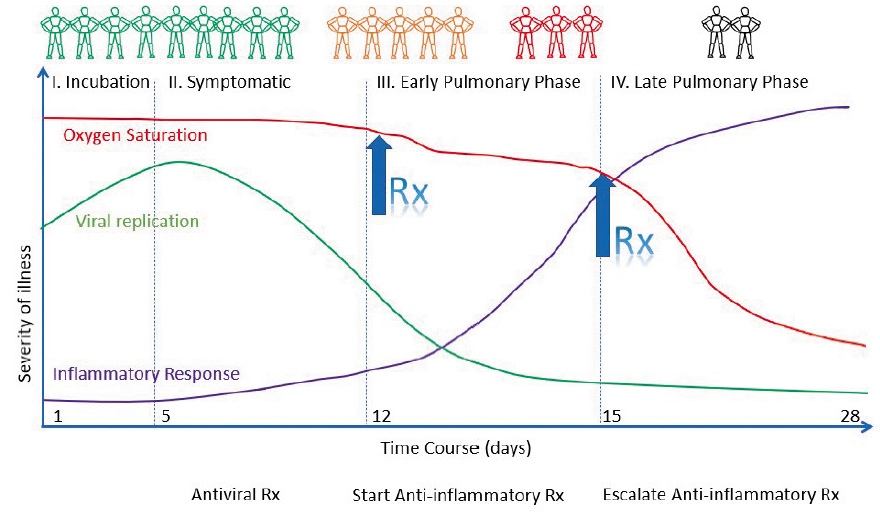 Рис. 3. Диференційований підхід до вибору лікувальної тактики залежно від стадії COVID-19
Рис. 3. Диференційований підхід до вибору лікувальної тактики залежно від стадії COVID-19
Клінічний спектр COVID‑19 варіює від безсимптомної інфекції до важких гострих респіраторних захворювань і смерті [8]. Існує нагальна потреба в противірусних препаратах для ефективного лікування цього захворювання. Завдяки своїм противірусним властивостям і відомим механізмам дії інтерферони I типу (IFN-α/β) можуть бути препаратами вибору серед противірусних засобів широкого спектра під час глобальних спалахів вірусних інфекцій [9].
У недавньому клінічному дослідженні були надані докази того, що лікування IFN-α2b прискорювало вірусний кліренс дихальних шляхів і знижувало рівні запальних біомаркерів – інтерлейкіну-6 (IL‑6) і С-реактивного білка (CRP) – у випадках COVID‑19 [2]. Під час попередніх епідемій, спричинених CoV (у 2002 р. – SARS-CoV і в 2012 р. – MERS-CoV), було надано докази того, що CoV кодують у своєму геномі фактори, що блокують вироблення IFN, у тому числі запобігають активації MyD88, пов'язаного з синтезом IFN і STAT1 (Signal transducer and activator of transcription 1, бере участь у позитивній регуляції генів за сигналами IFN) [9]. Важливо, що під час обох спалахів були наведені докази противірусних ефектів IFN I типу, що свідчить про те, що його застосування може нівелювати інгібувальну дію CoV [10, 11].
Настанови, видані експертною комісією ВООЗ, визначили IFN-α2b як потенційний противірусний засіб для лікування та профілактики COVID‑19 [12]. На початку спалаху Китайський уряд рекомендував використовувати IFN-α для лікування COVID‑19 [13]. Кілька клінічних досліджень, що оцінюють ефективність IFN-α2b для лікування COVID‑19, зареєстровано на сайті clinictrials.gov [14].
У EVMS Critical Care COVID-19 Management Protocol є рекомендації щодо застосування IFN при різних клінічних ситуаціях. Відповідно до цього протоколу, з метою профілактики COVID‑19 рекомендується IFN-α у вигляді назального спрея для медичних працівників і хворих на COVID‑19, які лікуються вдома. Також рекомендовано введення IFN-α/β підшкірно, у вигляді назального спрея або інгаляцій госпіталізованим пацієнтам з неважким перебігом хвороби [7].
Інтерферони (лат.: interferona; іnter – між + ferens – переносник) – клас низькомолекулярних глікопротеїнів, що виділяються клітинами організмів більшості хребетних тварин у відповідь на вторгнення чужорідних агентів, таких як віруси, деякі інші паразити та ракові білки. Завдяки IFN клітини стають несприйнятливими до цих агентів [15].
За типом IFN-рецепторів, через які вони передають свої сигнали, їх поділяють на три типи: IFN І, ІІ та ІІІ. Саме IFN I типу утворюються тоді, коли організм розпізнає потрапляння вірусу. Вони продукуються моноцитами і фібробластами. Окремі підтипи можуть бути отримані шляхом експресії генів людини. Коли IFN І потрапляє до збудника, він активує молекули, які запобігають утворенню та подвоєнню РНК і ДНК збудника. До IFN-α (лейкоцитарного) належить кілька видів білків з молекулярною масою 16–21 кДа (рис. 4) [15].
Рис. 4. Людський IFN-α
Найбільш вивченою властивістю IFN є його здатність запобігати розмноженню вірусів. Він утворюється в клітинах ссавців і птахів у разі потрапляння в організм інфекції. IFN – це активний противірусний агент, характерний для більшості типів клітин, і діє певною мірою проти більшості вірусів.
Фізіологічна реакція на вірусну інфекцію, як правило, ініціюється на клітинному рівні після реплікації [16]. Після потрапляння вірусу заражена клітина виявляє наявність реплікації вірусу за допомогою будь-якого з патернрозпізнавальних рецепторів (PRR, pattern recognition receptors) [17]. Ці рецептори служать вартовими для різноманітних мікроорганізмів як усередині, так і ззовні клітини, залучаючи різні структури, які розподіляються між різними патогенами. У разі зараження вірусом виявлення клітиною реплікації значною мірою опосередковується групою внутрішньоклітинних PRR, які вловлюють аберантні структури РНК, що зазвичай утворюються під час реплікації вірусу [17].
Залучення вірусоспецифічних структур РНК завершується олігомеризацією цих рецепторів та активацією факторів транскрипції, особливо факторів регулятора інтерферону (IRF) та ядерного фактора κB (NF-κB) [18]. Транскрипційна активація IRF і NF-κB призводить до запуску двох антивірусних програм. Перша – залучення клітинних противірусних захисних сил, що опосередковується транскрипційною індукцією IFN I і III типу з наступною активацією IFN-стимульованих генів (ISGs) [19]. Друга противірусна реакція полягає в залученні та координації певних субпопуляцій лейкоцитів, що реалізується переважно у вигляді секреції хемокінів [20, 21]. Ця потужна противірусна система чинить селективний тиск на віруси та призвела до еволюції незліченних контрзаходів проти вірусів [22].
IFN не виявляє пряму противірусну дію, але призводить до таких змін у клітині, які запобігають розмноженню вірусу. Утворення IFN можуть стимулювати не лише інтактні віруси, а й різні інші агенти, наприклад, деякі інактивовані віруси, дволанцюгові молекули РНК, синтетичні дволанцюгові олігонуклеотиди і бактеріальні ендотоксини. Біологічна активність інтерферону дуже висока.
Існує ще один шлях активації IFN. IFN запускає транскрипцію гена 2',5'-олігоаденілат-синтетази, який активує рибонуклеазу L, здатну розщеплювати вірусні РНК і мРНК. Крім того, рибонуклеаза L активує синтез ферменту протеїнкінази, яка блокує ініціацію трансляції, внаслідок чого припиняється трансляція вірусної і клітинної мРНК. Руйнуючи вірусну мРНК та блокуючи ініціацію трансляції, IFN виявляє противірусну дію проти будь-якого вірусного геному [15].
ІFN, що зараз виробляють фармацевтичні компанії, умовно поділяють за типом активного компонента на IFN-α, IFN-β, IFN-γ, а за способом виготовлення – на природні (препарати І покоління) та рекомбінантні (препарати ІІ покоління).
Перші природні IFN медичного призначення були отримані практично відразу ж після відкриття А. Айзекса та Ж. Лінденмана. Вже в 1961 р. було проведено перше клінічне дослідження з використанням препарату природного IFN, одержаного в лабораторії фірми Wellcome Ltd. Звичайно, перші препарати природних IFN не вирізнялись високою противірусною активністю та рівнем стандартизації. До того ж на початку 60-х років природні IFN одержували з лейкоцитів донорської крові. Сьогодні природні IFN-α, як правило, отримують шляхом інфікування вірусами лімфобластоїдних клітин людини або лейкоцитів крові донорів. Для продукції природних IFN-β використовують суперіндукцію культур фібробластів за допомогою синтетичних індукторів. Застосовують також методи, що підвищують вихід природних IFN, покращують ефективність очищення та концентрування кінцевого продукту.
Проте останніми роками все більше уваги приділяють рекомбінантним препаратам, розробленим за допомогою генно-інженерних технологій (наприклад, з використанням гена IFN-α2b людини та Escherichia coli як продуцента). Відзначається стрімке розширення масштабів їх використання при скороченні виробництва природних IFN, що значною мірою обумовлено дефіцитом і високою вартістю сировини (донорська кров) для їх виробництва.
Крім рекомбінантних випускають консенсусні IFN. Ці препарати являють собою нові задані комбінації амінокислотних послідовностей відомих субтипів IFN-α. Такі консенсусні IFN можуть бути ефективнішими, ніж рекомбінантні. Новими є препарати пролонгованої дії з покращеними фармакокінетичними властивостями, що досягається шляхом приєднання до молекули IFN ланцюга інертного полімеру, а саме поліетиленгліколю з молекулярною масою 12 або 40 кДа (пегільовані IFN). Такі препарати характеризуються принципово новими параметрами фармакокінетики та фармакодинаміки, що дає змогу підтримувати відносно сталу концентрацію IFN в організмі впродовж усього проміжку часу між послідовними введеннями препарату, що здійснюються підшкірно приблизно один раз на тиждень [23].
У Китаї було проведено дослідження, в якому визначали ефективність застосування IFN-α2b при COVID‑19 [2]. Особи з підозрою на COVID‑19 були госпіталізовані на основі первинних симптомів, таких як лихоманка, озноб, кашель, біль у горлі, головний біль, виділення з носа, міалгія, втомлюваність, задишка та/або діарея. На розсуд лікуючого лікаря в лабораторно підтверджених випадках COVID‑19 призначали противірусну терапію: IFN-α2b (5 мМО/мл) – n = 7; ARB (арбідолу гідрохлорид; Jiangsu Simcere Pharm. Co., таблетки, що диспергуються, по 100 мг) – n = 24; або комбінацію IFN-α2b та ARB – n = 46.
Відповідно до чинних на той час у лікарні практичних рекомендацій 5 мМО IFN-α2b (1 мл) додавали до 2 мл стерильної води та вводили у вигляді аерозолю за допомогою небулайзера та маски. Призначення IFN-α2b було дворазовим, тобто 10 мМО/день. ARB призначали по 200 мг (2 таблетки) тричі на добу, тобто 600 мг/добу.
Зразки мазка з горла перевіряли методом полімеразної ланцюгової реакції в реальному часі (RT-PCR) на SARS-CoV‑2. Використовуваний лабораторний аналіз на SARS-CoV‑2 базувався на рекомендаціях Центрів з контролю та профілактики захворювань США (CDC) [17]. Повний аналіз крові та біохімічні дослідження сироватки оцінювали відповідно до звичайних клінічних лабораторних процедур лікарні.
Вірусний кліренс визначали в разі 2 негативних тестів PCR підряд з інтервалом принаймні 24 год. Оцінюючи перебіг захворювання від дня появи симптомів (D0) до першої негативної (–) PCR, було виявлено значну різницю у швидкості очищення організму від вірусу у групах лікування. Зокрема, аналіз результатів показав, що лікування IFN-α2b, як самостійно, так і в поєднанні з ARB, прискорює вірусний кліренс порівняно з лікуванням лише ARB. Середня тривалість перебування вірусу в організмі становила 27,9 дня для пацієнтів, які отримували лише ARB, 21,1 дня – для тих, хто отримував лише IFN, та 20,3 дня – для тих, хто отримував IFN + ARB (від початку симптомів).
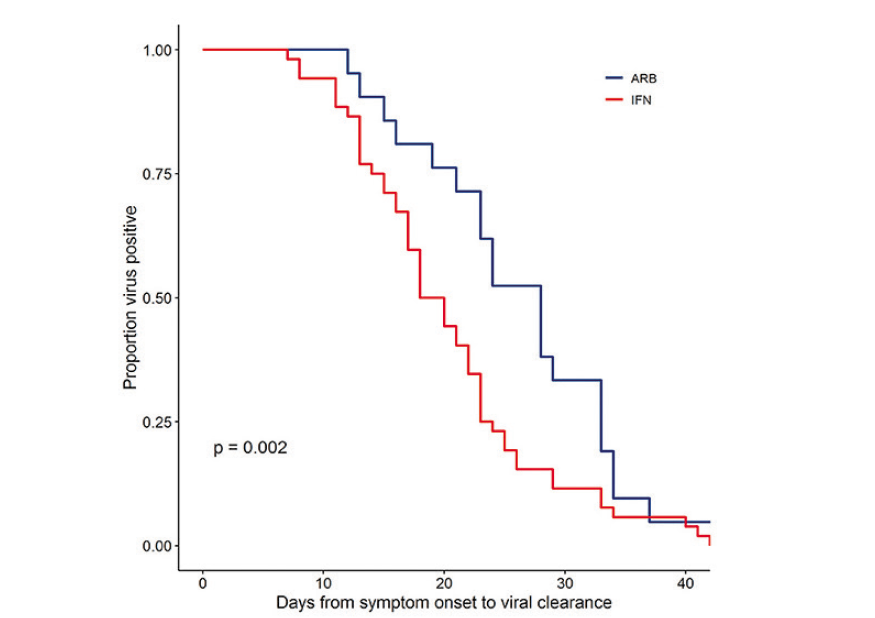
Враховуючи неоднорідність схем лікування, обраховували час до вірусного кліренсу для всіх випадків лікування IFN (об'єднали групу IFN з групою IFN + ARB, n = 53) і тих, хто отримував лише ARB (n = 24). Дані, наведені на рисунку 5, демонструють статистично значуще прискорення вірусного кліренсу верхніх дихальних шляхів у пацієнтів, які отримували IFN-α2b (20,4 доби, p = 0,002). Тобто лікування IFN прискорило кліренс вірусу на ~7 днів.
Рис. 5. Кліренс дихальних шляхів модифікованої групи IFN-α2b та ARB
Досліджували також рівні цитокінів у крові (IL‑2, IL‑4, IL‑10, IFN-γ, IL‑6, фактора некрозу пухлини-α (TNF-α) та біомаркерів запалення: CRP і прокальцитоніну (РСТ). Рівні РСТ, IL‑2, IL‑4, IL‑10, IFN-γ та TNF-α залишалися в межах норми впродовж усього перебігу захворювання, незалежно від групи лікування. Значна різниця виявлена в рівнях IL‑6 і CRP. Упродовж усього захворювання до його розрішення рівень IL‑6 залишався низьким у всіх пацієнтів, які отримували IFN, а в тих, хто отримував ARB (без IFN), спостерігалося значне підвищення рівня ІЛ‑6 (рис. 6). Схожа ситуація спостерігалась і з CRP.
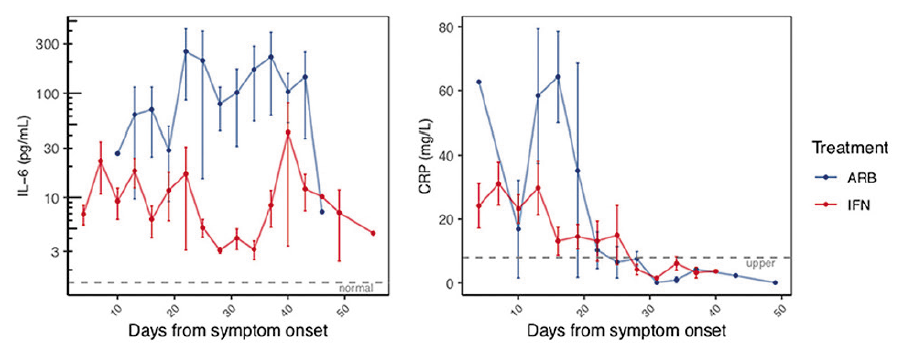 Рис. 6. Рівні маркерів запалення модифікованих груп IFN-α2b та ARB
Рис. 6. Рівні маркерів запалення модифікованих груп IFN-α2b та ARB
На основі цього дослідження можна зробити такі висновки. Терапія IFN-α2b скорочувала тривалість перебування SARS-CoV‑2 в організмі. Зниження рівнів маркерів гострого запалення, таких як CRP та IL‑6, корелювало з коротшим виділенням вірусу. IFN-α2b діє через функціональний ланцюг причинно-наслідкових зв'язків, де вірус-індуковане запалення є патофізіологічним фактором. У сукупності це підтверджує правомірність застосування IFN-α2b у терапії COVID‑19.
У ретроспективному когортному дослідженні 77 дорослих з помірнотяжким перебігом COVID‑19 у Китаї вивчали ефективність IFN-α2b. Учасники отримували IFN-α2b через небулайзер, IFN-α2b через небулайзер разом з уміфеновіром або лише уміфеновір. Кліренс верхніх дихальних шляхів від вірусу та зменшення системного запалення були швидшими у групах, які отримували IFN-α2b, аніж у групі, що приймала лише уміфеновір. Однак результати цього дослідження важко інтерпретувати, оскільки учасники з групи IFN-α2b з уміфеновіром були значно молодшими, ніж учасники групи лише уміфеновіру (середній вік у групі IFN-α2b з уміфеновіром становив 40 років проти 65 років у групі лише уміфеновіру), та мали на початку дослідження менше супутніх захворювань (15% проти 54% відповідно) [25].
На Кубі було проведено багатоцентрове проспективне дослідження, в якому взяли участь всі пацієнти з підтвердженою SARS-CoV‑2-інфекцією впродовж перших 33 днів епідемії в країні, з 11 березня по 14 квітня 2020 р. SARS-CoV‑2 було підтверджено на основі виявленння вірусу методом RT-PCR [26].
Пацієнти з підтвердженою SARS-CoV‑2-інфекцією, які дали інформовану згоду та не мали протипоказань для лікування IFN, описаних в інформаційному паспорті препарату, отримували терапію, схвалену кубинським протоколом з COVID‑19, а саме поєднання противірусних препаратів і внутрішньом'язового введення рекомбінантного IFN-α2b людини. 761 пацієнт (93,4%) отримував лікування у вигляді комбінації пероральних противірусних препаратів (лопінавір/ритонавір (LPV/RTV) і хлорохін) та внутрішньом'язового введення IFN-α2b тричі на тиждень упродовж 2 тиж. 53 пацієнти отримували лікування згідно із затвердженим протоколом лікування COVID‑19 без застосування IFN-α2b. Використовували LPV/RTV 250 мг, по 1 капсулі двічі на добу впродовж 30 днів, і хлорохін 150 мг, по 1 таблетці двічі на добу впродовж 10 днів. IFN-α2b вводили внутрішньом'язово 3 000 000 МО тричі на тиждень упродовж 2 тиж.
Для лікування педіатричних випадків дози препаратів були скориговані з урахуванням віку та маси або площі поверхні тіла (IFN: 100 000 МО/кг). Пацієнти з протипоказаннями або ті, хто відмовився від лікування IFN-α2b, отримували лише LPV/RTV і хлорохін. У тих випадках, коли хвороба прогресувала або стан був важким/критичним (потребував лікування у відділенні інтенсивної терапії), лікування IFN-α2b припиняли.
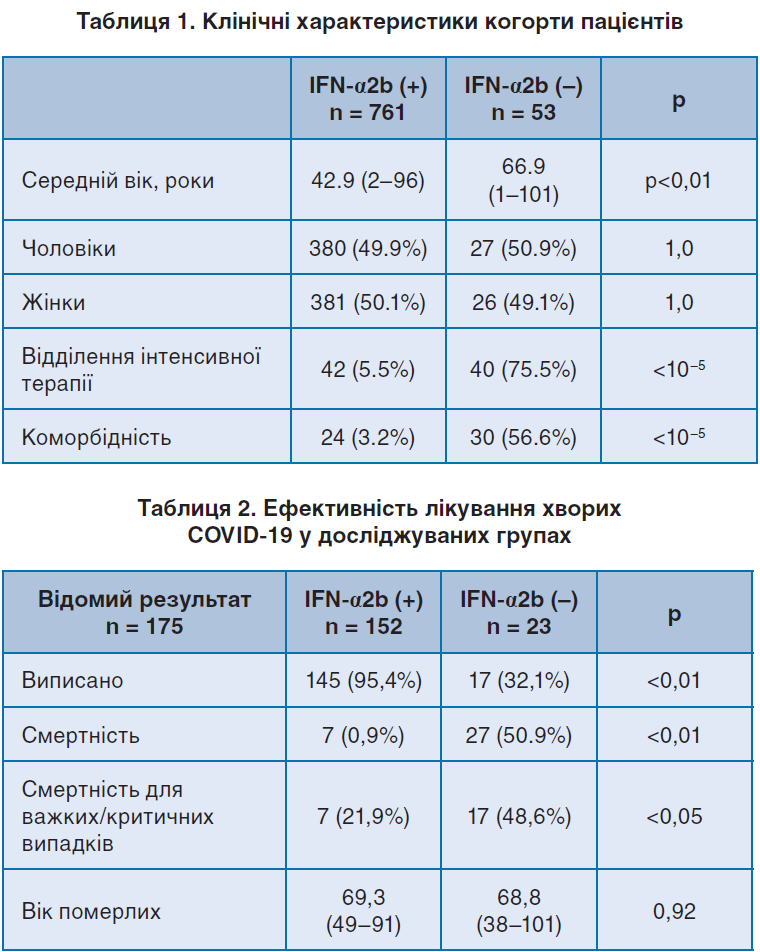
Як видно з таблиці 1, пацієнти, які не отримували IFN, були старшими та з більшою частотою супутніх захворювань (56,6% проти 3,2%), таких як високий кров'яний тиск, ішемічна хвороба серця та цукровий діабет. 14 квітня стаціонарне лікування отримували 639 (78,5%) пацієнтів (сюди ж належали пацієнти з ще не відомим результатом). Серед осіб з відомими результатами (табл. 2) найбільша частка тих, хто виявився PCR (–), була з групи, що отримувала IFN-α2b (95,4% проти 26,1%, р < 0,01).
На граничну дату (14 квітня 2020 р.) загальна летальність на Кубі становила 2,95% (MINSAP 2020). Летальність серед пацієнтів з групи IFN-α2b (+) становила 0,92 (р < 0,01). Ці показники були нижчими, аніж ті, що повідомляли ВООЗ того ж дня (ВООЗ 2020b) [20] = 6,34%. Клінічна, рентгенологічна та вірусологічна оцінки показали, що пацієнтів з несприятливим результатом захворювання (наявність клінічних/легеневих симптомів і/або виділення вірусу) було більше у групі, яка не отримувала IFN.
Таким чином, результати цього дослідження свідчать про ефективність IFN-α2b як противірусного засобу для лікування SARS-CoV‑2 і вказують на те, що його використання може сприяти одужанню від COVID‑19.
На Кубі проводили ще одне дослідження, яке повторно оцінювало внесок IFN-α2b у лікування COVID‑19 упродовж 98 днів епідемії в період з 11 березня по 17 червня 2020 р. [28]. Отже, було проведено проспективне дослідження для моніторингу терапевтичного ефекту IFN-α2b, що використовується в національному протоколі лікування COVID-19 на Кубі. Взяли участь пацієнти з позитивними результатами RT-PCR, які дали інформовану згоду та не мали протипоказань для лікування IFN.
Пацієнти отримували терапію відповідно до кубинського протоколу COVID‑19, а саме комбінацію пероральних противірусних препаратів (LPV/RTV і хлорохін) з внутрішньом'язовим або підшкірним введенням IFN-α2b. З 11 березня до 17 червня у 2 295 пацієнтів на Кубі було підтверджено зараження SARS-CoV‑2; 2 165 – проліковано IFN-α2b, а 130 – отримали лікування згідно з протоколом без IFN. Частка повністю вилікуваних пацієнтів була вищою у групі, що отримувала IFN-α2b, порівняно з групою, яка його не отримувала. За даними дослідників, лікування IFN-α2b зменшує ймовірність потреби в інтенсивній терапії та збільшує ступінь виживання хворих. Тобто це дослідження підтверджує попередні результати терапевтичної ефективності IFN-α2b при SARS-CoV‑2-інфекції.
Ключами до профілактики та контролю COVID‑19 є контроль за джерелами інфекції, переривання шляху передачі та захист сприйнятливих груп населення [29]. У Китаї проводилось дослідження з метою вивчення ефективності назальних крапель рекомбінантного людського IFN-α для профілактики COVID‑19 серед медичних працівників [6]. Усього в дослідженні взяли участь 2 944 медичні працівники, які були розподілені в групи низького або високого ризику залежно від того, чи вони безпосередньо контактували з пацієнтами з COVID‑19. Учасники групи з низьким ризиком отримували назальні краплі rhIFN-α (2–3 краплі в кожну ніздрю 4 рази на добу) впродовж 28 днів із захистом першого рівня; ті, хто входив до групи високого ризику, отримували назальні краплі rhIFN-α у поєднанні з тимозином-α1 (1,6 мг, підшкірна ін'єкція 1 раз на тиждень) разом із захистом другого або третього рівня.
Серед 2 944 досліджуваних 2 415 були включені до групи низького ризику, у тому числі 997 лікарів і 1 418 медсестер, середній вік яких становив 37,38 і 33,56 року відповідно. До групи високого ризику було включено 529 медичних працівників, у тому числі 122 лікаря та 407 медсестер, середній вік яких становив 35,24 і 32,16 року відповідно. Результати порівнювали з новими випадками COVID‑19 серед медичного персоналу провінції Хубей (у тому числі Ухань) за той самий період.
Захворюваність на COVID‑19 упродовж цих 28 днів дорівнювала нулю як у групі високого, так і низького ризику. Для контролю в період з 21 січня по 23 лютого 2020 р. спостерігали 2 035 нових випадків COVID‑19 серед медичного персоналу тієї ж області (провінція Хубей). Отримані результати показали, що назальні краплі rhIFN-α можуть ефективно запобігати COVID‑19 серед медичного персоналу. Також вони вказують на те, що назальні краплі rhIFN-α потенційно обіцяють захистити сприйнятливих здорових людей під час пандемії COVID‑19.
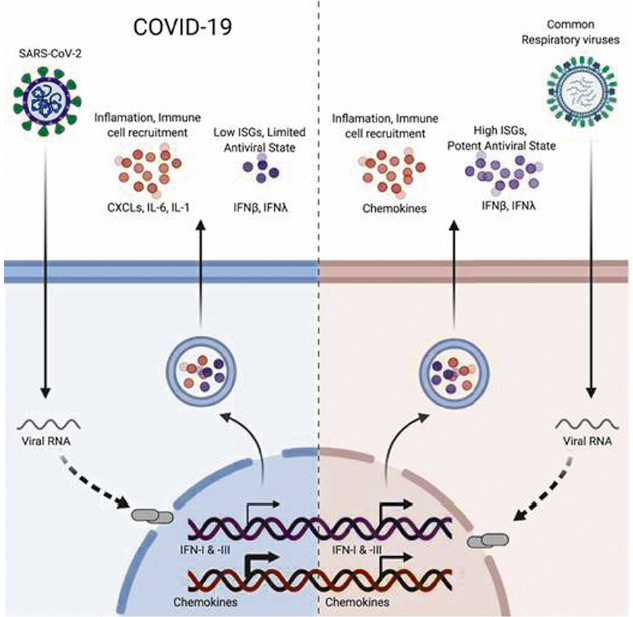
Факти свідчать, що кожен тип IFN може відігравати важливу роль у захисті організму хазяїна. Нещодавнє дослідження на основі даних scRNA-seq виявило, що келихоподібні та миготливі клітини носа експресують ангіотензин-перетворювальний фермент 2 (ACE2) – рецептор інвазії SARS-CoV‑2, а також вірусну протеазу TMRPSS2, що вказує на те, що ці клітини є початковими місцями інвазії та можуть бути резервуаром вірусу для передачі захворювання [30]. В іншій статті було показано, що IFN-α2 та IFN-γ керують експресією ACE2 в клітинах носового епітелію людини. Відмічено різке зменшення реплікації вірусу після додавання IFN I типу in vitro, припускаючи, що SARS-CoV‑2 може інгібувати наступну регуляцію ISG (рис. 7) [31].
Рис. 7. Різниця у механізмах дії SARS-CoV-2 та інших респіраторних вірусів на регуляцію IFN-стимульованих генів [31]
Клінічна симптоматика SARS-CoV‑1-інфекції, ймовірно, і SARS-CoV‑2-інфекції, залежить від порушення регуляції імунної відповіді в пацієнтів і затримки експресії IFN-I [32–34]. На основі моделей на тваринах було встановлено, що SARS-CoV‑1 індукує стійку цитокінову реакцію, яка, як правило, демонструє затримку продукції IFN-I, що завершується неправильним набором запальних популяцій моноцитів-макрофагів [32]. Ця динаміка відповідає і тому, що спостерігається в разі SARS-CoV‑2-інфекції, оскільки у відповідь на інфекцію, ймовірно, виробляється низький рівень IFN-I і -III. З огляду на помірний рівень реплікації вірусів, який спостерігають in vivo, одним з пояснень низької експресії IFN може бути те, що невелика частина клітин є рефрактерною до антагоністичного впливу SARS-CoV‑2, виробляючи достатню кількість IFN-I та/або IFN-III для активації імунних клітин та індукції ISG [31].
Таким чином, можна зробити висновок, що екзогенне додавання IFN I в клітини епітелію носа може запобігти інвазії та передачі вірусу шляхом створення високої локальної концентрації IFN, інгібуючи реплікацію вірусу та зменшуючи його резервування.
На ринку України вже багато років є препарат рекомбінантного людського IFN-α2 100 000 МО/мл у формі назальних крапель і спрея – Назоферон. Його ефективність вивчалась у численних дослідженнях щодо лікування та профілактики різних респіраторних захворювань серед усіх категорій населення [35–42]. Він зарекомендував себе як ефективний і безпечний засіб, який може використовуватись як педіатричними пацієнтами, так і вагітними жінками.
Список літератури
- Genomic characterization and epidemiology of 2019 novel coronavirus: implications for virus origins and receptor binding / R. Lu, X. Zhao, J. Li [et al.] Lancet. 2020. Vol. 395. P. 565–574. doi: 10.1016/S0140–6736(20)30251–8.
- Interferon-α2b Treatment for COVID‑19 / Q. Zhou, V. Chen, C. P. Shannon[et al.] Front. Immunol. 2020. Vol. 11. P. 1–6. https://doi.org/10.3389/fimmu.2020.01061
- Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China / C. Huang, Y. Wang, X. Li X [et al.] Lancet. 2020. Vol. 395(10223). P. 497–506.
- Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus–infected pneumonia in wuhan, china / D. Wang, B. Hu, C. Hu [et al.] JAMA. 2020. Vol. 323(11). P. 1061–1069.
- Letter: Strategies for Prevention and Control of 2019 Novel Coronavirus Infection Among Medical Staff / X. Wang, M. J. Wang, X.B., Jiang [et al.] Neurosurgery. 2020. Vol. 87, Issue 1. P. E57–E62. https://doi.org/10.1093/neuros/nyaa117.
- An experimental trial of recombinant human interferon alpha nasal drops to prevent COVID‑19 in medical staff in an epidemic area / Z. Meng, T. Wang, L. Chen [et al.] medRxiv. 2020. DOI: 10.1101/2020.04.11.20061473.
- EVMS Critical care COVID‑19 management protocol.2020. https://www.evms.edu/media/evms_public/departments/internal_medicine/EVMS_Critical_Care_COVID‑19_Protocol.pdf?fbclid=IwAR0HgHtQ9hgm7TFKGe7BrRYeB63VCK_fFDl6Y9GZFmerEVTmqrC24zAVYoU.
- Rothan H. A., Byrareddy S. N. The epidemiology and pathogenesis of coronavirus disease (COVID‑19) outbreak. J Autoimmun. 2020. Vol. 109. P. 102433.
- Wang B. X., Fish E. N. Global virus outbreaks: interferons as 1st responders. Semin Immunol. 2019. Vol. 43. P. 101300.
- Interferon alphacon‑1plus corticosteroids in severe acute respiratory syndrome / M. Loutfy, L. M. Blatt, K. A. Siminovitch [et al.] JAMA. 2003. Vol. 290. P. 3222–3228.
- Interferon-ß and mycophenolic acid are potent inhibitors of Middle East respiratory syndrome coronavirus in cell-based assays / B. J. Hart, J. Dyall, E. Postnikova [et al.] J Gen Virol. 2014. Vol. 95. P. 571–577.
- World Health Organization. (2020a). Clinical management of severe acute respiratory infection when novel coronavirus (2019-nCoV) infection is suspected: interim guidance, 28 January 2020. World Health Organization. https://apps.who.int/iris/handle/10665/330893.
- Qiu T, Liang S, Dabbous M, Wang Y, Han R, Toumi M. 2020. Chinese Guidelines Related to Novel Coronavirus Pneumonia. Preprints 2020:2020040207 [Epub ahead of print]; DOI: 10.20944/preprints202004.0207.v1.
- Belhadi D, Peiffer-Smadja N, Yazdanpanah Y, Mentre´ F, Laoue´nan C. 2020. A brief review of antiviral drugs evaluated in registered clinical trials for COVID‑19. MedRxiv. [Epub ahead of print]; DOI: 10.1101/2020.03.18.20038190.
- https://uk.wikipedia.org/wiki/%D0%86%D0%BD%D1%82%D0%B5%D1%80%D1%84%D0%B5%D1%80%D0%BE%D0%BD%D0%B8.
- TenOever B. R. The Evolution of Antiviral Defense Systems. Cell Host Microbe. 2016. Vol. 19. P. 142–149.
- Janeway C. A., Medzhitov R. Innate immune recognition. Annu. Rev. Immunol. 2002. Vol. 20. P. 197–216.
- Hur S. Double-Stranded RNA Sensors and Modulators in Innate Immunity. Annu. Rev. Immunol. 2019. Vol. 37. P. 349–375.
- Lazear H. M., Schoggins J. W., Diamond M. S. Shared and Distinct Functions of Type I and Type III Interferons. Immunity. 2019. Vol. 50. P. 907–923.
- Proudfoot A. E. Chemokine receptors: multifaceted therapeutic targets. Nat. Rev. Immunol. 2002. Vol. 2. P. 106–115.
- Sokol C. L., Luster A. D. The chemokine system in innate immunity. Cold Spring Harb. Perspect. Biol. 2015. Vol. 7. P. a016303.
- García-Sastre A. Ten Strategies of Interferon Evasion by Viruses. Cell Host Microbe. 2017. Vol. 22. P. 176–184.
- Дзюблик І. В. Інтерферони: природа, механізми дії та клінічне застосування препаратів інтерферону. Здоров'я дитини. 2016. № 5 (73). С. 79–84. http://dx.doi.org/10.22141/2224–0551.5.73.2016.78306.
- https://www.cdc.gov/coronavirus/2019-ncov/lab/rt-pcr-detection-instructions.html
- https://www.covid19treatmentguidelines.nih.gov/immune-based-therapy/immunomodulators/interferons/
- Therapeutic Effectiveness of Interferon-a2b Against COVID‑19: The Cuban Experience / R. Pereda, D. Gonza´lez, H. Blas Rivero [et al.] JOURNAL OF INTERFERON & CYTOKINE RESEARCH. 2020. Vol. 40, № 9. P. 438–442. DOI: 10.1089/jir.2020.0124
- World Health Organization. (2020b). Coronavirus disease (COVID‑2019) situation reports‑85, 14 April. World Health Organization. https://www.who.int/emergencies/diseases/novelcoronavirus‑2019/situation-reports.
- Therapeutic effectiveness of interferon alpha 2b treatment for COVID‑19 patient recovery / R. Pereda, D. Gonzalez, H. B. Rivero [et al.] // medRxiv. 2020. https://doi.org/10.1101/2020.07.28.20157974.
- Air, Surface Environmental, and Personal Protective Equipment Contamination by Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV‑2) from a Symptomatic Patient / SWX Ong, Y. K. Tan, P. Y. Chia [et al.] JAMA. 2020. Vol. 23(16). P. 1610–1612. doi:10.1001/jama.2020.3227.
- SARS-CoV‑2 entry factors are highly expressed in nasal epithelial cells together with innate immune genes / W. Sungnak, N. Huang, C. Bécavin [et al.] Nat Med. 2020. Vol. 26. P. 681–687. DOI: 10.1038/s41591–020–0868–6
- Imbalanced host response to SARS-CoV‑2 drives development of COVID‑19 / B.-M. Daniel, N.-P. Benjamin, L. Wen-Chun [et al.] Cell. Vol. 181. P. 1036–1045. https://doi.org/10.1016/j.cell.2020.04.026ll.
- Dysregulated Type I Interferon and Inflammatory Monocyte-Macrophage Responses Cause Lethal Pneumonia in SARS-CoV–Infected Mice / R. Channappanavar, A. R. Fehr, R. Vijay, [et al.] Cell Host Microbe. 2016. Vol. 19. P. 181–193.
- Pathogenic influenza viruses and coronaviruses utilize similar and contrasting approaches to control interferon-stimulated gene responses / V. D. Menachery, A. J. Eisfeld, A. Schäfer [et al.] MBio. 2014. Vol. 5. P. e01174–e14.
- Chemokine up-regulation in SARS-coronavirus-infected, monocyte-derived human dendritic cells / H. K. Law, C. Y. Cheung, H. Y. Ng [et al.] Blood. 2005. Vol. 106. P. 2366–2374.
- Чернышева О. Е., Сорока Ю. А. Интерферонотерапия в лечении острых респираторных вирусных заболеваний у детей. Здоров'я дитини. 2011. № 6 (33). С. 41–45.
- Абатуров А. Е., Агафонова Е. А. Интерферонотерапия острых респираторных вирусных инфекций у детей. Здоров'я дитини. 2017. № 3. С. 370–375.
- Давидова Ю. В., Ліманська А. Ю. Безпека використання препаратів інтерферону в лікуванні ГРВІ у вагітних високого ризику. Перинатология и педиатрия. 2016. № 1 (65). С. 27–32. doi 10.15574/PP.2016.65.27.
- Оптимизация лечения острых респираторных вирусных инфекций у детей / К. К. Орынбасарова, Л. С. Сагидуллина, Г. К. Ксетаева [и др.] Вестник КазНМУ. 2016. № 2. С. 61–64.
- Беш Л. В. Оцінка ефективності препаратів інтерферону в лікуванні гострих респіраторних вірусних інфекцій у дітей, які часто хворіють. Здоров'я дитини. 2015. № 2(61). С. 32–36.
- Крамарєв С. О., Євтушенко В. В. Оцінка ефективності рекомбінантного інтерферону альфа для профілактики та лікування респіраторних вірусних інфекцій у дітей. Здоров'я України. 2009. № 10. С. 52–53.
- Абатуров О. Є., Височина І. Л. Неспецифічна профілактика гострих респіраторних вірусних інфекцій у дітей. Современная педиатрия. 2012. № 8(48). С. 60–63.
- Кузнєцов С. В., Копейченко Т. С. Інтерферонотерапіягострих респіраторних вірусних інфекцій у дітей. Актуальная инфектология. 2016. № 1 (10). С. 48–50.