4 вересня, 2018
Ельтромбопаг у лікуванні імунної тромбоцитопенії

Імунна тромбоцитопенія (ІТП) – набутий розлад, що викликаний імунним руйнуванням тробомбоцитів і визначається як рівень тромбоцитів <100×109/л. Діти з ІТП зазвичай одужують без лікування, натомість у дорослих пацієнтів захворювання часто має хронічний характер. Міжнародна група з вивчення імунної тромбоцитопенії (IWG, 2009) рекомендує застосовувати саме термін «імунна тромбоцитопенія» (замість «ідіопатична пурпура»). Це пов’язано з кращим розуміннями патофізіології хвороби і тим, що в більшості дітей і дорослих пацієнтів немає пурпури. Крім того, не слід використовувати поняття «гостра імунна тромбоцитопенія», оскільки діагноз ІТП можна встановити лише ретроспективно.
Причинами первинної ІТП є поява патологічних антитромбоцитарних антитіл класу IgG (у 60-70% пацієнтів), порушений мегакаріоцитопоез і руйнування тромбоцитів, опосередковане Т-клітинами.
Можливі причини вторинної ІТП:
- антифосфоліпідний синдром;
- аутоімунна тромбоцитопенія (наприклад, синдром Еванса);
- загальний варіабельний імунодефіцит;
- інфекції (цитомегаловірус – CMV, Helicobacter pylori, вірус гепатиту С – HCV, вірус імунодефіциту людини – HIV, вірус вітряної віспи);
- лімфопроліферативні хвороби;
- побічний ефект трансплантації кісткового мозку;
- побічний ефект вакцинації;
- системний червоний вовчак.
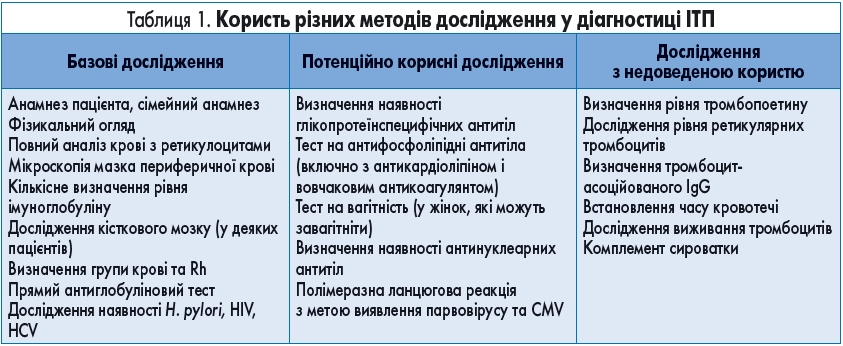
Діагноз ІТП зазвичай встановлюють на підставі результатів мікроскопії мазка периферичної крові, даних анамнезу та клінічного обстеження. Клінічна користь різних методів дослідження наведена в таблиці 1.
Метою лікування пацієнтів з хронічною ІТП є мінімізація ризику розвитку кровотечі шляхом підвищення рівня тромбоцитів до гемостатичного діапазону при максимальній переносимості та якомога нижчій частоті небажаних подій. Відповідь на лікування оцінюють за критеріями IWG (табл. 2), при цьому очікуваний час до отримання відповіді залежить від застосованої терапії (табл. 3).
Наразі ведення пацієнтів з ІТП здійснюється відповідно до рекомендацій Американського товариства гематології (ASH) 2011 р. Перегляд цих рекомендацій розпочався у 2015 р.; оновлений варіант очікується у 2018 р.
Рекомендації з діагностики та лікування ІТП (ASH, 2011)
Діти та підлітки
У дітей і підлітків з типовими проявами ІТП дослідження кісткового мозку не потрібне. Це дослідження також не є обов’язковим у дітей з відсутністю відповіді на внутрішньовенну терапію імуноглобуліном, до початку терапії кортикостероїдами та перед спленектомією. Визначення антинуклеарних антитіл є доцільним лише у випадках сумнівного діагнозу ІТП. Рутинне тестування на наявність інфекції Helicobacter pylori не показане.
У дітей без кровотеч або з легкими кровотечами (тобто тільки зі шкірними проявами – синцями та петехіями) можливе лише спостереження незалежно від рівня тромбоцитів.
У дітей, які потребують лікування, як першу лінію терапії можна призначати імуноглобулін в/в одноразово (0,8-1 г/кг маси тіла) або короткий курс кортикостероїдів. Порівняно з кортикостероїдами імуноглобулін дозволяє швидше підвищити рівні тромбоцитів.
Дітям зі зниженням вмісту гемоглобіну внаслідок кровотеч або з ознаками аутоімунного гемолізу терапія анти-D не рекомендується. Одноразове введення анти-D може призначатись як перша лінія терапії в Rh-позитивних дітей зі збереженою селезінкою, які потребують лікування.
 У дітей, у яких не досягнута відповідь на введення імуноглобуліну, анти-D або звичайних доз кортикостероїдів, як другу лінію терапії можна призначати дексаметазон у високій дозі або ритуксимаб. Ці препарати також можна використовувати як альтернативу спленектомії або за відсутності відповіді на спленектомію.
У дітей, у яких не досягнута відповідь на введення імуноглобуліну, анти-D або звичайних доз кортикостероїдів, як другу лінію терапії можна призначати дексаметазон у високій дозі або ритуксимаб. Ці препарати також можна використовувати як альтернативу спленектомії або за відсутності відповіді на спленектомію.
Спленектомія рекомендована дітям і підліткам з хронічною або персистуючою ІТП, які мають тяжкі та часто повторювані кровотечі, не відповідають на фармакотерапію (імуноглобулін, кортикостероїди, анти-D) або погано її переносять, або потребують покращення якості життя. Якщо це можливо, спленектомію слід відкласти принаймні на 12 міс від початку консервативного лікування.
Неімунізовані діти з ІТП в анамнезі повинні отримати першу дозу вакцини проти кору, краснухи та паротиту (MMR) за графіком. У дітей з ІТП, які вже отримали першу дозу вакцини MMR, рекомендовано визначити вакцинні титри. У разі повного імунітету (90-95% дітей) подальші дози вакцини MMR не вводять; в іншому випадку дитину слід вакцинувати повторно в рекомендованому віці.
Дорослі пацієнти
Дорослим з уперше встановленим діагнозом ІТП необхідно виконати тест на інфекцію HCV та ВІЛ. Подальші лабораторні дослідження показані лише за наявності інших змін (крім тромбоцитопенії та, можливо, залізодефіцитної анемії) у загальному аналізі або мазку крові. У пацієнтів з типовими проявами ІТП дослідження кісткового мозку не є необхідним незалежно від віку.
Лікування рекомендоване при зниженні рівня тромбоцитів <30×109/л.
Рекомендованою першою лінією терапії є пролонгований курс кортикостероїдів (наприклад, преднізолон у дозі 1 мг/кг перорально протягом 21 дня з наступною поступовою відміною). Альтернативними варіантами лікування є введення імуноглобуліну або кортикостероїдів коротким курсом (наприклад, дексаметазон по 40 мг перорально протягом 4 днів). Перевагу імуноглобуліну можна надавати у випадках, коли необхідно швидше збільшити рівень тромбоцитів. Крім того, імуноглобулін або анти-D (за наявності показань) можна використати у пацієнтів, яким кортикостероїди протипоказані. Анти-D слід застосовувати з обережністю через ризик розвитку тяжкого гемолізу.
Імуноглобулін вводять у дозі 1 г/кг одноразово. За необхідності введення можна повторити.
Пацієнтам, у яких не досягнута відповідь на лікування кортикостероїдами, рекомендована спленектомія – відкрита або лапароскопічна (однаково ефективні). Перед операцією рекомендована вакцинація проти пневмококової та менінгоковової інфекції. Крім інфекції, спленектомія асоціюється з такими ускладненнями, як кровотечі, потреба в переливанні крові або її компонентів, формування грижі, параліч нервів, а також інтраабдомінальні спайки, що можуть призводити до тромбозу та кишкової непрохідності.
За наявності протипоказань до спленектомії або рецидиву необхідно призначати агоністи рецепторів тромбопоетину. Ці препарати також можна застосовувати замість спленектомії в пацієнтів, у яких не отримана відповідь принаймні на один клас інших препаратів.
У рандомізованих клінічних дослідженнях ельтромбопаг продемонстрував ефективність у пацієнтів з персистуючою або хронічною ІТП зі збереженою або видаленою селезінкою. Препарат добре переноситься, небажані реакції зазвичай мають легкий характер. Після раптової відміни ельтромбопагу можливий рецидив тромбоцитопенії або тимчасове погіршення стану пацієнтів, тому протягом цього періоду необхідно бути настороженим щодо розвитку кровотеч. Крім того, слід періодично контролювати функцію печінки.
Альтернативою агоністам рецепторів тромбопоентину в другій лінії терапії є ритуксимаб. Проте через 1 рік лікування стійка відповідь досягається лише в 30% пацієнтів, частота довгострокової відповіді коливається від 18 до 35%.
Пацієнтам, які перенесли спленектомію, подальше лікування показане лише у разі рівня тромбоцитів <30×109/л.
Вагітні з ІТП у першій лінії терапії можуть отримувати кортикостероїди або імуноглобулін. Спосіб розродження обирають залежно від акушерських показань.
Пацієнтам з ІТП, асоційованою з HCV-інфекцією, за відсутності протипоказань рекомендована противірусна терапія. Проте необхідно контролювати рівень тромбоцитів через ризик поглиблення тромбоцитопенії внаслідок лікування інтерфероном. Якщо показане лікування ІТП, першою лінією терапії є введення імуноглобуліну.
Пацієнтам з ВІЛ-інфекцією та ІТП перед іншим лікуванням рекомендована антиретровірусна терапія (крім випадків, коли існує високий ризик розвитку кровотечі). Першою лінією ІТП у таких хворих може бути введення кортикостероїдів, імуноглобуліну або анти-D; за відсутності відповіді проводять спленектомію.
Пацієнтам з ІТП, які можуть отримувати антихелікобактерну терапію, рекомендований скринінг інфекції H. pylori з подальшим призначенням відповідного лікування в разі позитивного результату.
Нові підходи до лікування ІТП
З часу публікації рекомендацій ASH була проведена низка досліджень, у яких оцінювали нові стратегії лікування ІТП в дорослих пацієнтів.
У рандомізованому дослідженні була продемонстрована вища ефективність високодозової пульс-терапії дексаметазоном (перша лінія лікування) порівняно зі стандартною схемою з преднізолоном. У інших дослідженнях додавання ритуксимабу до дексаметазону підвищувало частоту ремісії у пацієнтів через 6 міс та 1 рік, проте це досягалось ціною вищої частоти небажаних явищ III і IV ступеня.
У ще одному дослідженні у пацієнтів з уперше діагностованою ІТП оцінювали ефективність високодозової терапії дексаметазоном (4 дні) з подальшим лікуванням ельтромбопагом у дозі 50 мг/добу з 5-го по 32-й день. Через 6 міс рівень тромбоцитів ≥30×109/л визначався у 75% пацієнтів, через 1 рік – у 67% пацієнтів.
Протягом багатьох років стандартною другою лінією лікування залишалася спленектомія. Проте нещодавнє дослідження показало, що цю операцію проводять менше ніж 25% пацієнтів. Через ризик приєднання інфекцій (підвищення в 5-30 разів у перші 90 днів зі збереженням значно підвищеного ризику розвитку інвазивних інфекцій і сепсису протягом життя), ризик виникнення тромбозу (>30 разів порівняно з загальною популяцією), легеневої гіпертензії та післяопераційних ускладнень спленектомію все частіше замінюють альтернативним лікуванням.
Ритуксимаб у другій лінії терапії, на жаль, не забезпечує достатньо високу частоту довготривалої ремісії (20% через 5 років порівняно з 60-70% для спленектомії). Деяким пацієнтам з початковою відповіддю на ритуксимаб можна вводити наступні дози, проте ефективність і безпека такого підходу не вивчені.
Останнім клінічним досягненням, що змінило стандарти другої лінії терапії хворих на ІТП, стало застосування антагоністів рецепторів тромбопоетину (ТПО). Ельтромбопаг – низькомолекулярний непептидний агоніст рецепторів ТПО для перорального прийому, схвалений для лікування пацієнтів віком від 1 року з хронічною ІТП, пацієнтів з хронічним гепатитом С та тромбоцитопенією, а також пацієнтів з апластичною анемією з недостатньою відповіддю на імуносупресивну терапію. Ельтромбопаг зв’язується з трансмембранним доменом рецептора ТПО, що активує проліферацію мегакаріоцитів із клітин-попередників у кістковому мозку та зрештою підвищує рівні тромброцитів.
Метааналіз 6 рандомізованих контрольованих досліджень показав, що ельтромбопаг значно підвищує рівень тромбоцитів і зменшує ризик розвитку кровотеч. Рівень тромбоцитів >50×109/л підтримувався у >80% пацієнтів, навіть серед хворих з високою рефрактерністю до попереднього лікування.
Дослідження EXTEND
У дослідженні III фази EXTEND (Eltrombopag Extended Dosing) вивчали показники безпеки, переносимості та ефективності тривалої підтримувальної терапії ельтромбопагом. У дослідження включали пацієнтів з хронічною первинною ІТП, які завершили участь в одному з попередніх досліджень ельтромбопагу: двох 6-тижневих і одному 6-місячному рандомізованих подвійних сліпих плацебо-контрольованих дослідженнях (TRA100773A, TRA100773B та RAISE) і відкритому дослідженні переміжного дозування (REPEAT). Критеріями участі в цих дослідженнях були хронічна ІТП (тромбоцитопенія принаймні протягом 6 міс), недостатня відповідь хоча б на один попередній варіант лікування та рівень тромбоцитів <30×109/л (<50×109/л у дослідженні REPEAT).
У дослідження EXTEND набирали пацієнтів незалежно від рівня тромбоцитів. Пацієнтів із вторинною ІТП або непереносимістю ельтромбопагу в анамнезі виключали. Протягом часу дослідження не дозволялось застосовувати нестероїдні протизапальні препарати (зокрема аспірин та інші саліцилати), розувастатин, правастатин, антикоагулянти, хінін і рослинні дієтичні добавки.
Початкова доза ельтромбопагу становила 50 мг 1 раз на день; залежно від рівня тромбоцитів дозу можна було зменшити до 25 мг/день (або рідше) або збільшити до 75 мг/день.
Дослідження складалося з 4 стадій.
Стадія 1: початок прийому ельтромбопагу в дозі 50 мг/день з подальшою титрацією дози для визначення такої, яка підвищила рівень тромбоцитів до ≥100×109/л.
Стадія 2: зниження дози або відміна супутніх препаратів для лікування ІТП з підтриманням рівня тромбоцитів ≥50×109/л за допомогою ельтромбопагу.
Стадія 3: титрація дози ельтромбопагу до мінімальної, необхідної для підтримання рівня тромбоцитів ≥50×109/л за мінімального застосування будь-яких інших препаратів для лікування ІТП.
Стадія 4: моніторинг безпеки та ефективності ельтромбопагу в мінімальній ефективній дозі.
Дослідження EXTEND почалося у червні 2006 р. і закінчилося в липні 2015 р. Середня тривалість ІТП до включення в дослідження становила 58,8 міс (від 9 до 552 міс). На момент включення 33% учасників отримували супутні препарати для лікування ІТП, 38% перенесли спленектомію і 70% мали початковий рівень тромбоцитів <30×109/л. До лікування ельтромбопагом найчастіше застосовували кортикостероїди (81%), імуноглобулін (46%) та ритуксимаб (23%).
 З 302 початково включених пацієнтів 135 (45%) завершили дослідження і 167 (55%) вибули з нього достроково; 60% пацієнтів отримували ельтромбопаг принаймні протягом 2 років, 35% – принаймні 3 роки. Причинами дочасного виходу з дослідження були виникнення небажаних явищ (14%), рішення пацієнта (13%), недостатня ефективність лікування (11%) та інші причини (13%). Найчастішими небажаними явищами, що стали причиною відміни лікування, були гепатобіліарні порушення (16 подій у 7 пацієнтів), катаракта (4 події у 4 пацієнтів) і тромбоз глибоких вен (3 події у 3 пацієнтів).
З 302 початково включених пацієнтів 135 (45%) завершили дослідження і 167 (55%) вибули з нього достроково; 60% пацієнтів отримували ельтромбопаг принаймні протягом 2 років, 35% – принаймні 3 роки. Причинами дочасного виходу з дослідження були виникнення небажаних явищ (14%), рішення пацієнта (13%), недостатня ефективність лікування (11%) та інші причини (13%). Найчастішими небажаними явищами, що стали причиною відміни лікування, були гепатобіліарні порушення (16 подій у 7 пацієнтів), катаракта (4 події у 4 пацієнтів) і тромбоз глибоких вен (3 події у 3 пацієнтів).
Загалом у 259 (85,8%) пацієнтів була отримана відповідь на лікування (досягнення рівня тромбоцитів ≥50×109/л за відсутності застосування «рятівної» терапії). Частота відповіді була дещо нижчою у пацієнтів з більш низьким початковим рівнем тромбоцитів (<30×109/л – у 81,5%; 30-50×109/л – у 98,1%; >50×109/л – у 92,3%), з видаленою селезінкою (80% vs 89,3% зі збереженою селезінкою) або таких, які раніше отримували ≥4 препаратів для лікування ІТП (79,6% vs 90,5% для пацієнтів, які отримували 1-3 препарати). Серед пацієнтів, у яких досягнуто зростання рівня тромбоцитів ≥50×109/л у попередньому дослідженні ельтромбопагу, 92-96% знову продемонстрували цю відповідь у дослідженні EXTEND.
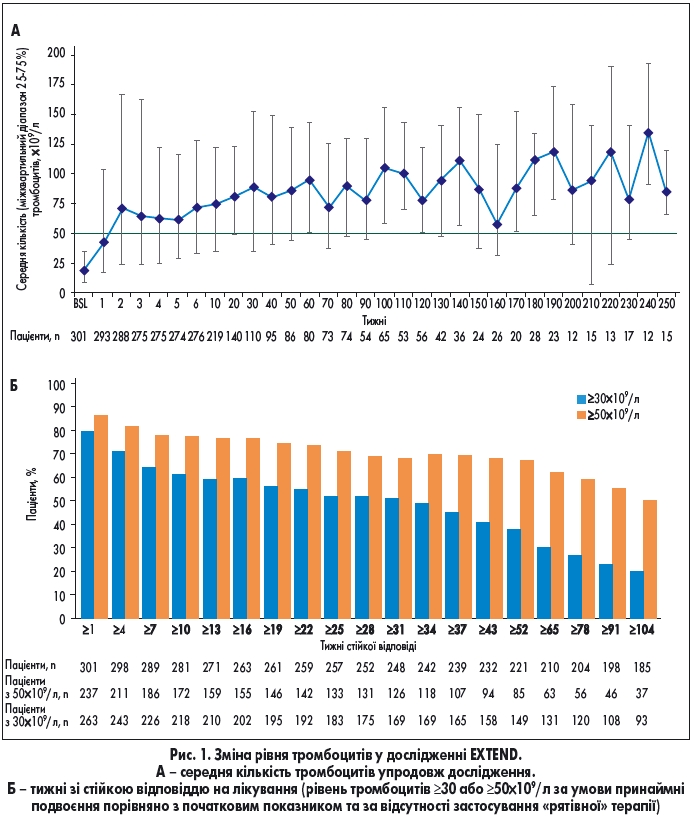
 Середній рівень тромбоцитів підвищувався до ≥50×109/л вже через 2 тижні лікування і залишався таким протягом 250 тижнів лікування (рис. 1А). Понад половина пацієнтів, які досягли рівня тромбоцитів >50×109/л (133/257; 52%), мали стабільний рівень тромбоцитів ≥50×109/л (або збільшення вдвічі порівняно з початковим рівнем) протягом принаймні 25 тижнів за відсутності потреби в «рятівній» терапії. 183 (71%) пацієнти з 257 досягли стабільного рівня тромбоцитів ≥30×109/л без застосування «рятівної» терапії упродовж цього періоду (рис. 1Б). Серед 101 пацієнта, які на початку отримували інше лікування ІТП, 34 (34%) повністю припинили застосування принаймні 1 супутнього препарату.
Середній рівень тромбоцитів підвищувався до ≥50×109/л вже через 2 тижні лікування і залишався таким протягом 250 тижнів лікування (рис. 1А). Понад половина пацієнтів, які досягли рівня тромбоцитів >50×109/л (133/257; 52%), мали стабільний рівень тромбоцитів ≥50×109/л (або збільшення вдвічі порівняно з початковим рівнем) протягом принаймні 25 тижнів за відсутності потреби в «рятівній» терапії. 183 (71%) пацієнти з 257 досягли стабільного рівня тромбоцитів ≥30×109/л без застосування «рятівної» терапії упродовж цього періоду (рис. 1Б). Серед 101 пацієнта, які на початку отримували інше лікування ІТП, 34 (34%) повністю припинили застосування принаймні 1 супутнього препарату.
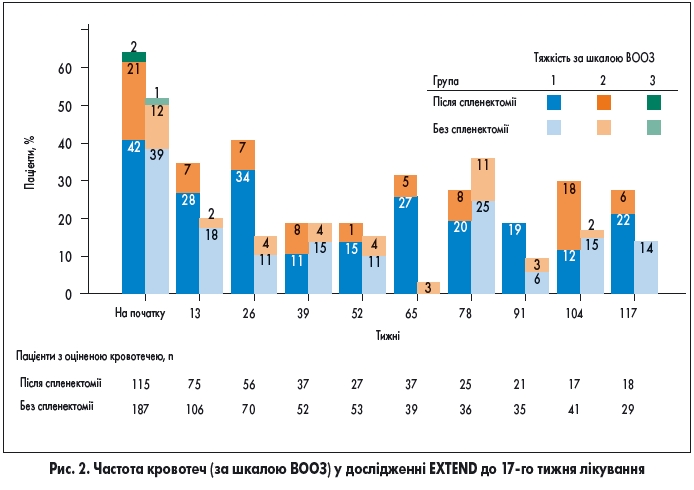
 До лікування ельтромбопагом симптоми кровотечі спостерігали у 171 (57%) пацієнта; через 1 рік цей показник знизився до 16%. Протягом дослідження частота кровотеч значно знижувалась як у хворих, які перенесли спленектомію, так і в пацієнтів зі збереженою селезінкою, при цьому переважна більшість кровотеч мали легкий характер (1 або 2 ступінь за шкалою ВООЗ; рис. 2). Частота кровотеч 3-4 ступеня становила лише 4,01 на 100 тис. пацієнтів на рік. За шкалою кровотеч IBLS більшість пацієнтів не мали жодних кровотеч.
До лікування ельтромбопагом симптоми кровотечі спостерігали у 171 (57%) пацієнта; через 1 рік цей показник знизився до 16%. Протягом дослідження частота кровотеч значно знижувалась як у хворих, які перенесли спленектомію, так і в пацієнтів зі збереженою селезінкою, при цьому переважна більшість кровотеч мали легкий характер (1 або 2 ступінь за шкалою ВООЗ; рис. 2). Частота кровотеч 3-4 ступеня становила лише 4,01 на 100 тис. пацієнтів на рік. За шкалою кровотеч IBLS більшість пацієнтів не мали жодних кровотеч.
Середня тривалість прийому ельтромбопагу становила 2,4 року (від 2 днів до 8,8 року). Зміни дози або частоти застосування препарату потребували 94% пацієнтів. Наприкінці дослідження більшість пацієнтів отримували ельтромбопаг 50 мг/день (23%) або 75 мг/день (39%); 108 пацієнтів (36%) приймали препарат у переміжному режимі (25 мг через день або рідше).
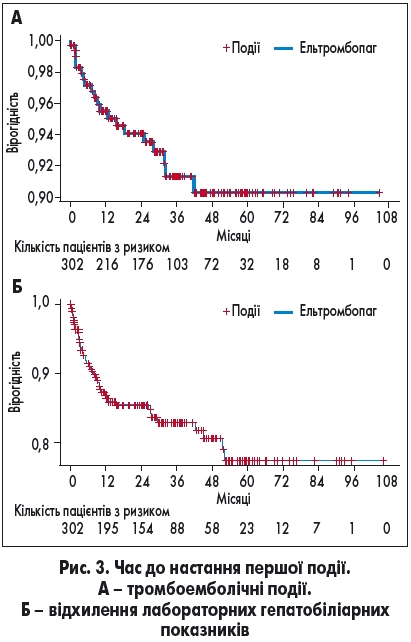
Найчастішими небажаними подіями були головний біль, назофарингіт та інфекції верхніх дихальних шляхів. Більшість подій мали легкий характер (1 або 2 ступінь). Важливо зазначити, що вірогідність розвитку тромбоемболічних подій і відхилення лабораторних гепатобіліарних показників значно зменшувалася після 1 року лікування ельтромбопагом (рис. 3).
Таким чином, дослідження EXTEND показало, що підтримувальна терапія ельтромбопагом є ефективною, безпечною і добре переноситься навіть за тривалого (протягом років) застосування препарату. У пацієнтів з хронічною ІТП, у яких не отримана відповідь на попереднє лікування, прийом ельтромбопагу сприяв підтриманню рівня тромбоцитів у гемостатичному діапазоні, зменшенню частоти кровотеч і потреби в застосуванні супутніх препаратів.
Підготував Олексій Терещенко
Тематичний номер «Онкологія» № 3 (54), червень-липень 2018 р.