17 червня, 2020
Ельтромбопаг при мієлодиспластичному синдромі чи гострому мієлоїдному лейкозі з тяжкою тромбоцитопенією

Рандомізоване плацебо-контрольоване дослідження ІІ фази ASPIRE
Мієлодиспластичний синдром (МДС) і гострий мієлоїдний лейкоз (ГМЛ) є гетерогенними групами клональних розладів кісткового мозку, що характеризуються неефективним гемопоезом і проліферацією бластів. Тромбоцитопенія часто асоційована зі значним ризиком розвитку ускладнень, в тому числі клінічно значимих кровотеч, які є предикторами ранньої смерті. Сучасні опції лікування тромбоцитопенії обмежені. Трансфузія тромбоцитів має короткотривалий терапевтичний ефект та супроводжується розвитком рефрактерності. Гіпометилювальні агенти можуть збільшувати кількість тромбоцитів, проте у багатьох пацієнтів не досягається відповідь на таке лікування, а в деяких такий терапевтичний підхід може зумовити прогресування захворювання чи його рецидив. Вищезазначене окреслює потребу в пошуку альтернативних засобів лікування тромбоцитопенії у хворих з МДС чи ГМЛ.
Агоністи рецепторів тромбопоетину, такі як ельтромбопаг і роміплостим, досліджують в аспекті лікування тромбоцитопенії при МДС чи ГМЛ. Ельтромбопаг – агоніст рецепторів тромбопоетину для перорального застосування, схвалений для лікування хронічної імунної тромбоцитопенії та тяжкої апластичної анемії. За даними преклінічних досліджень, введення ельтромбопагу забезпечувало потенційний антилейкемічний ефект без стимуляції проліферації злоякісних кістковомозкових мононуклеарних чи лейкемічних клітинних ліній. Протипухлинний ефект ельтромбопагу був продемонстрований, щонайменше частково, завдяки його здатності до хелатування заліза та модуляції міжклітинного гомеостазу заліза. У попередніх клінічних дослідженнях виявлено, що застосування ельтромбопагу добре переноситься пацієнтами з МДС чи ГМЛ та супроводжується зниженням частоти кровотеч, пов’язаних із тромбоцитопенією.
У рамках дослідження ASPIRE (A Study of eltromboPag In myelodysplastic syndRomes and acutE myeloid leukaemia) оцінювали ефективність лікування ельтромбопагом пацієнтів з МДС чи ГМЛ і тромбоцитопенією. Нижче наведено результати відкритої фази (частина 1 – з оцінюванням ефективності, безпеки та критеріїв для ескалації доз у наступній частині дослідження) та рандомізованої фази (частина 2 – з оцінюванням ефективності та безпеки ельтромбопагу у порівнянні з плацебо).
Результати. До першої частини дослідження було включено 17 пацієнтів. Відповідь тромбоцитів на проведене лікування спостерігалась у 4 (24%) хворих протягом 2 тижнів лікування; у 10 хворих відмічалось зменшення потреби у трансфузії тромбоцитарної маси. Для другої частини дослідження режим дозування коригували до мінімального інтервалу тривалістю 2 тижні перед збільшенням дози зі 100 до 200 мг на добу та з 200 до 300 мг на добу (50-100 мг на добу та 100-150 мг на добу для східноазіатської популяції).
Друга частина дослідження проходила із залученням 145 хворих з 61 центру по всьому світу, які були рандомізовані в групи ельтромбопагу (n=98) та плацебо (n=47). Більшість пацієнтів були похилого віку, з тяжкою тромбоцитопенією, очікуваними поганим прогнозом, короткою виживаністю та низькою якістю життя. На початку дослідження у групі ельтромбопагу було більше пацієнтів з порушеннями каріотипу при аналогічному співвідношенні хворих, які були залежними від трансфузії тромбоцитарної маси. В обох групах у більшості пацієнтів кількість тромбоцитів становила >10×109/л. Загалом 70 (48%) хворих завершили 12-тижневе лікування. Пацієнти групи ельтромбопагу частіше виходили з дослідження через побічні ефекти (n=31; 32%), з групи плацебо – через рішення лікаря (n=8; 17%).
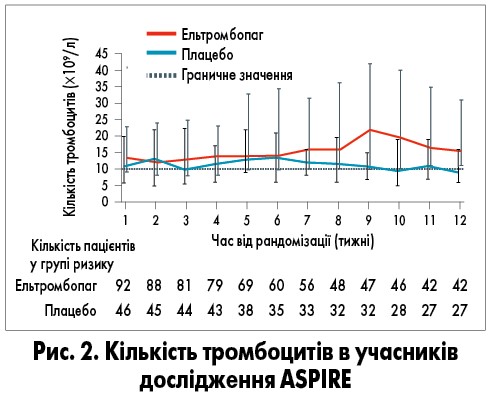
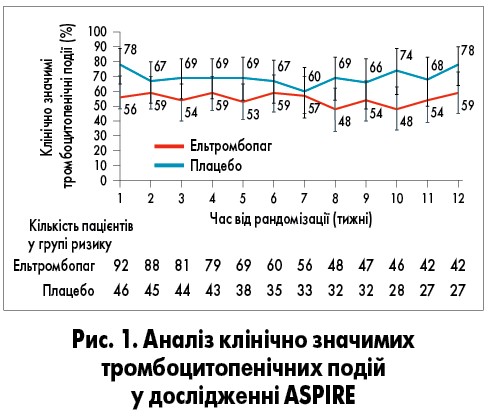 Пацієнти, які отримували ельтромбопаг, мали набагато менше клінічно значимих тромбоцитопенічних подій протягом 5‑12‑го тижня, ніж у групі плацебо: 54% (95% довірчий інтервал – ДІ – 43-64) проти 69% (95% ДІ 57-80) відповідно (відносний ризик 0,20; 95% ДІ 0,05-0,87; p=0,032; рис. 1). Різниця між групами була нижчою, ніж очікувалось. Середня щотижнева частка пацієнтів з кількістю тромбоцитів <10×109/л з 5-го по 12-й тижні була значно нижчою у групі ельтромбопагу порівняно з плацебо та становила 27% (95% ДІ 18-35) проти 51% (95% ДІ 37-62; р=0,0013) відповідно (рис. 2). Середня частка щотижневих трансфузій тромбоцитарної маси з 5-го по 12-й тижні у групах була зіставною – 51% в групі ельтромбопагу (95% ДІ 41-61) проти 52% в групі плацебо (95% ДІ 40-64; р=0,83). Середня щотижнева частка клінічно значимих тромбоцитопенічних подій була меншою в групі ельтромбопагу протягом усіх 12 тижнів.
Пацієнти, які отримували ельтромбопаг, мали набагато менше клінічно значимих тромбоцитопенічних подій протягом 5‑12‑го тижня, ніж у групі плацебо: 54% (95% довірчий інтервал – ДІ – 43-64) проти 69% (95% ДІ 57-80) відповідно (відносний ризик 0,20; 95% ДІ 0,05-0,87; p=0,032; рис. 1). Різниця між групами була нижчою, ніж очікувалось. Середня щотижнева частка пацієнтів з кількістю тромбоцитів <10×109/л з 5-го по 12-й тижні була значно нижчою у групі ельтромбопагу порівняно з плацебо та становила 27% (95% ДІ 18-35) проти 51% (95% ДІ 37-62; р=0,0013) відповідно (рис. 2). Середня частка щотижневих трансфузій тромбоцитарної маси з 5-го по 12-й тижні у групах була зіставною – 51% в групі ельтромбопагу (95% ДІ 41-61) проти 52% в групі плацебо (95% ДІ 40-64; р=0,83). Середня щотижнева частка клінічно значимих тромбоцитопенічних подій була меншою в групі ельтромбопагу протягом усіх 12 тижнів.
 У двох пацієнтів отримано повну відповідь на лікування: в одного (1%, повна відповідь кісткового мозку) в групі ельтромбопагу і в одного (2%, повна морфологічна відповідь) у групі плацебо. Близько 1/5 пацієнтів обох груп мали стабілізацію захворювання (18% в групі ельтромбопагу та 21% в групі плацебо). Слід враховувати, що дані 36 (37%) з 98 пацієнтів групи ельтромбопагу та 8 (17%) з 47 пацієнтів групи плацебо були недоступними для оцінювання ефекту, що могло вплинути на кінцевий результат дослідження.
У двох пацієнтів отримано повну відповідь на лікування: в одного (1%, повна відповідь кісткового мозку) в групі ельтромбопагу і в одного (2%, повна морфологічна відповідь) у групі плацебо. Близько 1/5 пацієнтів обох груп мали стабілізацію захворювання (18% в групі ельтромбопагу та 21% в групі плацебо). Слід враховувати, що дані 36 (37%) з 98 пацієнтів групи ельтромбопагу та 8 (17%) з 47 пацієнтів групи плацебо були недоступними для оцінювання ефекту, що могло вплинути на кінцевий результат дослідження.
Прогресування захворювання спостерігалося у 61 (62%) хворого, який отримував ельтромбопаг, та у 36 (77%) групи плацебо. Трансформація ГМЛ відмічена у 31 (62%) пацієнта групи ельтромбопагу та у 16 (73%) хворих групи плацебо. Медіана виживаності без прогресування становила 1,08 міс при лікуванні ельтромбопагом та 0,94 міс при використанні плацебо (відношення ризиків 0,99; 95% ДІ 0,68-1,43; р=0,94).
Протягом другої частини дослідження померло 47 (48%) пацієнтів, які отримували ельтромбопаг, та 18 (38%) з групи плацебо. Медіана загальної виживаності складала 4,3 міс при лікуванні ельтромбопагом та 4,6 міс в групі плацебо (відношення ризиків 0,97; 95% ДІ 0,64-1,48; р=0,89).
Максимальна середня тривалість незалежного від трансфузій тромбоцитарної маси періоду для хворих групи ельтромбопагу становила 26,3 дня, для плацебо – 25,4 дня (p=0,94). На початку 32% пацієнтів з групи ельтромбопагу та 28% з групи плацебо не мали кровотеч. При подальшому аналізі частка пацієнтів без кровотеч була більшою після лікування ельтромбопагом, що особливо виражено на 12‑му тижні (53 проти 22%). Покращення гематологічної картини в обох групах було аналогічним. Медіана кількості кістковомозкових бластів не відрізнялась між групами на початку дослідження та через 12 тижнів.
Відсутня значима відмінність між групами щодо якості життя, яку оцінювали шляхом опитування з використанням форм FACT-Th18 та EQ‑5D. Про побічні явища дослідники повідомляли у 98% хворих групи ельтромбопагу та 100% групи плацебо. Найбільш частими були петехії, носові кровотечі, пірексія, діарея та слабкість. Пропорція у групах була приблизно однаковою, за винятком петехій і слабкості, які частіше виникали у групі ельтромбопагу. Про тяжкі ускладнення повідомляли у 58% хворих групи ельтромбопагу та у 68% групи плацебо. Найбільш частими були пневмонія, сепсис, пірексія та фебрильна нейтропенія.
Обговорення. ASPIRE – перше рандомізоване дослідження з оцінювання ефективності ельтромбопагу у режимі монотерапії у пацієнтів з МДС і ГМЛ та тяжкою тромбоцитопенією. Дослідження досягло першочергової мети щодо зменшення клінічно значимих тромбоцитопенічних подій (≥1 геморагічних ускладнень ≥3 ступеня тяжкості, кількість тромбоцитів <10×109/л або трансфузія тромбоцитарної маси). Слід відмітити, що різниця між групами була меншою за таргетну. Дані попередніх досліджень агоністів рецепторів тромбопоетину свідчать про можливість зменшення тромбоцитопенічних наслідків у пацієнтів з МДС і ГМЛ. Результати досліджень I та II фази показали, що ельтромбопаг може індукувати істотне збільшення кількості тромбоцитів у пацієнтів з МДС групи низького та 1-го середнього ризику, збільшення кількості тромбоцитів при МДС і ГМЛ та покращення стану при інших гематологічних порушеннях. Результати дослідження II фази дали підстави припустити, що роміплостим може знижувати частоту розвитку кровотеч та призначень трансфузії тромбоцитарної маси у пацієнтів з МДС групи низького та 1-го середнього ризику.
В ASPIRE досліджували популяцію тяжкохворих пацієнтів, яким було не показане інше лікування з приводу ГМЛ і МДС, у котрих кровотечі були очікуваним і звичним ускладненням. Частка пацієнтів без кровотеч була більшою у групі ельтромбопагу, що дає підстави говорити про ефективність ельтромбопагу у зменшенні геморагічних ускладнень. Профіль безпеки був очікуваним для ельтромбопагу у хворих із МДС чи ГМЛ і тяжкою тромбоцитопенією.
У попередніх доклінічних та більшості клінічних досліджень показано, що ельтромбопаг не стимулює ріст бластів кісткового мозку при МДС чи ГМЛ. У дослідженні ASPIRE не виявлено прогресування МДС чи клінічного погіршення лейкозу. Частка пацієнтів зі стабілізацією захворювання та криві загальної виживаності не мали достовірних відмінностей між групами. Проте транзиторне збільшення кількості бластів у периферичній крові під час лікування роміплостимом в осіб з МДС групи низького та 1-го середнього ризику припускало потенційний зв’язок з трансформацією ГМЛ. Віддалені результати показали, що короткострокове призначення роміплостиму не підвищує частоту трансформації ГМЛ. Загалом, беручи до уваги вимоги до лікування тромбоцитопенії у популяціях високого ризику з очікуваними поганими результатами, результати ASPIRE та інших клінічних досліджень свідчать на користь монотерапії ельтромбопагом при МДС чи ГМЛ завдяки його важливим клінічним перевагам.
Зменшення частоти розвитку кровотеч і клінічно значимих геморагічних подій в ASPIRE не супроводжувалось гематологічним покращенням чи зростанням незалежності від трансфузії тромбоцитів, що пояснюється стадією захворювання залучених пацієнтів. Також, незважаючи на рандомізацію, групи мали певні відмінності, що могло вплинути на результат. Хоча ефект ельтромбопагу щодо частоти трансфузій тромбоцитарної маси та гематологічного покращення був незначним, автори дослідження ASPIRE роблять висновок, що цей препарат можна застосовувати як монотерапію у разі обмежених терапевтичних альтернатив у деяких хворих з МДС та ГМЛ і тяжкою тромбоцитопенією.
Загалом результати дослідження ASPIRE свідчать, що лікування пацієнтів із запущеними формами МДС та ГМЛ ельтромбопагом зменшує частоту клінічно значимих тромбоцитопенічних подій і кровотеч 3-4 ступеня тяжкості. Проте не відмічається гематологічного покращення чи зменшення потреби у призначенні трансфузій тромбоцитарної маси. Профіль безпеки лікування відповідав симптоматиці МДС чи ГМЛ з тяжкою тромбоцитопенією та поганим прогнозом. Разом із результатами попередніх клінічних досліджень ці дані свідчать про потенціал ельтромбопагу до збільшення кількості тромбоцитів і зменшення геморагічних ускладнень в осіб з МДС чи ГМЛ, які не отримують лікування, спрямованого на модифікацію перебігу захворювання.
Підготувала Олена Поступаленко
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 2 (63) 2020 р.




