16 червня, 2020
Монотерапія пазопанібом після попереднього лікування при метастатичній саркомі матки

Результати одноцентрового ретроспективного дослідження
Саркома матки належить до групи рідкісних гетерогенних сарком м’яких тканин (СМТ), характеризується агресивним перебігом і несприятливим прогнозом. Найпоширенішим гістологічним підтипом саркоми матки є лейоміосаркома (ЛМС) – 60% випадків, після якої ідуть ендометріальна стромальна саркома (ЕСС), недиференційована саркома та інші. При локалізованій пухлині, незалежно від її гістологічного підтипу, методом вибору є хірургічне лікування (резекція). Через те, що багато пацієнтів мають первинну метастатичну хворобу, а більше половини – рекурентне метастатичне захворювання після оперативного втручання, саркома матки вважається прогностично несприятливою. За наявності метастазів, як і при різних субтипах СМТ, традиційна цитотоксична терапія у лікуванні саркоми матки є недостатньо ефективною.
Пазопаніб – багатомішеневий інгібітор тирозинкінази з високою спорідненістю до рецепторів фактора росту ендотелію судин (Vascular Endothelial Growth Factor Receptors, VEGFRs) для перорального застосування. На основі результатів дослідження III фази пазопаніб вважається стандартним методом лікування пацієнтів з метастатичними, неадипоцитарними СМТ після неефективності традиційного курсу хіміотерапії. Про протипухлинну активність монотерапії пазопанібом також свідчать дані ретроспективного дослідження за участю хворих із СМТ з Кореї. Широке застосування пазопанібу для лікування СМТ зумовлено зручністю його прийому (перорально) та більш сприятливим профілем токсичності. Проте, коли йдеться про саркому матки – агресивну пухлину, що швидко прогресує, – популяція пацієнтів, залучена у клінічні дослідження, не завжди відображає усі клінічні випадки, з якими стикається у своїй практиці онколог. При виборі терапевтичної тактики у кожному конкретному випадку слід враховувати власний досвід лікування онкологічних хворих, потенційну токсичність обраної схеми, особливо у пацієнтів із симптомами або ознаками зниження ефективності терапії, активність хіміотерапевтичних агентів. Це стало підставою проведення одноцентрового ретроспективного дослідження, метою якого було вивчення ефективності монотерапії пазопанібом пацієнтів із саркомою матки, яким раніше проводили хіміотерапію.
Матеріали та методи
У ретроспективному дослідженні була проаналізована медична документація 35 дорослих пацієнток із саркомою матки, які приймали пазопаніб (Вотрієнт) у монотерапії. Слід зазначити, що досліджувана група приймала пазопаніб винятково на розсуд онколога, тому хворі, які брали участь у дослідженнях раніше, були виключені з цього аналізу. Критеріями виключення також були відсутність вимірюваних метастазів; випадки гістологічно підтверджених остеосаркоми, хондросаркоми, ліпосаркоми, саркоми Юїнга, примітивної нейроектодермальної пухлини чи інших пухлин, виключених із дослідження ІІІ фази; наявність інших злоякісних новоутворень протягом останніх 5 років, а також тяжкої супутньої патології, що унеможливлювала прийом стандартної дози пазопанібу (800 мг/день).
Усі пацієнти отримували пазопаніб у стартовій дозі 800 мг/добу перорально безперервно. Крім того, хворим призначали супровідну терапію (препарати крові, знеболювальні засоби). Перед застосуванням пазопанібу хворим був проведений повний комплекс обстеження (загальний і біохімічний аналіз крові, рентгенографія органів грудної клітки, комп’ютерна томографія всіх уражених ділянок). Через кожні 4 тижні здійснювали моніторинг стану хворого, оскільки введення пазопанібу повторювали через 4 тижні. Терапію припиняли у разі об’єктивно підтвердженого прогресування захворювання (згідно з критеріями відповіді солідних пухлин RECIST), тяжкої токсичності чи погіршення функції печінки, відмови пацієнта від терапії. Дозу препарату коригували на початку кожного нового циклу із врахуванням токсичності попереднього циклу.
Відповідь на терапію оцінювали через кожні 8 тижнів шляхом комп’ютерної томографії органів грудної клітки та черевної порожнини або тих самих методів, які застосовували перед призначенням пазопанібу. Усі побічні ефекти були зафіксовані та класифіковані відповідно до критеріїв Національного інституту раку США (CTCAE).
Первинною кінцевою точкою дослідження була частота відповіді (ЧВ), вторинні кінцеві точки включали виживаність без прогресування (ВБП), загальну виживаність (ЗВ) і профіль токсичності.
Результати
Характеристики пацієнтів, включених у дослідження, були такими. Середній вік пацієнтів становив 57 років (36-70 років). Приблизно у 77% хворих була гістологічно підтверджена ЛМС, меншою була кількість пацієнтів з недиференційованою плеоморфною саркомою, ЕСС та недиференційованою саркомою. Усі хворі отримували інтенсивну хіміотерапію, зокрема половина з них – 2 режими та більше. Через відсутність чітких стандартів хіміотерапії при СМТ попередні схеми включали етопозид + іфосфамід + цисплатин (n=15), доцетаксел + гемцитабін (n=14), монотерапію доксорубіцином (n=9), доксорубіцин + цисплатин (n=7), монотерапію іфосфамідом (n=6) та доксорубіцин + іфосфамід (n=4). Найчастішою локалізацією метастазів були легені, заочеревинний простір та очеревина. На момент підведення підсумків протягом середнього терміну спостереження 34 міс 39 пацієнтів мали прогресування захворювання, 22 з них померли.
Найчастішою причиною припинення терапії було прогресування захворювання (80%). Загалом терапію пазопанібом пацієнти переносили добре; найчастішими проявами токсичності були артеріальна гіпертензія, стоматит, втома та анемія 1 та 2 ступеня. У пацієнтів спостерігали тимчасове та зворотне підвищення функціональних показників печінки. Смертельних випадків, пов’язаних із лікуванням, протягом дослідження не було.
Об’єктивну відповідь на лікування пазопанібом отримано у 10 пацієнтів (ЧВ 29%; 95% довірчий інтервал – ДІ – 14-44%), включаючи одну повну відповідь. В 11 осіб відмічали стабільний перебіг хвороби. У пацієнтів з ЛМС відповідь на терапію пазопанібом досягалася швидше (9/27, 33%) порівняно з тими, хто мав гістологічно підтверджену недиференційовану плеоморфну саркому (1/3, 33%) та ЕСС (0%).
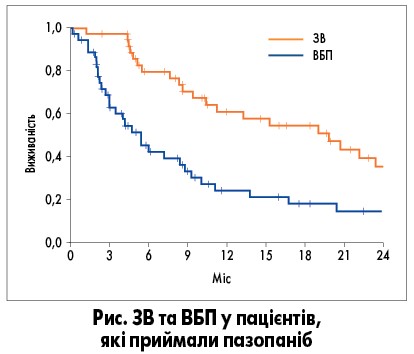 Медіани ВБП та ЗВ становили 5,8 міс (95% ДІ 3,6-8,1) та 20 міс (95% ДІ 11,6-28,4) відповідно (рис.). На відміну від ЧВ, ВБП (медіана 5,8 міс; 95% ДІ 2,5-9,1 vs 3,0 міс; 95% ДІ 0-7,6; p=0,680) та ЗВ (20,0 міс vs не досягнуто; p=0,404) були однаковими як у разі ЛМС, так і інших гістологічних субтипів саркоми.
Медіани ВБП та ЗВ становили 5,8 міс (95% ДІ 3,6-8,1) та 20 міс (95% ДІ 11,6-28,4) відповідно (рис.). На відміну від ЧВ, ВБП (медіана 5,8 міс; 95% ДІ 2,5-9,1 vs 3,0 міс; 95% ДІ 0-7,6; p=0,680) та ЗВ (20,0 міс vs не досягнуто; p=0,404) були однаковими як у разі ЛМС, так і інших гістологічних субтипів саркоми.
Обговорення
Це ретроспективне дослідження обмеженої групи пацієнтів показало, що так звана терапія порятунку пазопанібом у хворих із саркомою матки може бути активною незалежно від стану хворих, кількості метастатичних вогнищ та добре переноситься. ВБП та ЗВ становили 5,8 та 20,0 міс відповідно. Більшість проявів токсичності були тимчасовими та минущими. Тяжкі прояви негематологічної токсичності (стоматит, діарея) 3 та 4 ступеня виникли лише у 3-6% пацієнтів. Отримані результати порівнювали з даними проспективного клінічного дослідження та ретроспективного дослідження, проведеного в Кореї. Клінічна ефективність пазопанібу була більш значущою у пацієнтів з ЛМС (об’єктивна відповідь досягнута у 33% хворих) порівняно з іншими гістологічними субтипами саркоми (об’єктивна відповідь досягнута у 13% хворих).
Незважаючи на те що дослідження було ретроспективним і охоплювало обмежену категорію хворих, на основі отриманих даних можна зробити висновок, що пазопаніб не матиме значущого ефекту для пацієнтів з різними гістологічними субтипами СМТ, за винятком ЛМС.
СМТ матки – це рідкісна агресивна мезенхімальна пухлина, і клінічні рішення щодо ведення таких пацієнтів ухвалюються на основі характеристик новоутворення. За наявності метастатичних вогнищ ефективним є застосування доксорубіцину, іфосфаміду, таксанів, гемцитабіну та трабектедину. За даними ретроспективних досліджень ІІІ фази пероральне застосування пазопанібу передбачалося у випадку невдачі попередньо проведеної хіміотерапії у хворих з неадипоцитарними СМТ. Нещодавно опубліковані результати аналізу двох досліджень, які загалом включали 44 пацієнток з СМТ матки. Хоча автори дійшли висновку, що ефективність пазопанібу є зіставною у пацієнтів з СМТ матки та СМТ іншої локалізації, більшість (89%) мали підтверджену ЛМС. У цьому дослідженні виявлено, що такі гістологічні субтипи, як ЕСС та недиференційована саркома, не відповідають на лікування пазопанібом. Ці гістологічні підтипи, ймовірно, відрізняються між собою за клінічними та біологічними ознаками, проте досі невідомо які саме фактори зумовлюють неефективність пазопанібу.
Вибір найефективнішої схеми лікування хворих з метастатичними формами СМТ залишається темою для дискусій, тому при веденні таких пацієнтів слід враховувати їх індивідуальні особливості, загальний стан, наявні симптоми та гістологічний підтип саркоми. Початковий вибір хіміотерапевтичних агентів для моно- чи комбінованої терапії має ґрунтуватися на їх перевагах у кожному конкретному випадку. Нещодавно отримані попередні результати лікування метастатичних СМТ деякими таргетними засобами. Окрім пазопанібу, нове моноклональне антитіло, оларатумаб (блокатор PDGFR), у поєднанні з доксорубіцином покращує виживаність. Проте зазначене дослідження ще триває, і невідомо, скільки пацієнток із СМТ матки у нього включено.
Сильною стороною цього дослідження є те, у ньому взяли участь пацієнти, котрі отримувати пазопаніб в умовах клінічної практики. Тобто отримані результати є відображенням реалій, які можуть відрізнятися від даних рандомізованих контрольованих досліджень на відібраній групі пацієнтів. Обмеженням цього дослідження є ретроспективний характер, який може спричинити похибку при відборі хворих і втрату деяких даних. До слабких місць дослідження належали відсутність проведення загального рентгенологічного огляду, змінність методів візуалізаційної діагностики та різні інтервали між скануваннями. Однак ми вважаємо, що це краще відображає реальний досвід онкологів, які лікують пацієнтів із СМТ матки.
Kim H.-J. et al. Pazopanib monotherapy in the treatment of pretreated, metastatic uterine sarcoma: a single-center retrospective study. J Gynecol Oncol. 2018 Jan; 29(1): e3. https://doi.org/10.3802/jgo.2018.29.e3.
Переклала з англ. Ілона Цюпа
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 2 (63) 2020 р.




