9 жовтня, 2020
Клінічні рекомендації Американської колегії гастроентерології: хронічний панкреатит
Історично хронічний панкреатит (ХП) визначали як незворотний запальний стан підшлункової залози (ПЗ), що спричиняє екзо- й ендокринну дисфункцію різного ступеня вираженості.
Проте нещодавно парадигма змінилася й акцент у діагностиці змістився на раннє виявлення патологічного процесу, що лежить в основі цього захворювання, а в лікуванні – на зміну природного перебігу хвороби та мінімізацію несприятливих наслідків.
Нині найбільш визнаним є таке визначення: ХП – це патологічний фіброзно-запальний синдром у ПЗ в осіб із різними факторами ризику (генетичними, з боку довкілля тощо), в яких розвивається стійка патологічна відповідь на ураження паренхіми залози чи її перенавантаження. Найпоширенішим симптомом ХП є біль у животі; частота розвитку інших симптомів (екзокринна недостатність, цукровий діабет – ЦД) є дуже варіабельною. ХП зазвичай спричиняють токсичні впливи на кшталт уживання алкоголю чи тютюнопаління, генетичні поліморфізми та рецидивні напади гострого панкреатиту (ГП), хоча в багатьох пацієнтів анамнез останнього відсутній. Діагноз зазвичай установлюється на основі візуалізаційних досліджень (томографії), а ендоскопічне ультразвукове дослідження (ЕУЗД) та показники функції ПЗ відіграють вторинну роль. Єдиним способом лікування ХП є тотальна панкреатектомія, хоча труднощі у відборі пацієнтів і властиві цьому втручанню ускладнення роблять його досить непривабливим варіантом. У цих рекомендаціях представлено практичний підхід до діагностики та лікування ХП.
Нещодавні вдосконалення продовжують змінювати розуміння ХП, зокрема підходи до визначення, діагностики й лікування. До 2016 р. захворювання визначали на основі традиційного клініко-патологічного підходу, прив’язуючи типові ознаки та симптоми до визначеного патологічного стану, тобто хронічного запалення та незворотного фіброзу без інфекції. Головною проблемою в установленні діагнозу було отримання тканини ПЗ для біопсії – золотого стандарту патологічної діагностики, особливо за умови високого співвідношення ризик/користь, пов’язаного з виконанням дослідження. Три консенсусні конференції в м. Марсель (Франція), проведені в 1963-1989 рр., визначали ХП на основі клінічних, функціональних і гістологічних даних [3-5]. У 1984 р. було запропоновано т. зв. кембриджське визначення, що представило оцінку даних ендоскопічної ретроградної холангіопанкреатографії як сурогат й альтернативу біопсії [6]. Відповідно до цього визначення, ХП – це тривале запальне захворювання ПЗ, що характеризується незворотними морфологічними змінами й зазвичай спричиняє біль та/або стійку втрату функції. Кембриджське визначення виступало підґрунтям важливості візуалізаційних методів діагностики ХП та більшості консенсусних документів і клінічних рекомендацій протягом подальших трьох декад. Однак традиційне клініко-патологічне визначення та підходи до досліджень, які ґрунтувалися на постулатах Коха, не змогли надати пояснення складних причин хвороби й особливостей лікування окремих пацієнтів, а також дати можливість змінити природний перебіг ХП [7, 8]. Нові технології та наукові відкриття протягом 1984-2019 рр. підтвердили, що сучасні дані не можна інтегрувати в стару клініко-патологічну парадигму, бо ранній ХП – стадію, на якій таргетне лікування є найефективнішим, – не може бути діагностований відповідно до клініко-патологічного визначення, оскільки останнє потребує наявності незворотних морфологічних змін [9].
Традиційна клініко-патологічна система, що визначає синдром ХП як незворотне пошкодження ПЗ, може призвести до років затримки між появою симптомів і встановленням діагнозу й зазвичай неспроможна виявити вихідну етіологію процесу, передбачити перебіг хвороби та виступити підґрунтям для лікувально-профілактичних втручань. Саме тому 2016 р. було створено нове механістичне визначення ХП, згодом схвалене провідними профільними товариствами [15, 16]. Це визначення вказує, що характеристиками термінальних стадій хвороби є атрофія ПЗ, її фіброз, больовий синдром, стриктури та деформації протоків, кальцифікація, екзо- й ендокринна дисфункції залози, проте також визначає механізм розвитку захворювання.
Важливо розрізняти дисфункцію ПЗ, споріднені з панкреатитом захворювання (СПЗ) і хвороби ПЗ. Прикладами дисфункції ПЗ є генетична мутація в локусі гена CFTR, яка спричиняє варіації в експресії чи сплайсингу РНК, або зміни в послідовності амінокислот, які призводять до дефектів у процесингу, транспортуванні РНК і відкриванні іонних каналів. Дисфункція може бути компенсована адаптивними механізмами. Прикладом СПЗ є білкова дисфункція, що запобігає нормальній відповіді клітин панкреатичної протоки за умови сильної стимуляції чи стресу цих клітин. У разі перевищення порогу компенсаторних можливостей продукуються сигнали, здатні спричиняти ознаки та симптоми хвороб, зокрема напад ГП [17]. Своєю чергою, хвороби ПЗ – це стани, що асоціюються з такими патологіями, як ГП, рецидивний ГП (РГП), ХП та різні комплексні синдроми, що вражають ПЗ, наприклад муковісцидоз.
Існує мало досліджень, присвячених ХП, у яких застосовували би нове визначення, тому метою цих рекомендацій є систематичний огляд тематичної літератури та створення чітких керівних вказівок для лікарів.
Діагностика ХП
Рекомендація 1. Як першу лінію діагностики ХП рекомендовано застосовувати комп’ютерну (КТ) або магнітно-резонансну (МРТ) томографію. У зв’язку з інвазивністю та низькою специфічністю ЕУЗД має застосовуватися лише тоді, коли після проведення КТ/МРТ діагноз остаточно не з’ясовано.
Доказова база. Діагноз ХП часто встановлюється на основі низки параметрів, у т. ч. ризику хвороби, впливу провокувальних факторів, результатів візуалізаційних досліджень, визначення функції ПЗ. Імовірно, найціннішими діагностичними тестами при ХП є ретельний збір анамнезу та фізикальне обстеження. Збір анамнезу (оцінка факторів ризику, сімейний анамнез, природа та характер болю, наявність попередніх епізодів ГП, стеатореї та/або симптомів вітамінодефіцитів) є надзвичайно важливим. Однак у пацієнтів із клінічними симптомами запальних розладів із боку ПЗ (епізоди ГП у анамнезі, характерний біль та/або мальдигестія) та/або факторами ризику першим обстеженням для встановлення діагнозу ХП має бути КТ або МРТ. Систематичний огляд і метааналіз 43 досліджень за участю 3460 пацієнтів із підозрою на ХП виявили, що чутливість ЕУЗД, МРТ, КТ становить відповідно 81, 78, 75% і достовірно не відрізняється. Специфічність також виявилася зіставною [19]. Для встановлення діагнозу ХП запропоновано низку інших візуалізаційних методів, у т. ч. ЕУЗД із контрастом, ендоскопічну ретроградну холецистопанкреатографію (ЕРХПГ), черезшкірне УЗД, еластографію ПЗ [6, 21-24]. Однак необхідні для включення цих методів у першу лінію обстежень рандомізовані контрольовані дослідження (РКД) високої якості наразі відсутні.
Практичний клінічний підхід. Ключовим компонентом визначення ХП є виявлення типових морфологічних змін ПЗ, тому візуалізація виступає сурогатом гістологічного дослідження. За відсутності однозначно узгодженого золотого стандарту діагностики ХП та складності отримання високоякісного й репрезентативного гістологічного зразка, КТ/МРТ є зручними тестами для клініцистів і мають застосовуватись як первинне обстеження для встановлення діагнозу. ЕУЗД має використовуватись, якщо після проведення зрізового візуалізаційного дослідження діагноз залишається сумнівним або якщо існує підозра на захворювання з мінімальними змінами (ХП без доказів фіброзування), що не візуалізується на КТ/МРТ. ХП залишається діагнозом, який інтегрує та збалансовує клінічний сценарій, наявність факторів ризику та виключення інших хвороб у ході диференційної діагностики.
Рекомендація 2. Якщо ХП не підтверджений після КТ/МРТ або ЕУЗД, а клінічна підозра на зазначений діагноз залишається високою, пропонується виконувати магнітно-резонансну холангіопанкреатографію із секретиновим підсиленням (МРХПГ‑с).
Доказова база. МРХПГ‑с забезпечує хорошу візуалізацію головних і бічних проток залози за рахунок стимуляції вивільнення бікарбонатів із протокових клітин. Цей метод також дає змогу визначити ступінь надходження панкреатичного соку до дванадцятипалої кишки, що може корелювати з тяжкістю ХП та допомогти у визначенні стану екзокринної функції [25-27]. Зважаючи на вартість, МРХПГ‑с має застосовуватися лише тоді, коли діагноз не підтверджено за допомогою методів першої лінії.
Практичний клінічний підхід. Якщо КТ/МРТ та ЕУЗД не змогли виявити ознак ХП, із метою виявлення незначних змін проток ПЗ (розширення бічних відгалужень, ектазії) може застосовуватися МРХПГ‑с. Візуалізаційні дослідження, що визначають структуру залози, є найчутливішими до змін, спричинених фіброзом (розтягнення проток, кальцифікація). Проте не слід установлювати діагноз ХП виключно на основі результатів МРХПГ‑с або інших візуалізаційних досліджень.
Ключова концепція 1. Визначення функції ПЗ є важливим методом діагностики екзокринної недостатності ПЗ (ЕНПЗ), однак її роль у встановленні діагнозу ХП є лише допоміжною.
 Доказова база. Погляди на застосування визначення функції ПЗ для діагностики ХП є суперечливими. Такі обстеження використовуються для виявлення ЕНПЗ, а оскільки в більшості пацієнтів із ХП клінічно значуща ЕНПЗ відсутня, то чутливість цього методу для встановлення діагнозу ХП є низькою. Це частково зумовлено великими резервними можливостями ПЗ, унаслідок чого лише значна втрата функції (в межах 90%) призводить до появи клінічних симптомів (стеаторея, азоторея, вітамінодефіцити) [31]. РКД, систематичні огляди та метааналізи з цього питання відсутні, тому останнє може виступати лише допоміжним методом обстеження [22, 32-34].
Доказова база. Погляди на застосування визначення функції ПЗ для діагностики ХП є суперечливими. Такі обстеження використовуються для виявлення ЕНПЗ, а оскільки в більшості пацієнтів із ХП клінічно значуща ЕНПЗ відсутня, то чутливість цього методу для встановлення діагнозу ХП є низькою. Це частково зумовлено великими резервними можливостями ПЗ, унаслідок чого лише значна втрата функції (в межах 90%) призводить до появи клінічних симптомів (стеаторея, азоторея, вітамінодефіцити) [31]. РКД, систематичні огляди та метааналізи з цього питання відсутні, тому останнє може виступати лише допоміжним методом обстеження [22, 32-34].
Методи визначення функції ПЗ поділяють на прямі та непрямі. Вибір методу залежить від доступності, досвіду використання, вартості тощо. Хоча золотим стандартом діагностики повної недостатності ПЗ може вважатися 72-годинне вимірювання жиру в калі, в більшості досліджень використовується виявлення клінічної стеатореї чи зниженого рівня еластази калу. Жоден із цих методів не є високоточним, тому зазначені підходи, ймовірно, недооцінюють поширеність клінічно значущої мальдигестії.
Найчастіше застосовується визначення фекальної еластази. Недоліком методу є те, що його точність для діагностики ЕНПЗ залежить від обраного порогового значення. Своєю чергою, трипсин та/або трипсиноген сироватки вже не використовуються, оскільки повідомлено про їх підвищення при непанкреатичному болю та погану кореляцію з результатами візуалізаційних досліджень.
Практичний клінічний підхід. Наявність ЕНПЗ не є незалежним свідченням ХП, оскільки при низці станів секреція бікарбонатів знижена з народження, проте не призводить до втрати тканини ПЗ та її морфологічних змін. Тому виявлення ЕНПЗ має застосовуватись як додаткове обстеження для пацієнтів, у яких раніше не було діагностовано ХП.
Рекомендація 3. Якщо клінічні та функціональні докази ХП є потужними, але візуалізаційні дослідження не дають можливості зробити остаточний висновок, рекомендовано застосовувати гістологічне дослідження як золотий стандарт діагностики ХП у пацієнтів високого ризику.
Доказова база. Зважаючи на значне поширення тонкоголкової біопсії (ТГБ) під контролем ЕУЗД, можливості отримання тканини ПЗ для гістологічного аналізу стали безпечнішими та простішими з технічної точки зору [36, 37]. Однак обмеженнями гістологічної оцінки є можливе отримання недіагностичного зразка, вогнищева природа запальних змін, суб’єктивна оцінка гістологічної картини. РКД, систематичні огляди чи метааналізи, що розглядають гістологічну оцінку як золотий стандарт діагностики ХП, відсутні. Утім, гістологічне дослідження може виступати золотим стандартом, особливо для виключення ХП. Проведення гістологічної оцінки слід розглядати лише в пацієнтів високого ризику, якщо клінічні, функціональні та візуалізаційні обстеження не дали змогу встановити клініко-патологічний діагноз, а пацієнт дав свідому інформовану згоду.
Практичний клінічний підхід. Хоча гістологічне дослідження часто використовується для виключення ХП, чутливість методу для встановлення діагнозу є низькою.
Етіологія ХП
Ключова концепція 2. У пацієнтів із клінічними ознаками ХП слід ретельно визначати всі фактори ризику. Це надає інформацію щодо механізмів, які лежать в основі хвороби, дає змогу виявити модифіковані фактори ризику, ідентифікувати потенційні мішені для терапевтичного втручання й отримати значущі для прогнозу дані.
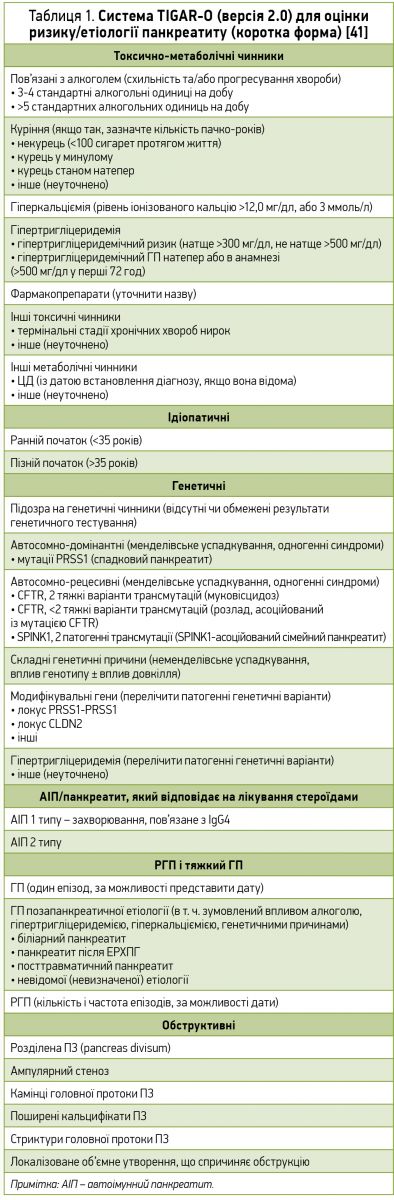
 Доказова база. РКД, систематичні огляди та метааналізи, що фокусуються на питанні порядку обстеження з метою визначення етіології ХП, відсутні [40]. Для допомоги в категоризації етіології ХП було створено систему TIGAR-O [5, 41]. Цей акронім включає T (токсично-метаболічні причини), I (ідіопатичні), G (генетичні), A (автоімунні), R (рецидивний гострий або тяжкий панкреатит) та O (обструкція) (табл. 1). Подібною мультифакторною класифікаційною системою є M-ANNHEIM. Ця абревіатура включає M – множинні фактори ризику, A – вживання алкоголю, NN – уживання нікотину та харчові фактори, H – спадкові чинники, E – чинники з боку еферентних проток, I – імунологічні фактори, M – інші, в т. ч. рідкісні метаболічні фактори [22]. Система M-ANNHEIM надає діагностичні критерії щодо етіології, стадії та тяжкості захворювання (табл. 2).
Доказова база. РКД, систематичні огляди та метааналізи, що фокусуються на питанні порядку обстеження з метою визначення етіології ХП, відсутні [40]. Для допомоги в категоризації етіології ХП було створено систему TIGAR-O [5, 41]. Цей акронім включає T (токсично-метаболічні причини), I (ідіопатичні), G (генетичні), A (автоімунні), R (рецидивний гострий або тяжкий панкреатит) та O (обструкція) (табл. 1). Подібною мультифакторною класифікаційною системою є M-ANNHEIM. Ця абревіатура включає M – множинні фактори ризику, A – вживання алкоголю, NN – уживання нікотину та харчові фактори, H – спадкові чинники, E – чинники з боку еферентних проток, I – імунологічні фактори, M – інші, в т. ч. рідкісні метаболічні фактори [22]. Система M-ANNHEIM надає діагностичні критерії щодо етіології, стадії та тяжкості захворювання (табл. 2).
Практичний клінічний підхід. Первинний підхід до оцінки стану пацієнтів із підозрою на хвороби ПЗ та ХП передбачає ретельний збір анамнезу, фізикальне обстеження та виявлення біомаркерів. Анамнез має включати дати та кількість попередніх епізодів ГП, дату початку ЦД (за його наявності), мальдигестію, наявність зниження маси тіла, стан кісткової системи (наявність переломів) і нирок, захворювання органів, асоційовані з муковісцидозом (хвороби легень, синусити, неплідність у чоловіків). Сімейний анамнез має охоплювати родичів щонайменше до 3 ступеня спорідненості та стосуватися таких хвороб, як панкреатит, муковісцидоз, ЦД та рак ПЗ. Представлений у класифікації TIGAR-O список етіологій є керівною вказівкою щодо провідних факторів ризику та біомаркерів ХП. Висновок про стадію захворювання можна зробити також на основі визначення сироваткового рівня жиророзчинних вітамінів. Візуалізаційні дослідження є доцільними у визначенні обструктивної етіології захворювання (анатомічні мальформації, кальцифікати, пухлини тощо). Якщо етіологія нез’ясована, пацієнт молодше 35 років або має сімейний анамнез хвороб ХП, захворювання зберігається після лікувального втручання, показано генетичне тестування. Необхідно також провести диференційну діагностику з автоімунним запаленням ПЗ, запаленням і фіброзом острівцевих клітин унаслідок тривалого ЦД, хворобами нирок зі вторинними змінами ПЗ, впливом імуносупресантів (наприклад, циклоспорину), віковою атрофією чи фіброзом, внутрішньопротоковими папілярними новоутвореннями, цистаденомою острівцевих клітин, десмопластичною відповіддю на новоутворення ПЗ, запальним впливом об’ємного утворення, що перекриває протоки, тощо [9].
Рекомендація 4. Пацієнтам із клінічними доказами СПЗ або ймовірним ХП, у яких етіологія процесу невідома, особливо особам молодого віку, рекомендовано генетичне тестування.
Доказова база. За минулі дві декади виявлено кілька генів, асоційованих із ХП. Первинною метою генетичного тестування є виявлення розладів, які лежать в основі панкреатиту, з метою допомоги в прийнятті медичних рішень і профілактиці розвитку незворотного ХП [2]. Наприклад, у ході генетичного дослідження можна виявити певні варіанти гена CFTR, які супроводжуються розладами роботи ПЗ або муковісцидозом, що може проявлятись як РГП або ХП. Генетичне тестування дає важливу інформацію щодо етіології СПЗ на ранніх стадіях, оскільки здатне виявити дисфункціональні гени, типи клітин і механізми. Ця інформація може стати підґрунтям для підтверджувальних досліджень (наприклад, визначення хлоридів поту) та встановлення високої чи низької ймовірності захворювання [2]. Хоча визначення етіології СПЗ не завжди дає можливість одразу призначати спеціалізоване лікування, воно може припинити виснажливі інвазивні дороговартісні обстеження. Визначення генетичної етіології також допомагає в прийнятті рішення щодо радикального лікування, наприклад тотальної панкреатектомії з автотрансплантацією острівців ПЗ (ТПАО). Слід зауважити, що генетичне тестування має обмежену цінність для пацієнтів із термінальними стадіями ХП, адже до цього часу запальний процес уже незворотно пошкодив залозу. Винятком є виявлення генів, асоційованих зі спадковими захворюваннями, що допомагає прийняти клінічне рішення стосовно інших членів сім’ї чи дати пацієнту можливість узяти участь у клінічних дослідженнях.
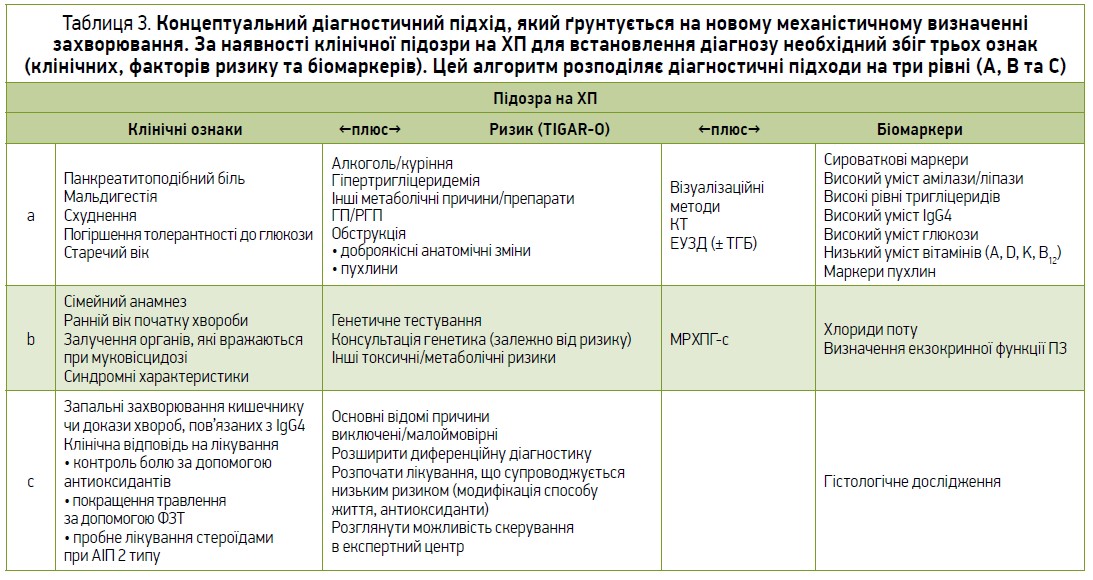
У таблиці 3 представлено діагностичну концепцію в контексті нового механістичного визначення ХП.
Практичний клінічний підхід. Виявлення мутацій зародкової лінії не дає можливості встановити діагноз ХП, але забезпечує виявлення популяції пацієнтів із високою поширеністю СПЗ та ХП, збільшуючи точність менш чутливих або специфічних біомаркерів, а також установити дисфункціональний механізм, який лежить в основі патологічного процесу. Це важливо для пацієнтів будь-якого віку, оскільки таргетна терапія (наприклад, CFTR-модулювальні препарати) може безпосередньо впливати на механізм розвитку хвороби. Щонайменше пацієнтам з ідіопатичним ХП варто здійснити аналіз мутацій генів PRSS1, SPINK1, CFTR і CTRC.
Природний перебіг і клінічні симптоми ХП
Ключова концепція 3. Для прогнозування прогресування ХП необхідно виявити захворювання, що лежать в основі запалення ПЗ.
Доказова база. Головними клінічними проявами ХП є виснажливий біль у животі, дефіцит жиророзчинних вітамінів (і пов’язані з ним стани на кшталт остеопорозу), ризик злоякісних утворень ПЗ та розвиток ендокринної недостатності (ЦД). Дослідження підтверджують, що близько 60% випадків ХП розвиваються з ГП та РГП, і навпаки: близько 10% випадків ГП та 30% випадків РГП прогресують до ХП. Етіологія процесу відіграє важливу роль, оскільки прогресування ГП до ХП у разі алкогольної етіології відбувається вдвічі швидше, ніж за умови генетичних чи ідіопатичних причин і вп’ятеро швидше, ніж при біліарному ГП [42].
Дефіцит жиророзчинних вітамінів спостерігається в меншості пацієнтів із ХП. Поширеність ЕНПЗ у великих дослідженнях природного перебігу ХП становить 40-75% [46, 47]. Ризик є найбільшим при алкогольному та фіброзно-кальцифікувальному панкреатиті.
Практичний клінічний підхід. Загалом етіологія ХП не визначає швидкості прогресування, появи ЕНПЗ, хронічного сильного болю чи ризику злоякісних новоутворень. Однак у разі певних видів ХП етіологія визначає прогноз і симптоми.
Ключова концепція 4. Розвиток ЦД при ХП є, найімовірніше, пов’язаним із тривалістю захворювання, хоча інші етіологічні чинники (індекс маси тіла, куріння) також можуть впливати на ризик.
Доказова база. Ризик ендокринної недостатності ПЗ – ЦД типу 3c – не є наслідком певної специфічної етіології процесу [50]. Найвагомішим етіологічним чинником є тривалість хвороби; додаткову роль відіграє куріння [10, 51].
Практичний клінічний підхід. Хоча в пацієнтів з ожирінням імовірність ЦД 2 типу вища, в пацієнтів із вираженим ХП частіше виявляється низький індекс маси тіла та ЦД типу 3с унаслідок втрати острівцевих клітин. Поява ЦД разом зі втратою ваги є потенційним показником аденокарциноми проток ПЗ.
Рекомендація 5. Пацієнтам із наявним ХП рекомендовано припинити вживання алкоголю.
Доказова база. РКД, систематичні огляди та метааналізи, присвячені вивченню впливу припинення вживання алкоголю на природний перебіг ХП, відсутні. Утім, наявні окремі повідомлення про те, що припинення вживання алкоголю зменшує вираженість болю при ХП [52, 53].
Практичний клінічний підхід. Хоча доказова база є обмеженою, суворе уникнення алкоголю має бути наріжним каменем будь-якого лікування ХП.
Рекомендація 6. Пацієнтам із ХП рекомендовано припинити куріння.
Доказова база. Тютюнопаління вважають фактором ризику ХП, хоча з цього питання наявні лише одноцентрові дослідження [57-59]. Існують окремі повідомлення про зменшення прогресування кальцифікації ПЗ у разі припинення куріння відразу після встановлення діагнозу ХП [60].
Практичний клінічний підхід. Хоча доказова база є обмеженою, суворе припинення тютюнопаління має бути наріжним каменем лікування ХП.
Ключова концепція 5. Нині немає доказів переваг скринінгових обстежень для виявлення злоякісних новоутворень у пацієнтів із ХП.
Доказова база. Стосовно цього питання надзвичайно мало якісних доказів [48].
Практичний клінічний підхід. Наразі немає визначених переваг скринінгу пацієнтів із ХП з метою виявлення аденокарциноми проток ПЗ. Це пов’язано з інвазивністю та дороговартісністю дослідження, складністю скринінгу у зв’язку зі структурними змінами ПЗ при ХП та неможливістю змінити природний перебіг захворювання навіть за умови виявлення пухлини на ранній стадії.
Лікування болю при ХП
Ключова концепція 6. Слід з обережністю розглядати можливість проведення елективних інтервенційних втручань у пацієнтів, які активно вживають алкоголь. Випадки пацієнтів, які потребують невідкладних процедур із приводу ускладнень ХП, варто розглядати окремо.
Доказова база. РКД, систематичні огляди та метааналізи з цього питання відсутні. З медичної точки зору є суперечливим питання, чи доцільно проводити агресивні ендоскопічні або хірургічні втручання пацієнтам, які активно шкодять собі шляхом подальшого вживання алкоголю. Із соціальної точки зору такі хворі також потребують допомоги й мають бути заохочені до припинення зловживання. Ургентні втручання мають проводитися й у пацієнтів, які продовжують активно вживати алкоголь.
Практичний клінічний підхід. Загалом елективні інтервенційні втручання в пацієнтів, які активно вживають алкоголь, мають проводитися з обережністю. Ургентні втручання необхідно виконувати за необхідності. У пацієнтів, які намагаються зменшити чи припинити вживання алкоголю, проте епізодично все одно вживають, слід розглядати кожен випадок окремо.
Рекомендація 7. У пацієнтів з обструктивним ХП для довготривалого усунення болю рекомендовано віддавати перевагу хірургічному втручанню над ендоскопічним, якщо ендоскопічні підходи до дренування ПЗ першої лінії виявилися невдалими.
Доказова база. У пацієнтів із ХП часто має місце больовий синдром унаслідок обструкції проток ПЗ. Ендоскопічні декомпресійні процедури включають ЕРХПГ зі сфінктеротомією, видалення каменів, дилатацію стриктури та стентування протоки ПЗ. Деякі декомпресійні операції також передбачають часткову панкреатектомію. Якісна доказова база обмежена. У дослідженні Cahen і співавт. [61] було виявлено, що хірургічне дренування протоки ПЗ супроводжувалося меншим больовим синдромом і кращими показниками загального здоров’я, ніж ендоскопічне. Через 24 міс спостереження повного чи часткового усунення болю було досягнуто в 32% пацієнтів групи ендоскопії та 75% осіб групи хірургічного втручання.
Практичний клінічний підхід. Хоча показано, що хірургічна декомпресія протоки ПЗ забезпечує краще усунення болю в довготривалій перспективі, ніж ендоскопічна, вона рідко виступає лікуванням першої лінії та зазвичай застосовується за невдачі ендоскопічного підходу. У пацієнтів із симптоматичною обструкцією протоки ПЗ доцільно спочатку проводити ендоскопічне дренування за допомогою ЕРХПГ та/або ЕУЗД, залишаючи хірургічні втручання на випадок невдач ендоскопії чи для пацієнтів, які не бажають проходити множинні ендоскопічні втручання.
Рекомендація 8. При ХП із больовим синдромом рекомендовано розглянути застосування антиоксидантної терапії, хоча її переваги в знеболенні досить обмежені.
Доказова база. Точний механізм зменшення болю при застосуванні антиоксидантів невідомий; більшість теорій схиляються до того, що ці засоби чинять протизапальну дію, зменшуючи окисний стрес. Рандомізоване дослідження (n=2009), в якому порівнювали ефект суміші п’яти антиоксидантних засобів (селен, аскорбінова кислота, β-каротин, α-токоферол, метіонін) і плацебо, виявило: через 6 міс пацієнти групи антиоксидантів мали достовірно меншу кількість днів із больовим синдромом на місяць і меншу потребу в аналгетиках [67]. Інше подвійне сліпе рандомізоване дослідження антиоксидантної терапії (дріжджі з селеном, α-токоферол, аскорбінова кислота, метіонін) у пацієнтів з алкогольним ХП не виявило переваг лікування над плацебо [68]. У двох метааналізах було показано, що антиоксиданти знижували вираженість болю, проте ефект був незначним [70, 71].
Практичний клінічний підхід. Хоча дані щодо антиоксидантної терапії при ХП обмежені, а їх наукова правдоподібність під питанням, ці препарати є безпечними та здатні зменшувати біль, тому можна розглянути їх застосування, особливо на ранніх етапах захворювання. У клінічних дослідженнях переважно застосовувалися такі антиоксиданти, як селен, аскорбінова кислота, β-каротин і метіонін. Визначити оптимальні засіб і дозу наразі неможливо.
Ключова концепція 7. Опіати можуть бути розглянуті для лікування больового синдрому при ХП лише в тих пацієнтів, у яких усі інші доцільні терапевтичні можливості зазнали невдачі.
Доказова база. Аргументами на користь лікування опіоїдами є їхня ефективність і невисока вартість, аргументами проти – ризик звикання та зловживання, розвиток толерантності, побічні ефекти (наприклад, закрепи). РКД, систематичні огляди та метааналізи з цього питання відсутні.
Практичний клінічний підхід. З огляду на ризик звикання, зловживання та формування толерантності, слід уникати опіатів у лікуванні болю при ХП. Призначення опіатів виправдане лише за рефрактерного болю.
Рекомендація 9. Застосування ферментів ПЗ із метою зменшення болю при ХП не рекомендовано.
Доказова база. Пацієнти з ХП часто отримують ферменти ПЗ із метою усунення симптоматичної ЕНПЗ. Хоча сприятливі ефекти цього лікування не викликають сумнівів, роль ферментів в усуненні болю не така зрозуміла. Кокранівський огляд 10 рандомізованих досліджень (2009) не виявив однозначного результату щодо ефективності ферментів у разі больового синдрому внаслідок ХП [74].
Практичний клінічний підхід. Загалом ферментна терапія не має застосовуватись як форма контролю болю при ХП. Однак пацієнти з ЕНПЗ зазвичай відзначають зменшення спазмів у животі внаслідок ферментозамісної терапії (ФЗТ). Якщо хворі відзначають зменшення болю на тлі ФЗТ, доцільно її продовжувати, особливо зважаючи на низький ризик застосування ферментних засобів і відсутність альтернативних аналгетиків.
Рекомендація 10. Для лікування ХП рекомендовано розглянути можливість застосування блокади сонячного сплетіння.
Доказова база. Блокада сонячного сплетіння передбачає ін’єкційне введення відповідних ліків у ділянку гангліїв сонячного сплетіння та навколо них. Найчастіше застосовується комбінація місцевого анестетика та стероїда, наприклад бупівакаїн + тріамцинолон [77]. Перевагою методу є те, що одна процедура здатна зменшити біль на 3-6 міс, знизивши або усунувши потребу в пероральних аналгетиках, а також те, що втручання проводиться швидко й за потреби може бути повторене. Недоліками є ризики самої процедури (кровотеча, алергічна реакція тощо) та ризики необхідної при ній седації.
Практичний клінічний підхід. Блокада сонячного сплетіння є методом низького ризику, що дає змогу зменшити рефрактерний біль у деяких пацієнтів із ХП без застосування опіоїдів. Блокаду можна повторювати за потреби, зазвичай із частотою 1 раз на 3 міс.
Ключова концепція 8. ТПАО слід залишити для вибраних пацієнтів із рефрактерним хронічним болем, у яких інші методи контролю симптомів зазнали невдачі.
Доказова база. Існує потреба в проведенні подальших досліджень із цього питання. Пацієнти, для котрих розглядається можливість проведення ТПАО, мають пройти мультидисциплінарне обстеження у вузькоспеціалізованому експертному центрі зі з’ясуванням ризику ЦД типу 3с та потенційних дисмоторних розладів роботи кишечнику.
Практичний клінічний підхід. Застосування ТПАО слід розглядати лише в тих пацієнтів, у яких інші методи лікування зазнали невдачі.
Ключова концепція 9. Експериментальні методи терапії мають застосовуватися лише в клінічних дослідженнях.
Доказова база. З метою лікування рефрактерного болю при ХП було випробувано низку різних експериментальних методів (стимуляція нервів спинного мозку, трансмагнітна стимуляція мозку, безпосередня променева терапія ложа ПЗ). Дані щодо ефективності цих методів обмежені окремими серіями випадків і ретроспективними когортними дослідженнями, тому рекомендовано обмежити їх застосування межами клінічних досліджень.
Практичний клінічний підхід. Усіх пацієнтів, у яких терапевтичні та хірургічні підходи зазнали невдачі, варто скеровувати до експертного центру з можливістю проведення експериментальної терапії.
Лікування ЕНПЗ при ХП
Рекомендація 11. Пацієнтам із ХП та ЕНПЗ рекомендована ФЗТ із метою зменшення ускладнень мальнутриції.
Доказова база. Переваги ФЗТ включають зменшення вираженості симптомів, набір ваги, покращення всмоктування жирів, жиророзчинних вітамінів і слідових елементів, зменшення наслідків мальдигестії (наприклад, ризику переломів при остеопорозі), покращення якості життя, зменшення смертності. У більшості рандомізованих досліджень ФЗТ показником ефективності виступав коефіцієнт абсорбції жирів (КАЖ), виміряний протягом 72 год. Нормальний КАЖ становить >93%, тобто з калом має втрачатися лише близько 7% харчових жирів.
Застосуванню ФЗТ у разі ХП присвячено 17 РКД [82-98]. Щоденне дозування варіювало від <50 тис. до >700 тис. од. ліпази. Деякі дослідження порівнювали різні препарати чи різні дозування, інші – ФЗТ із плацебо. Час призначення ФЗТ відрізнявся (до та під час прийому їжі). У деяких дослідженнях на додачу до ФЗТ призначався H2-інгібітор або інгібітор протонної помпи. Проведений у 2009 р. Кокранівський огляд оцінював ефективність ФЗТ у зниженні болю, зменшенні стеатореї та покращенні якості життя [74]. Аналіз 10 РКД (n=361) не виявив достовірного зменшення болю та зниження використання аналгетиків. Ферменти достовірно зменшували вміст жиру в калі та продемонстрували статистично незначущу тенденцію до збільшення маси тіла й покращення якості життя. У недавнішому метааналізі було проаналізовано 17 досліджень [99]. ФЗТ достовірно покращувала КАЖ порівняно з вихідним значенням (83,7±6,0 на тлі ФЗТ; 63,1±15,0 – вихідний рівень; р<0,00001). Екскреція азоту з калом і вага калових мас також зменшилися (р<0,001). У деяких дослідженнях ФЗТ зменшувала флатуленцію та покращувала консистенцію калових мас. У семи дослідженнях, які порівнювали ФЗТ із плацебо, ФЗТ підвищувала КАЖ до 83,26±5,5 порівняно з 67,46±7,0 для плацебо (р<0,0001). Порівняння високо- та низькодозової ФЗТ виявило дещо більший КАЖ на тлі дозування >60 тис. од. ліпази на добу, але різниця виявилася недостовірною. Отже, ФЗТ покращує всмоктування жирів і білків порівняно з вихідним рівнем або плацебо. Дослідження з тривалим періодом спостереження встановили достовірне покращення в параметрах нутритивного статусу, вазі, симптоматиці та якості життя [100-102].
Практичний клінічний підхід. ЕНПЗ слід запідозрити в осіб із тривалим ХП або в пацієнтів із ХП та схудненням, мальнутрицією, проносами, стеатореєю, остеопорозом чи остеопенією. Для встановлення цього діагнозу часто достатньо клінічної картини без формального визначення вмісту жирів у калі. Найдоступнішим діагностичним тестом є визначення еластази калу. Лікування має включати ФЗТ в адекватному дозуванні (щонайменше 40-50 тис. од. ліпази на кожен прийом їжі) під час їди. Доцільно визначити рівень жиророзчинних вітамінів і щільність кісткової тканини на початку лікування та надалі з періодичними інтервалами.
Ключова концепція 10. Стан пацієнтів із ХП слід періодично оцінювати на предмет мальнутриції, в т. ч. виявляти остеопороз і дефіцит жиророзчинних вітамінів.
Доказова база. Одноцентрові дослідження виявили в пацієнтів із ХП підвищений ризик розвитку остеопорозу та, відповідно, переломів [104-106]. Хворі на ХП належать до групи ризику дефіциту жиророзчинних вітамінів, а також цинку та магнію незалежно від доведеної наявності ЕНПЗ [108, 109]. Ступінь дефіциту зазвичай залежить від ступеня ЕНПЗ.
Практичний клінічний підхід. Хоча з цього питання існує мало якісних доказів, у пацієнтів із ХП слід періодично оцінювати вміст жиророзчинних вітамінів і цинку. І, хоча тематична доказова база також відсутня, хворим на ХП рекомендується часте дробне харчування без обмеження жирів.
Список літератури знаходиться в редакції.
Gardner T.B., Adler D.G., Forsmark C.E. et al. ACG clinical guideline:
chronic pancreatitis. Am. J. Gastroenterol. 2020; 115: 322-339.
Переклала з англ. Лариса Стрільчук
Медична газета «Здоров’я України 21 сторіччя» № 16 (485), 2020 р.