21 листопада, 2020
Пацієнт після інсульту: що заважає функціональному відновленню?
 Щорічна міжнародна неврологічна конференція «XII Нейросимпозіум» була успішно проведена 8‑10 вересня 2020 року в Одесі в очному форматі та додатково транслювалась у режимі онлайн. Цей науковий захід сприяв поширенню знань щодо новітніх досягнень у неврології та просвіті представників медичної спільноти. Доповідь, присвячену новим можливостям подолання наслідків найбільш грізного порушення функціонування мозку – інсульту, представила доцентка кафедри неврології № 1 Національної медичної академії післядипломної освіти імені П.Л. Шупика, д. мед. н. Тетяна Іванівна Насонова.
Щорічна міжнародна неврологічна конференція «XII Нейросимпозіум» була успішно проведена 8‑10 вересня 2020 року в Одесі в очному форматі та додатково транслювалась у режимі онлайн. Цей науковий захід сприяв поширенню знань щодо новітніх досягнень у неврології та просвіті представників медичної спільноти. Доповідь, присвячену новим можливостям подолання наслідків найбільш грізного порушення функціонування мозку – інсульту, представила доцентка кафедри неврології № 1 Національної медичної академії післядипломної освіти імені П.Л. Шупика, д. мед. н. Тетяна Іванівна Насонова.
Т.І. Насонова статистично обґрунтувала значну актуальність глобальної проблеми інсульту, що у 25% випадків розвивається у віці до 65 років. Після перенесеного інсульту 40% становлять особи молодше 55 років із помірним та тяжким ступенем інвалідизації, лише 10‑20% повертаються до праці (8% зберігають професійну придатність), 20‑43% потребують стороннього догляду, а в 25% до кінця першого року виникає деменція (Phipps et al., 2011; Grimaud et al., 2011).
Основні постінсультні синдроми включають:
- Синдром верхнього рухового нейрона (наявний у 88% пацієнтів), що клінічно маніфестує у вигляді порушення функції ходьби, паралічу та парезу, зміни м’язового тонусу (спастичність).
- Больовий синдром (48‑80% осіб страждають на хронічний біль), що частіше асоційований зі спастичністю (Bowler et al., 2002; Каse et al., 1998).
- Когнітивні (у 40‑70% хворих) та афективні розлади – постінсультна патологічна втома, тривога, апатія, депресія (у 30‑68%) (Burvil et al., 1995; Leys et al., 2005).
Відомо, що когнітивні та психоемоційні порушення після інсульту уповільнюють відновлення неврологічних функцій, погіршують прогноз і якість життя пацієнтів, збільшують тривалість госпіталізації, підвищують ризик повторного інсульту і смерті. Факторами розвитку когнітивних порушень і сповільненого відновлення рухів після інсульту є (Дамулін, 2002):
- особливості преморбідного когнітивного статусу;
- локалізація вогнища;
- ініціація дегенеративних процесів внаслідок нейрозапалення при інсульті (рівень експресії цитокінів, дисбаланс про- та антиінфламаторних систем, що особливо актуально у разі COVID‑19);
- інсульти в анамнезі;
- блокада глімфатичної системи (гліальних клітин, що виконують функцію самоочищення мозку);
- виснаження перфузійного резерву;
- мультиінфарктне ураження.
Лекторка торкнулася питання результативності та ефективності методів терапії інсульту. Сучасні дослідження свідчать, що довгостроковий результат після peперфузійного лікування є відносно сприятливим, у пролікованих пацієнтів поліпшуються сила і функції рук порівняно з контрольною групою. Проте емоційні та когнітивні проблеми зберігаються. Через п’ять років 44% хворих були залежними від сторонньої допомоги саме внаслідок когнітивних порушень (Muhr et al., 2017). У дослідженні L.J. Broome et al. (2016) встановлено, що тромболізис не впливав на когнітивні функції в короткостроковому і віддаленому періодах. Виключення становили порушення функції мови та синдром ігнорування, що поліпшувалися, але пізніше ефект нівелювався.
На жаль, сучасні можливості когнітивної реабілітації обмежені. В огляд A. Bahar-Fuchs et al. (2013) було включено 11 рандомізованих клінічних випробувань, в яких проводили аналіз ефективності когнітивних тренувань, і лише одне з них показало обнадійливі результати. Проте методики нейрореабілітації не мають бути ігноровані за таких патологій, як хвороба Паркінсона, хвороба Альцгеймера, стан після гострого порушення мозкового кровообігу.
Застосування можливих потенційно та достовірно ефективних методів нейрореабілітації є виправданим. Так, 2012 р. дослідники із клініки Мейо (США) вперше описали лікворний шлях елімінації з мозку продуктів обміну, що функціонує переважно під час сну (Lliff et al., 2014). Глімфатична система є дренажною та допомагає виводити продукти метаболізму, що накопичились у паренхімі мозку протягом дня (наприклад, β-амілоїд).
Нейрони, гліальні і судинні клітини функціонально тісно пов’язані і формують особливі «нейроваскулярні одиниці», порушення роботи яких проявляється ендотеліальною дисфункцією (Bennaroch, 2007). З іншого боку, деякі клінічні фактори впливають на відновлення пацієнтів після інсульту. Синдроми неглекту (зорово-просторових порушень) і «відштовхування» значною мірою погіршують реабілітаційний прогноз та потенціал пацієнтів, що перенесли інсульт (Karnath et al., 2002; Roller, 2004).
Не менш вагомою з точку зору порушення реалізації можливості успішної реабілітації є проблема постінсультної астенії, що виникає навіть при незначних навантаженнях, зберігається протягом тривалого часу, не зменшується після відпочинку та розвивається приблизно у 53‑77% пацієнтів (Torres-Harding, 2005; Staub, 2007).
Т.І. Насонова наголосила на тому, що наявність серцево-судинних факторів ризику, як-то ожиріння, куріння, зловживання алкоголем, артеріальна гіпертензія, цукровий діабет, гіперхолестеринемія, нераціональне харчування, протягом 10 років у середньому віці (20‑60 років) є вагомим предиктором розвитку не лише інфаркту та інсульту, але й когнітивних порушень, які можуть сягнути ступеня деменції (Diener, 2011).
Щодо питання реабілітації, ранніх втручань при інсульті, головними напрямами є застосування збагачення оточення та мультимодальної стимуляції («дзеркальна терапія», ментальне тренування, віртуальна реальність), неінвазивної стимуляції мозку (стимуляція постійним током, транскраніальна магнітна стимуляція, залучення роботів) та фармакотерапія (статини, антидепресанти, модулятори функції мембран, нейропротекція).
Оптимістичним є факт спонтанного самостійного відновлення після інсульту. В 16‑42% пацієнтів протягом 6‑10 тижнів відбувається значне поліпшення стану, що не пов’язано зі статтю, віком, домінантною півкулею, підтипом інсульту, характером лікування. Предиктором покращання є зменшення неврологічного дефіциту в перший тиждень після інсульту (Kwakkel et al., 2007).
Безумовно, в арсеналі лікаря є допоміжні медикаментозні методи, що підвищують шанси на повноцінне відновлення після інсульту. В даному контексті спікерка привернула увагу до препарату Мілдронат® (мельдонію дигідрат) виробництва АТ «Гріндекс», що здійснює терапевтичний вплив завдяки (Котов та співавт., 2015):
- оборотному конкурентному інгібуванню γ-бутиробетаїнгідроксилази;
- індукції біосинтезу NO;
- поліпшенню ендотеліальної функції, сповільненню агрегації тромбоцитів, збільшенню еластичності еритроцитів, зменшенню периферичного опору без ефекту «обкрадання» (вазопротекції);
- зниженню рівня карнітину;
- інгібуванню β-окислення жирних кислот, стимуляції окислення глюкози;
- відновленню транспорту АТФ, оптимізації споживання кисню, запобіганню ушкодженню клітинних мембран (цитопротекції).
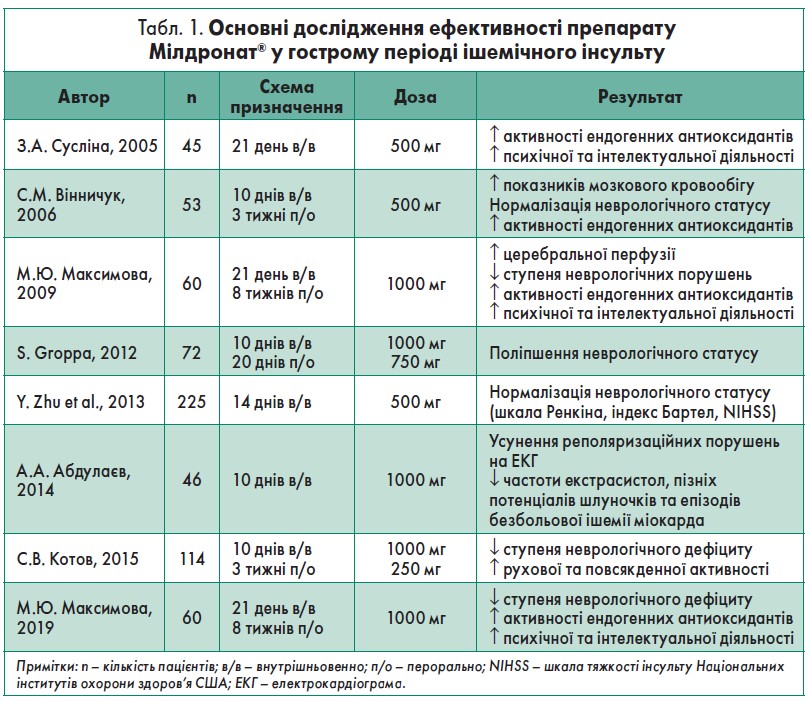
Мілдронат® є унікальним у плані реалізації одночасно принаймні п’яти функцій: він є антигіпоксантом, енерго-, вазокоректором, цитопротектором та антиоксидантом (Шишкова, 2018). Препарат гармонійно зіставляється з потребами пацієнта, який переніс інсульт, для запобігання розвитку синдрому неглекту, постінсультної астенії, функціональних порушень, інвалідизації та зниженню якості життя. Результати основних досліджень ефективності препарату Мілдронат® представлені в таблиці 1.
Доповідачка сформулювала висновки основних досліджень ефективності препарату Мілдронат®:
- Застосування препарату сприяє поліпшенню показників за модифікованою шкалою Ренкіна та NIHSS, індексу Бартел через 21 день у 87% пацієнтів групи втручання (Максимова та співавт., 2019).
- Терапія зменшує ступінь церебральної гіпоперфузії в лобному, тім’яному та скроневому сегментах (Максимова, 2009).
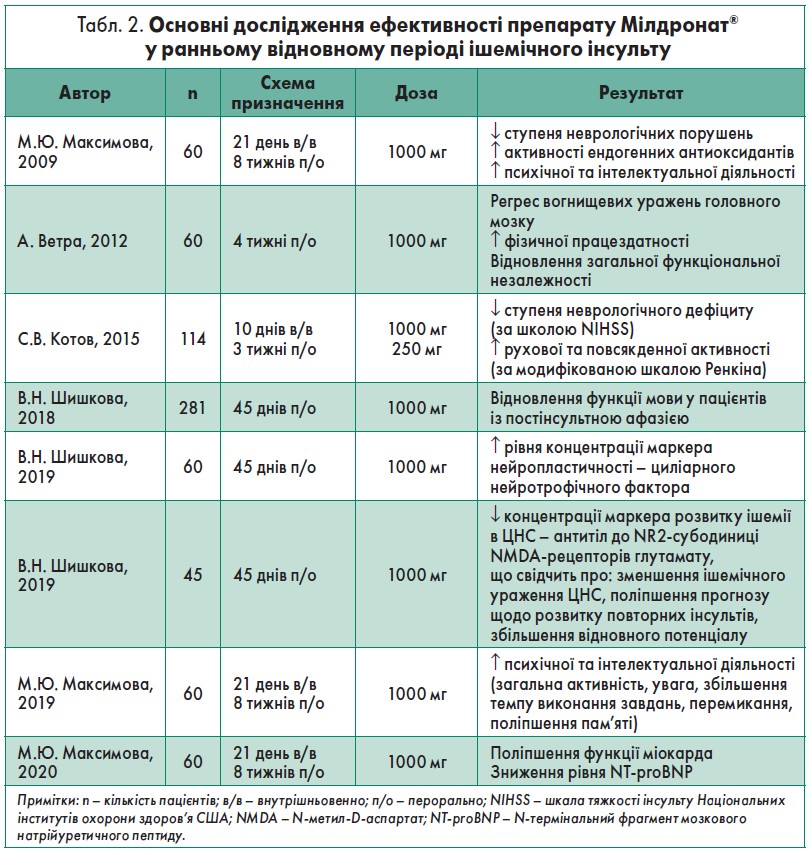
- У ранньому відновному періоді препарат чинить широкий спектр позитивних ефектів (табл. 2), що стосується пізнього відновного періоду – сприяє поліпшенню орієнтації та пам’яті, стійкості та ходи (Дамулін, 2013).
Підсумовуючи, спікерка зазначила, що патологія гострого порушення мозкового кровообігу є результатом мультифакторного впливу, може «ховатися» за безліччю клінічних масок та потребує залучення широкого спектра терапевтичних і реабілітаційних заходів. Один із варіантів ефективного медикаментозного впливу – застосування препарату Мілдронат®, який призначають за такою схемою залежно від індивідуального випадку:
- Гостра фаза порушення мозкового кровообігу або хронічна недостатність мозкового кровообігу: 500‑1000 мг в/в протягом 10‑14 днів із подальшим переходом на пероральне приймання.
- Підгостре порушення мозкового кровообігу: 500‑1000 мг перорально протягом 4‑6 тижнів.
- Хронічне порушення мозкового кровообігу: 500‑1000 мг перорально протягом 4‑6 тижнів, повторні курси (зазвичай 2‑3 рази на рік) можливі після консультації.
Підготувала Маргарита Марчук
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 3 (54) 2020 р.