22 грудня, 2020
Як діагностувати серцеву недостатність зі збереженою фракцією викиду: алгоритм HFA–PEFF
У загальній популяції осіб віком від 60 років 4,9% мають серцеву недостатність зі збереженою фракцією викиду (СНзбФВ), що в масштабах Європи становить кілька мільйонів хворих. Поширеність очікувано зростатиме у зв’язку зі збільшенням тривалості життя, пандемією ожиріння та цукрового діабету. СНзбФВ вже сьогодні становить більш ніж половину всіх випадків госпіталізацій внаслідок СН. Асоціація серцевої недостатності (HFA) Європейського товариства кардіологів (ESC) розробила оновлений комплексний діагностичний алгоритм HFA–PEFF для пацієнтів із підозрою на СНзбФВ. Представляємо до вашої уваги ключові положення цього покрокового протоколу.
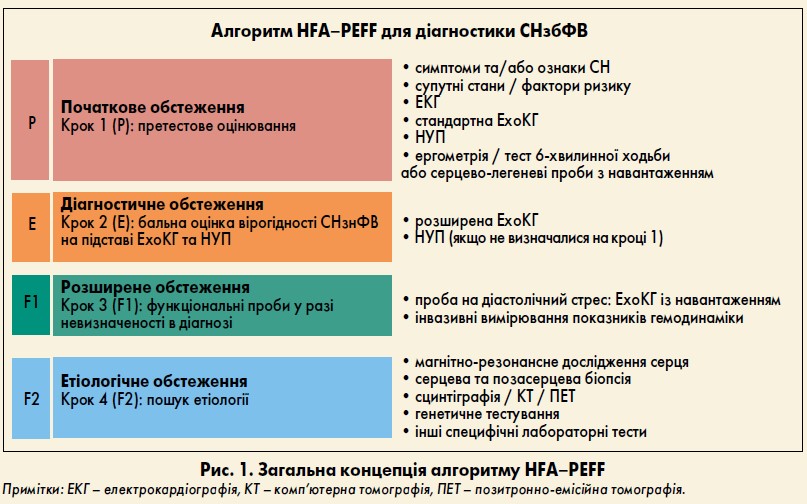
HFA ESC 2007 р. опублікувала консенсус із діагностики діастолічної СН. З того часу термінологія змінилася спочатку на «СН із нормальною фракцією викиду», а згодом було введене нове поняття «СН зі збереженою фракцією викиду». Для СНзбФВ експертна група запропонувала одну систему бального оцінювання, а також додаткові діагностичні критерії, проте вони відрізнялися за ехокардіографічними (ЕхоКГ) пороговими показниками, визнанням ролі коморбідних станів, біомаркерів, даними інвазивного дослідження гемодинаміки та стресових тестів. Окрім того, останніми роками значно розширилися знання патофізіології СНзбФВ та були запроваджені нові діагностичні методи. Цю інформацію було враховано при розробці нового комплексного діагностичного алгоритму HFA–PEFF для пацієнтів із підозрою на СНзбФВ (рис. 1, 2).
До пацієнтів, які, ймовірно, мають СНзбФВ, слід віднести осіб похилого віку, частіше жінок, із множинними супутніми захворюваннями та станами, зі збереженою ФВ лівого шлуночка (ЛШ) за даними стандартної ЕхоКГ та інших простих методів обстеження, що вказують на наявність СН. Так, про це можуть свідчити підвищений рівень натрійуретичних пептидів (НУП) або розвиток фібриляції передсердь (ФП).
Крок 1 (Р) алгоритму спрямований на виявлення вищезазначених типових ознак СНзбФВ, виключення або підтвердження інших специфічних причин симптомів, що нагадують СН. Альтернативними причинами симптомів можуть бути ішемічна хвороба серця, патологія клапанів, легеневі захворювання, анемія. Якщо результати даного етапу позитивні, слід перейти до наступного – Е, що включає деталізовану ЕхоКГ, визначення рівня НУП (якщо не було виконано на першому кроці), а також підсумкове оцінювання імовірності СНзбФВ у балах.
До кроку 2 (F1) слід перейти, якщо результати попереднього (Е) сумнівні. Залежно від можливостей закладу і стану пацієнта, можуть бути застосовані інвазивні чи неінвазивні стресові тести. Завершальний крок F2 – це спроба визначити етіологію ураження міокарда, якщо клінічний діагноз СНзбФВ вже встановлено на попередніх кроках.
Крок 1: претестове оцінювання
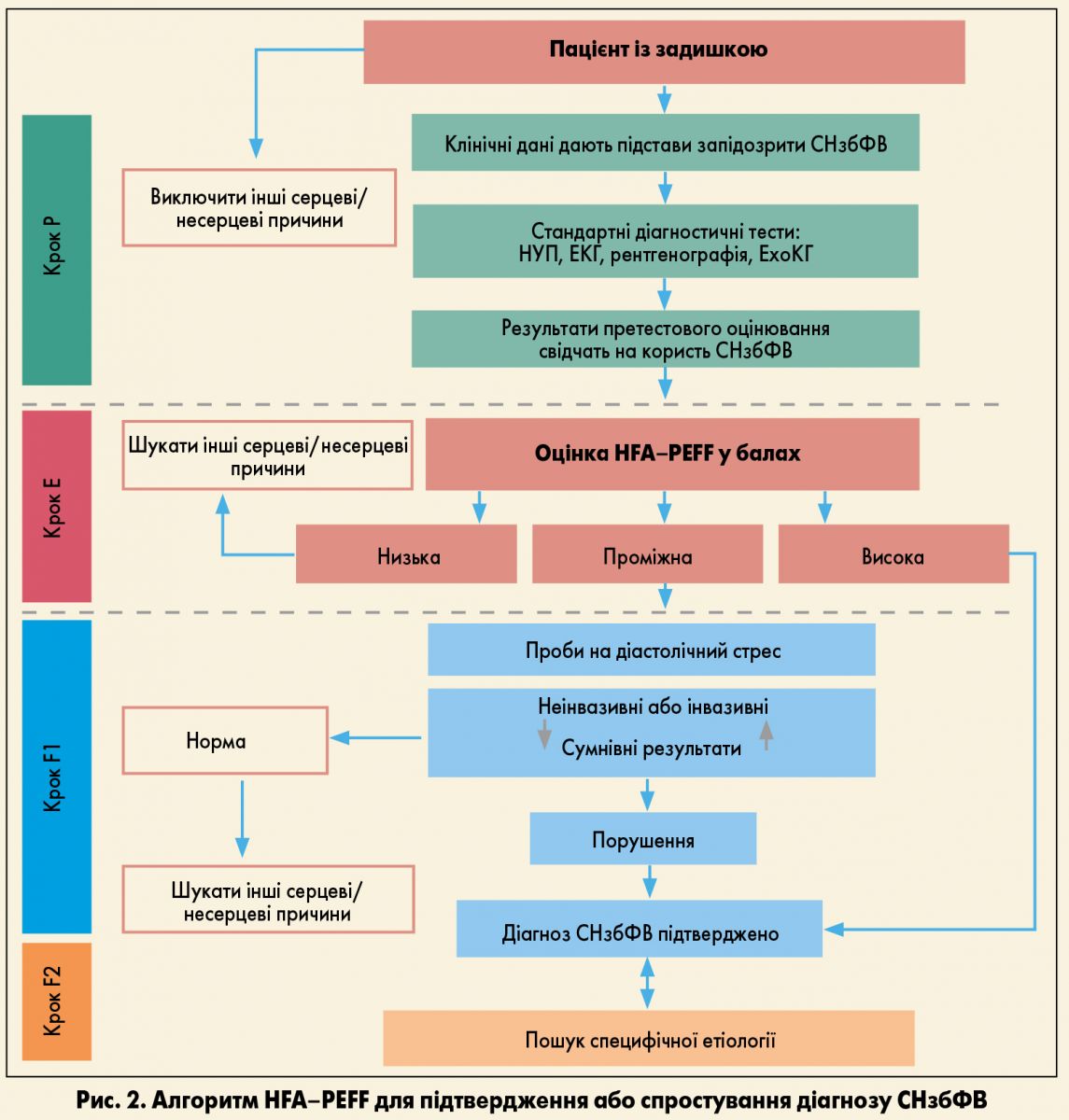
Крок 1 (Р) є обов’язковим для кожного пацієнта з симптомами та/або ознаками, що нагадують СН. Він включає деталізоване збирання анамнезу, виконання електрокардіограми (ЕКГ), аналізів крові, стандартної ЕхоКГ із метою виключення інших причин симптомів, таких як СН зі зниженою ФВ або патології клапанів серця, а також виявлення ішемії міокарда, аритмій, анемії або захворювань легень (рис. 2).
Симптоми та ознаки
Задишка під час навантажень – клас II або III за критеріями Нью-Йоркської асоціації серця (NYHA) – являє собою високочутливий маркер діагнозу СН, але має помірну специфічність (близько 50%) щодо серцевих причин симптомів. Ортопное – досить специфічна ознака, хоча має незначну чутливість. Особи із СНзбФВ часто скаржаться на знижені працездатність та виснаженість, які не відповідають серцевим порушенням, що визначаються у стані спокою. У пацієнтів похилого віку, з надмірною вагою та детренованістю зменшена здатність до навантажень, задишка при напруженні та периферичні набряки також можуть мати несерцеві причини.
Електрокардіографія
Пацієнти можуть мати ЕКГ-ознаки гіпертрофії ЛШ, такі як індекс Соколова – Лайона ≥3,5 мВ; порушення реполяризації та/або збільшення лівого передсердя (ЛП). Проте патогномонічних ознак СНзбФВ не існує, тож ЕКГ має низьку діагностичну цінність щодо цього діагнозу. Важливою знахідкою на ЕКГ може стати ФП, причиною якої часто буває СНзбФВ.
Лабораторні аналізи
Рекомендовано призначати наступні тестування: загальний аналіз крові; рівень натрію, калію, сечовини та креатиніну (з обчисленням швидкості клубочкової фільтрації); печінкові проби, HbA1С (метаболічний синдром та цукровий діабет 2-го типу є поширеними коморбідностями); тиреотропний гормон; феритин та насичення трансферину для виключення анемії. Анемія, пов’язана із СНзбФВ, посилює симптоми та знижує толерантність до навантажень.
Натрійуретичні пептиди
У численних дослідженнях в первинній практиці встановлено, що сироваткові рівні мозкового натрійуретичного пропептиду (NT-proBNP) <125 пг/мл (чи нг/л) або пептиду BNP <35 пг/мл з імовірністю 95‑99% виключають наявність СН будь-якого типу. Головним тригером вивільнення НУП є високий кінцево-діастолічний тиск на стінки ЛШ, який обернено пропорційний до товщини стінки. Звідси зрозуміло, що предиктивна цінність НУП справджується здебільшого для СНзнФВ, за якої ЛШ дилатований. Проте низькі рівні НУП не обов’язково виключають наявність СНзбФВ, за якої гіпертрофія ЛШ компенсує стрес стінки.
Встановлено, що до 20% хворих з інвазивно підтвердженою СНзбФВ мають рівні НУП, нижчі за порогові значення. Це становить обмеження для діагностичного застосування НУП. Тому важливо підкреслити, що за новим алгоритмом розрахунку ймовірності СНзбФВ може бути діагностовано навіть у тих випадках, коли рівні НУП нижчі за межові показники.
Ехокардіографія
Стандартну ЕхоКГ слід виконувати у кожного пацієнта із задишкою при клінічній підозрі на СН, за виключенням випадків, коли всі ознаки, перераховані далі, відсутні або негативні. ЕхоКГ може виключити альтернативні причини задишки, такі як СНзнФВ, патологія клапанів, первинна легенева гіпертензія або перикардіальний випіт.
Фактори ризику та інші клінічні ознаки, які вказують на наявність СНзбФВ у симптомних пацієнтів
- Вік ≥70 років
- Надмірна вага / ожиріння
- Метаболічний синдром / цукровий діабет
- Фізична детренованість
- Артеріальна гіпертензія
- Патологічні ознаки на ЕКГ (ФП тощо)
- Підвищені рівні НУП:
NT-proBNP ≥125 пг/мл, BNP ≥35 пг/мл
ФВ ЛШ слід виміряти (а не розрахувати), найкраще на дво-/тривимірних зображеннях. Значення ≥50% відповідають збереженій ФВ незалежно від віку, статі та етнічної належності. Також слід визначити діаметри та об’єми ЛШ. Діагноз СНзбФВ імовірний, якщо ЛШ не дилатований, ФВ збережена, наявні концентричне ремоделювання або гіпертрофія ЛШ, а також збільшене ЛП. ЕхоКГ-ознаки у стані спокою, типові для фенотипу СНзбФВ, часто виявляються у асимптомних пацієнтів, які мають ризик прогресування до клінічно явної СНзбФВ. Варто зауважити, що наявність структурних уражень на ЕхоКГ підтримує діагноз СНзбФВ, але їхня відсутність не виключає такого діагнозу.
Проби з навантаженням
Співіснуючий стеноз епікардіальних коронарних артерій у пацієнтів із СНзбФВ може бути причиною смерті, тому його слід виявляти та лікувати. Коронарна мікроваскулярна дисфункція є частиною патофізіології СНзбФВ, а отже, неінвазивні проби з навантаженням іноді дають хибно-позитивні результати.
Незважаючи на це, при підозрі на ІХС потрібно розглядати можливість застосування велоергометрії / тредміл-тесту, або методів із вищою чутливістю до ішемії, таких як добутамінова стресова проба з ЕхоКГ, серцевою магнітно-резонансною томографією (МРТ) чи сцинтіграфією, або процедур з анатомічним доступом до коронарних артерій – комп’ютерно-томографічної (КТ) чи інвазивної ангіографії.
Проби з навантаженням надають інформацію про здатність до виконання навантажень, відповідь артеріального тиску (що може бути гіпертензивною) та частоти серцевих скорочень (ЧСС) на навантаження. Хронотропна неспроможність наявна у 33‑77% пацієнтів із СНзбФВ і визначається як нездатність досягати 70‑80% від очікуваної максимальної ЧСС. Знижена здатність відновлювати ЧСС після навантажень має прогностичну цінність. Зменшена здатність до їхнього виконання – це пікове робоче навантаження ≤75% від розрахункового значення для відповідного віку.
У пацієнтів похилого віку з підозрою на СНзбФВ відстань 6-хвилинної ходьби ≤300 м можна розглядати як недостатню, хоча слід брати до уваги, що на результати цього тесту можуть впливати несерцеві, а також серцево-легеневі стани.
Якщо на першому кроці є підстави підозрювати наявність СНзбФВ, підтвердити чи спростувати діагноз допомагають специфічніші обстеження наступного етапу.
Крок 2: бальна оцінка ймовірності СНзбФВ на підставі розширеної ЕхоКГ та визначення НУП
Не існує єдиного неінвазивного діагностичного критерію СНзбФВ, тому рекомендовано оцінювати ймовірність діагнозу на підставі комбінованих показників ЕхоКГ та НУП. Деякі з них визначають під час попереднього кроку.
ЕхоКГ-показники функції та морфології
На кроці 1 автори документа рекомендують проведення стандартної ЕхоКГ із вимірюванням принаймні ФВ та діаметра ЛШ. На кроці 2 ЕхоКГ має бути більш деталізованою. Проте всі зазначені далі показники можуть бути визначені у межах однієї процедури.
Максимальна швидкість ранньодіастолічного руху фіброзного кільця мітрального клапана в септальній та латеральній частинах (е’):
- великий критерій для осіб <75 років – септальна е’ <7 см/с або латеральна е’ <10 см/с;
- великий критерій для осіб ≥75 років – септальна е’ <5 см/с або латеральна е’ <7 см/с.
Коментар. Показник е’ визначається, головним чином, релаксацією ЛШ. Він відображає збільшення поздовжнього розміру ЛШ і залежить від переднавантаження. Швидкість поздовжнього руху е’ зменшується з віком; нормативні значення для осіб похилого віку нижчі за ті, які 2007 р. містив консенсус HFA. До розрахунку HFA–PEFF включений критерій е’ з огляду на вік. Його слід вимірювати відповідно до рекомендацій Європейської асоціації серцево-судинної візуалізації (EACVI), що були опубліковані 2016 р.
Середнє відношення Е/е’ в септальній та латеральній частинах:
- великий критерій – середнє відношення Е/е’ ≥15;
- малий критерій – середнє відношення Е/е’ 9‑14.
Коментар. Відношення максимальної швидкості ранньодіастолічного потоку на мітральному клапані (Е), виміряної методом пульсового Доплера між верхівками мітральних стулок, до максимальної швидкості ранньодіастолічного руху фіброзного кільця мітрального клапана в септальній та латеральній частинах (е’), виміряної методом пульсового тканинного Доплера, відображає середнє значення тиску заклинювання у легеневих капілярах – mPCWP. Мітральний індекс Е/е’ корелює з жорсткістю ЛШ та фіброзом і меншою мірою залежить від віку, ніж е’. Також він має діагностичну цінність під час навантажень. На індекс Е/е’ меншою мірою впливають зміни об’єму, але він залежить від виразності гіпертрофії ЛШ.
Максимальна швидкість потоку регургітації на тристулковому клапані (TR) або систолічний тиск у легеневій артерії (PASP):
- великий критерій – TR >2,8 м/с;
- великий критерій – PASP >35 мм рт. ст.
Коментар. PASP обчислюється за модифікованим рівнянням Бернулі як максимальна швидкість ТR, помножена на 4, плюс розрахункове значення тиску в правому передсерді. Підвищений PASP та знижена функція правого шлуночка – важливі предиктори смертності при СНзбФВ. Навіть помірне підвищення PASP може призводити до поглиблення дисфункції шлуночків, оскільки зміщення міжшлуночкової перетинки ліворуч перешкоджає наповненню ЛШ. PASP >35 мм рт. ст. відрізняє хворих на СНзбФВ від таких з артеріальною гіпертензією. Максимальна швидкість ТR >2,8 м/с свідчить про підвищений PASP і слугує непрямим маркером діастолічної дисфункції ЛШ.
Глобальний поздовжній стрейн (GLS) ЛШ у систолу: малий критерій – GLS <16%.
Коментар. Міокардіальний стрейн (від англ. strain – напруження, розтягнення, деформація) – це зміни довжини волокон міокарда при переході зі стану релаксації до скорочення, що виражаються у відсотках. Систолічний GLS ЛШ не залежить від кута вимірювання, як при застосуванні методики тканинної доплерометрії. Глобальний стрейн визначається за допомогою методу спекл-трекінг ЕхоКГ як середнє значення систолічних стрейнів усіх сегментів ЛШ в апікальних чотири-/двокамерній та поздовжньо-осьовій позиціях. Знижений поздовжній систолічний та ранньодіастолічний стрейни ЛШ виявляли за наявності СНзбФВ. Знижений GLS є предиктором госпіталізацій із приводу СН, серцево-судинної смерті або зупинки серця. Він корелює з інвазивними вимірюваннями жорсткості ЛШ та рівнями НУП.
Індекс об’єму лівого передсердя (LAVI):
- великий критерій для пацієнтів із синусовим ритмом – LAVI >34 мл/м2;
- великий критерій для осіб із ФП – LAVI >40 мл/м2;
- малий критерій для пацієнтів із синусовим ритмом – LAVI 29‑34 мл/м2;
- малий критерій для хворих на ФП – LAVI 34‑40 мл/м2.
Коментар. Максимальний об’єм ЛП, виміряний у кінці систоли на дво-/тривимірних зображеннях та віднесений до площі поверхні тіла (LAVI), є непрямим показником тиску наповнення ЛШ. Він точніше відображає хронічне ремоделювання ЛП, ніж площа ЛП чи його діаметр та корелює з іншими ЕхоКГ-показниками діастолічної функції ЛШ. Значення LAVI від 29 до 34 мл/м2 запропоноване як малий критерій, оскільки це відповідає верхній межі норми для здорових осіб. У пацієнтів без ФП та патології клапанів серця LAVI >34 мл/м2 є незалежним предиктором смерті, розвитку СН, ФП та ішемічного інсульту. У пацієнтів із СНзбФВ та постійною формою ФП LAVI на 35% збільшений порівняно з такими із СНзбФВ та синусовим ритмом. В осіб із постійною формою ФП може бути наявний високий LAVI, навіть якщо вони не мають діастолічної дисфункції ЛШ. Тому для пацієнтів із синусовим ритмом та ФП рекомендовані окремі порогові значення LAVI.
Індекс маси лівого шлуночка (LVMI) та відносна товщина його стінки (RWT):
- великий критерій: LVMI ≥149 г/м2 у чоловіків, LVMI ≥122 г/м2 у жінок, або RWT >0:42;
- малий критерій: LVMI ≥115 г/м2 у чоловіків, LVMI ≥95 г/м2 у жінок, або RWT >0:42, або кінцево-діастолічна товщина стінки ЛШ ≥12 мм.
Коментар. Потовщення стінки ЛШ у діастолу при недилатованому серці вказує на його гіпертрофію. Спочатку вона розвивається у базальних сегментах міжшлуночкової перетинки, потовщення якої в цьому місці ≥12 мм часто зустрічається серед осіб похилого віку. Наявність ізольованої гіпертрофії перетинки недостатня для заключення про глобальне ремоделювання ЛШ або його гіпертрофію. Для оцінки геометрії ЛШ зазвичай використовують показник RWT, що обчислюється як товщина задньої стінки ЛШ, помножена на 2 і поділена на кінцево-діастолічний внутрішній діаметр ЛШ (LVPW 2 / LVIDD). Також застосовують LVMI, нормалізований за площею поверхні тіла або зростом.
Описано чотири можливі патерни:
- Норма (LVMI в межах норми, RWT ≤0,42).
- Концентричне ремоделювання (LVMI в межах норми, RWT >0,42).
- Концентрична гіпертрофія (підвищений LVMI, RWT >0,42).
- Ексцентрична гіпертрофія (підвищений LVMI, RWT ≤0,42).
У пацієнтів із СНзбФВ можна виявити як концентричну гіпертрофію ЛШ, так і концентричне ремоделювання. Відсутність гіпертрофії ЛШ за даними ЕхоКГ не виключає наявності СНзбФВ.
Натрійуретичні пептиди:
- великий критерій для пацієнтів із синусовим ритмом – NT-proBNP >220 пг/мл або BNP >80 пг/мл;
- великий критерій для хворих на ФП – NT-proBNP >660 пг/мл або ВNP >240 пг/мл;
- малий критерій для осіб із синусовим ритмом – NT-proBNP 125‑220 пг/мл або BNP 35‑80 пг/мл;
- малий критерій для пацієнтів із ФП – NT-proBNP 375‑660 пг/мл або BNP 105‑240 пг/мл.
Коментар. На кроці 1 рекомендований єдиний пороговий критерій НУП для забезпечення максимальної чутливості щодо виявлення серцевої патології. На кроці 2 з метою збільшення специфічності великим критерієм СН слугують вищі граничні значення НУП. Окрім того, межові показники НУП вказано для двох груп – пацієнтів із синусовим ритмом або ФП. Рівні НУП завжди слід оцінювати у клінічному контексті. Точні порогові значення для діагностики СНзбФВ в осіб із синусовим ритмом та ФП не встановлені. Проте відомо, що середні рівні НУП у хворих на ФП втричі вищі, ніж у таких із синусовим ритмом. У симптомних пацієнтів із СНзбФВ та ФП показники НУП ще вищі.
Обчислення та інтерпретація балів HFA–PEFF
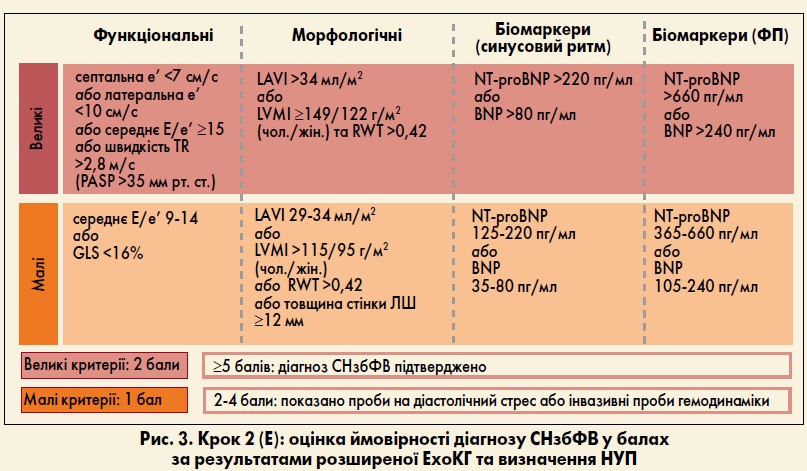
Бальна система оцінювання має функціональний, морфологічний та біомаркерний домени. У кожному з доменів великому критерію присвоюється 2 бали, малому – 1 бал (рис. 3). Окремі домени можуть надати максимально 2 бали, якщо кожен із великих критеріїв є позитивним, або 1 бал, якщо негативними є великі, але виконуються всі малі критерії. Якщо в одному домені позитивні кілька великих критеріїв, йому також присвоюється 2 бали. Якщо позитивними є декілька малих критеріїв, домен набирає 1 бал. Великі й малі критерії не додаються в межах одного домену. Бали плюсуються, лише якщо належать до різних доменів. Наприклад, два великі (Е/е’ >15 та TR >2,8 м/с) та один малий критерій (GLS <16) у функціональному домені дають загальну оцінку домену 2 бали.
Сукупний показник HFA–PEFF становитиме 5 балів, якщо принаймні ще один малий (наприклад, LAVI <34 мл/м2; потовщення стінки ЛШ >12 мм) та один великий критерій (наприклад, BNP у пацієнта з синусовим ритмом >80 пг/мл) будуть наявні в морфологічному та біомаркерному доменах відповідно.
Важливо зазначити, що для діагностики СНзбФВ не обов’язково мати всі параметри з кожного домену (що є типовою ситуацією на практиці). Систему HFA–PEFF можна застосовувати навіть за відсутності результатів деяких досліджень, що збільшує її практичну цінність.
Загальна оцінка ≥5 балів свідчить на користь діагнозу СНзбФВ, тоді як показник ≤1 означає дуже низьку ймовірність СНзбФВ і вказує на необхідність продовження діагностичного пошуку для встановлення альтернативних причин симптомів. Пацієнти із проміжними оцінками (2‑4 бали) потребують поглибленого обстеження (крок 3, рис. 4).
Крок 3: функціональні проби
На кроці 3 (F1) підтвердженням того, що симптоми СН зумовлені патологією серця, можуть бути порушення гемодинаміки, зокрема зменшені ударний об’єм та серцевий викид, підвищений тиск наповнення ЛШ, які виявляються як у стані спокою, так і під час навантажень. У типового пацієнта похилого віку із множинними супутніми станами наявність ізольованих структурних та/або функціональних аномалій серця у спокої не завжди дозволяє підтвердити або виключити діагноз СНзбФВ.
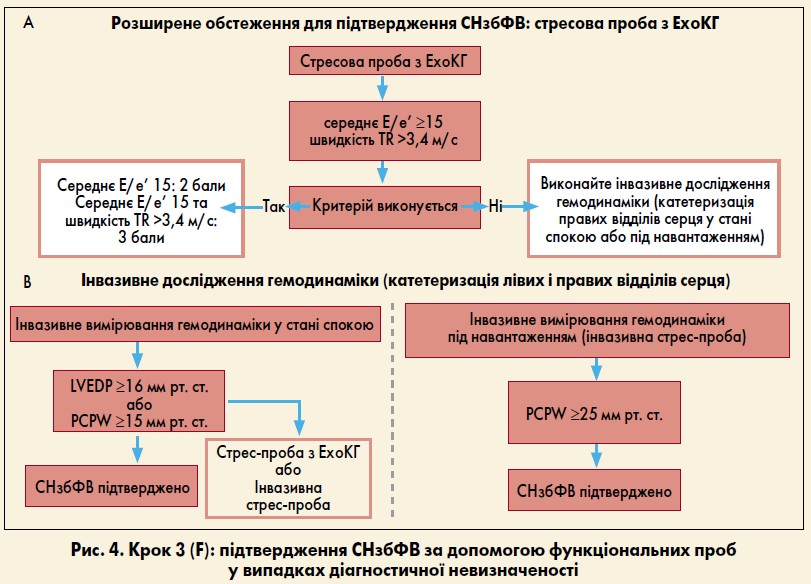
Якщо при інвазивному дослідженні у стані спокою виявлено високий тиск наповнення ЛШ (кінцево-діастолічний тиск – LVEDP ≥16 мм рт. ст., PCWP ≥16 мм рт. ст.), діагноз можна вважати підтвердженим. В інших випадках рекомендовано оцінити ці параметри під час навантаження – неінвазивно, методом стрес-ЕхоКГ або інвазивного вимірювання гемодинаміки з використанням критеріїв, вказаних на рисунках 2, 4.
ЕхоКГ під навантаженням: тест на діастолічний стрес
У багатьох пацієнтів із СНзбФВ симптоми з’являються під час навантаження і переважно зумовлені зростанням тиску наповнення ЛШ, що необхідно для підтримки адекватного наповнення шлуночка і ударного об’єму. Тому вимірювання ЕхоКГ-показників під навантаженням може виявити масковану діастолічну і систолічну дисфункцію ЛШ. Зазвичай визначають відношення Е/е’ та максимальну швидкість TR, які вказують на підвищення mPCWP та PASP відповідно.
В ідеалі слід проводити велосипедний тест у положенні напівлежачи з візуалізацією безпосередньо під час навантаження або ж тест на тредмілі / велоергометрі у вертикальній позиції з візуалізацією під час або одразу після максимального навантаження, але універсальних адаптованих протоколів не існує. EACVI та Американське товариство ехокардіографії (ASE) рекомендують покроковий протокол: початок із 25 Вт при 60 уд./хв, потім підвищення навантаження на 25 Вт з інтервалом 3 хв до досягнення максимального розрахункового робочого навантаження та/або максимальної ЧСС (220 – вік у роках) або ж появи обмежувальних симптомів. Для пацієнтів, які не можуть його виконати, запропонований протокол на велоергометрі у положенні напівлежачи із поступовим збільшенням навантаження: починаючи з 15 Вт при 60 уд./хв, із кроком збільшення на 5 Вт щохвилини, до субмаксимальної цільової ЧСС 100‑110 уд./хв або появи обмежувальних симптомів.
Збільшення лише швидкості потоку регургітації на тристулковому клапані (TR) не підтверджує діагнозу СНзбФВ, оскільки може бути зумовлене нормальною гіпердинамічною відповіддю на навантаження (через підвищення легеневого кровотоку) за відсутності діастолічної дисфункції ЛШ. Середнє співвідношення Е/е’ під навантаженням ≥15 додає 2 бали до загальної оцінки HFA–PEFF. Співвідношення Е/е’ ≥15 при максимальній швидкості TR >3,4 м/с додає 3 бали до попереднього аналізу на кроці 2. Якщо підсумкова оцінка за результатами кроків 2 та 3 становить ≥5 балів, діагноз СНзбФВ слід вважати підтвердженим.
На кроці 4 (F2) більшість випадків СНзбФВ пов’язані з поширеними факторами ризику і коморбідними станами, але специфічну етіологію завжди слід мати на увазі. Автори даного документа постулюють, що виявлення специфічних причин СНзбФВ може допомогти у виборі засобів цілеспрямованої терапії.
Специфічні хвороби серцевого м’яза, що можуть проявитися фенотипом СНзбФВ, включають гіпертрофічні кардіоміопатії, міокардити та хронічну запальну кардіоміопатію, автоімунні захворювання, неінфільтративні та інфільтративні кардіоміопатії, ідіопатичний або набутий ендоміокардіальний фіброз, хвороби накопичення та інші генетичні розлади, зокрема ранні стадії кардіоміопатій, асоційованих із м’язовою дистрофією. Також слід підозрювати токсичний вплив ліків або важких металів, вплив радіації та метаболічні причини, пов’язані з гормональними чи нутритивними розладами. Тригерний чинник може подіяти задовго до появи симптомів. Наприклад, радіаційно-індукована СНзбФВ розвивається через 10‑15 років, навіть якщо пацієнт отримав низьку дозу опромінення на серце 3,3 Гр.
Етіологічний пошук може включати стандартні стрес-тести з навантаженням, які здатні виявити ішемію міокарда, аномальну відповідь АТ на навантаження, хронотропну неспроможність, надшлуночкові та шлуночкові аритмії. Ці знахідки можуть бути негайно трансльовані у стратегії ведення пацієнта: підбір антиішемічної терапії, покращення контролю артеріального тиску, відміну препаратів із брадикардитичним ефектом (наприклад, β-блокатора, що був призначений раніше для лікування артеріальної гіпертензії), терапію порушень ритму, асоційованих із навантаженням.
Складнішими методами етіологічної діагностики є магнітно-резонансна томографія серця, що найточніше визначає об’єми й маси ЛШ і ЛП, рубці та ішемію міокарда, зумовлену патологією епікардіальних коронарних судин або мікроваскулярною дисфункцією, а також стресова перфузійна візуалізація для виявлення дифузних субендокардіальних дефектів. Регіональний та дифузний міокардіальний набряк (на Т2-зображеннях) та інфільтрацію або фіброз кількісно оцінюють із використанням ефекту пізнього посилення сигналу при контрастуванні гадолінієм (LGE) або Т1-картування. В окремих випадках для уточнення специфічної етіології можуть бути застосовані міокардіальна біопсія, сцинтіграфія з (99m)Tc для виявлення амілоїдозу, позитронно-емісійна томографія, а також спеціалізовані генетичні та лабораторні тести.
Слід зауважити, що автори алгоритму не мали наміру об’єднати під терміном «СНзбФВ» усі можливі причини клінічного синдрому СН із нормальною ФВ. Натомість вони наголошують, що важливо завжди розглядати ймовірність встановлення специфічної етіології, якщо підтверджено клінічний діагноз СНзбФВ. Неміокардіальні причини, які можуть імітувати симптоми СН (констриктивний перикардит, первинна патологія клапанів серця), не слід вважати складовими синдрому СНзбФВ.
Підготував Сергій Романюк
Оригінальний текст документа, включно зі списком літератури, читайте на сайті
www.escardio.org
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (72) 2020 р.