27 грудня, 2020
Складне питання клінічної панкреатології – діагностика раку підшлункової залози: актуальність проблеми, реалії та перспективи
На клінічному прикладі
 Протягом останніх років спостерігається збільшення захворюваності на рак підшлункової залози (ПЗ) у багатьох країнах, особливо Західної Європи та Північної Америки. У 2018 р. захворюваність (стандартизований показник, світовий стандарт, ASR) у країнах, де поширений рак ПЗ, становила: в Ізраїлі – 22 на 100 тис. населення, у Фінляндії – 7,9; Японії – 9,7; Данії – 7,8; Бельгії – 8,7; Франції – 8,9; США – 7,7; Великобританії – 7,1; Угорщині – 10,8. У США щороку реєструють близько 50 тис. хворих на рак ПЗ, а 26 тис. осіб помирають від цього захворювання [1-4]. В Україні наприкінці 2018 р. серед усіх злоякісних захворювань рак ПЗ посідав 8-ме місце у чоловіків і 9-те – у жінок. Захворюваність становить 7,3 на 100 тис. населення [5]. Менше поширений рак ПЗ у країнах Азії й Африки (ASR в Індії – 0,85; Таїланді – 2,0; Ірані – 3,1; Китаї – 5,2 на 100 тис. населення). Середній вік хворих дорівнює 60-65 років. Чоловіки хворіють дещо частіше за жінок [1-4].
Протягом останніх років спостерігається збільшення захворюваності на рак підшлункової залози (ПЗ) у багатьох країнах, особливо Західної Європи та Північної Америки. У 2018 р. захворюваність (стандартизований показник, світовий стандарт, ASR) у країнах, де поширений рак ПЗ, становила: в Ізраїлі – 22 на 100 тис. населення, у Фінляндії – 7,9; Японії – 9,7; Данії – 7,8; Бельгії – 8,7; Франції – 8,9; США – 7,7; Великобританії – 7,1; Угорщині – 10,8. У США щороку реєструють близько 50 тис. хворих на рак ПЗ, а 26 тис. осіб помирають від цього захворювання [1-4]. В Україні наприкінці 2018 р. серед усіх злоякісних захворювань рак ПЗ посідав 8-ме місце у чоловіків і 9-те – у жінок. Захворюваність становить 7,3 на 100 тис. населення [5]. Менше поширений рак ПЗ у країнах Азії й Африки (ASR в Індії – 0,85; Таїланді – 2,0; Ірані – 3,1; Китаї – 5,2 на 100 тис. населення). Середній вік хворих дорівнює 60-65 років. Чоловіки хворіють дещо частіше за жінок [1-4].
Діагностика раннього раку ПЗ майже неможлива. За даними японських авторів, пухлини діаметром до 2 см діагностують випадково, при цьому всі сучасні методи діагностики таких пухлин недостатньо інформативні. Так, за допомогою ультразвукового дослідження (УЗД) пухлини ПЗ виявляють, за даними різних авторів, у 30-50% випадків і навіть шляхом комп’ютерної томографії – тільки в 40-70% випадків. Діагноз рак ПЗ встановлюють в основному через 6 міс після появи перших симптомів, тому на момент діагностування 80% хворих мають метастази [1-4].
Значна поширеність та утруднена діагностика раку ПЗ є проблемою сучасної медицини, особливо на етапі первинної медичної допомоги.
Мета – на клінічному прикладі проаналізувати можливості та складні аспекти діагностики і ведення раку ПЗ, перспективи лікування та прогнозу.
Клінічний випадок
Пацієнт В., 57 років, звернувся до гастроентеролога зі скаргами на ниючий біль у правому підребер’ї, дискомфорт і важкість в епігастральній ділянці, відчуття гіркоти в роті, пожовтіння шкірних покривів, потемніння сечі, біль у грудному відділі хребта, швидку втомлюваність, загальну слабкість.
Актуальні аспекти анамнезу життя та хвороби. Anamnesis vitae: гіпертонічна хвороба ІІ стадії 3 ступеня протягом багатьох років, варикозне розширення вен нижніх кінцівок. 9 міс тому переніс гострий інфаркт міокарда, було проведено коронарографію. Постійно приймає антикоагулянти, статини, гіпотензивні засоби. Близько 6 років тому прооперований з приводу пахвинної та пупкової грижі.
Anamnesis morbi: вважає себе хворим протягом 1 міс, з моменту появи першої кровотечі із варикозно розширених вен стравоходу. Пожовтіння шкірних покривів відмічає протягом 1 тижня. Госпіталізований з приводу кровотечі.
Status presens objectivus (на момент госпіталізації). Загальний стан середнього ступеня тяжкості. Тілобудова пропорційна, індекс маси тіла – 25,3. Шкірні покриви чисті, жовтяничні. Склери жовті. Язик вологий, обкладений білим нальотом біля кореня. Щитоподібна залоза та периферичні лімфатичні вузли не збільшені. Частота дихальних рухів – 19/хв. Перкуторно – над легенями ясний легеневий звук. Аускультативно над легенями вислуховується везикулярне дихання, дещо ослаблене в нижніх відділах. Серцева діяльність ритмічна, тони ослаблені. Артеріальний тиск – 130/80 мм рт. ст. Пульс – 71 уд./хв, ритмічний, задовільних властивостей. Живіт візуально симетричний, бере участь в акті дихання. На передній черевній стінці відмічається пупкове випинання. При пальпації живіт м’який, чутливий у правому підребер’ї. Печінка збільшена, +7 см з-під краю ребрової дуги, значно ущільнена. Селезінка пальпується, збільшена в розмірах. Відрізки товстої кишки без особливостей. Симптоми подразнення очеревини негативні. Перистальтика задовільна. Симптом Пастернацького негативний з обох боків. Наявні варикозно розширені вени правої нижньої кінцівки, відмічається пастозність нижніх кінцівок. Діурез: сеча темного кольору, сечовипускання – 5-6 разів на добу. Дефекація не порушена, 1-2 рази на добу, кал оформлений, без патологічних домішок.
Дані лабораторного дослідження. За результатами загального аналізу крові у пацієнта виявлена анемія середнього ступеня тяжкості, зсув лейкоцитарної формули вліво, підвищення швидкості осідання еритроцитів до 31 мм/год. У біохімічному аналізі крові – гіпоальбумінемія (рівень альбуміну знижений на 25,6%), відмічаються підвищення рівнів аспартатамінотрансферази на 63,9%, загального білірубіну – у 10 разів, прямого білірубіну – у 45 разів, гамма-глутамілтрансферази – у 3 рази, лужної фосфатази – на 5,6%, С-реактивного протеїну – на 5,0%, зниження рівнів ліпопротеїдів високої щільності на 81,2%, холестерину – на 46,8%. Також у пацієнта спостерігалося різке підвищення рівня альфа-фетопротеїну у 174 рази.
Вірус гепатиту С. Позитивний результат дослідження на РНК вірусу гепатиту С методом полімеразної ланцюгової реакції.
УЗД органів черевної порожнини. Печінка збільшена: права частка – 160 мм, ліва – 98 мм, ехогенність середня, ехоструктура – неоднорідна, грубозерниста; портальна вена – 14 мм, судинний малюнок дещо розширений, внутрішньопечінкові жовчні протоки – дещо розширені. У правій частці – поодинокі утворення підвищеної однорідної ехоструктури, максимальний розмір – 37×26 мм. Жовчний міхур – деформований, диференціюється нечітко, розмір – 39×20 мм, стінка – 6 мм, потовщена, вміст – із конкрементом розміром 14 мм. Холедох – норма. ПЗ візуалізується нечітко, збільшена, розміром 32×20×30, ехогенність підвищена, ехоструктура неоднорідна, контури нерівні, розмиті, вірсунгова протока не розширена. Чепцева сумка вільна. Нирки – без особливостей. Селезінка збільшена, 155×71 мм, ехогенність – середня, ехоструктура – однорідна. Селезінкова вена – 6 мм. Вільна рідина у малому тазі об’ємом 187 см3, у підпечінковій ділянці – 750 см3.
Еластографія печінки. Ознаки дифузного критичного фіброзу печінки в межах F4 (за Metavir).
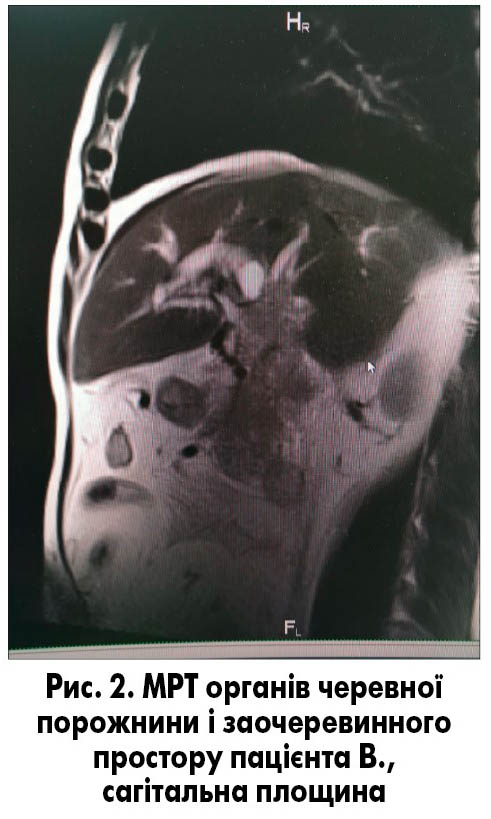
Магнітно-резонансна томографія (МРТ) органів черевної порожнини і заочеревинного простору. МР-картина об’ємного утворення перипортальної зони із залученням у процес головки ПЗ, міхурової протоки, жовчного міхура, паренхіми перипортальних відділів S4b, S5, S6 печінки, з обструкцією позапечінкових і дилатацією внутрішньопечінкових жовчних шляхів, яку слід диференціювати від аденокарциноми головки ПЗ або жовчного міхура, не виключено синхронний процес. Тромбоз портальної вени із залученням її внутрішньопечінкових гілок, селезінкових і верхньої брижової вен. Перипортальна, портокавальна, аортокавальна лімфаденопатія вторинного характеру. Карциноматоз очеревини. Виражений асцит. Спленомегалія.
МР-недифернційована нефрома правої нирки, кістозні нефроми правої та лівої нирок, достовірно не виключено tuberculisis renal cell carcinomas (рис. 1, 2).
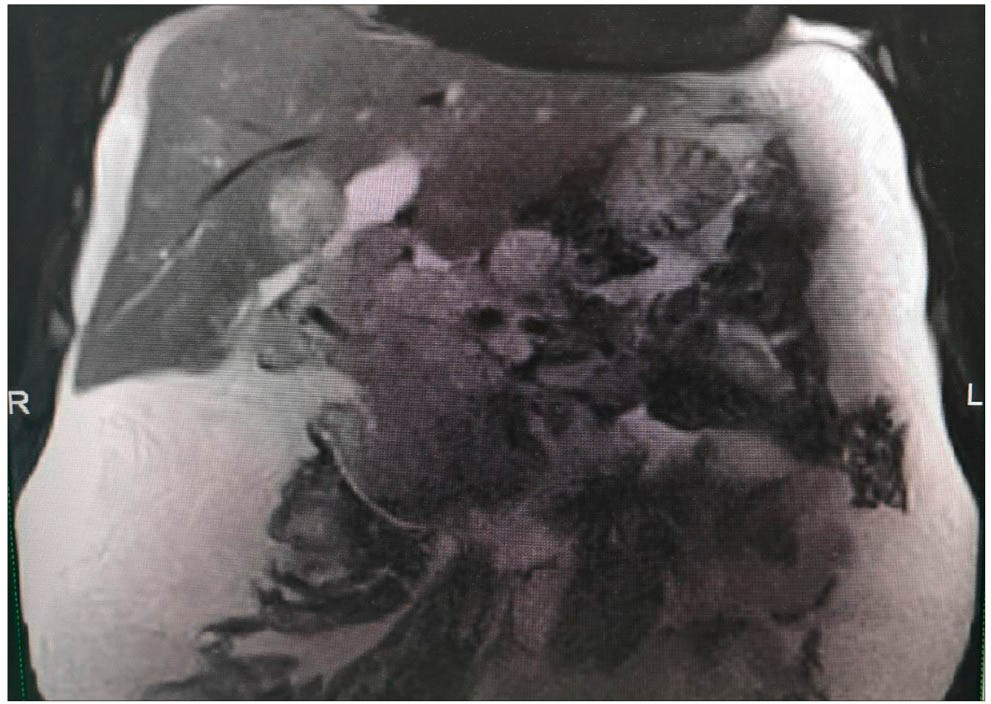 Рис. 1. МРТ органів черевної порожнини і заочеревинного простору пацієнта В., корональна площина
Рис. 1. МРТ органів черевної порожнини і заочеревинного простору пацієнта В., корональна площина
 Рентгенограма грудного відділу хребта. Деформівний спондильоз, спондилоартроз грудного відділу хребта.
Рентгенограма грудного відділу хребта. Деформівний спондильоз, спондилоартроз грудного відділу хребта.
Електрокардіограма. Ритм синусовий, нерегулярний, частота серцевих скорочень – 67 уд./хв, вольтаж збережений, електрична вісь серця горизонтальна. Суправентрикулярна екстрасистолія. Неповна блокада правої ніжки пучка Гіса. Дифузні дисметаболічні зміни міокарда.
Ехокардіоскопія. Діастолічна дисфункція лівого шлуночка за релаксаційним типом.
Езофагогастродуоденоскопія. Хронічний гастродуоденіт ІІ стадії. Гастроезофагеальна рефлюксна хвороба, ступінь А. Дуоденогастральний рефлюкс. Гастродуоденостаз.
Консультація кардіолога. Ішемічна хвороба серця. Стенокардія напруження, ІІІ функціональний клас (ФК). Постінфарктний (без Q-інфаркт міокарда) кардіосклероз. Стенозивний коронаросклероз, коронарографія, ангіопластика, коронарне стентування (один стент). Багатосудинне ураження. Суправентрикулярна екстрасистолія. Гіпертонічна хвороба ІІІ стадії 2 ступеня. Серцева недостатність І стадії, ІІ ФК за NYHA. Дуже високий кардіоваскулярний ризик.
Консультація невролога. Гостра торакалгія вертеброгенного генезу, недиференційована форма, з больовим, м’язово-тонічним синдромами.
Консультація онколога. Рак головки ПЗ, Т3N1M1, IV стадія, IV клінічна група (цироз печінки, асоційований з гепатитом С, В-С за Чайлдом – П’ю; печінково-клітинна недостатність 2-3 ступеня; карциноматоз очеревини; асцит; больовий синдром). Рекомендовано: нагляд дільничного онколога, симптоматична терапія за місцем проживання, вирішення питання про призначення наркотичних аналгетиків – за необхідності за місцем проживання.
Обговорення
На жаль, у такому стані спеціальне лікування (хіміотерапія) не проводиться. Пацієнту показана симптоматична терапія в умовах хоспісу/відділення паліативної допомоги або ведення сімейним лікарем за консультативної підтримки онколога за місцем проживання.
Безумовно, це класичний приклад пізнього діагностування раку ПЗ. У разі виявлення цієї патології на більш ранньому етапі у вигляді ущільнення чи об’ємного утворення у ПЗ лікареві слід якомога швидше з’ясувати: це пухлинний процес чи ні (виконати дослідження на базові пухлинні маркери, при підозрі на пухлину – біопсію, а якщо маркери вкрай високі, то можна обійтися і без неї в операбельному випадку). Чи випадок операбельний, безумовно, визначає спеціаліст-онколог.
Якщо встановлено діагноз злоякісної пухлини, проводиться стадіювання (уточнення поширення процесу) раку ПЗ і вирішується питання про операбельність. Якщо пухлина умовно-операбельна, призначають передопераційну хіміопроменеву терапію, а після цього оцінюють можливість операції. Єдиним куративним методом лікування (тобто здатним вилікувати пацієнта) у разі раку головки ПЗ є оперативне втручання (панкреатодуоденальна резекція).
Для терапевта і гастроентеролога важливо враховувати доказові фактори ризику раку ПЗ, наявність яких дає змогу запідозрити у пацієнтів можливість виникнення цієї грізної патології. Так, у 30% випадків карцинома ПЗ пов’язана з курінням. Доведено, що куріння в 2 рази підвищує ризик розвитку раку ПЗ. Зловживання алкоголем, недостатня кількість у раціоні свіжих фруктів і овочів також є істотними факторами ризику – 20% випадків. У 2 рази підвищується ризик раку ПЗ у хворих на цукровий діабет. Спадковість має значення у 5-10% усіх випадків цієї патології. Хвороба частіше пов’язана з такими спадковими станами, як аденоматозний поліпоз, неполіпозний колоректальний рак, синдроми Гіппеля – Ліндау і Гарднера. Дуже важливо пам’ятати, що до раку ПЗ у 5% випадків призводить хронічний панкреатит, тому вести таких пацієнтів потрібно надзвичайно уважно.
Лікарям і медичним працівникам слід враховувати, що на ранньому етапі рак ПЗ проявляється симптомами, схожими з такими інших захворювань. Серед них – запор (у 13% випадків), слабкість (у 23%), загальне нездужання і здуття живота (у 31%). Розвиток цукрового діабету часто маскує цю хворобу. Іноді у людини підозрюють пептичну виразку шлунка або захворювання жовчного міхура. Більш специфічні симптоми раку ПЗ розрізняють залежно від розташування пухлини у залозі. Основні симптоми раку ПЗ – біль і жовтяниця. Їх відзначають 90% пацієнтів. Жовтяниця – це дуже важлива і часта ознака ураження ПЗ злоякісною пухлиною. Як правило, жовтяницю супроводжують світлий кал, темна сеча, свербіж. Біль може локалізуватися в спині або верхній частині лівого квадранта живота. Третій симптом раку ПЗ – втрата маси тіла при нормальному апетиті. Це пов’язано із порушенням зовнішньосекреторної функції ПЗ, яке проявляється стеатореєю: з калом виділяється підвищена кількість жирних кислот і нейтрального жиру. Це свідчить про важливість виявлення цього синдрому у пацієнтів із хронічним панкреатитом або іншими нозологіями, які є «ризиковими» за раком ПЗ. Нудота, блювання та відсутність апетиту спостерігаються майже в половині випадків раку ПЗ і зумовлені стисканням шлунка і дванадцятипалої кишки.
Серед лабораторних параметрів при підозрі на рак ПЗ важливими є показники біохімічного аналізу крові і онкомаркери. Найбільш значущим з онкомаркерів є СА-19-9, що є пунктом усіх протоколів ведення раку ПЗ і хронічного панкреатиту.
Для точної верифікації раку ПЗ використовують також сучасні інструментальні методи. На жаль, тільки у 20% випадків карциному ПЗ діагностують, коли пухлина обмежена самою ПЗ. Одним з першочергових обстежень є спіральна комп’ютерна томографія (КТ) із подвійним контрастуванням. Для підтвердження і/або уточнення діагнозу проводять пункційну біопсію під контролем КТ або УЗД. Сучасний метод дослідження позитронно-емісійну томографію (ПЕТ-КТ) застосовують для визначення стадії захворювання у пацієнтів з потенційно операбельним раком ПЗ. Крім того, ПЕТ-КТ призначають для виявлення можливого рецидиву хвороби. Також для діагностики використовують трансабдомінальну ультрасонографію, ендоскопічну ретроградну панкреатохолангіографію, ендоскопічне УЗД з аспіраційною біопсією.
Як вже відзначалося, хірургічне втручання – основний метод лікування раку ПЗ, який достовірно підвищує виживаність. Після резекції ПЗ з пухлиною (панкреатодуоденальної резекції) призначають хіміотерапію. Інші лікувальні підходи полягають у зменшенні вираженості окремих симптомів. При больовому синдромі застосовують знеболювальні препарати, радіо- і хіміотерапію. У разі жовтяниці виконують ендоскопічне стентування – оперативне втручання, що полягає в накладенні обхідного анастомозу. При обструкції дванадцятипалої кишки (приблизно у 5% пацієнтів) проводять оперативне лікування (накладення анастомозу між шлунком і порожньою кишкою або ендоскопічне стентування). Хіміотерапія при раку ПЗ лише сприяє істотному зменшенню больових відчуттів.
Таким чином, потрібна настороженість сімейних лікарів, терапевтів, гастроентерологів, ендокринологів та інших спеціалістів щодо можливого раку ПЗ при появі у пацієнтів усіх вищенаведених симптомів. Слід також знати можливості лабораторної та інструментальної верифікації діагнозу і вчасно направляти хворих для консультативної та діагностично-лікувальної допомоги.
Висновки
Рання діагностика раку ПЗ в Україні та світі залишається недостатньою. Наведений приклад наочно демонструє необхідність своєчасної оцінки факторів ризику розвитку цієї патології, що могла б дозволити раніше її виявити, а також забезпечити більш ефективну і раціональну тактику лікування. Тільки онкологічна настороженість, професійна грамотність і готовність до командної роботи заради блага пацієнта з патологією ПЗ, а особливо з раком органа, можуть вирішити проблему збільшення виживаності таких пацієнтів, подовження і покращення якості їхнього життя.
Література
- Bray F., Ferlay J., Soerjomataram I., Siegel R.L., Torre L.A., Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer Journal for Clinicians. 2018; 68 (6): 394-424.
- Neoptolemos J.P., Palmer D.H., Ghaneh P., Psarelli E.E., Valle, J.W., Halloran C.M., Faluyi O., (...), Buchler M.W. Comparison of adjuvant gemcitabine and capecitabine with gemcitabine monotherapy in patients with resected pancreatic cancer (ESPAC-4): a multicentre, open-label, randomised, phase 3 trial. The Lancet. 2017; 389 (10073): 1011-1024.
- Neoptolemos J.P., Kleeff J., Michl P., Costello E., Greenhalf W., Palmer D.H. Therapeutic developments in pancreatic cancer: Current and future perspectives. Nature Reviews Gastroenterology and Hepatology. 2018; 15 (6): 333-348.
- Cros J., Raffenne J., Couvelard A., Pote N. Tumor Heterogeneity in Pancreatic Adenocarcinoma. Pathobiology. 2018; 85 (1-2): 64-71.
- Білинський Б.Т. Медичні помилки в онкології. Львів: Афіша, 2013. – 324 с.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 4 (58) 2020 р.



