26 січня, 2021
Практичні аспекти ведення пацієнтів з алергічним ринітом під час пандемії COVID‑19: специфічна імунотерапія та вибір оптимального антигістамінного препарату
Пандемія Covid‑19 зробила 2020 рік знаковим для всього світу та свого роду викликом для світової медичної спільноти. Covid‑19 не лише переформатував наше життя, перевівши багато його аспектів у режим онлайн, але й зумовив створення цілої низки рекомендацій щодо ведення пацієнтів із різноманітними хронічними захворюваннями в сучасних епідеміологічних умовах.
 11-12 вересня 2020 року, за підтримки Асоціації алергологів України, у рамках проекту «Життя без алергії», відбулася науково-практична конференція МОЗ України «Сучасна світова практика ведення пацієнтів з алергічними захворюваннями в період COVID‑19». На початку заходу з вступним словом до присутніх звернувся президент Світової алергологічної організації (WAO) Ігнаціо Дж. Ансотеджі (Іспанія). Із доповідями щодо особливостей ведення пацієнтів в умовах COVID‑19 виступили провідні вітчизняні та зарубіжні експерти з Німеччини, Болгарії та Великої Британії.
11-12 вересня 2020 року, за підтримки Асоціації алергологів України, у рамках проекту «Життя без алергії», відбулася науково-практична конференція МОЗ України «Сучасна світова практика ведення пацієнтів з алергічними захворюваннями в період COVID‑19». На початку заходу з вступним словом до присутніх звернувся президент Світової алергологічної організації (WAO) Ігнаціо Дж. Ансотеджі (Іспанія). Із доповідями щодо особливостей ведення пацієнтів в умовах COVID‑19 виступили провідні вітчизняні та зарубіжні експерти з Німеччини, Болгарії та Великої Британії.
Неабияку зацікавленість слухачів викликав виступ заступника голови Інституту медичної статистики та обчислювальної біології (IMSB) медичного факультету Кельнського університету, голови цільової групи Європейського ринологічного товариства (ERS) ISCOANA, члена керівного комітету Німецької академії оториноларингології з розробки рекомендацій з риносинуситу і раптової глухоти, голови ЛОР-відділення Європейської академії алергії, доктора медичних наук, професора Ральфа Месгеса (Німеччина). Темою доповіді став алергічний риніт під час COVID‑19.
Сьогодні, на етапі другої хвилі пандемії COVID‑19, на прийом часто приходять пацієнти із симптомами алергічного риніту (АР), які вважають, що в них коронавірусна хвороба. Але між цими двома захворюваннями є чіткі відмінності (AАААІ, 2020).
Основні відмінності між алергічними захворюваннями та COVID‑19
Клінічні прояви
Алергічними симптомами зазвичай є закладеність носа, нежить, чхання, свербіж і сльозотеча. Алергічна астма може проявлятися кашлем, епізодами візингу та задишкою. Шкірні прояви включають сухість та свербіж. Деякі пацієнти скаржаться на головні болі та втому (AАААІ, 2020).
Що ж до COVID‑19, то він за перебігом більше нагадує грип чи гостре респіраторне захворювання. Типовими симптомами є лихоманка (90%), сухий кашель (68%), втома, виділення мокротиння (33%), задишка (19%), біль у горлі (14%), міалгія та, рідко, діарея. Згідно з інформацією Всесвітньої організації охорони здоров’я (ВООЗ), закладеність носа спостерігається в 5%, а ін’єкція кон’юнктиви – лише в 0,8% підтверджених випадків COVID‑19. SARS-CoV‑2 може спричиняти легкий фолікулярний кон’юнктивіт і, ймовірно, передається через аерозольний контакт із кон’юнктивою. Припускають, що втрата смаку або нюху може бути важливим раннім симптомом захворювання і поводом для проведення тестування на COVID‑19. Додаткові шкірні симптоми, такі як ураження стоп і пальців на ногах, що нагадують «озноб», цілком можуть бути проявом захворювання (AАААІ, 2020).
Демографічні дані
Алергічні захворювання (АЗ), зокрема АР, на відміну від COVID‑19 частіше виникають у дітей і молодих людей. Водночас COVID‑19 у дітей спостерігається рідко та протікає доволі легко. Але в небагатьох осіб віком до 19 років розвивається тяжкий (2,5%) або загрозливий для життя перебіг (0,2%).
У загальній популяції 80% випадків COVID‑19 характеризуються легким та помірним перебігом, у тому числі підтип як без пневмонії, так і з пневмонією. Частота тяжких випадків становить 13,8%, а життєво небезпечні стани, зокрема дихальна недостатність (ДН), септичний шок та/або органна/поліорганна недостатність, розвиваються в 6,1% пацієнтів. Частка пацієнтів зі справді безсимптомним перебігом невідома.
Загалом рівень смертності при зараженні SARS-CoV‑2 в пацієнтів віком до 60 років становить менше 1%, від 60 до 69 – 3,5%, від 70 до 79 – 8% і старше 80 років – 15%. Ці показники напряму залежать від наявності супутніх захворювань та доступності медичної допомоги (AАААІ 2020).
Основою профілактики зараження SARS-CoV‑2 є мінімізація контакту з вірусом. Для цього пацієнтам треба обов’язково використовувати засоби індивідуального захисту (ЗІЗ) та обмежити відвідування закладів охорони здоров’я. Оцінку контролю симптомів захворювання проводять, використовуючи сучасні цифрові методи, одним з яких є мобільний додаток MACVIA-LR. Його зручний інтерфейс дає пацієнтам можливість швидко описувати та відслідковувати зміни в симптоматиці АР, а лікарю – оцінювати перебіг та корегувати лікування. На жаль, згаданий додаток поки недоступний українською і російською мовами, тому його можна замінити телефонним дзвінком або відеоконсультацією (AАААІ 2020).
Міжнародні гайдлайни з ведення пацієнтів з АР в умовах пандемії COVID‑19
Рекомендації щодо ведення пацієнтів з та без COVID‑19 в умовах пандемії викладені в кількох міжнародних настановах, основними з яких є:
- Позиційний документ Європейської академії алергології та клінічної імунології (EAACI) та робочої групи ініціативи ARIA (Алергічний риніт і його вплив на бронхіальну астму) «Практичні міркування щодо організації алергологічної клініки» (Pfaar O. et al., 2020).
- Позиційний документ німецької робочої групи ARIA у співпраці з австрійською та швейцарською робочими групами ARIA, Німецьким товариством прикладної алергології (AEDA), Німецьким товариством алергології та клінічної імунології (DGAKI), Товариством дитячої алергології (GPA) у співпраці з ініціативною групою (AG) з клінічної імунології, алергології та екологічної медицини Німецького товариства оториноларингології та хірургії голови та шиї (DGHNO-KHC) та Європейською академією алергії та клінічної імунології (EAACI) «Алерген-специфічна імунотерапія при пандемії COVID‑19» (Klimek L. et al., 2020).
Основні практичні моменти, з якими стикається практикуючий лікар в умовах пандемії, стосуються специфічної імунотерапії (СІТ) та фармакотерапії АР.
Специфічна імунотерапія
Як при СІТ, так і при COVID‑19 в організмі виникає низка імунологічних феноменів, відображених у таблиці (Klimek L. et al., 2020).
Імунологічні зміни при СІТ та COVID‑19 у деяких моментах є взаємовиключними, тому при інфікуванні SARS-CoV‑2 немає сенсу продовжувати імунотерапію. Згідно з позиційними документами EAACI/ARIA та «Алерген-специфічна імунотерапія при пандемії COVID‑19»:
- Пацієнтам з АР та підозрою на або інфікуванням SARS-CoV‑2 (позитивна ПЛР або IgM) необхідно відмінити сублінгвальну та підшкірну СІТ до клінічного видужання (Pfaar O. et al., 2020; Klimek L. et al., 2020).
- Пацієнтам з АР без підозри на інфікування SARS-CoV‑2 та необтяженим епідеміологічним анамнезом варто продовжити сублінгвальну чи підшкірну СІТ. Необхідно забезпечити пацієнта достатньою кількістю таблеток для сублінгвальної СІТ, щонайменше на 14 днів карантину (Pfaar O. et al., 2020; Klimek L. et al., 2020).
Фармакотерапія
Незважаючи на те що СІТ – це єдина високоефективна етіологічна терапія АР, її отримує невеликий відсоток хворих. Крім того, для пацієнтів з АР та супутнім COVID‑19 треба розглянути інші терапевтичні опції.
Відповідно до позиційного документу EAACI/ARIA, незалежно від того, чи заражений хворий на АР SARS-CoV‑2 чи ні, йому рекомендується продовжувати лікування інгаляційними глюкокортикостероїдами та антигістамінними препаратами (АГП) ІІ покоління (Pfaar O. et al., 2020).
P. Matricardi та співавт. виконали метааналіз мультицентрових рандомізованих контрольованих клінічних досліджень, в якому порівнювали ефективність СІТ та фармакотерапії, зокрема АГП ІІ покоління, у зменшенні симптомів АР (Matricardi P.M. et al., 2011).
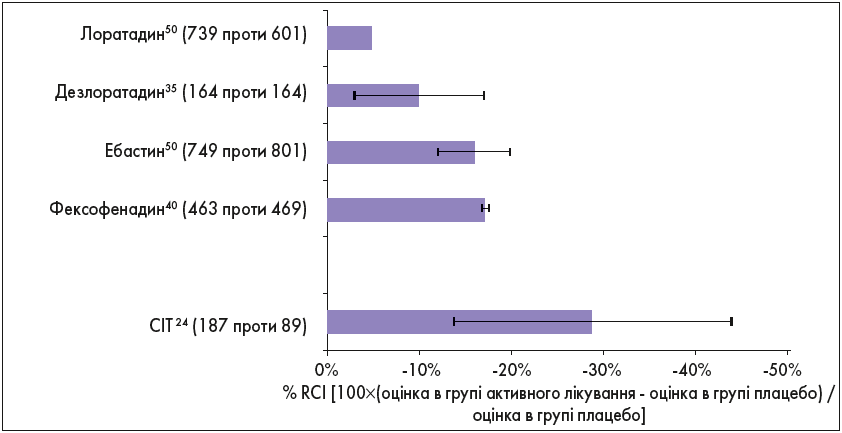
Оцінку проводили за Сумарним показником тяжкості назальних симптомів (TNSS), Шкалою загальної оцінки симптомів (TSS) або й за тим, і за іншою протягом першого сезону пилкування після початку лікування. Ефективність визначали як відсоток зменшення оцінки згідно з даними TSS та TNSS, що були отримані при активному лікуванні, у порівнянні з плацебо (відносний клінічний вплив [RCI]), та стандартизовану середню різницю (SMD) у групах лікування проти плацебо.
Зменшення симптомів було більш вираженим у пацієнтів, які отримували СІТ (рис. 1).
Рис. 1. Порівняна ефективність СІТ та АГП ІІ покоління в зменшенні симптомів АР (Matricardi P.M. et al., 2011)
Однак у цьому дослідженні не було даних з ефективності новітнього АГП ІІ покоління біластину. Kimihiro Okubo та співавт. (2017) провели багатоцентрове рандомізоване подвійне сліпе плацебо-контрольоване паралельне дослідження III фази з вивчення ефективності й безпеки біластину в японських пацієнтів із цілорічним АР (ЦАР).
Випадковим чином 765 пацієнтів було розподілено на 3 групи, кожна з яких протягом 2 тиж отримувала біластин (20 мг 1 раз на день), фексофенадин (60 мг двічі на день) або плацебо (256, 254 та 255 пацієнтів відповідно). Усі пацієнти щодня описували в щоденнику свої назальні та очні симптоми. Первинною кінцевою точкою була середня зміна TNSS від вихідного рівня на 2-му тиж лікування (10-13 днів). Значно меншою вона була в групі біластину (-0,98), якщо порівняти з плацебо (-0,63; р=0,023). Досліджувані препарати переносилися добре.
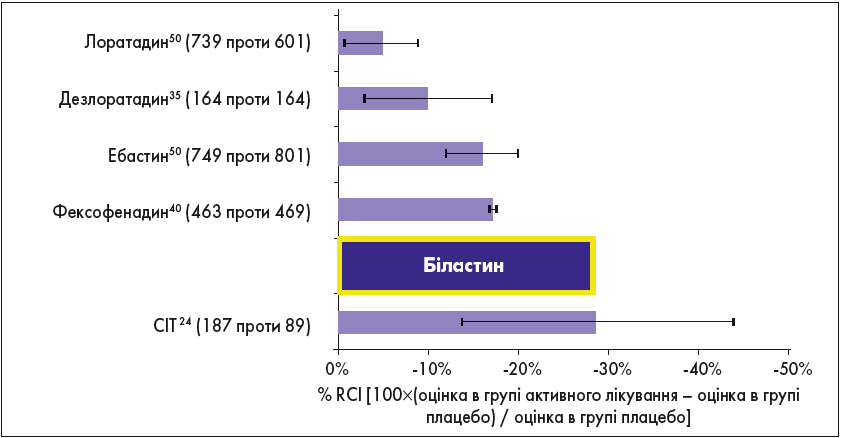
Якщо екстраполювати отримані в японському дослідженні результати на метааналіз P. Matricardi та співавт., ми побачимо показники ефективності, зображені на рисунку 2 (Matricardi P.M. et al., 2011; Okubo K. et al., 2017).
Рис. 2. Порівняна ефективність СІТ та АГП ІІ покоління в зменшенні симптомів АР з екстраполюванням даних, отриманих у дослідженні K. Okubo та співавт. (Matricardi P.M. et al., 2011; Okubo K. et al., 2017)
Таким чином, призначення біластину пацієнтам з АР дає можливість досягнути ефективності, порівняної із СІТ. Це особливо важливо для хворих, яким СІТ доводиться зупинити через зараження SARS-CoV‑2.
Ще однією перевагою біластину (Ніксар) є швидкість настання дії. Середня зміна TNSS від вихідного рівня була достовірно нижчою в групі біластину (-0,99), ніж у групі плацебо (-0,28; р<0,001) або фексофенадину (-0,62; р=0,032) уже в 1-й день лікування (рис. 3) (Okubo K. et al., 2017).
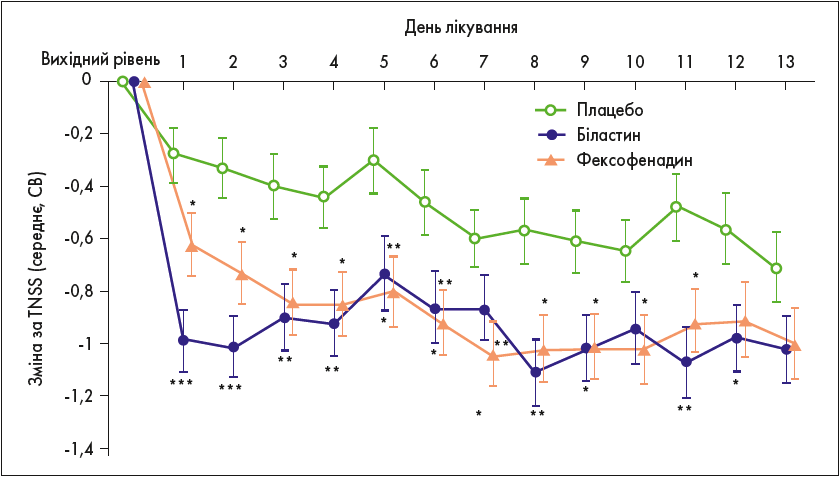 Рис. 3. Щоденна зміна TNSS від вихідного рівня протягом періоду лікування для біластину, фексофенадину та плацебо (Okubo K. et al., 2017)
Рис. 3. Щоденна зміна TNSS від вихідного рівня протягом періоду лікування для біластину, фексофенадину та плацебо (Okubo K. et al., 2017)
Отже, біластин (Ніксар) забезпечує ефективний контроль над симптомами АР уже в 1-й день прийому, що зберігається протягом усього періоду лікування.
Для оцінки профілю безпеки біластину (Ніксар) у пацієнтів із COVID‑19 необхідно зрозуміти патогенетичні зміни, які супроводжують і визначають перебіг та зумовлюють розвиток ускладнень (рис. 4).
 Рис. 4. Різні варіанти клінічного перебігу COVID‑19 та траєкторії адаптивної імунної відповіді й поширення вірусу (Matricardi P.M. et al., 2020)
Рис. 4. Різні варіанти клінічного перебігу COVID‑19 та траєкторії адаптивної імунної відповіді й поширення вірусу (Matricardi P.M. et al., 2020)
Від моменту інфікування SARS-CoV‑2 і до появи перших симптомів пацієнт може безсимптомно виділяти вірус у навколишнє середовище протягом 5 днів. При появі симптомів більш як у 80% інфікованих перебіг захворювання вважається легким або помірним. Це зумовлено наявністю вродженого природного механізму імунного захисту, представленого IgM, IgА та манозозв’язувальним лектином (MЗЛ) у слизовій респіраторного тракту. При зниженні напруженості вродженого імунітету перебіг захворювання більш тяжкий, а якщо зниження імунітету поєднується з високим рівнем вірусного навантаження, COVID‑19 може ускладнюватися ДН та іншими станами, які в кінцевому рахунку призведуть до смерті.
У нормі в осіб зі збереженим природним імунітетом і помірним вірусним навантаженням через 2 тиж після маніфестації захворювання можна виявити невелике підвищення IgG. Цікаво те, що в пацієнтів із тяжким перебігом рівень IgG буде дуже високим.
Імунологічні зміни, які супроводжують інфікування SARS-CoV‑2, описані в першій цілісній імунологічній моделі COVID‑19, створеній P. Matricardi та співавт. (2020).
Кількісний баланс між вродженим імунітетом (природні антитіла IgM та IgA, MЗЛ) та кумулятивною експозиційною дозою SARS-CoV‑2 є вирішальним фактором, який визначає швидкість проникнення вірусу в нижні дихальні шляхи та альвеоли. Якщо це відбувається до формування адаптаційної імунної відповіді, SARS-CoV‑2 швидко розмножується й викликає тяжку пневмонію.
Ще одним фактором, який підвищує кумулятивну експозиційну дозу SARS-CoV‑2, окрім відсутності або неправильного використання ЗІЗ, є дихання ротом. При інтенсивних заняттях спортом люди зазвичай починають дихати через рот. У слизовій рота відсутні фактори природного захисту (IgM та IgA, MЗЛ), здатні зв’язувати частину вірусних часток. Якщо під час інкубаційного періоду та на ранніх стадіях захворювання спортсмен дихає ротом, він вдихає не лише гетерологічні (тобто від інших інфікованих спортсменів), але й власні вірусні частинки, що містяться у видихуваному повітрі. У результаті SARS-CoV‑2 повторно вдихається та проникає в нижні дихальні шляхи та альвеоли (гіпотеза вірусної аутоінгаляції). Це явище спричинює ранню тяжку пневмонію в молодих здорових людей, які не мають супутньої патології.
Якщо вірус вже досяг альвеол і відбулася його масивна реплікація, ускладнення можуть виникнути при виробленні високоафінних антитіл. Хоча антитіла можуть обмежувати інвазійну здатність вірусу, ненейтралізуючі антитіла також підсилюють інфекцію, активуючи систему комплементу, систему коагуляції та викликаючи цитокіновий шторм, спричинений IL‑6, що призводить до ускладнень.
Ускладнення COVID‑19 пов’язані з підвищеним ризиком тромбозу та проявляються тромбоемболією легеневої артерії, міокардитом та нефропатією. Безпечність біластину при всіх цих ускладненнях пояснюється його фармакологічними властивостями та фармакокінетичним профілем.
Такі АГП ІІ покоління, як лоратадин та дезлоратадин, метаболізуються печінкою. Це може впливати на систему коагуляції, і без того спровоковану інфекцією SARS-CoV‑2. Для біластину цей ризик не характерний, оскільки препарат не метаболізується в печінці.
Навіть якщо в пацієнта з COVID‑19 є ниркова недостатність, йому можна призначати біластин, не хвилюючися про профіль безпеки. Біластин не метаболізується, а виводиться в незміненому вигляді з калом (67%) та із сечею (33%). Якщо нирки не працюють через COVID‑19, вмикається механізм шунтування, і виведення препарату більшою мірою забезпечує печінка (Jauregizar N. et al., 2009).
Кардіоваскулярна безпека біластину оцінювалася в дослідженні В. Tyl та співавторів. Було показано, що біластин не індукував подовження інтервалу QT, навіть у дозі, яка перевищувала терапевтичну вп’ятеро (Tyl B. et al.). Таким чином, біластин безпечний для застосування в пацієнтів із серцево-судинними ускладненнями, пов’язаними з COVID‑19.
Представники ініціативної групи ARIA створили чек-лист з оцінки фармакологічних властивостей, фармакодинаміки, ефективності та побічних реакцій усіх пероральних АГП ІІ покоління. Саме біластин (Ніксар) відповідає всім необхідним вимогам, представленим у цьому документі.
Це означає, що є всі підстави вважати біластин препаратом вибору, який може безпечно та ефективно використовуватися пацієнтами з АЗ як без COVID‑19, так і інфікованим SARS-CoV‑2. Дозу препарату не потрібно корегувати пацієнтам похилого віку та хворим із порушеною функцією нирок або печінки, а зручний режим прийому (1 таблетка 1 раз на добу) забезпечує високу прихильність до лікування. Це напряму впливає на ступінь контролю над симптомами захворювання, а отже – мінімізує кількість відвідувань сімейного лікаря, що зменшує ризик інфікування SARS-CoV‑2.
Література
- American Academy of Allergy, Asthma & Immunology. An Update on COVID‑19 for the Practicing Allergist/immunologist, 2020. https://education.aaaai.org/resources-for-a-i-clinicians/Update-for-AI_COVID‑19
- Pfaar O. et al. (2020). COVID‑19 pandemic: Practical considerations on the organization of an allergy clinic – an EAACI/ARIA Position Paper. https://onlinelibrary.wiley.com/doi/pdfdirect/10.1111/all.14453
- Klimek L. et al. (2020). Allergen immunotherapy in the current COVID‑19 pandemic: A position paper of AeDA, ARIA, EAACI, DGAKI and GPA: Position paper of the German ARIA GroupA in cooperation with the Austrian ARIA GroupB, the Swiss ARIA GroupC, German Society for Applied Allergology (AEDA)D, German Society for Allergology and Clinical Immunology (DGAKI)E, Society for Pediatric Allergology (GPA)F in cooperation with AG Clinical Immunology, Allergology and Environmental Medicine of the DGHNO-KHCG and the European Academy of Allergy and Clinical Immunology (EAACI)H. Allergologie select, 4, 44-52. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7304289/
- Klimek, Ludger et al. Handling of allergen immunotherapy in the COVID‑19 pandemic: An ARIA-EAACI statement. Allergy vol. 75,7 (2020): 1546-1554. doi:10.1111/all.14336. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7264744/
- Matricardi P.M., Kuna P., Panetta V., Wahn U., Narkus A. Subcutaneous immunotherapy and pharmacotherapy in seasonal allergic rhinitis: a comparison based on meta-analyses. J Allergy Clin Immunol. 2011 Oct;128(4):791-799.e6. https://www.jacionline.org/article/S0091-6749(11)00662-2/fulltext
- Okubo K., Gotoh M., Asako M., Nomura Y., Togawa M. et al. Efficacy and safety of bilastine in Japanese patients with perennial allergic rhinitis: A multicenter, randomized, double-blind, placebo-controlled, parallel-group phase III study. Allergol Int. 2017 Jan;66(1):97-105. https://www.sciencedirect.com/science/article/pii/S1323893016300855?via%3Dihub
- Matricardi P. M. et al. The first, holistic immunological model of COVID‑19: Implications for prevention, diagnosis, and public health measures. Pediatric allergy and immunology: official publication of the European Society of Pediatric Allergy and Immunology vol. 31,5 (2020): 454-470. https://onlinelibrary.wiley.com/doi/10.1111/pai.13271
- Jauregizar N., de la Fuente L., Lucero M.L. et al. Pharmacokinetic-pharmacodynamic modelling of the antihistaminic (H1) effect of bilastine. Clin Pharmacokinet. 2009;48(8):543-54. https://pubmed.ncbi.nlm.nih.gov/19705924/
- Tyl B., Kabbaj M., Azzam S., Sologuren A. et al. Lack of significant effect of bilastine administered at therapeutic and supratherapeutic doses and concomitantly with ketoconazole on ventricular repolarization: results of a thorough QT study (TQTS) with QT-concentration analysis. J Clin Pharmacol. 2012 Jun;52(6):893-903. https://pubmed.ncbi.nlm.nih.gov/21642470/
Підготувала Ганна Кирпач
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (53), 2020 р.