20 лютого, 2021
Діагностика та лікування есенціальної гіпертензії у дорослих пацієнтів в амбулаторній практиці
Ми продовжуємо знайомити читачів із практичними настановами найкращих медичних центрів світу. Представляємо огляд оновлених рекомендацій з есенціальної гіпертензії 2019 року від колективу медичної школи Мічиганського державного університету (м. Енн-Арбор, штат Мічиган, США).
Діагностика артеріальної гіпертензії
Вимірювання артеріального тиску
Офісні обчислення артеріального тиску (АТ) слід проводити у спокійному оточенні, після 5-хвилинного відпочинку пацієнта, у положенні сидячи, з опорою ніг на підлогу, а рук – на стіл на рівні серця. Перше вимірювання потрібно виконувати на обох руках, і якщо АТ однаковий, вибір руки надалі не має значення. Проте бажано все ж фіксувати показники на одній руці, що забезпечить вищу достовірність результатів. Упродовж 30 хвилин до вимірювання пацієнти не повинні курити, вживати кофеїн та робити фізичні вправи. Хворих слід інформувати про результати обчислення, їхнє значення та план наступного спостереження. Автоматизоване офісне вимірювання АТ має переваги над неавтоматизованим. Підвищення АТ при офісному обчисленні має бути підтверджене домашнім. Оцінку серцево-судинного (СС) ризику краще проводити за середнім показником АТ, визначеним відповідно до результатів, отриманих під час кількох візитів.
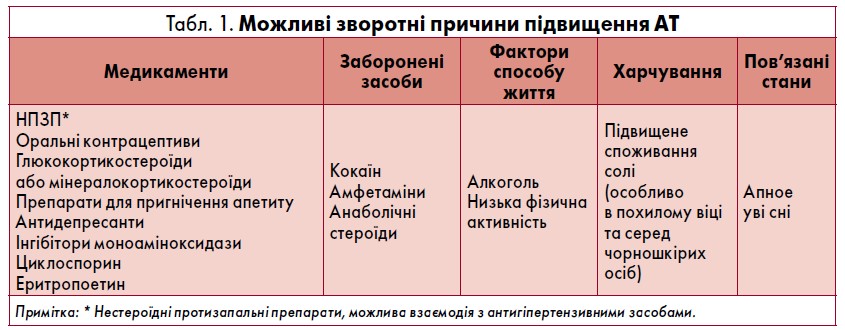
Частота повторних вимірювань АТ залежить від початкового рівня АТ та ступеня артеріальної гіпертензії (АГ). Якщо при першому вимірюванні АТ нормальний (<120/80 мм рт. ст.), надалі потрібно вимірювати АТ принаймні один раз на рік (думка експертів). Краще фіксувати АТ на кожному візиті. Якщо початковий рівень АТ відповідає прегіпертензії (120‑139/80‑89 мм рт. ст.), слід вимірювати АТ кожні шість місяців. Якщо АТ ≥140/90 мм рт. ст., варто обстежити пацієнта для виявлення зворотних причин АГ, які можна усунути (табл. 1). Аортальна регургітація може зумовити розвиток ізольованої систолічної АГ.
Класифікація АГ та план ведення пацієнта
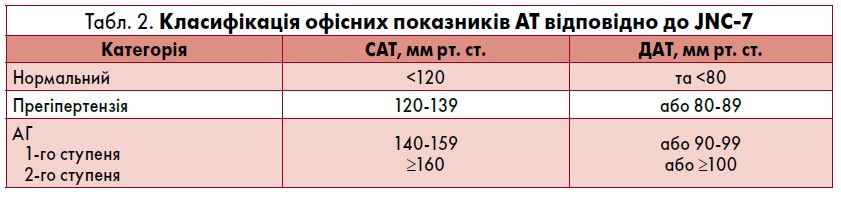
Національні та міжнародні рекомендації по-різному визначають АГ. Актуальною залишається класифікація, надана у 7-й доповіді Об’єднаного національного комітету з попереджання, розпізнання, оцінки й лікування підвищеного АТ США (JNC‑7) (табл. 2), поки не буде досягнуто нового експертного консенсусу. Згідно з настановою Американської колегії кардіологів та Американської асоціації серця (АСС/АНА, 2017), АГ визначено як АТ ≥130/80 мм рт. ст. Проте, відповідно до канадських рекомендацій 2018 р., а також документа Європейського товариства кардіологів (ESC) та Європейського товариства гіпертензії (ESH), АГ встановлюють, якщо АТ ≥140/90 мм рт. ст. за даними офісного вимірювання. В усіх настановах наголошено на значущості зростання АТ ≥130/80 мм рт. ст. в осіб із підвищеним СС-ризиком.
Моніторування АТ у домашніх умовах можна проводити двома способами:
- Домашній моніторинг АТ (ДМАТ) – пацієнт або особа, що доглядає за ним, записують параметри АТ, зафіксовані домашнім тонометром. Цей спосіб потребує певної обізнаності та навчання правильній техніці вимірювання. Перевагу слід надавати тонометрам із плечовою манжетою, оскільки реєстрування показників на зап’ясті та пальцях дають недостовірні результати. В умовах клініки варто переконатися у правильності техніки вимірювання та перевірити калібрування домашнього тонометра, якщо результати моніторування АТ вдома планується брати за основу при прийнятті терапевтичних рішень.
- Амбулаторне моніторування АТ (АМАТ) – автоматизовані вимірювання АТ поза клінікою за допомогою спеціального приладу для носіння протягом певного періоду часу (зазвичай 24 год). Це вартісний, але надійний спосіб отримання інформації про АТ пацієнта. Результати АМАТ на додачу до офісних вимірювань допомагають точніше визначати СС-ризик.
ДМАТ і АМАТ допомагають виявляти пацієнтів, у яких АТ, виміряний на візитах до клініки, відрізняється від такого за її межами. Також ці методи здатні виявляти випадки резистентної АГ.
АГ білого халата (синдром «білого халата») визначається як підвищений АТ під час візитів до лікарні при нормальних значеннях поза її межами. Цей стан досить поширений (понад 20% пацієнтів із підвищеним АТ) і може призводити до призначення хибного лікування, якщо не буде розпізнаний. Показники ДМАТ і АМАТ можуть допомагати у виявленні такої АГ.
Маскована АГ визначається як підвищений АТ у домашніх умовах при нормальних значеннях на візитах до клініки. Цей стан майже так само поширений, як АГ білого халата. Пацієнти можуть мати гіпертрофію лівого шлуночка (ЛШ) або ж ураження інших органів-мішеней незважаючи на наявні нормальні показники офісного АТ. Як ДМАТ, так і АМАТ нерідко допомагають у виявленні маскованої АГ, після чого може бути проведено інтенсифікацію терапії для покращення СС-прогнозу.
Лабораторні тести та діагностичні процедури при первинному зверненні
Пацієнтам із вірогідно есенціальною гіпертензією до початку терапії слід призначити діагностичні тести/аналізи та виміряти показники, як-то:
- електрокардіографія (ЕКГ);
- рівень глюкози у крові;
- вміст креатиніну;
- рівень кальцію;
- рівень калію;
- аналіз на гематокрит;
- ліпідна панель;
- загальний аналіз сечі.
Скринінг на цукровий діабет (ЦД) має особливе значення.
Вторинну або ускладнену АГ слід запідозрити за відсутності відповіді на звичайні заходи зниження АТ, якщо раніше контрольована АГ стала неконтрольованою, а також коли спостерігаються раптове підвищення АТ, злоякісна АГ. У разі підозри на вторинну та/або ускладнену АГ варто розглянути інші діагностичні тести та/або направлення для отримання спеціалізованої допомоги.
Можливі причини вторинної та/або ускладненої АГ:
- хронічне чи гостре захворювання нирок;
- реноваскулярна гіпертензія;
- апное уві сні;
- первинний альдостеронізм;
- коарктація аорти;
- постійна терапія кортикостероїдами, синдром Кушинга;
- феохромоцитома.
- захворювання щитоподібної або паращитоподібних залоз.
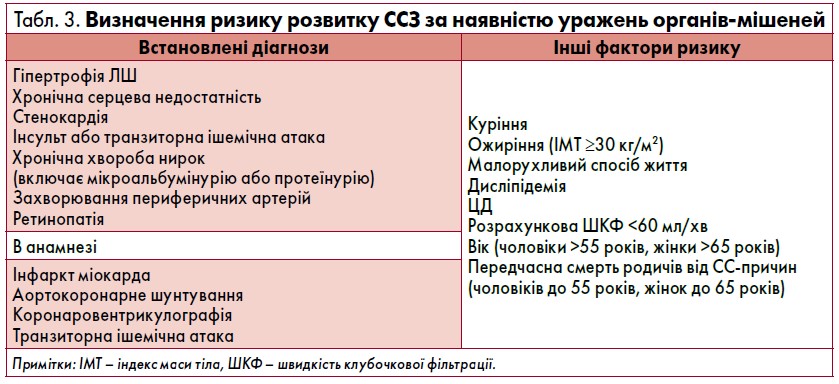
Ризик розвитку серцево-судинних захворювань (ССЗ) у пацієнтів з АГ визначається не лише рівнем АТ, але й наявністю уражень органів-мішеней (табл. 3).
Лікування АГ
Цільові значення АТ визначають залежно від виявленої сукупності факторів ризику. Для пацієнтів без атеросклеротичного серцево-судинного захворювання (АСССЗ), тих, що мають розрахунковий 10-річний ризик АСССЗ <10%, а також осіб без хронічної хвороби нирок (ХХН) метою лікування є рівень систолічного АТ (САТ) <140 мм рт. ст., діастолічного АТ (ДАТ) <90 мм рт. ст.
Ризик АСССЗ обчислюють за допомогою калькулятора АСС/АНА. Для пацієнтів з АСССЗ, тих, що мають розрахунковий 10-річний ризик АСССЗ ≥10% або ХХН, цільовий АТ становить <130/80 мм рт. ст., якщо відсутня імовірність розвитку гіпотензії (немає ортостатичної гіпотензії, серцевої недостатності, вік не старечий). Варто розглядати цільовий АТ <140/90 мм рт. ст., коли наявні фактори ризику гіпотензії. Хворих на ХХН стадій 3В‑5 слід обстежувати частіше через підвищену вірогідність появи гіперкаліємії.
Дані клінічних досліджень, розглянуті у JNC‑7, підтримують зниження САТ до <140 мм рт. ст. та ДАТ до <90 мм рт. ст. Цю рекомендацію було підтверджено групою експертів 8-го Об’єднаного національного комітету для вікових груп до 60 років. Згідно з JNC‑8, у пацієнтів ≥60 років рекомендовано знижувати САТ до <150 мм рт. ст., ДАТ до <90 мм рт. ст. У настанові ACC/AHA (2017) йдеться про доцільність зниження САТ і ДАТ до <130 та <80 мм рт. ст. відповідно на підставі нових результатів, отриманих у дослідженні SPRINT. Було показано, що пацієнти з підвищеним АТ і ризиком АСССЗ отримують додаткове покращення клінічного прогнозу при агресивнішому лікуванні АГ, зокрема, більшому зниженні САТ.
У настановах поза межами США, як-то канадські та європейські (ESC/ESH, 2018), вказано цільовий САТ <140 мм рт. ст. і ДАТ <90 мм рт. ст. для дорослих без ризику, а також САТ і ДАТ <130 та <80 мм рт. ст. відповідно – за наявності ризику. В усіх рекомендаціях наголошено на необхідності точних автоматизованих вимірювань офісного офісного або домашнього АТ. Стійке зниження САТ на 10 мм рт. ст. або ДАТ на 5‑6 мм рт. ст. у пацієнтів з АГ скорочує вірогідність розвитку інсульту на 35‑40%, а ішемічної хвороби серця (ІХС) – на 20‑25%.
В осіб із ЦД цілі зниження АТ вивчали у кількох рандомізованих дослідженнях, зокрема ACCORD. У випробування SPRINT не включали хворих на ЦД. У цієї категорії пацієнтів доцільним визнане зниження ДАТ до 90, а також 80 мм рт. ст. Необхідно слідкувати, щоб ДАТ був не нижчим за 70 мм рт. ст., оскільки такі показники асоціюються з підвищеним ризиком смерті.
Вибір терапії
Зміни способу життя рекомендовані всім пацієнтам із підвищеним АТ. До них належать: нормалізація маси тіла, обмеження вживання алкоголю та солі до 2,4 г/день, підтримання адекватного рівня фізичних навантажень, відмова від куріння. Інші дієтичні чинники також мають значення. Споживання продуктів, багатих на кальцій, може зумовлювати дуже незначне зниження АТ (САТ -1,27; ДАТ -0,24 мм рт. ст.). Немає даних стосовно ефекту магнію на рівень АТ. Харчові жири не впливають на АТ. Ситуативне вживання кофеїну може підвищувати АТ, проте якщо робити це часто, ефект зазвичай нівелюється звиканням. Дотримання раціону харчування з низьким вмістом натрію та насичених жирів, що збагачений овочами, фруктами та молочними продуктами низької жирності, сприяє зниженню АТ (дієта DASH).
Потреба в медикаментозній терапії визначається ступенем тяжкості АГ та іншими факторами ризику. Пацієнтам із прегіпертензією, але без чинників ризику чи уражень органів-мішеней слід надавати рекомендації щодо корекції способу життя. Особам з АГ 1-го ступеня та без факторів ризику можна рекомендувати пробну модифікацію способу життя протягом 12 місяців. Проте у світлі доказів користі від раннього зниження АТ до цільових рівнів більшість експертів наголошують вже при АГ 1-го ступеня призначати медикаментозну терапію разом із корекцією способу життя. Згодом, після досягнення цільового рівня АТ, можна спробувати знизити дозу або відмінити препарати, якщо модифікація способу життя виявилася успішною.
Пацієнти з АГ 2-го ступеня, що мають ЦД або ураження органів-мішеней, повинні отримувати медикаментозну терапію разом із корекцією способу життя. Початкова комбінація тіазидного діуретика з іншим антигіпертензивним засобом є раціональною. Хворі, які недостатньо відповідали на попередню терапію або демонструють знижений комплаєнс, можуть отримати переваги від початкової сумісної терапії.
Вибір препаратів. За даними численних рандомізованих контрольованих досліджень, тіазидні діуретики у середніх/високих дозах (наприклад, хлорталідон по 25 мг/добу) так само ефективні, як і препарати інших класів, щодо зниження ризику СС-подій і мають переваги у профілактиці інсульту та хронічної серцевої недостатності (ХСН). Більшість пацієнтів потребуватимуть призначення ≥2 ліків для досягнення контролю, і з них лише у невеликої частки спостерігатиметься непереносимість тіазидних діуретиків.
Вибір додаткового або альтернативного препарату має бути індивідуалізованим для досягнення цільового АТ з огляду на наступні вимоги:
- приймання препаратів один раз на день;
- зниження ризику СС-ускладнень, продемонстроване у клінічних дослідженнях;
- вибір з огляду на лікування супутніх станів;
- потенційно менший тягар побічних ефектів з урахуванням коморбідних станів та способу життя;
- прийнятна вартість лікування;
- фіксовані комбінації можуть бути фармакоекономічно вигідними і покращувати комплаєнс.
Всі лікарські засоби, що належать до одного класу, мають схожі фізіологічні ефекти. Виключенням є блокатори кальцієвих каналів (БКК) та β-блокатори, серед яких виділяють підкласи з відмінними фізіологічними ефектами. Якщо монотерапія неефективна у досягненні цільового АТ, слід додати другий препарат або замінити на такий іншого класу з фізіологічними ефектами, що різняться. Поєднання ліків, які належать до одного класу, не є раціональним.
Згідно з результатами рандомізованих контрольованих досліджень, діуретики, β-блокатори, інгібітори ангіотензинперетворювального ферменту (АПФ) та дигідропіридинові БКК тривалої дії виявили здатність зменшувати захворюваність та смертність, пов’язані з СС-подіями. У великому багатоцентровому рандомізованому випробуванні ALLHAT проводили пряме зіставлення старих і нових антигіпертензивних засобів у профілактиці захворюваності та смертності через ССЗ. Дослідники порівнювали початкові режими терапії з використанням тіазидних діуретиків, іПФ, БКК тривалої дії та α-блокатора. Бета-блокатори і препарати центральної дії застосовували як другу лінію лікування; майже три чверті пацієнтів потребували призначення двох або більше ліків.
Бета-блокатори використовували для підсилення терапії найчастіше. Гілку дослідження із призначенням α-блокатора зупинили достроково через значні побічні ефекти. Всі інші ліки показали зіставну ефективність за первинною кінцевою точкою (здатністю попереджати коронарні події). Тіазидний діуретик (хлорталідон) у середніх та високих дозах виявив перевагу за вторинними критеріями ефективності (інсульт і ХСН). Ці результати відтворювалися в усіх вікових групах і клінічних підгрупах, зокрема у пацієнтів із ЦД, ІХС та гіперліпідемією.
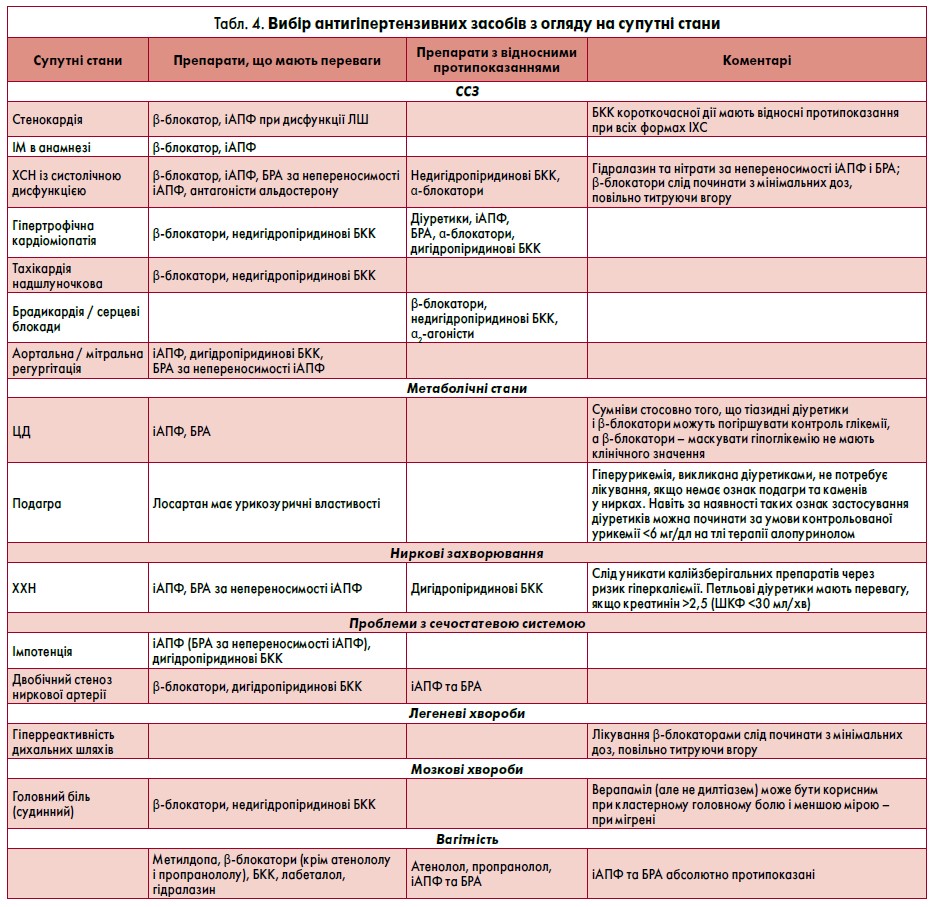
Наявність інших факторів ризику, супутніх захворювань та профілі побічних ефектів можуть впливати на вибір засобів для первинної терапії. Для початку лікування однаковою мірою підходять іАПФ, блокатори рецепторів ангіотензину (БРА) та БКК. Не слід надавати перевагу β-блокаторам у межах початкової терапії в пацієнтів похилого віку, якщо немає інших підстав для їхнього призначення, таких як ішемічна хвороба серця або ХСН (табл. 4). У нещодавніх метааналізах виявлено, що β-блокатори можуть бути менш ефективними у профілактиці інсульту порівняно з іншими класами антигіпертензивних засобів.
Немає чітких рекомендацій стосовно вибору певних лікарських комбінацій на підставі даних про користь щодо поліпшення клінічного прогнозу (наприклад, іАПФ/БКК чи іАПФ/діуретик). Масштабні, добре сплановані дослідження, як-то ACCOMPLISH, де порівнювали сумісне застосування беназеприлу/амлодипіну та беназеприлу/гідрохлоротіазиду, а також ACCELERATE – аліскірен та амлодипін проти монотерапії кожним із компонентів, дозволяють припустити, що комбінація блокатора ренін-ангіотензинової системи та БКК може мати переваги над іншими комбінаціями і режимами монотерапії. Спільне використання іАПФ/БРА, іАПФ / прямого інгібітора реніну та БРА / прямого інгібітора реніну не рекомендоване при веденні пацієнтів з АГ.
Моніторування АТ
У дослідженнях не визначено оптимального методу контролю за досягненням цілей антигіпертензивної терапії. Тому наступні рекомендації відображають консенсусну думку робочої групи.
Вимірювання АТ. Усіх пацієнтів, в яких встановлено діагноз АГ, слід навчати домашньому моніторуванню АТ. Хворим варто рекомендувати придбати електронний тонометр для самостійних вимірювань із манжетою належного розміру. Автоматичні (самонадувні) та напівавтоматичні електронні пристрої однаково ефективні. Напівавтоматичні коштують дешевше, але складніші у використанні.
Пацієнтів слід проінструктувати фіксувати АТ щоденно, щонайменше двічі – одразу після пробудження та перед вечерею (можна додатково вимірювати і в інший час) до досягнення цільового рівня АТ на тлі терапії. Після стабілізації контролю АТ достатньо вимірювати АТ щомісяця. Показники слід записувати в щоденник і надавати лікареві. Пристрої, що вимірюють АТ на зап’ясті та пальцях, не варто використовувати для моніторування.
Прегіпертензія. Повторні вимірювання АТ слід виконувати принаймні щорічно.
АГ 1-го ступеня. Після призначення антигіпертензивної терапії більшість пацієнтів потребують її корекції під час щомісячних візитів або частіше, доки не буде досягнуто цільового рівня АТ. Антигіпертензивний ефект препаратів зазвичай стабілізується протягом перших двох тижнів. На кожному візиті слід вимірювати АТ, проводити оцінку побічних ефектів, прихильності хворого до терапії, нових уражень органів-мішеней, якщо вони з’являються.
Якщо протягом 1‑3 місяців АТ не знижується до цільового рівня:
- Слід переконатися, що пацієнт виконує призначення.
- Потрібно перевірити, чи є доза препарату достатньою.
- Варто переконатися у відсутності зворотних причин АГ (табл. 1).
- Необхідно додати другий препарат з іншого класу.
Після досягнення стійкого цільового рівня АТ наступні візити для спостереження можна планувати з інтервалом 3‑6 місяців. Принаймні щорічно слід визначати сироваткові рівні калію та креатиніну. Також може бути корисним аналіз на мікроальбумінурію.
АГ 2-го ступеня. Рекомендації зі спостереження загалом ті самі, що для осіб з АГ 1-го ступеня. Проте може виникати потреба у частіших візитах для корекції медикаментозної терапії, поки не буде досягнуто контролю над АТ.
Додаткові коментарі. Більшість пацієнтів потребуватимуть призначення двох або більше препаратів для досягнення мети. Комбінації ліків із фіксованими дозами можуть спрощувати режим терапії та сприяти прихильності, але генеричні засоби поодинці зазвичай дешевші. Якщо АТ не піддається контролю після кількох спроб оптимізації лікування або призначення комбінацій трьох та більше препаратів, слід направити пацієнта для отримання спеціалізованої медичної допомоги (до фахівця з АГ). Непереносимість лікарських засобів може бути ознакою неналежної терапії через виразний ефект «білого халата». В таких випадках цінну інформацію можна отримати при проведенні амбулаторного або домашнього моніторування АТ.
Резистентна АГ визначається як недосягнення цільового АТ у пацієнтів, що прихильні до лікування і приймають належно підібрані комбінації з трьох препаратів у повних дозах, одним з яких є діуретик.
Після виключення альтернативних причин АГ слід переглянути терапію і спробувати визначити причину недосягнення цільового АТ. Особливої уваги потребує вибір типу та режиму приймання діуретиків з огляду на функцію нирок. Так, тіазидні діуретики втрачають свій ефект при зниженні ШКФ до рівня <30 мл/хв. У складних випадках слід направити пацієнта на консультацію до спеціаліста з АГ.
Особливі категорії пацієнтів
АГ у вагітних. Вагітні з неускладненою АГ 1-го ступеня зазвичай не потребують лікування, якщо в них низький розрахунковий СС-ризик, нормальна функція нирок і немає уражень інших органів-мішеней. За цими жінками слід уважно спостерігати протягом вагітності. Прееклампсію або інші види АГ, пов’язані з вагітністю, слід лікувати у фахівця, обізнаного з такими станами. Якщо жінка з АГ, що потребує лікування, планує вагітність, вона має приймати антигіпертензивні препарати протягом 3‑6 місяців до зачаття.
Для терапії АГ під час вагітності рекомендовані наступні препарати (в порядку переваги):
- Метилдопа – препарат із найбільшим досвідом застосування. Слабкими сторонами є часті побічні ефекти та необхідність приймання кілька разів на день.
- Бета-блокатор із/без діуретика (варто уникати застосування атенололу, який може викликати затримку внутрішньоутробного росту плода) – відносно популярні й часто використовуються як препарати першої лінії.
- Лабеталол.
- БКК.
Діуретики також є прийнятними лікарськими засобами. При вагітності протипоказані іАПФ, БРА та інгібітори реніну.
Продовження скринінгу на ЦД. Такі терапевтичні заходи рекомендовані при вперше виявленому підвищенні АТ >135/80 мм рт. ст. Для пацієнтів з АГ оптимальний інтервал скринінгу не встановлений. Американська діабетична асоціація (ADA), спираючись на думку експертів, рекомендує проводити скринінг на ЦД з інтервалами три роки.
Пацієнти похилого віку. Користь від лікування АГ у старшій віковій категорії добре обґрунтована. В дослідженні HYVET підтверджене суттєве зниження СС-ризику та смертності внаслідок терапії АГ у пацієнтів після 80 років при досягненні цільового рівня 150/80 мм рт. ст. Від наступного зниження АТ <150 мм рт. ст. чітких переваг не встановлено. Зменшення ДАТ <65 мм рт. ст. теоретично підвищує ризик. Не визначено відносного ризику зниження САТ <150 мм рт. ст., якщо така терапія також впливає на зменшення ДАТ до значень <65 мм рт. ст.
Ортостатичне падіння АТ є поширеною проблемою в похилому віці. Для виявлення ортостатичної АГ у літніх осіб, які отримують антигіпертензивну терапію, слід вимірювати АТ у положенні лежачи і стоячи. Вибір препаратів для лікування АГ у даної когорти хворих проводять за тими самими принципами, що і в решті вікових груп. Застосування β-блокаторів слід уникати, якщо немає переконливих показань окрім АГ, таких як ІХС або ХСН. У похилому віці рекомендовано починати терапію з нижчих доз і повільніше їх титрувати.
Підготував Сергій Романюк
Оригінальний текст документа,
включно зі списком літератури, читайте на сайті www.med.umich.edu
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 6 (73) 2020 р.