15 березня, 2021
НПЗП у лікуванні больових синдромів: на першому місці – питання безпеки
Найпопулярнішим інструментом аналгетичної терапії в медичній практиці завдяки поєднанню ефективності, безпеки, доступності та зручності застосування є нестероїдні протизапальні препарати (НПЗП). Вони швидко й ефективно долають гострі больові синдроми (БС), а в лікуванні деяких хронічних захворювань (зокрема, ревматичних) відіграють роль не тільки симптомомодифікувальної, а й патогенетичної терапії, сповільнюють прогресування патологічного процесу.
Якщо передбачувана тривалість лікування НПЗП ≥4 тиж (навіть у разі епізодичного чи прийому ліків на вимогу), вважається, що пацієнт застосовує НПЗП хронічно; це асоціюється зі збільшенням ризику розвитку побічних ефектів. Безпека цього класу засобів і стратегії профілактики НПЗП-асоційованих побічних ефектів регулярно стають темою для обговорення під час спеціалізованих медичних заходів.
Ефективність і безпека НПЗП: розвіюємо міфи
 Вибору НПЗП з огляду на ефективність і безпеку в терапевтичній практиці присвятила online-доповідь у рамках Міжнародного науково-практичного форуму «Сучасна сімейна медицина в розрізі різних спеціальностей, експертна думка» (25-26 листопада 2020 року) доктор медичних наук, професор Єлизавета Давидівна Єгудіна.
Вибору НПЗП з огляду на ефективність і безпеку в терапевтичній практиці присвятила online-доповідь у рамках Міжнародного науково-практичного форуму «Сучасна сімейна медицина в розрізі різних спеціальностей, експертна думка» (25-26 листопада 2020 року) доктор медичних наук, професор Єлизавета Давидівна Єгудіна.
– Однією з найважливіших характеристик НПЗП, що визначає їхній протизапальний потенціал і значно впливає на профіль безпеки, є селективність щодо ізоформ ферменту циклооксигенази (ЦОГ). Цей показник оцінюють за співвідношенням ступеня інгібування ЦОГ‑1 до ЦОГ‑2: якщо коефіцієнт >1:5, НПЗП вважається селективним, >1:50 – високоселективним.
До неселективних НПЗП належать диклофенак, ібупрофен, індометацин, кеторолак, кетопрофен, напроксен тощо; до селективних інгібіторів ЦОГ‑2, що менше впливають на ЦОГ‑1, – лорноксикам, мелоксикам, набуметон, німесулід тощо; до високоселективних інгібіторів ЦОГ‑2, що в терапевтичних дозах практично не діють на ЦОГ‑1, – парекоксиб, рофекоксиб, целекоксиб, еторикоксиб тощо.
Доведено, що за тривалого/постійного застосування НПЗП (доволі поширена ситуація в практиці ревматолога) зростає кумулятивна частота появи побічних ефектів, тому правильний вибір препарату з позиції «користь/ризик» є вкрай важливим. Для короткострокового/епізодичного прийому за інтенсивного БС (наприклад, у разі гострого подагричного артриту (ГПА), гострого БС у нижній ділянці спини (БНС) тощо) рекомендуються засоби з потужною дією. У метааналізі W. Stam і співавт. (29 досліджень, >18 тис. пацієнтів) установлено, що максимальну знеболювальну активність за остеоартрозу (ОА) мали диклофенак і еторикоксиб. Метааналіз 74 досліджень (>58 тис. учасників), проведений B.R. da Costa та співавт. (2017), теж продемонстрував максимальний знеболювальний ефект диклофенаку 150 мг і еторикоксибу 60 мг, а також підтвердив, що цей ефект є дозозалежним. Аналгетичну активність напроксену, мелоксикаму науковці оцінюють як значно нижчу, що слід ураховувати при терапії гострих БС.
Істотних відмінностей в ефективності знеболення при різних способах застосування НПЗП (пероральному прийомі, внутрішньовенному (в/в), внутрішньом’язовому (в/м), внутрішньораневому введенні, використанні ректальних супозиторіїв) немає, за винятком переваги в/в уведення в разі ниркової кольки (Combe B. et al., 2001). Введення НПЗП в/в, в/м може розглядатись як короткочасна опція за гострого БС високої інтенсивності, зокрема в разі травм, ниркової та біліарної кольок, при хірургічних втручаннях, ГПА тощо (Motov S. et al., 2017; Fraquelli M. et al., 2016).
Золотим стандартом знеболення серед НПЗП вважається диклофенак; він максимально ефективно пригнічує синтез прозапального простагландину (ПГ) Е2 (на 93%, що перевищує показники рофекоксибу, мелоксикаму, ібупрофену, напроксену), а в дослідженні MELISSA продемонстрував кращу ефективність порівняно з мелоксикамом (Hawkey C. et al., 1998; Hecken A. et al., 2000). Початок дії диклофенаку (75 мг / 3 мл) спостерігається вже через 20 хв, максимальна концентрація в синовіальній рідині – через 2-4 год і підтримується приблизно 12 год (для мелоксикаму в/м 1,5 мл – 60-90 хв і 5-6 год відповідно).
Також для лікування гострого БС широко використовується німесулід. Висока концентрація препарату в крові відзначається вже через 30 хв, а знеболювальний і протизапальний ефекти реалізуються через 1-3 год після прийому.
Для тривалого використання (лікування ревматоїдного артриту, анкілозивного спондиліту) раджу обирати НПЗП із нижчим аналгетичним потенціалом, але кращим профілем безпеки. Також варто брати до уваги зміну парадигми стосовно призначення парацетамолу: в настановах із лікування ОА (2017) його рекомендували як засіб першочергового вибору, проте в останньому документі, що з’явився торік, ступінь доказовості рекомендації змінився із «сильний» на «дуже слабкий». Знеболювальна активність парацетамолу досить низька, а ризик гепатотоксичної дії є високим. Недоцільно застосовувати комбінацію парацетамолу та НПЗП в одній таблетці через потенційне збільшення ризику гепатотоксичності.
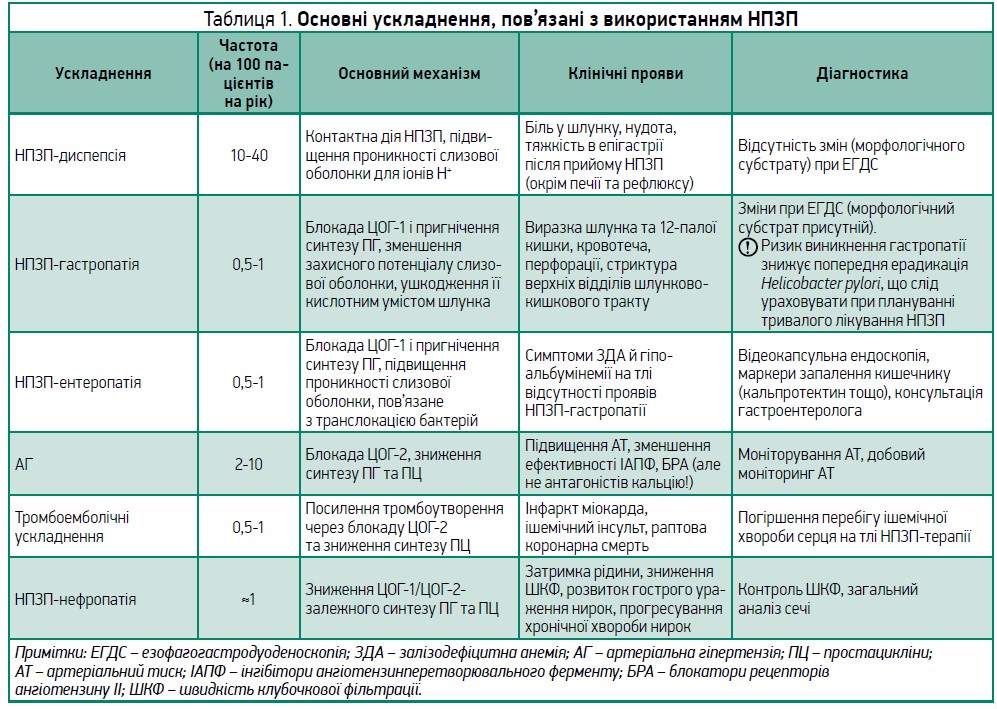
Слід розуміти, що повністю безпечних НПЗП не існує: кожному представнику класу притаманні гастро-, кардіо-, нефро- та гепатотоксичність. Основні НПЗП-асоційовані ускладнення наведено в таблиці 1.
Максимальне підвищення АТ фіксується через 4 тиж прийому НПЗП. Для контролю АГ рекомендуються регулярний моніторинг показників, оцінка затримки рідини. Якщо пацієнт уже отримує ІАПФ/БРА, не варто збільшувати їхню дозу; краще доповнити терапію антагоністами кальцію, адже вони є препаратами вибору в описаній ситуації.
Усі НПЗП збільшують імовірність серцево-судинних ускладнень: із максимальним ризиком асоціюється прийом еторикоксибу (1,97), меншим (за порядком зменшення) – етодолак, індометацин, диклофенак, рофекоксиб, мелоксикам, ібупрофен, целекоксиб, напроксен (Varas-Lorenzo C. et al., 2013). У пацієнтів із дуже високим серцево-судинним ризиком (ССР) краще уникати тривалої терапії НПЗП; із високим ССР – застосовувати їх з обережністю, в мінімальних дозах нетривалими курсами; з помірним ССР – обережно, в стандартних дозах; із низьким ССР дозволяється прийом будь-яких НПЗП (Cheuk-Chun Szeto et al., 2020).Деякі неселективні НПЗП (ібупрофен, напроксен, індометацин) здатні конкурувати з ацетилсаліциловою кислотою (АСК) за зв’язування з ЦОГ‑1 і нівелювати її кардіопротекторний ефект (Capone M. L. et al., 2005). Взаємодії кетопрофену, целекоксибу, диклофенаку й мелоксикаму з АСК не зафіксовано. Щоб уникнути можливої взаємодії, краще приймати АСК та НПЗП з інтервалом щонайменше 2 год або використовувати НПЗП із режимом застосування 1 р/добу та розділяти їх з АСК у часі. Якщо пацієнт приймає подвійну антиагрегантну терапію, то дозу та тривалість застосування НПЗП слід мінімізувати, а для запобігання появі гастроінтестинальних кровотеч – призначити інгібітори протонної помпи (ІПП).
Для лікування НПЗП-диспепсії рекомендовано ІПП, тоді як використання антацидів і блокаторів Н2-рецепторів небажане (Cheuk-Chun Szeto et al., 2020). Із метою запобігання НПЗП-гастропатії в пацієнтів із високим гастроінтестинальним ризиком рекомендується застосування селективних НПЗП + ІПП; помірним – неселективних НПЗП + ІПП або селективних НПЗП; низьким – допускається призначення будь-яких НПЗП. При ЗДА краще віддавати перевагу селективним НПЗП (Cheuk-Chun Szeto et al., 2020).
Усі НПЗП здатні зумовлювати порушення функції печінки (із зіставною частотою). В епідеміологічному дослідженні, що об’єднувало 400 тис. осіб, які приймали НПЗП, не виявили істотних відмінностей між німесулідом, диклофенаком, ібупрофеном та іншими препаратами групи щодо гепатотоксичного впливу (Traversa G. et al., 2003). Отримані дані допомогли розвіяти міф про високу гепатотоксичність і небезпеку німесуліду. Вказують на хорошу переносимість німесуліду й дані Європейського агентства з лікарських засобів (EMA, 2012, 2015): препарат визнано одним із 5 найбезпечніших для печінки НПЗП (разом із целекоксибом, диклофенаком, кетопрофеном, напроксеном); сприятливим із позиції впливу на гастроінтестинальний тракт і серцево-судинну систему (Cheuk-Chun Szeto et al., 2020).
Нефротоксичні реакції на тлі терапії НПЗП трапляються рідко, проте всі представники класу можуть провокувати порушення роботи нирок; даних на користь якогось із препаратів у ракурсі нефротоксичності немає. Пацієнтам із тяжкою хронічною нирковою недостатністю, а також помірною на тлі антигіпертензивної терапії (ІАПФ/БРА/діуретики) слід уникати прийому НПЗП; рекомендується моніторинг функції нирок до старту терапії та через тиждень від початку лікування, а також у разі затримки рідини та клінічних ознак погіршення функції нирок.
Тактика призначення НПЗП при БНС
 Професор кафедри анестезіології та інтенсивної терапії Національної медичної академії післядипломної освіти ім. П. Л. Шупика (м. Київ), доктор медичних наук Марина Анатоліївна Тріщинська під час виступу в рамках онлайн-заходу «Клініко-практичні аспекти в сучасній неврології» (24 листопада 2020 року) розглянула питання діагностики та лікування БС, зокрема БНС.
Професор кафедри анестезіології та інтенсивної терапії Національної медичної академії післядипломної освіти ім. П. Л. Шупика (м. Київ), доктор медичних наук Марина Анатоліївна Тріщинська під час виступу в рамках онлайн-заходу «Клініко-практичні аспекти в сучасній неврології» (24 листопада 2020 року) розглянула питання діагностики та лікування БС, зокрема БНС.
– Гострий біль (≈80% випадків) з’являється в результаті ушкодження тканин і триває <3 міс, має захисну роль, зникає після загоєння рани / ліквідації травми, швидко усувається на тлі терапії аналгетиками. Його класифікують як симптом – сигнал небезпеки. Хронічний біль (20% випадків) зберігається після усунення початкового ушкодження (існує незалежно від нього), триває >3 міс, не чинить захисної функції та не усувається за допомогою аналгетиків, спричиняє адаптацію й інвалідизацію, погіршує якість життя пацієнтів.
 Різні механізми появи болю взаємодоповнюються, умовно кажучи, «передають естафету» один одному. Якщо не усунути гострий БС вчасно, він трансформується в хронічний.
Різні механізми появи болю взаємодоповнюються, умовно кажучи, «передають естафету» один одному. Якщо не усунути гострий БС вчасно, він трансформується в хронічний.
Залежно від етіології виокремлюють декілька варіантів болю в спині (табл. 2).
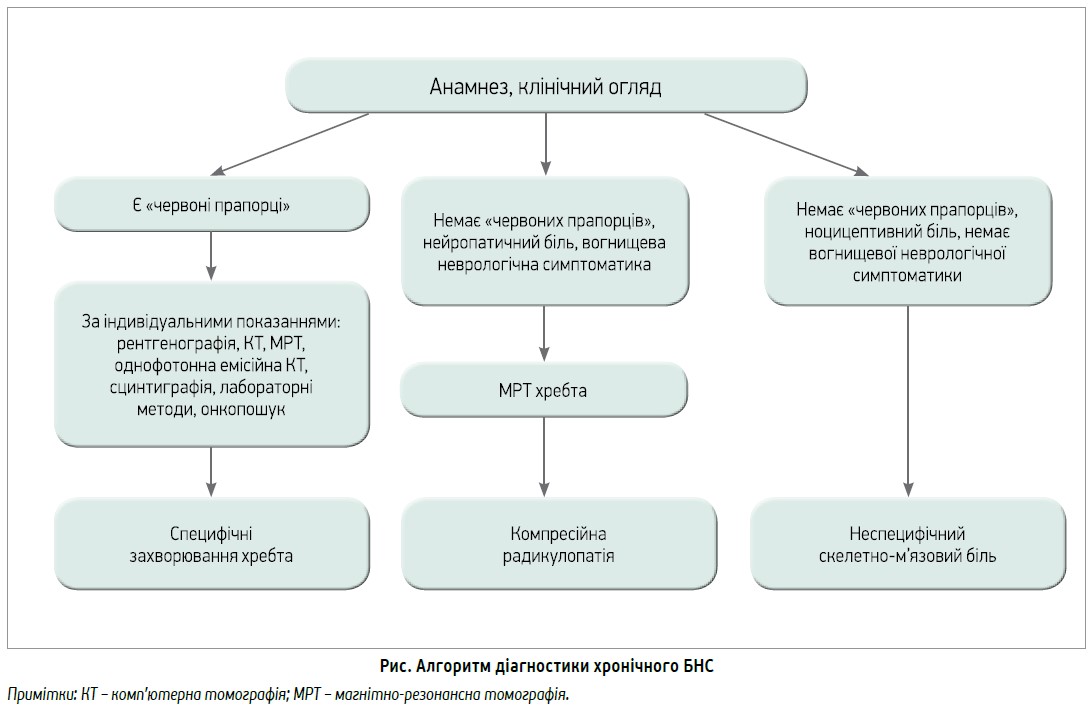
Алгоритм діагностики хронічного БНС наведено на рисунку.
Обрання терапевтичної тактики залежить від виду БС і наявності т. зв. жовтих прапорців, які є факторами хронізації болю. У разі гострого БС краще віддати перевагу короткочасному прийому препаратів з інтенсивною дією; хронічного – тривалому застосуванню засобів, які мають помірну активність. Комплексне лікування включає НПЗП, локальне введення місцевих анестетиків, міорелаксанти, вітаміни групи В (В1, В6, В12 у комплексі), лікувальну гімнастику, хірургічні втручання. Відповідно до світових рекомендацій (O’Connell N.E., Cook C. E. et al., 2017) НПЗП є золотим стандартом для усунення як гострих, так і хронічних БНС.
Найпоширеніші ускладнення НПЗП-терапії – гастроінтестинальні. Щоб запобігти їхній появі, слід виявляти та корегувати фактори ризику шлунково-кишкових кровотеч; здійснювати ерадикацію H. pylori перед тривалим лікуванням НПЗП; використовувати НПЗП із мінімальною гастротоксичністю та в оптимальних дозуваннях, комбінувати їх з ІПП, проводити максимально нетривалі курси терапії.
Високою ефективністю та відносно сприятливим гастроінтестинальним профілем характеризується диклофенак. У пацієнтів високого ризику повторних шлунково-кишкових кровотеч комбінація диклофенаку 75 мг + омепразолу 20 мг виявилася зіставною за ефективністю та переносимістю з терапією целекоксибом 200 мг. НПЗП із константою кислотної дисоціації ≈4, до яких належить і диклофенак, мають гідрофільну/ліпофільну полярність, активно переміщаються в зону запалення, здатні проникати в усі тканини.
У клінічній практиці я широко використовую диклофенак, зокрема призначаю різні форми препарату Диклоберл® («Берлін-Хемі»). За невідкладних станів для швидкого усунення БС рекомендую застосовувати Диклоберл® N 75 мг в/м: максимальна концентрація препарату в крові досягається через 20 хв, а ефект триває протягом 4 год. Диклоберл® ретард (капсули повільного вивільнення, 100 мг диклофенаку) призначений для контролю БС помірної інтенсивності (патологія суглобів, вивихи тощо) та підходить для тривалого застосування, використовується 1 р/добу: максимальна концентрація в крові спостерігається через 5 год після прийому, підтримується протягом 24 год. Хочу акцентувати увагу на такій допоміжній речовині препарату Диклоберл® ретард, як еудрагіт (кополімер амонію метакрилату). Його наявність сприяє доставці діючої речовини в усі відділи шлунково-кишкового тракту, досягненню високих концентрацій препарату в крові, пролонгації дії.
Диклоберл® у формі супозиторіїв для ректального введення (50 і 100 мг) використовується з метою усунення БС на тлі урологічної та гінекологічної патологій. Максимальна концентрація в крові спостерігається через 1 год після прийому, підтримується протягом 5 год.
Наразі НПЗП – одна з найпопулярніших категорій ліків як серед пацієнтів, так і в колі медичних спеціалістів. Зворотний бік використання цих високоефективних засобів – широкий спектр побічних ефектів. Саме в майстерному управлінні ризиками полягає ключове завдання клініцистів. І правильний вибір НПЗП у конкретній клінічній ситуації – обов’язкова умова для успішного балансування між «допомогти» та «не нашкодити».
Підготувала Олександра Марченко
Медична газета «Здоров’я України 21 сторіччя» № 3 (496), 2021 р.