27 березня, 2021
Роль мікробіоти кишечнику в перебігу COVID-19
Сьогодні людство зіштовхнулося з пандемією COVID-19 та відсутністю специфічного лікування нової хвороби. Саме тому надзвичайно важливим та актуальним став пошук можливих механізмів впливу на захисні сили людського організму. Вагоме значення для підтримки імунного статусу має мікробіота кишечнику (МК), адже 70-80% імунних клітин містяться саме у цьому органі. Неправильне харчування, стрес, вік, прийом антибактеріальних препаратів, а також наявність тих чи інших захворювань можуть спровокувати розвиток дисбіозу (E. Thursby, N. Juge, 2017). Дисбіоз асоціюється зі сприйнятливістю організму до інфекцій, які в подальшому змінюють кишкову флору, що збільшує ризик приєднання вторинної інфекції (N.T. Groves et al., 2020). Тому не дивно, що при COVID-19 більш тяжкий перебіг та висока смертність спостерігаються серед пацієнтів старшого віку, особливо при вираженій коморбідності (зокрема супутній артеріальній гіпертензії, цукровому діабеті, бронхолегеневих захворюваннях, хворобі нирок тощо), тобто станах, які асоціюються із порушенням МК (R. Fernandes, 2019).
Хоча коронавірус в основному уражає легені, у 5-10% пацієнтів переважають скарги з боку шлунково-кишкового тракту (ШКТ), такі як блювання, діарея, абдомінальний біль та прояви ентероколіту (M. Du et al., 2020). Ці симптоми можуть виникати внаслідок прямого впливу SARS-CoV-2 на ентероцити кишечнику за рахунок існування осі «легені – кишечник» або реалізуватися шляхом імунорегуляторних механізмів (А. Dumas et al., 2018). Вісь «легені – кишечник» є двонаправленою, а це означає, що мікробні метаболіти та ендотоксини кишечнику можуть впливати на легені та навпаки (B. Dhar, A. Mohanty, 2020). Мікроорганізми та продукти їх обміну, які потрапляють на слизову оболонку кишечнику, фагоцитуються антигенпрезентуючими клітинами (АПК), що зумовлює їх транспортування у мезентеріальні лімфатичні вузли та може стимулювати Т- і В-клітини. Активовані лімфоцити можуть переміститися до кишечнику або легень (рис.).
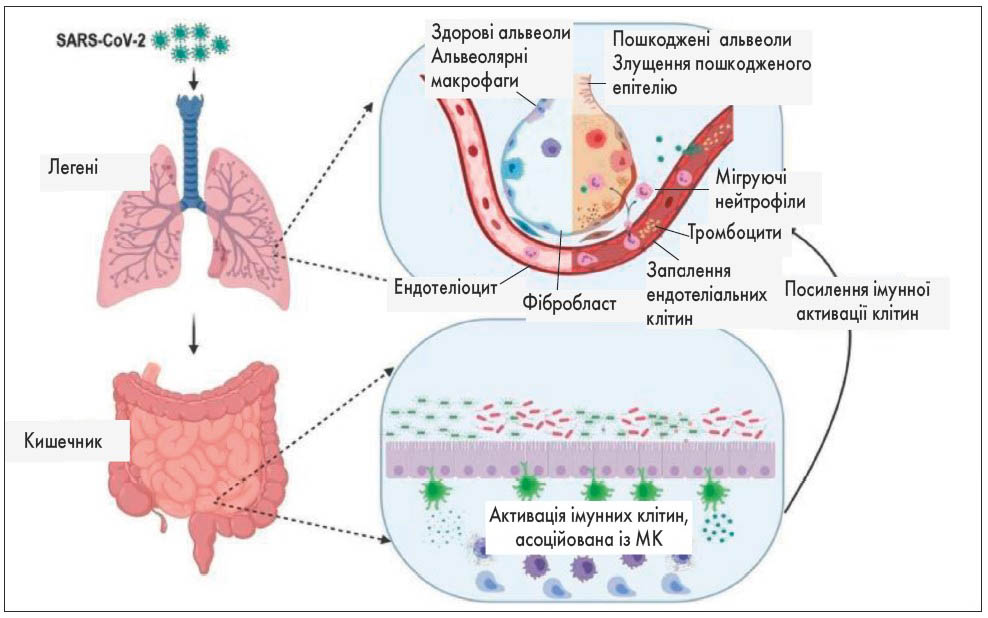 Рис. Вісь «легені – кишечник». МК активує імунні клітини, посилюючи імунну активацію легень
Рис. Вісь «легені – кишечник». МК активує імунні клітини, посилюючи імунну активацію легень
Збагачення мікробіоти легень кишковими видами Bacteroides спостерігається в багатьох випадках захворювання на COVID-19 (D. Vander Lelie, S. Taghavi, 2020) та пов’язане з підвищенням рівня плазматичних запальних маркерів. Також повідомляється про збільшення рівня Enterobacteriaceae та Lachnospiraceae у тяжкохворих пацієнтів із гострим респіраторним дистрес-синдромом (Y. He et al., 2020).
SARS-CoV-2 інфікує клітини-мішені шляхом зв’язування поверхневого глікопротеїну – шипу вірусу (S-білка) із рецептором ангіотензинперетворюючого фермента 2 типу (АПФ2), який міститься у легенях, серці, печінці та кишечнику і є важливим регулятором ренін-ангіотензин-альдостеронової системи (РААС) (M. Hoffmann et al., 2020).
Модулюючи активність АПФ2, вірус SARS-CoV-2 сприяє накопиченню ангіотензину (АТ) ІІ та зниженню протективних ефектів АТ 1-7, що може бути одним із пояснень тяжкого перебігу COVID-19 у людей із супутніми захворюваннями, пов’язаними з гіперактивацією РААС, а саме – із хворобами респіраторної, серцево-судинної системи, нирок та цукровим діабетом (K. Kuba et al., 2013).
Проте відома й інша функція АПФ2, яка не пов’язана з РААС та полягає у впливі на транспорт нейтральної амінокислоти триптофану через мембрану епітеліоцитів кишечнику, впливаючи на його гомеостаз та якісний і кількісний склад МК (T. Perlol, J.M. Penninger, 2013). Порушена функція АПФ2 може потенціювати розвиток дисбіозу і бути причиною гастроінтестинальних проявів у хворих на COVID-19 (K. Kotfis, K. Skonieczna-Zydecka, 2020).
Ще однією причиною тяжкого перебігу COVID-19 є гіперреактивність імунної системи, або так звана цитокінова буря, яка характеризується посиленням системної запальної відповіді та масивним вивільненням цитокінів (Y. Tang et al., 2020). Розвиток цитокінової бурі є відображенням неконтрольованого порушення регуляції імунної функції. Існуючі дослідження демонструють розвиток лімфоцитопенії у хворих на COVID-19 (N. Fathi, N. Rezaei, 2020) за рахунок Т-хелперів та Т-супресорів, але при цьому кількість незрілих Т-клітин зростає, що й зумовлює розвиток гіперреактивності. Також зменшується кількість Т-клітин пам’яті, що може сприяти виникненню рецидивів у цих хворих (C. Qin et al., 2019). Існують дані, що CD4 Т-клітини у хворих із тяжким перебігом COVID-19 є високоактивованими та поглинають інші імунні клітини, у той час як експресія індукованих інтерфероном (ІФН) генів знижується, що дозволяє припустити пригнічення утворення ІФН у цих пацієнтів (B. Kalfaoglu et al., 2020). Проте С. Huang та співавт. (2020) виявили підвищені рівні різноманітних цитокінів, у тому числі й ІФН-γ та α, у хворих на COVID-19 незалежно від тяжкості їх стану. Пояснення цих суперечливих фактів може бути пов’язане із надходженням ІФН у плазму з різних тканин, у тому числі з кишечнику (M. Swiecki, M. Colonna, 2011).
Повідомляється про підвищення рівнів IL-8, IL-23 та зниження IL-10 у випорожненнях пацієнтів із COVID-19, що свідчить про імунологічні механізми залучення ШКТ (G.J. Britton et al., 2020). Кілька досліджень продемонстрували, що у порівнянні зі здоровими особами, у хворих на COVID-19 спостерігається значно менше бактеріальне різноманіття, більша кількість умовно-патогенних бактерій, таких як Streptococcus, Rothia, Veillonella та Actinomyces і зниження рівня корисних симбіонтів, таких як Agathobacter, Fusicatenibacter, Roseburia та Ruminococcaceae UCG-013. Зміни складу МК зберігаються навіть після припинення виділення вірусу, а це дозволяє припустити, що інфекція або/та госпіталізація можуть бути пов’язані з тривало діючим несприятливим впливом на МБ, що потенційно може бути причиною більш тривалого періоду одужання (S. Gu et al., 2020; T. Zuo et al., 2020).
Отже, МК може слугувати індикатором індивідуальної чутливості до COVID-19, а зміни нормального складу та функції МК можуть спровокувати розвиток атипової запальної реакції. Встановлено, що переважання лактобактерій сприяє вищому рівню IL-10 та є предиктором більш сприятливого прогнозу хворих на COVID-19, а збільшення кількості Klebsiella, Streptococcus та Ruminococcus gnavus сприяє підвищенню рівня прозапальних цитокінів та більш тяжкому перебігу захворювання (D. Van der Lelie, S. Taghavi, 2020).
Механізми противірусної дії пробіотиків досі незрозумілі, проте вважається, що вони блокують процеси реплікації, інтерналізації вірусу, зупиняють подальше поширення інфекції, а також впливають на АПФ2 (A.K. Azkur et al., 2020). Bacillus, лакто- та біфідобактерії мають здатність збільшувати активність природних клітин-кілерів, T-супресорів або Т-хелперів, зменшувати кількість B-лімфоцитів, підвищувати концентрацію IgA у слині, а також рівні IL-10 та ІФН-α, що свідчить про їх імунну активність проти поширених інфекцій верхніх дихальних шляхів, у тому числі й COVID-19.
Біфідобактерії – це грампозитивні анаеробні пробіотики, що також інгібують IL-17, IL-6, фактор некрозу пухлин α (ФНП-α) та С-реактивний білок (E.Y. Kong et al., 2018). Проведені дослідження демонструють, що Bifidobacterium lactis Bl-04 асоціюється зі значним зменшенням частоти захворювань верхніх дихальних шляхів (N.P. West et al., 2014), а також впливає на реплікацію риновірусу та зменшує його виділення із носовим секретом (R.B. Turner et al., 2017). Взаємодіючи з імунними клітинами, пробіотики відіграють важливу роль у підтримці імунного гомеостазу, а також забезпечують підтримку сталого рівня pH кишечнику, протидіють інвазії та колонізації патогенних мікроорганізмів і можуть впливати на АПФ2, знижуючи рівень АТІІ (N. Li et al., 2019).
Відомо що пребіотики, зокрема такі як інулін та масляна кислота, регулюють рівні про- та протизапальних цитокінів та модулюють лімфоїдну тканину ШКТ, а тому показані до використання у комплексі із пробіотиками (N.L. Keim, R.J. Martin, 2014; N.P. West et al., 2013).
Таким чином, здорова МК відіграє важливу роль у підтримці власних захисних сил організму та сприяє легшому перебігу вірусних інфекцій, у тому числі й COVID-19. Потенційно корисною в цьому напрямку може бути модифікація МК за допомогою комбінації пробіотиків із пребіотиками або симбіотиків. У цьому аспекті цікавим є засіб Колонзак компанії Acinо. Серед ефектів засобу Колонзак варто відзначити його здатність покращувати кишковий бар’єр та попереджувати проникнення патогенних бактерій із просвіту кишечнику в кров’яне русло, а також пригнічувати ріст та розмноження патогенних бактерій.
Колонзак випускається у формі капсул. До їх складу входять: масляна кислота 250 мг, фруктоолігосахариди (інулін) 100 мг, Bifidobacterium bifidum Bb-06 SD6576 18 мг (1,8×109 КУО), Bifidobacterium lactis Bl-04 ATCC SD5219. Рекомендована доза 1-2 капсули на добу. Засіб протипоказаний дітям віком до 12 років, вагітним та у період грудного вигодовування.
Підготувала Ольга Нестеровська
UA-COLO-PUB-022021-023
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (59) 2021 р.



