30 березня, 2021
Перспективи використання ксиліту як засобу для селективного пригнічення проліферації ракових клітин
Важливим напрямом лікування онкологічних хворих є супровідна терапія, яка вирішує низку проблем, пов’язаних із пухлиною чи небажаними явищами, зумовленими основним протипухлинним лікуванням. Сьогодні опубліковано чимало наукових робіт, присвячених цій тематиці. Результати досліджень показують, що деякі засоби, які застосовуються як допоміжна терапія в онкологічних пацієнтів, мають потенційні протиракові властивості. У попередньому номері вміщено короткий огляд дослідження N. Tomonobu та співавт. (2020), у якому висвітлено протипухлинну дію ксиліту, зумовлену регулюванням рівня глутатіону. У цій статті пропонуємо ознайомитися з не менш цікавими результатами наукової роботи D. Trachootham та співавторів.
Вибіркове інгібування проліферації клітин раку ротової порожнини як наслідок пригнічення гліколізу при частковому заміщенні глюкози ксилітом
При різних видах раку спостерігають підвищену утилізацію глюкози. Це зумовлює необхідність пошуку альтернативного вуглеводу, який забезпечуватиме нормальні тканини енергією, але уповільнюватиме ріст пухлин. D. Trachootham та співавт. (Partial substitution of glucose with xylitol suppressed the glycolysis and selectively inhibited the proliferation of oral cancer cells. Nutrition and cancer. 2017; 69 (6): 862-872) дослідили вплив цукрових спиртів на проліферацію клітин раку ротової порожнини в порівнянні з нетрансформованими клітинами.
Зміна енергетичного обміну є особливістю раку [1], тому надходження поживних речовин впливає не тільки на стан хворого на рак, а й на прогресування захворювання [2]. Переконливі дані свідчать про те, що підбір дієти відіграє важливу роль у підвищенні виживаності онкохворих і в запобіганні рецидиву раку [2, 3]. Розуміння відмінностей в метаболізмі ракових і нормальних клітин є важливим для розроблення відповідного дієтичного харчування для онкопацієнтів. Доведено, що збільшення поглинання глюкози і швидкості її переробки є критичним для проліферації, трансформації клітин багатьох видів раку та його прогресування [5, 6].
Гліколіз – початковий процес метаболізму глюкози. У нормальних клітинах за адекватної кількості кисню цей процес є аеробним. Глюкоза перетворюється на піруват, а потім на ацетил-Со-А, з якого в циклі Кребса генерується АТФ [7]. В умовах гіпоксії нормальні клітини переходять на анаеробний гліколіз, при якому утворюється лактат. Ракові клітини можуть використовувати як аеробний, так і анаеробний варіант навіть за нормального рівня кисню (так званий ефект Варбурга). Глюкоза є основним джерелом енергії для нормальної тканини, але також і основним «паливом» для росту ракових клітин і прогресування захворювання. Це зумовлює пошук альтернативного вуглеводу, який буде забезпечувати енергією нормальні клітини, але не сприятиме росту та метастазуванню раку [6].
Ксиліт і сорбіт є потенційними кандидатами на цю роль. У нормальних клітинах людини ксиліт метаболізується через пентозофосфатний шлях [8]. Ксиліт – це п’ятивуглецевий цукровий спирт, що в невеликій кількості міститься у ягодах і фруктах, тканинах рослин і тварин [9]; 1 г цієї речовини дає 2,4 ккал енергії. Ксиліт має низький глікемічний індекс, володіє інгібуючими властивостями щодо бактерій (входить до складу жувальних гумок, зубних паст). Примітно, що ксиліт пригнічував ріст каріогенних бактерій Streptococcus mutans шляхом інгібування анаеробного гліколізу [12, 13]. Оскільки посилення гліколізу спостерігається в багатьох ракових клітинах [6, 14], можна припустити, що ксиліт здатний впливати на продукцію ними енергії.
Рак ротової порожнини з високою частотою рецидивів (30%) і смертністю (50%) є шостим за поширеністю у світі [16]. Неправильне харчування є серйозною проблемою для пацієнтів, які перенесли рак ротової порожнини, і прямо пов’язане з низьким рівнем виживаності [17, 18]. Тому оптимізація харчування має важливе значення для профілактики раку ротової порожнини [19]. Доведено, що клітини цього виду раку використовують глюкозу як основне джерело енергії [20]. Однак досі не було відомо про вплив ксиліту на проліферацію клітин раку ротової порожнини.
Часткове заміщення глюкози ксилітом значуще пригнічує проліферацію клітин раку ротової порожнини, але не впливає на ріст імморталізованих нетрансформованих клітин
Клітини шести видів плоскоклітинної карциноми ротової порожнини (CAL‑27, FaDu, SCC4, SCC9, SCC15 і SCC25) і однієї лінії нетрансформованих кератиноцитів ротової порожнини (OKF6/TERT2) культивували в середовищах, які містили 1 мг/мл глюкози і 5,8 мг/мл ксиліту або сорбіту, що забезпечувало таку ж кількість енергії, як для контрольної групи (4,5 мг/мл глюкози).
Як показано на рисунку 1, часткова заміна глюкози в культуральному середовищі на ксиліт (або сахарозу та ксиліт) сприяла значному зменшенню кількості проліферуючих клітин раку ротової порожнини (рис. 1А) і при цьому не чинила впливу на проліферацію нетрансформованих епітеліальних клітин ротової порожнини (рис. 1Б).
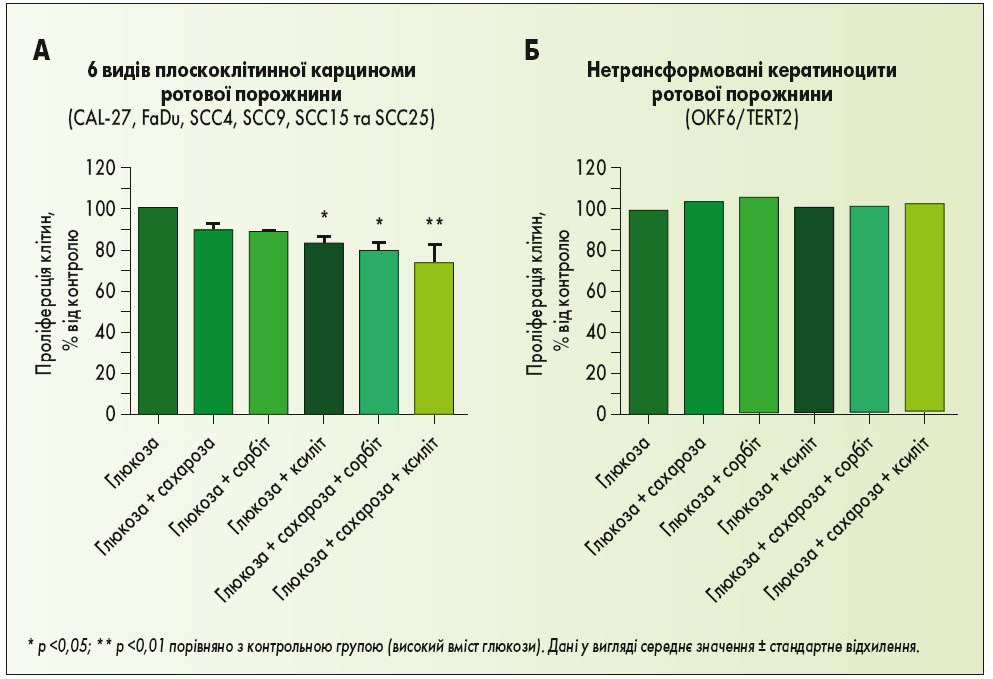 Рис. 1. Часткове заміщення глюкози ксилітом значуще пригнічує проліферацію клітин раку ротової порожнини, але не імморталізованих нетрансформованих клітин. A – 18 експериментів з 6 лініями клітин раку ротової порожнини (по 3 для кожної); Б – 3 експерименти з нетрансформованими кератиноцитами ротової порожнини
Рис. 1. Часткове заміщення глюкози ксилітом значуще пригнічує проліферацію клітин раку ротової порожнини, але не імморталізованих нетрансформованих клітин. A – 18 експериментів з 6 лініями клітин раку ротової порожнини (по 3 для кожної); Б – 3 експерименти з нетрансформованими кератиноцитами ротової порожнини
Це свідчить про селективну протиракову активність ксиліту. Примітно, що хоча часткове заміщення глюкози тільки сахарозою або тільки сорбітом незначно зменшувало кількість проліферуючих ракових клітин (без статистично значущої різниці), комбінація сахарози і ксиліту або сорбіту синергічно пригнічувала проліферацію клітин раку ротової порожнини.
Оскільки результати дослідження з резазурином показали, що протираковий ефект ксиліту був сильнішим, ніж сорбіту, саме ксиліт був обраний для підтвердження його супресивного ефекту на 3 клітинних лініях раку ротової порожнини (CAL‑27, FaDu і SCC4) за допомогою аналізу оцінки життєздатності клітин з 3-(4,5-диметилтіазол‑2-іл)-2,5‑дифенілтетразолію бромідом, заснованого на визначенні активності дегідрогенази мітохондрій. Як показано на рисунку 2, після 72-годинної інкубації середня кількість проліферуючих клітин раку ротової порожнини значуще зменшувалася при культивуванні в середовищах із низьким рівнем глюкози і ксилітом (1,0 і 5,8 мг/мл відповідно). Щодо нетрансформованих клітин ніякого ефекту не спостерігалося. Оскільки вплив середовища з низьким вмістом глюкози значно не відрізнявся від впливу середовища з її високим вмістом (4,5 мг/мл глюкози), ефект інгібування росту в цьому разі, ймовірно, був зумовлений саме впливом ксиліту.
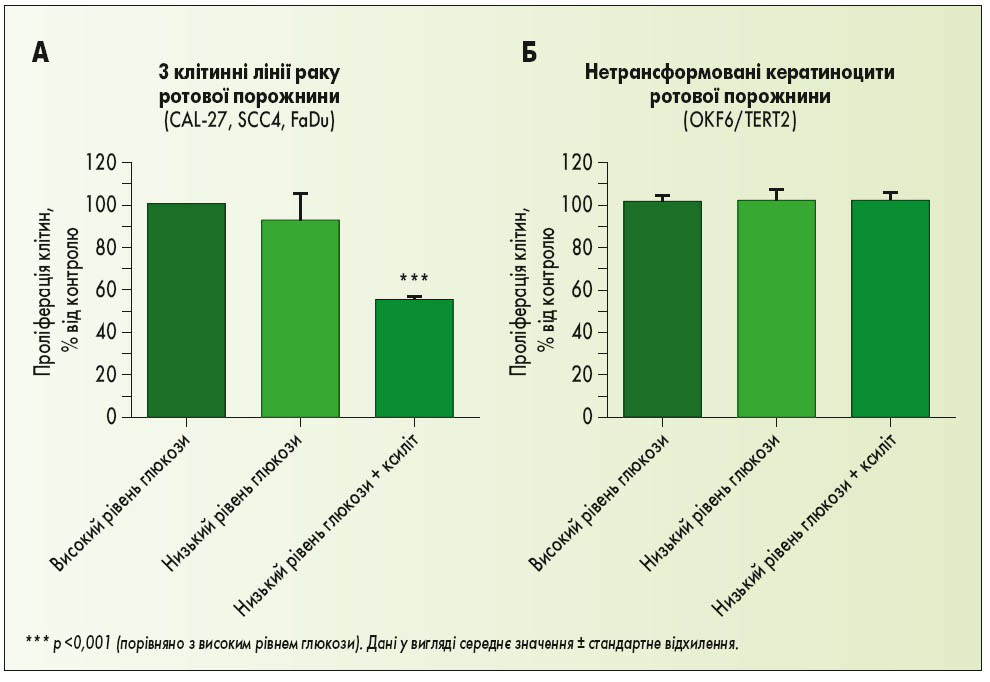 Рис. 2. Низький рівень глюкози в поєднанні з ксилітом (але не лише низький рівень глюкози) сприяв вибірковому пригніченню проліферації клітин раку ротової порожнини. A – 9 експериментів на 3 різних клітинних лініях раку ротової порожнини (CAL‑27, SCC4, FaDu, по 3 для кожної); Б – 3 експерименти з нетрансформованими кератиноцитами ротової порожнини (OKF‑6/TETRT2)
Рис. 2. Низький рівень глюкози в поєднанні з ксилітом (але не лише низький рівень глюкози) сприяв вибірковому пригніченню проліферації клітин раку ротової порожнини. A – 9 експериментів на 3 різних клітинних лініях раку ротової порожнини (CAL‑27, SCC4, FaDu, по 3 для кожної); Б – 3 експерименти з нетрансформованими кератиноцитами ротової порожнини (OKF‑6/TETRT2)
Часткове заміщення глюкози ксилітом значуще пригнічує синтез АТФ у клітинах раку ротової порожнини, а додавання D-ксилулози зумовлює посилення супресії
Оскільки цукор є основним субстратом для енергетичного резерву – АТФ, необхідного для проліферації клітин, ефект пригнічення росту клітин ксилітом може бути наслідком зменшення вироблення АТФ. Було показано, що часткова заміна глюкози в культуральних середовищах на ізокалоричну кількість ксиліту призвела до істотного зниження утворення АТФ через 24 год після інкубації.
Оскільки ксиліт має бути перетворений на D-ксилулозу до енергетичного метаболізму, то в разі зумовленої зниженою утилізацією ксиліту раковими клітинами затримки синтезу АТФ можна очікувати відновлення синтезу АТФ при надходженні D-ксилулози. Для перевірки цієї гіпотези ксиліт частково замінили на D-ксилулозу в середовищі з низьким вмістом глюкози і досліджували, чи може D-ксилулоза «врятувати» АТФ-супресивний ефект ксиліту. З’ясувалося, що часткова заміна ксиліту на D-ксилулозу не відновлювала синтез АТФ, але натомість значуще потенціювала ефект його пригнічення ксилітом.
Було також показано, що часткове заміщення ксиліту D-ксилулозою посилювало пригнічувальну дію ксиліту на проліферацію клітин. Ґрунтуючись на цих висновках, D. Trachootham та співавт. вважали малоймовірною гіпотезу про те, що пригнічення синтезу АТФ було зумовлене зниженням використання ксиліту, і постулювали, що такий ефект може бути результатом впливу ксиліту на метаболізм глюкози.
Часткове заміщення глюкози ксилітом значуще пригнічує активність гліколітичного ферменту фосфофруктокінази у клітинах раку ротової порожнини
Оскільки метаболізм глюкози першочергово регулюється активністю фосфофруктокінази (ФФК) і було показано, що ксиліт інгібує активність ФФК бактерій [13], дослідники оцінили вплив ксиліту на активність ФФК клітин людини. З’ясувалося, що при заміщенні глюкози ксилітом спостерігалося значуще пригнічення активності ФФК (протягом 24 год) і проліферації клітин (протягом 72 год). Отримані дані свідчать про те, що зниження синтезу АТФ, імовірно, є результатом інгібування активності гліколітичного ферменту ФФК. Цікаво, що в порівнянні з високим рівнем глюкози комбінація високого рівня глюкози і ксиліту пригнічувала активність ФФК, але не впливала на життєздатність клітин. Дослідники припустили, що надлишок глюкози може компенсувати зниження активності ФФК. На противагу цьому комбінація низького рівня глюкози і ксиліту забезпечувала інгібування і активності ФФК, і проліферації клітин порівняно лише з низьким вмістом глюкози. Ці результати показали, що часткове заміщення глюкози ксилітом може бути ефективним підходом для пригнічення активності ФФК, утворення АТФ і проліферації клітин.
Обговорення й висновки
Отримані результати дозволяють припустити, що часткова заміна глюкози на цукрові спирти, особливо ксиліт, може бути корисною для пацієнтів, які перенесли рак ротової порожнини. Часткове заміщення глюкози ксилітом забезпечувало нормальну проліферацію нетрансформованих клітин, проте значно пригнічувало проліферацію клітин раку ротової порожнини.
Дизайн дослідження був розроблений з урахуванням фактичного споживання компонентів людиною. Оскільки, відповідно до стандартів харчування [23], використання ксиліту з їжею обмежене 30 г на день, ксиліт, безумовно, не може повністю замінити глюкозу в раціоні. Можна застосувати схему часткової заміни – зниження кількості глюкози і додавання ксиліту. D. Trachootham та співавт. першими повідомили про оцінку протипухлинного ефекту ксиліту в дослідженні з дизайном на основі принципів дієти.
Список літератури знаходиться в редакції.
Матеріал підготовлений за підтримки фармацевтичної компанії «Юрія-Фарм».
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 1 (68) 2021 р.



