10 квітня, 2021
Вибір оптимальної протиепілептичної терапії у пацієнтів з епілепсією та супутніми патологіями
Значна частка пацієнтів з епілепсією страждають на супутні захворювання. Тип коморбідності є важливим фактором при виборі тактики лікування епілепсії, тож приймаючи рішення щодо призначення протиепілептичних препаратів (ПЕП), лікар має враховувати наявні супутні патології у хворого, спираючись на наукові докази. J. Ruiz-Gimenez et al. виконали огляд досліджень із метою виявлення наукових даних щодо методів лікування епілепсії у пацієнтів з урахуванням коморбідних станів та надання відповідних рекомендацій. Пропонуємо до вашої уваги ключові положення даного матеріалу, опублікованого у виданні Seizure (2010; 19: 375‑382).
У пацієнтів з епілепсією поширеність супутніх захворювань порівняно із загальною популяцією є більшою. В осіб з епілепсією в анамнезі найчастіше мають місце інсульт, цукровий діабет, хвороби серця, високий артеріальний тиск, астма, хронічний бронхіт, виразка шлунка/кишечника, артрит, захворювання щитоподібної залози, мігрень, хвороба Альцгеймера та рак. На додачу, епілепсія пов’язана зі збільшенням поширеності психічних розладів, особливо тривожних станів та депресії (Tellez-Zenteno et al., 2005, 2007). Також супутні захворювання можуть бути безпосередньою причиною розвитку епілепсії (Ryvlin, 2006). Окрім запобігання виникненню нападів як основної клінічної мети, виявлення та урахування терапії коморбідних станів також мають бути першочерговими завданнями лікаря.
При виборі протиепілептичного лікування у пацієнтів із супутніми патологіями слід приділяти особливу увагу потенційним побічним ефектам та медикаментозній взаємодії (Elliott et al., 2009; Hinnell et al., 2010). Останнім часом на фармринку з’явилася низка ПЕП, багато з яких мають покращений фармакокінетичний профіль і переносяться ліпше, ніж «старі» ПЕП. Це робить їх потенційно корисними для осіб з епілепсією та іншими супутніми захворюваннями (Bialer, 2006).
Незважаючи на різноманіття доступних ПЕП, не було проведено систематичних досліджень, присвячених аналізу оптимальних ПЕП для пацієнтів з епілепсією та іншими коморбідностями. J. Ruiz-Gimenez et al. виконали пошук у базі даних Medline та Кокранівській бібліотеці на предмет наукових досліджень щодо лікування епілепсії в осіб із супутніми патологіями. Для виявлення доступних клінічних рекомендацій, основаних на фактичних доказах, автори використовували інформаційну базу Канадської медичної асоціації (CMA; www.cma.ca), Національного інформаційного центру із рекомендацій (www.guideline.gov), Національної бібліотеки з питань охорони здоров’я (www.library.nhs.uk) та інші веб-джерела.
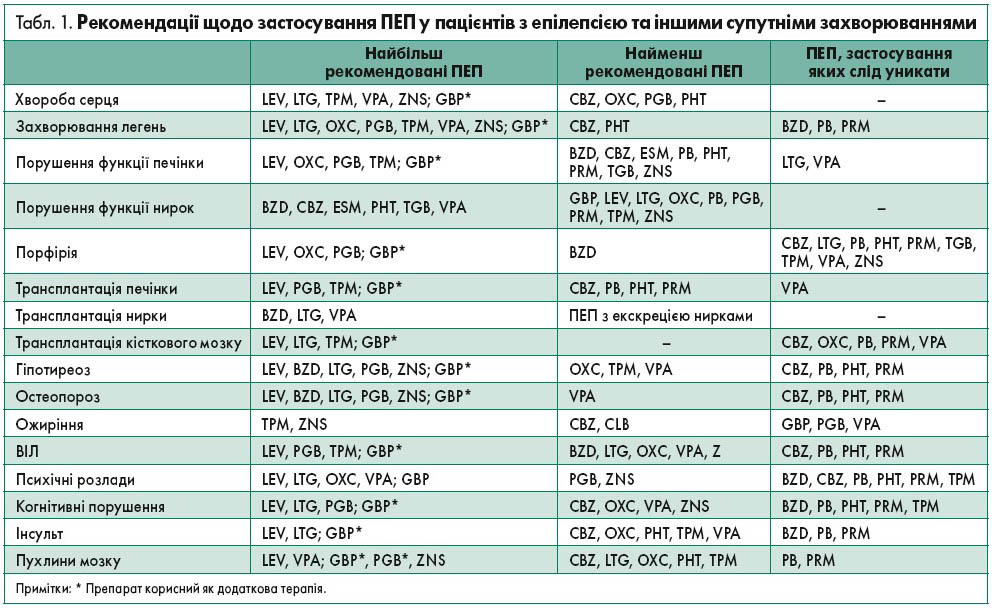
Рекомендації щодо застосування ПЕП у пацієнтів з епілепсією та іншими супутніми захворюваннями наведені в таблиці 1.
Кардіоваскулярні захворювання
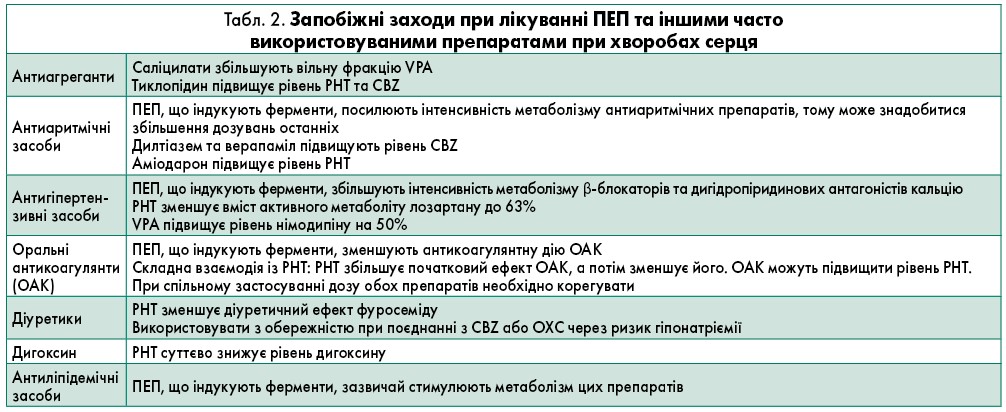
При довгостроковому протиепілептичному лікуванні пацієнтам із хворобами серця слід з обережністю застосовувати карбамазепін (CBZ), окскарбазепін (OXC), фенітоїн (PHT) та уникати їх використання у разі порушення атріовентрикулярної провідності (Kaul et al., 2000). Прегабалін (PGB) доцільно обережно призначати особам із серцевою недостатністю внаслідок систолічної дисфункції лівого шлуночка (Murphy et al., 2007). Загалом варто уникати ПЕП, що індукують ферменти, через численні взаємодії з ліками, які зазвичай використовують при патологіях серця (табл. 2) (Patsalos, Perucca, 2003).
Найбільш рекомендованими ПЕП є леветирацетам (LEV), ламотриджин (LTG), топірамат (TPM), вальпроат (VPA). Габапентин (GBP) може бути корисним як додаткова терапія.
Хвороба легень
Парентеральне використання барбітуратів, бензодіазепінів (BZD) та PHT може спричинити пригнічення дихання. Тому в пацієнтів із порушенням дихання слід контролювати частоту серцевих скорочень, дихання та показники оксиметрії. Парентеральне введення VPA являє собою безпечну альтернативу (Agarwal et al., 2007; Mehta et al., 2007). LEV також є ефективним у зазначених клінічних ситуаціях (Nau et al., 2009). При тривалому лікуванні осіб із порушеннями дихання необхідно уникати призначення ПЕП, які можуть викликати респіраторну депресію, наприклад барбітуратів та BZD. ПЕП, що індукують ферменти, знижують концентрацію теофіліну, який здатен зменшувати концентрацію CBZ і PHT (Patsalos, Perucca, 2003).
Захворювання печінки
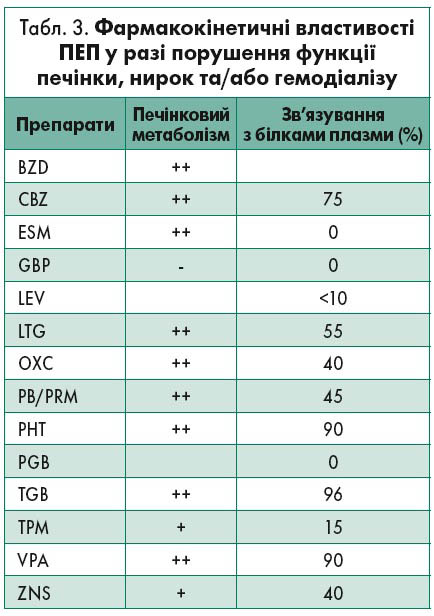 При ураженні функції печінки метаболізм деяких ПЕП порушується. Тому за наявності дисфункції печінки важливо враховувати фармакокінетику ПЕП (табл. 3). Застосування фенобарбіталу (PB) доцільно уникати за ургентного лікування епілептичних нападів у пацієнтів із патологією печінки, адже він може викликати або посилити печінкову енцефалопатію. BZD також можуть спричинити розвиток печінкової енцефалопатії, тож їх призначають у разі крайньої необхідності та у нижчих дозах, ніж зазвичай. Особам із захворюванням печінки VPA протипоказаний через його гепатотоксичність, а PHT слід застосовувати з обережністю через можливу інтоксикацію (Ahmed, Siddiqi, 2006). LEV є найбільш рекомендованою терапевтичною альтернативою у хворих на патологію печінки (Ramael et al., 2006; Blio et al., 2008).
При ураженні функції печінки метаболізм деяких ПЕП порушується. Тому за наявності дисфункції печінки важливо враховувати фармакокінетику ПЕП (табл. 3). Застосування фенобарбіталу (PB) доцільно уникати за ургентного лікування епілептичних нападів у пацієнтів із патологією печінки, адже він може викликати або посилити печінкову енцефалопатію. BZD також можуть спричинити розвиток печінкової енцефалопатії, тож їх призначають у разі крайньої необхідності та у нижчих дозах, ніж зазвичай. Особам із захворюванням печінки VPA протипоказаний через його гепатотоксичність, а PHT слід застосовувати з обережністю через можливу інтоксикацію (Ahmed, Siddiqi, 2006). LEV є найбільш рекомендованою терапевтичною альтернативою у хворих на патологію печінки (Ramael et al., 2006; Blio et al., 2008).
Захворювання щитоподібної залози
ПЕП, що індукують ферменти (CBZ, PB, PHT, PRM), впливають на метаболізм гормонів щитоподібної залози, спричиняючи зниження рівня загального та вільного тироксину. Ця модифікація зазвичай є субклінічною і змінюється на протилежну в разі відміни ПЕП, особливо у здорових пацієнтів. Однак це може мати клінічне значення у хворих на гіпотиреоз, які перебувають на замісній терапії (Simko, Horacek, 2007). До того ж VPA може призвести до субклінічного оборотного підвищення вмісту тиреотропного гормону (Vainionpaa et al., 2004). Хоча даних про вплив ПЕП другого покоління наразі бракує, імовірно, що ПЕП із помірним ефектом індукції ферментів (OXC, TPM) також діють на гормони щитоподібної залози, тоді як ПЕП, які не індукують ферменти, не впливають на них (Perucca, 2006).
Психічні розлади
В осіб із психічними розладами зазвичай частіше мають місце побічні ефекти, пов’язані з лікуванням, і нерідко потрібне триваліше застосування ПЕП (Beavis et al., 2007). Тому за можливості краще використовувати монотерапію (Huber et al., 2005).
При довгостроковому лікуванні слід уникати застосування ПЕП із седативним ефектом або потенційним зниженням когнітивних функцій внаслідок терапії, таких як BZD, CBZ, PB, PHT, PRM та TPM. Діазепам або мідазолам рекомендовані для ургентного лікування тривалих та кластерних нападів. За можливості доцільно застосовувати ПЕП, що асоційовані з нижчою частотою когнітивного дефіциту, як-от LEV, LTG, GBP, OXC та VPA (Coppola et al., 2008). Пацієнтам із порушенням координації чи ходи необхідно уникати використання CBZ, LTG, OXC, PB, PHT та PRM, із серйозними поведінковими проблемами – TPM, LEV та ZNS (Huber et al., 2005).
Для оптимізації лікування ПЕП у пацієнтів із супутніми психічними розладами слід враховувати такі моменти:
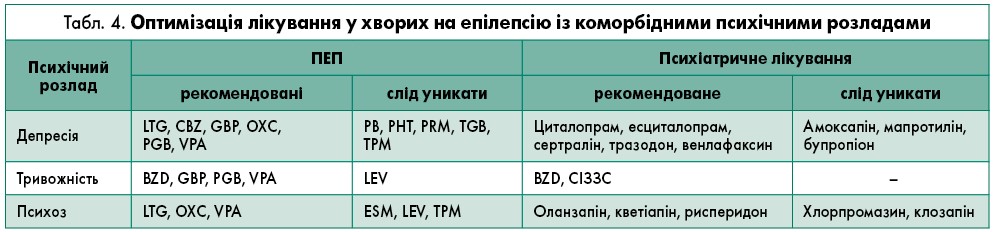
1. Можливий вплив ПЕП на симптоми психічних розладів. Залежно від типу коморбідної психічної патології, деякі ПЕП є більш дієвими, ніж інші (табл. 4) (Ovsiew, 2004; Brodtkorb, Mula, 2006).
2. Фармакологічні взаємодії. ПЕП, що індукують ферменти, здатні знижувати рівень інших психотропних препаратів у плазмі, як-то антипсихотики, трициклічні антидепресанти (ТЦА) та селективні інгібітори зворотного захоплення серотоніну (СІЗЗС), що перешкоджає контролю симптомів в осіб із психічними розладами. Взаємодія між VPA та амітриптиліном або нортриптиліном може призвести до збільшення концентрації цих препаратів у плазмі до 60%, спричиняючи інтоксикацію. Між ПЕП та літієм значущої взаємодії немає (Patsalos, Perucca, 2003).
ТЦА можуть пригнічувати метаболізм ПЕП та зумовлювати розвиток токсичності. Те саме відбувається з деякими СІЗЗС, такими як флуоксетин, пароксетин та флувоксамін, хоча вони мають кращий фармакокінетичний профіль, ніж ТЦА. Циталопрам, есциталопрам, сертралін, тразодон та венлафаксин не чинять суттєвого впливу на метаболізм ПЕП (Mula et al., 2004). Більшість антипсихотиків різною мірою порушують метаболізм ПЕП у печінці. Слід уникати приймання клозапіну пацієнтам з епілепсією, тоді як оланзапін, кветіапін та рисперидон зазвичай не потребують корегування дози, навіть якщо застосовувати їх у комбінації з ПЕП, що індукують ферменти (Brodtkorb, Mula, 2006).
Також слід враховувати загальні побічні ефекти, які можуть бути посилені під впливом медикаментозної взаємодії. СІЗЗС здатні спричиняти розвиток гіпонатріємії, тому їх слід застосовувати з обережністю у поєднанні з CBZ або OXC (Ovsiew, 2004).
3. Потенційний епілептогенний ефект антидепресантів та антипсихотиків. Зазвичай епілептогенний ризик низький при лікуванні ТЦА, СІЗЗС і антипсихотиками. Мінімальним він є при використанні цих препаратів у терапевтичному діапазоні з повільним титруванням дози та уникненням складних комбінацій. Винятки становлять такі антидепресанти, як амоксапін, мапротилін, бупропіон, та деякі антипсихотики – клозапін та хлорпромазин, що мають вищий епілептогенний ризик (Mula et al., 2004).
Когнітивні порушення
Когнітивні порушення як наслідок зниження функціонального резерву мозку або дегенеративних захворювань на тлі ПЕП можуть посилюватися. Перш ніж розпочинати лікування, важливо оцінити когнітивний стан пацієнтів, особливо похилого віку. Серед ПЕП, що чинять найбільший негативний ефект на когнітивні функції, – BZD, PB, PRM, дещо менший – PHT, TPM, найменшою мірою впливають LEV, LTG, PGB, GBP. Загалом застосування препаратів у високих дозах та комбінована терапія посилюють шкідливий потенціал ПЕП із точки зору когнітивного функціонування (Hommet et al., 2008).
Інсульт
Традиційні ПЕП, як-от BZD, CBZ, PHT, PB та VPA, із різних причин є менш рекомендованими препаратами для хворих після інсульту. Наявні дані про затримання функціонального відновлення внаслідок їх використання у пацієнтів з інсультом (Naidech et al., 2005). Крім того, ці ПЕП можуть значно взаємодіяти з саліцилатами та пероральними антикоагулянтами.
Такі ПЕП, як LEV, LTG, GBP, OXC та TPM, імовірно, не взаємодіють з антиагрегантами чи антикоагулянтами та не впливають на функціональний прогноз після інсульту (Patsalos, Perucca, 2003). Вивчення впливу LEV і GBP в осіб, що перенесли інсульт, показало їх ефективність та безпеку в цій когорті хворих (Kutlu et al., 2008; Belcastro et al., 2008). У пацієнтів літнього віку з епілепсією після інсульту LTG і GBP є дієвішими, ніж CBZ (Rowan et al., 2005).
Пухлини головного мозку
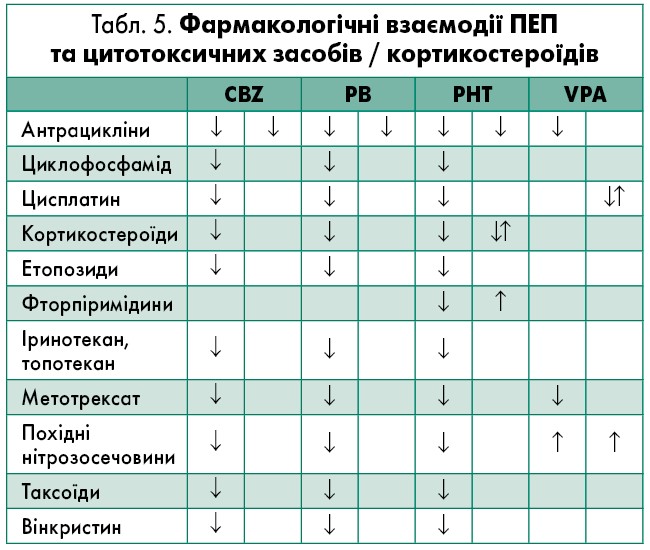 У пацієнтів із пухлинами головного мозку слід враховувати фармакологічні взаємодії ПЕП, цитотоксичних препаратів та кортикостероїдів (табл. 5). Також у таких хворих необхідно контролювати переносимість ПЕП через високу частоту побічних ефектів. Повідомлялося про тяжкі шкірні реакції у пацієнтів, яким проводили опромінення головного мозку, при застосуванні CBZ, PHT або PB, (Van Breemen et al., 2007). PHT для внутрішнього введення є варіантом вибору в гострих клінічних ситуаціях.
У пацієнтів із пухлинами головного мозку слід враховувати фармакологічні взаємодії ПЕП, цитотоксичних препаратів та кортикостероїдів (табл. 5). Також у таких хворих необхідно контролювати переносимість ПЕП через високу частоту побічних ефектів. Повідомлялося про тяжкі шкірні реакції у пацієнтів, яким проводили опромінення головного мозку, при застосуванні CBZ, PHT або PB, (Van Breemen et al., 2007). PHT для внутрішнього введення є варіантом вибору в гострих клінічних ситуаціях.
Відповідь хворих на лікування звичайними ПЕП варіює: 70, 51 і 44% осіб із пухлиною мозку, які отримували CBZ, PHT та VPA відповідно, мали стійкі судоми (Wick et al., 2005). У проспективних дослідженнях за участю пацієнтів із пухлиною мозку LEV продемонстрував хорошу ефективність та переносимість у режимі монотерапії (Lim et al., 2009). В обсерваційному дослідженні серед осіб із гліомою найвищий рівень відповіді на лікування був отриманий при застосуванні комбінації VPA та LEV (Van Breemen et al., 2009).
Підготувала Олена Коробка
UA-LEVI-PUB-032021-061
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 1 (56) 2021 р.