15 травня, 2021
Застосування азитроміцину при COVID‑19: механістичне обґрунтування та докази користі
Брак часу на розроблення та випробування нових специфічних ліків від коронавірусної хвороби (COVID-19) зумовлює інтерес до вже добре вивчених і запроваджених у практику препаратів. У контексті сучасних відомостей про патогенез COVID‑19 науковців і клініцистів насамперед цікавлять засоби з противірусними та протизапальними властивостями, що могли би зменшувати вірусне навантаження, вгамовувати цитокіновий шторм або обмежувати запальне ураження легень. Прикладом добре відомого препарату, що становить особливий інтерес в умовах пандемії, є азитроміцин*. Цей макролідний антибіотик характеризується широким спектром активності проти грампозитивних і грамнегативних бактеріальних збудників, а також добре задокументованими протизапальними й імунорегуляторними ефектами [1].
 Існують переконливі докази ефективності азитроміцину в лікуванні хронічних запальних процесів, як-от дифузний бронхіоліт, бронхіоліт після трансплантації, нееозинофільна астма. Застосування азитроміцину також асоціюється з поліпшенням клінічних наслідків при інших вірусних пневмоніях, зокрема грипозній [2] і риновірусній [3], а також у пацієнтів із гострим ураженням легень іншої етіології, котрі лікувалися у відділеннях інтенсивної терапії [4]. Інтерес до препарату підсилювався повідомленнями про активність азитроміцину in vitro проти SARS-CoV‑2; це зумовило те, що в деяких клініках азитроміцин почали призначати для лікування COVID‑19 на початку пандемії. Згодом повідомлялося про його користь у неконтрольованих серіях випадків і перших клінічних дослідженнях.
Існують переконливі докази ефективності азитроміцину в лікуванні хронічних запальних процесів, як-от дифузний бронхіоліт, бронхіоліт після трансплантації, нееозинофільна астма. Застосування азитроміцину також асоціюється з поліпшенням клінічних наслідків при інших вірусних пневмоніях, зокрема грипозній [2] і риновірусній [3], а також у пацієнтів із гострим ураженням легень іншої етіології, котрі лікувалися у відділеннях інтенсивної терапії [4]. Інтерес до препарату підсилювався повідомленнями про активність азитроміцину in vitro проти SARS-CoV‑2; це зумовило те, що в деяких клініках азитроміцин почали призначати для лікування COVID‑19 на початку пандемії. Згодом повідомлялося про його користь у неконтрольованих серіях випадків і перших клінічних дослідженнях.
Фармакологічний профіль
Молекула азитроміцину являє собою 15-членний кільцевий макролід класу азалідів. Цей антибіотик зарекомендував себе як досить безпечний і, крім легких побічних ефектів із боку шлунково-кишкового тракту, зазвичай добре переноситься [5]. Препарат швидко всмоктується після прийому всередину та має тривалий період напіввиведення; його великий об’єм розподілу зумовлений високим внутрішньоклітинним накопиченням, причому в тканинах досягається в 100 разів вища концентрація, ніж у плазмі крові [6]. В особливо великих кількостях азитроміцин захоплюють лейкоцити, а також епітеліальні клітини та фібробласти. Накопичення в лейкоцитах забезпечує ефективну доставку до місць зараження та запалення [7]. Азитроміцин також перетинає гематоенцефалічний бар’єр і концентрується в тканинах центральної нервової системи. Ця властивість також привертає до себе увагу під час пандемії, оскільки зростає обізнаність про неврологічні ускладнення COVID‑19 унаслідок інфільтрації й активації резидентних запальних клітин і, можливо, прямої тропності вірусу SARS-CoV‑2 до нервових клітин [8].
Нещодавно було узагальнено дані експериментів in vitro щодо інгібувальних концентрацій азитроміцину проти SARS-CoV‑2 й інших вірусів [9]. In vivo в гомогенатах легеневої тканини азитроміцин досягає концентрацій, які значно перевищують 90% ефективної концентрації, через 3 дні пероральної терапії дозою 500 мг [6]. У когортних дослідженнях, які оцінювали ефект азитроміцину в госпіталізованих пацієнтів із грипозною пневмонією [2] чи з гострим ураженням легень іншої етіології в умовах відділення інтенсивної терапії [4], пацієнти потребували дещо довших курсів лікування тривалістю 5 або 8 днів.
Противірусні ефекти
Азитроміцин має пряму та непряму противірусну активність у бронхіальних епітеліальних клітинах та інших клітинах організму хазяїна [1]. Крім SARS-CoV‑2, це також було показано для грипу, риновірусу, лихоманки денге, еболавірусу, парагрипів, вірусу Зіка й ентеровірусу [9]. Обговорюється декілька механізмів противірусного ефекту азитроміцину. Вірус SARS-CoV‑2 за допомогою шипового білка прикріплюється до ангіотензинперетворювального ферменту‑2 (АПФ‑2), що є першим етапом проникнення до клітин організму хазяїна. Віртуалізовані методи механічного моделювання продемонстрували, що азитроміцин може перешкоджати цьому процесу через його спорідненість із точкою зв’язування шипового білка й АПФ‑2. Також азитроміцин може конкурентно пригнічувати взаємодію вірусів із клітинами через його вражаючу молекулярну схожість із гангліозидом клітин хазяїна GM1, який зв’язується з відповідною ділянкою молекули шипового білка [10].
Після зв’язування з рецепторами вірус потрапляє до клітин або шляхом злиття мембран, або через опосередкований рецепторами ендоцитоз. У разі останнього закислення ендосом спричиняє вивільнення нуклеокапсиду з генетичним матеріалом вірусу. Азитроміцин втручається на цьому рівні, оскільки хімічно є слабкою основою, що накопичується внутрішньоклітинно та присутня всередині ендосом [9].
На подальших етапах вірусного циклу віруси використовують внутрішньоклітинні антиапоптотичні сигнальні шляхи для власного виживання й реплікації [11]. Саме тому, наприклад, блокування сигнального шляху PI3K/AKT/mTOR пригнічує реплікацію MERS-CoV [12]. Рапаміцин (сиролімус) – відомий інгібітор mTOR макролідної структури, проте азитроміцин також виявив здатність впливати на mTOR-сигналювання [12, 13]. Крім того, азитроміцин чинить непрямі противірусні ефекти, стимулює внутрішньоклітинну мРНК-експресію противірусних генів, а також генів, які стимулюють продукцію інтерферону в інфікованих клітинах. Це може підсилити противірусну дію, опосередковану інтерфероновим шляхом, і допомагає підтримувати баланс ранньої відповіді вродженого імунітету [14, 15].
Протизапальний ефект і модуляція функції макрофагів
Азитроміцин має добре задокументовані імуномодуляторні властивості, що можуть впливати на перебіг COVID‑19. По-перше, на моделях in vitro з клітинами респіраторного епітелію азитроміцин зменшував продукцію слизу та збільшував товщину епітеліального бар’єра [16], а також пригнічував активність матриксної металопротеази (ММР) на моделі зараження клітин бактеріальними ліпополісахаридами. Внаслідок цього зменшується прозапальна сигналізація, що допомагає зберегти цілісність клітин та епітеліальну бар’єрну функцію. По-друге, азитроміцин є потужним модулятором реакцій моноцитів і макрофагів на цитокіни; він може збалансувати імунну відповідь при COVID‑19, пригнічуючи сигналізацію NF-κB [17] та зменшуючи вивільнення класичних маркерів диференціації активованих M1-макрофагів, зокрема IL‑8, IL‑6, TNF і фактора, що стимулює колонії гранулоцитів-макрофагів [18]. Азитроміцин сприяє поляризації макрофагів від фенотипу М1 до М2, тим самим збільшуючи їхню фагоцитарну здатність [19].
Крім того, азитроміцин впливає на функцію нейтрофілів, пригнічує хемоатрактанти та молекули адгезії в активованих клітинах судинного ендотелію, обмежує активацію нейтрофілів, утворення нейтрофільних позаклітинних пасток (NET) [18, 20]. NET являють собою сітку позаклітинних волокон, які складаються здебільшого з ДНК нейтрофілів і захоплюють патогени для подальшого знищення. Нейтрофілія та NETоз роблять внесок у розвиток таких патологічних станів, як гіперзапалення та гіперкоагуляція за тяжкого перебігу COVID‑19, а також можуть з’являтися вторинно внаслідок бактеріальної коінфекції.
Нарешті, азитроміцин впливає на TGF-β-індуковану диференціацію міофібробластів, секрецію колагену фібробластами та ремоделювання позаклітинного матриксу; це відбувається за рахунок пригнічення продукції ММР [21] і фактора ендотеліального росту [22]. Зрештою ці ефекти азитроміцину обмежують руйнівні наслідки запалення, формування фіброзу та ремоделювання судин.
Клінічне застосування азитроміцину при COVID‑19
Позитивні повідомлення про ефекти азитроміцину при інших респіраторних вірусних захворюваннях спонукали до швидкого початку інтервенційних досліджень для оцінки його ефективності при COVID‑19. На момент написання огляду в базі даних клінічних випробувань clinicaltrials.gov за ключовими словами azithromycin, COVID знайдено 121 дослідження на різних стадіях виконання. На початку пандемії, за прикладом ранніх нерандомізованих серій спостережень французької групи в Марселі [23, 24], азитроміцин найчастіше призначався як допоміжний засіб до гідроксихлорохіну. Наразі від використання гідроксихлорохіну здебільшого відмовляються, але описані ефекти азитроміцину переважно встановлені в пацієнтів, які отримували комбінацію гідроксихлорохін-азитроміцин (порівняно з одним гідроксихлорохіном). Декілька опублікованих досліджень оцінювали монотерапію азитроміцином. За дизайном більшість досліджень були ретроспективними.
У дослідженнях, які вивчали монотерапію азитроміцином проти стандартної медичної допомоги госпіталізованим пацієнтам, повідомлялося про широкий діапазон ефектів – від зниження скорегованого відношення шансів (ВШ) для смертності (ВШ 0,60; 95% ДІ 0,42-0,85) у ретроспективній когорті Albani та співавт. [25] до недостовірного підвищення ВШ до 1,30 (95% ДI 0,65-2,64) за даними Kuderer і співавт. [26]. Ще більша відмінність результатів простежується в дослідженнях, які оцінювали ефекти додавання азитроміцину до гідроксихлорохіну: від покращення виживаності (скорегований відносний ризик 0,294; 95% ДI 0,218-0,396) у роботі Arshad і співавт. [27] до суттєвого підвищення 30-денної смертності (скореговане ВШ 2,93; 95% ДI 1,79-4,79) за даними Kuderer і співавт. [26]. У групі амбулаторних пацієнтів Guérin і співавт. [28] повідомляли про статистично значуще прискорення клінічного одужання пацієнтів, які отримували азитроміцин: 12,9 проти 25,8 дня в контрольній групі (p<0,0001).
Дані щодо підвищеної смертності в групах азитроміцину потребують окремого аналізу. Підвищена смертність у групах комбінованої терапії азитроміцином і гідроксихлорохіном у поєднанні з даними про збільшення частоти побічних ефектів у деяких дослідженнях може свідчити про небажану взаємодію ліків з ефектом пролонгації інтервалу QT [26, 29, 30]. Проте ці дані були отримані в ретроспективних дослідженнях із високим ступенем упередженості, тому причинно-наслідковий зв’язок є сумнівним. Цікаво, що в групах монотерапії азитроміцином не повідомлялося про підвищений ризик побічних ефектів. Cavalcanti та співавт. [29] не виявили підвищення частоти побічних ефектів, тоді як у групі гідроксихлорохіну спостерігали пролонгацію інтервалу QTc і підвищення рівня трансаміназ. Аналогічно Rosenberg і співавт. [30] відзначали підвищену частоту випадків зупинки серця в групі комбінованої терапії гідроксихлорохіном та азитроміцином (скореговане ВШ 2,13; 95% ДI 1,12-4,05) і під час порівняння гідроксихлорохіну з азитроміцином (ВШ 2,97; 95% ДI 1,56-5,64), але не виявили небажаного впливу в групі монотерапії азитроміцином під час порівняння з іншими препаратами (ВШ 0,64; 95% ДI 0,27-1,56).
Ретроспективний характер більшості досліджень накладає певні обмеження на інтерпретацію результатів. Взаємодії між ліками можуть підвищувати госпітальну смертність; з іншого боку, при нетривалому спостереженні неможливо виявити довготривалі переваги терапії азитроміцином, як-от сповільнення прогресування фіброзу. Слід ураховувати упередженість при включенні пацієнтів, яка завжди притаманна ретроспективним дослідженням. Оскільки рішення про призначення того чи іншого лікування не було визначене заздалегідь протоколом дослідження, пацієнти з легшим перебігом захворювання мали вищу ймовірність отримати призначення азитроміцину в монотерапії чи не отримати взагалі жодного з препаратів. Натомість пацієнтам, які перебували в тяжчому стані, лікарі здебільшого призначали комбіновану терапію. Крім того, на вибір тієї чи іншої терапії впливали численні фактори, крім початкових характеристик і тяжкості захворювання, зокрема доступність ліків і локальні клінічні протоколи [1].
Довідка «ЗУ»
Існують обмежені докази клінічної користі азитроміцину в лікуванні COVID‑19. Монотерапія азитроміцином безпечна та може спричинити прискорене одужання амбулаторних пацієнтів; натомість вплив на виживаність госпіталізованих пацієнтів є сумнівним. Дані щодо впливу на інтервал QT обґрунтовують ретельне моніторування ЕКГ під час застосування азитроміцину, особливо в разі призначення в комбінації з іншими ліками, що пролонгують інтервал QT, а також у пацієнтів із факторами ризику. Розпочинати терапію азитроміцином можна тоді, коли тривалість QTc <450 мс; її слід припинити, якщо інтервал перевищує 500 мс або якщо він підвищився більш ніж на 60 мс після початку терапії [31, 32].
Профілактика бактеріальної суперінфекції
Частота емпіричних призначень антибіотиків пацієнтам із COVID‑19, особливо в стаціонарі, дуже висока [33]. Лікарів до цього спонукають труднощі диференційної діагностики з атиповими пневмоніями та страх перед бактеріальною суперінфекцією. Рання бактеріальна коінфекція дійсно була важливим чинником тяжкого перебігу та смертності при історичних пандеміях грипу. Проте при COVID‑19 сукупні дані свідчать про набагато менший ризик бактеріальної коінфекції та не підтримують рутинне застосування антибіотиків. Незважаючи на те що азитроміцин може покращити результати в обмежених випадках суперінфекції, антибактеріальна профілактика не є вагомим аргументом для його систематичного застосування; її варто зважувати з ризиком резистентності збудників [1].
Вікно можливостей для застосування азитроміцину
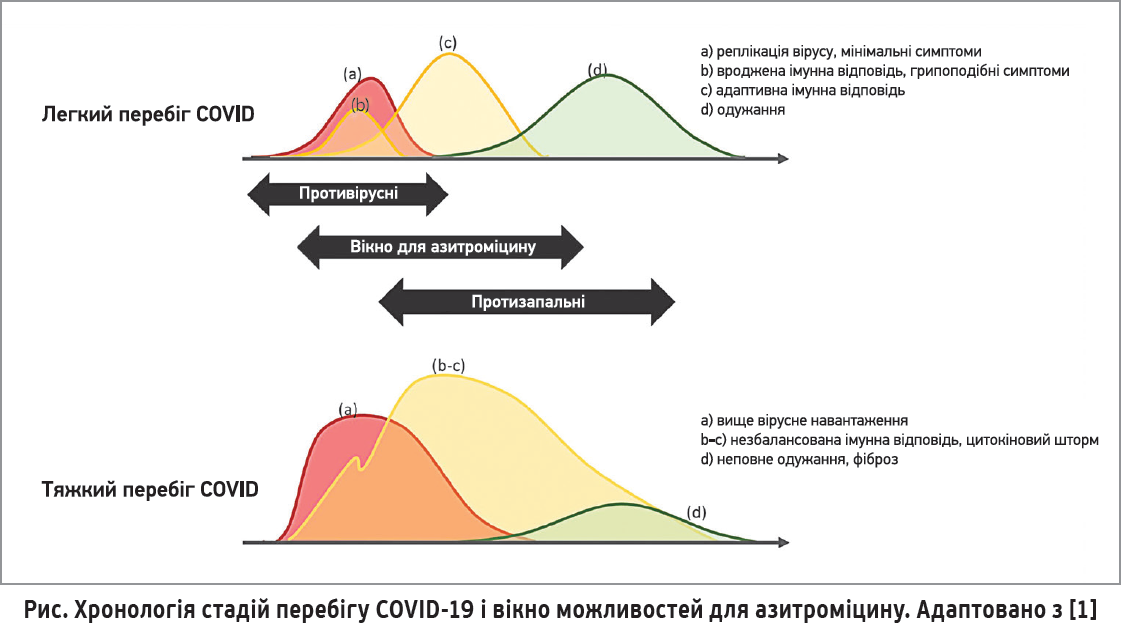
Більшість втручань мають оптимальний часовий інтервал для застосування. З механістичного погляду початок терапії азитроміцином до чи під час ранньої фази запалення є найраціональнішим (рис.). На цьому ранньому етапі противірусний ефект усе ще може бути актуальним. Однак залишається незрозумілим, чи суттєво азитроміцин пригнічує реплікацію вірусів in vivo. Наявні докази [1] краще підтверджують імуномодуляторну дію азитроміцину на запальні шляхи, що є ключовими в прогресуванні тяжкої COVID‑19. Ефекти азитроміцину здатні збалансувати адаптивну імунну відповідь, стимулювати клітинний імунітет і запобігти подальшому цитокіновому шторму. Незабаром очікуються результати великих рандомізованих контрольованих досліджень азитроміцину за участю госпіталізованих пацієнтів, зокрема RECOVERY [34].
Отже, сприятливий профіль безпеки, доступність і плейотропні механізми азитроміцину зумовили значний інтерес до цього препарату як можливої терапії COVID‑19. Його вплив на ранню фазу запалення найкраще підтверджується результатами досліджень і має особливе значення за появи перших симптомів, а також тоді, коли пацієнт звертається по медичну допомогу. Перед початком лікування азитроміцином необхідна комплексна оцінка можливих взаємодій з іншими лікарськими засобами, котрі впливають на інтервал QT, а також серцево-судинних факторів ризику, особливо тоді, коли пропонується використання в першій лінії терапії. Клінічні докази ефективності залишаються неоднозначними, але через масштаб нинішньої пандемії навіть незначний ефект лікування може реалізуватися в значуще абсолютне зниження захворюваності та смертності від COVID‑19.
Список літератури знаходиться в редакції.
* На українському фармацевтичному ринку представлений препарат азитроміцину Зиромин (компанія «Уорлд Медисин»). – Прим. ред.
Gyselinck I., Janssens W., Verhamme P., Vos P. Rationale for azithromycin in COVID-19: an overview of existing evidence. BMJ Open Respiratory Research 2021; 8: e000806.
Адаптований переклад з англ. Ігоря Петренка