17 червня, 2021
Бронхообструктивний синдром/візинг у дітей. Сучасні принципи діагностики та лікування
 Бронхообструктивний синдром (БОС) – це гетерогенний патологічний стан, який може бути проявом різноманітних нозологій, є одним із найпоширеніших симптомокомплексів у педіатричній практиці.
Бронхообструктивний синдром (БОС) – це гетерогенний патологічний стан, який може бути проявом різноманітних нозологій, є одним із найпоширеніших симптомокомплексів у педіатричній практиці.
Порівняно з європейськими країнами та зокрема із сусідньою Польщею в Україні рідше встановлюють діагноз бронхіальна астма (БА) у дітей. Так, поширеність БА серед дитячого населення у нашій країні становить 1,4-2,1% залежно від регіону проживання, у той час як у Польщі вона сягає 3,5-4,1%. Проте в Україні частіше зустрічаються такі діагнози, як обструктивний бронхіт (6,5-7,5% порівняно з 2,7-3,2% у Польщі) та візинг (11,5-13,0% порівняно з 4,8-5,2% у Польщі).
Епідеміологія та етіопатогенез
Згідно з визначенням та патогенезом, БОС означає звуження (обструкцію) дихальних шляхів, яке виникає на рівні просвіту бронхів у результаті як зворотної бронхоконстрикції, наприклад, при бронхіальній астмі (БА) та вірус-індукованому візингу, так і незворотної бронхообструкції, що розвивається при муковісцидозі, компресії бронхів пухлиною, порушенні просвіту через потрапляння стороннього тіла тощо. Свистяче дихання або свистячі хрипи при аускультації над легенями також можуть бути зумовлені обструкцією дихальних шляхів на рівні носоглотки, гортані або трахеї. Тому при появі на перший погляд класичних симптомів обструкції респіраторного тракту, таких як свистяче дихання і/або свистячі хрипи, для більш чіткого розуміння причини їх виникнення замість терміна «бронхообструктивний синдром» рекомендовано використовувати загальноприйнятий у світі термін wheezing (візинг) – синдром свистячого дихання.
Візинг – це високочастотні свистячі звуки, що виникають у результаті турбулентного руху потоку повітря при обструкції великих, середніх і дрібних бронхів, мають поліфонічний характер та зазвичай вислуховуються на видиху і поєднуються з посиленою роботою м’язів видиху.
Сьогодні відомо, що рецидивуючий візинг спостерігається у значної частини дітей віком до 5 років та, як правило, пов’язаний з інфекціями верхніх дихальних шляхів, які виникають у цій віковій групі в середньому 6-8 разів на рік (Глобальна ініціатива з бронхіальної астми – Global Strategy for Asthma Management and Prevention, GINA, 2021).
З метою оцінювання синдрому свистячого дихання у дітей віком до 6 років симптоми прийнято поділяти на 3 групи:
- перший епізод візингу у дітей віком до 2 років;
- вірус-індукований візинг:
- неатопічний візинг;
- атопічний візинг;
3. візинг при інших захворюваннях.
Перший епізод обструкції нижніх дихальних шляхів (свистячого дихання), який виникає у дітей до 2 років під час вірусної інфекції, є проявом гострого бронхіоліту, а у дітей старше 2 років – обструктивного бронхіту (в англомовній літературі його називають гострим бронхітом). Повторювані епізоди бронхообструкції, головним чином, за рахунок спазму гладеньких м’язів бронхів у дітей віком 1-5 років вважаються вірус-індукованим візингом, що відповідає застарілому терміну «рецидивуючий обструктивний бронхіт» (рис. 1).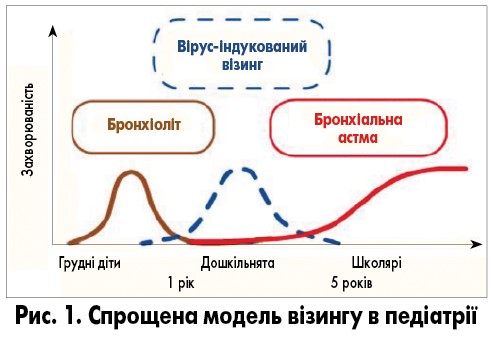
Вірус-індукований візинг може бути атопічним (спровокованим різними тригерами) або неатопічним (епізодичний вірусний візинг). Маркерами атопічного візингу в дітей дошкільного віку виступають наявність у дитини віком до 3 років атопічного дерматиту або БА в одного з її батьків, а епізоди бронхоспазму, зокрема свистячого дихання, у цьому випадку спостерігаються як при вірусних інфекціях, так і при плачу, сміху, фізичній активності, зміні кліматичних умов, контакті з тваринами, пасивному курінні тощо. Приблизно у 2/3 випадків цей фенотип візингу в подальшому трансформується в БА, що зумовлює необхідність проведення профілактичного або базового лікування. Відомо, що прояви бронхообструкції, які вперше виникли у дітей віком старше 6 років, часто пов’язані з алергічними станами та з великою ймовірністю будуть турбувати дітей і у віці 11 років та старше (G.D. Sharma, 2019).
На противагу цьому при неатопічному візингу епізоди свистячого дихання виникають лише на тлі вірусних інфекцій та у більшості випадків зникають після досягнення дитиною 6-річного віку. Причиною неатопічного вірус-індукованого візингу у дітей старшого віку, як правило, є риновіруси, а у дітей молодшого віку – параміксовіруси (С.В. Царьов, 2015).
Відомо, що фенотипи візингу з віком можуть змінюватися. Тому в частини пацієнтів неатопічний візинг все ж може трансформуватися в атопічний або в БА (О.В. Катілов, А. Валіуліс, А. Басустаогли, 2020). Також варто зазначити, що респіраторна вірусна інфекція може бути як тригером загострення, так і етіологічним фактором БА та сприяти розвитку сенсибілізації (С.В. Царьов, 2015).
У 2018 р. був запропонований новий алгоритм оцінки ризику розвитку БА у дітей раннього віку з рецидивуючим візингом – педіатрична шкала оцінки ризику розвитку астми (Pediatric Asthma Risk Score – PARS; табл. 1).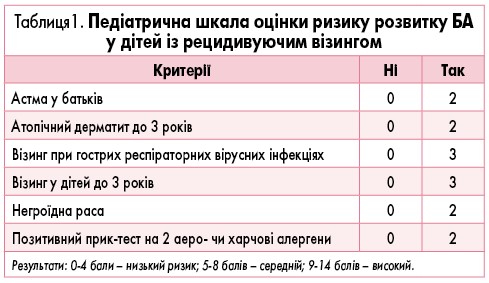
Діагностика
У дітей старше 5 років симптоми візингу в поєднанні з задишкою та відчуттям стиснення в грудній клітці, що виникають у нічний та вранішній час, є характерними ознаками БА. Для підтвердження діагнозу БА у цій віковій групі рекомендоване проведення спірометрії або пікфлоуметрії.
Передбачувана ймовірність діагнозу БА, що базується на симптомах, у дітей віком 5 років і молодше, які страждають на вірус-індукований кашель, візинг або важке дихання.
Терапія БА та візингу у дітей
Оцінка ступеня тяжкості вірус-індукованого візингу та загострення БА має важливе значення і визначає терапію: обсяг фармакотерапії, дози препаратів, місце проведення терапії (амбулаторно чи стаціонарно) і необхідність подальшої профілактики (рис. 2).
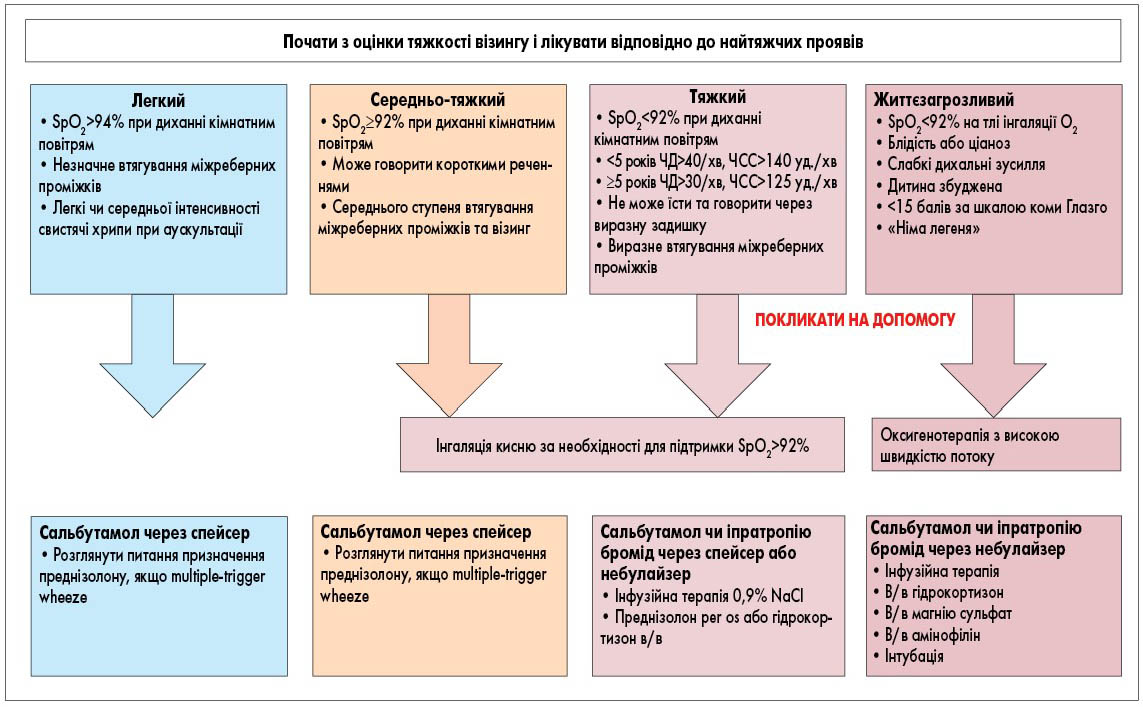 Рис. 2. Клінічна оцінка ступеня тяжкості візингу і його лікування відповідно до проявів
Рис. 2. Клінічна оцінка ступеня тяжкості візингу і його лікування відповідно до проявів
Препаратом 1-ї лінії терапії, незалежно від тяжкості стану пацієнта, є інгаляція сальбутамолу через спейсер або небулайзер. Дози сальбутамолу для терапії першого етапу (стартової терапії) при вірус-індукованому візингу і БА вказані в таблиці 2. При застосуванні сальбутамолу через небулайзер препарат не розводять, зазвичай 1 доза = 1 небула.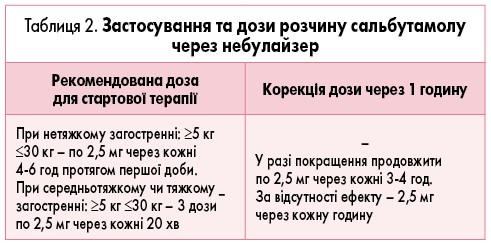
Іпратропію бромід – препарат другого ряду, його застосовують у разі відсутності або недостатнього ефекту від сальбутамолу (Sh.J. Patel, S.J. Teach, 2019). При БОС не рекомендовано застосовувати іпратропію бромід у монотерапії, тільки в комбінації з β2-агоністами. Спочатку комбіновану терапію β2-агоністами + іпратропію бромід використовують при тяжкому або загрозливому для життя загостренні.
У разі послаблення диспное і поліпшення стану дитини дози препаратів зменшують.
Особливості використання іпратропію броміду
Необхідно звернути увагу на те, що у цій віковій групі іпратропію бромід може використовуватися тільки у відділенні інтенсивної терапії при тяжкому і загрозливому для життя загостренні БА або вірус-індукованого візингу, адже відповідно до висновків Кокранівського метааналізу, комбінація β2-агоніста короткої дії з холінолітиком викликає на 44% більше побічних ефектів (таких як сухість у роті, тривожність, тремор, серцебиття, головний біль та помутніння зору), ніж монотерапія β2-агоністом короткої дії (S.W. Kirkland et al., 2017). Іпратропію бромід може спричинити розширення зіниць та параліч акомодації. При цьому побічні ефекти з боку очей можуть тривати довше, ніж терапевтичне вікно іпратропію броміду. Таким чином, інгаляційні антихолінергічні препарати як монотерапія для лікування загострення БА та вірус-індукованого візингу у дітей до 5 років не рекомендовані (GINA, 2021).
Клінічний випадок
Хлопчик, 2 роки, гостра анізокорія.
Анамнез: синдром Ді Джорджа, правобічна полімікрогірія, лівобічна геміплегія та судомний розлад. З приводу бронхіальної астми застосував іпратропію бромід через спейсер.
Об’єктивно: максимальне розширення лівої зіниці, на світло не реагує; реакції правої зіниці в нормі. Неврологічний статус у нормі.
Враховуючи обтяжений неврологічний анамнез, була виконана комп’ютерна томографія головного мозку, патологічних змін не виявлено.
Діагноз: ятрогенна анізокорія внаслідок застосування іпратропію броміду.
Обґрунтування: іпратропію бромід є антагоністом ацетилхоліну, який може спричинити розширення зіниць і параліч акомодації. Ефект від аерозольного застосування засобу настає через 30-60 хв і триває 5-6 год. У даному клінічному випадку гостра анізокорія виникла через 5 год після застосування іпратропію броміду, через 12 год реакція на світло була слабка, зіниця залишалася розширеною до 48 год, після чого нормалізувалася (рис. 3).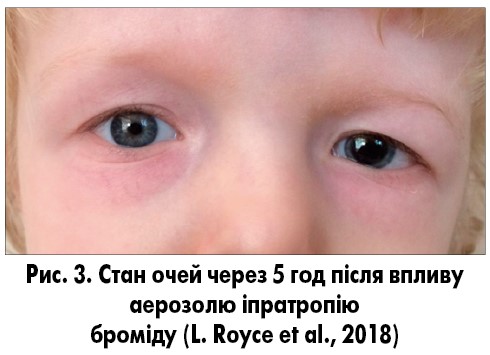
Тривалий і односторонній ефект свідчить про локальне поглинання іпратропію броміду.
Пацієнти зі схильністю до розвитку глаукоми повинні особливо ретельно піклуватися про захист очей. Ризик гострого нападу глаукоми підвищується як при потраплянні в очі розпиленого іпратропію, так і при застосуванні в комбінації з β2-агоністами. Є повідомлення про окремі випадки ускладнень з боку органа зору (збільшення внутрішньоочного тиску, вузькокутову глаукому, біль в очах). Згідно з інструкцією, препарати з іпратропію бромідом для небулізації містять незначний об’єм спеціальних допоміжних речовин.
Інгаляційний сальбутамол – бронхолітик № 1 у лікуванні бронхообструкції
Однією з найважливіших властивостей β2-агоністів є їх селективність по відношенню до β2-адренорецепторів. Селективні β2-агоністи мають менший вплив на кардіальні β-адренорецептори, що, відповідно, знижує ризик виникнення побічних ефектів, таких як тахікардія, аритмія, тремор, гіпоксемія та гіпокаліємія. У цьому аспекті очевидну перевагу має сальбутамол, селективність якого в 11,5 разу вища, ніж у фенотеролу (А.Г. Чучалін та ін., 2008).
Не менш важливим моментом, на який потрібно звернути увагу при виборі β2-агоніста з короткотривалою дією, є його доведена безпека. Це питання активно вивчається вже десятки років. Так, було продемонстровано зростання смертності від БА у Новій Зеландії в 1976 р., коли на ринок вийшов фенотерол, але згодом, після заборони цього препарату в 1989 р., смертність зменшилася (C.K. Billington et al., 2017). У рекомендаціях британського Національного інституту охорони здоров’я і удосконалення медичної допомоги (National Institute for Health and Care Excellence, NICE) за 2019 р. вказано, що в цій країні β2-агоніст фенотерол навіть не зареєстрований.
Таким чином, саме сальбутамол сьогодні залишається золотим стандартом для купірування загострень БА і вірус-індукованого візингу у дітей, починаючи з перших днів життя, і дорослих (Британське торакальне товариство – British Thoracic Society, BTS; Шотландська міжколегіальна мережа клінічних настанов – Scottish Intercollegiate Guidelines Network, SIGN, 2019). При цьому потрібно пам’ятати, що інгаляційна форма сальбутамолу забезпечує пряму доставку препарату до уражених тканин та має значно менше побічних ефектів у порівнянні з його пероральною формою. Окрім цього, інгаляційний сальбутамол ефективний у менших дозах, а його дія розвивається значно швидше (GINA, 2021).
У дослідженні Grimwood та співавт. було продемонстровано більш виражене поліпшення функції легень при застосуванні інгаляційного сальбутамолу порівняно з пероральною формою. При цьому бронхорозширювальний ефект при пероральному прийомі тривав значно довше (Grimwood et al., 1981; рис. 4).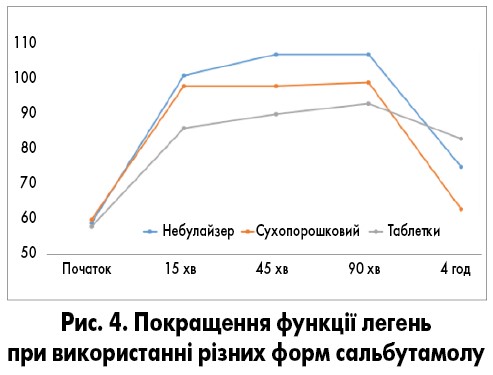
Як обрати доставковий пристрій?
Що стосується пристрою для доставки інгаляційного препарату, то при загостренні БА та вірус-індукованого візингу ряд безперечних переваг має небулайзерна терапія, яка може бути використана на всіх етапах надання медичної допомоги (у домашніх умовах, у кареті швидкої, поліклініці, стаціонарі тощо). Застосування небулайзера не вимагає координації вдиху з інгаляцією препарату, що особливо важливо для дітей раннього віку, а також у старших дітей при зміненому психічному стані під час загострення (збудженні чи загальмованості).
На українському фармацевтичному ринку препарат 1-ї лінії для лікування загострень БА та вірус-індукованого візингу сальбутамол представлений фармацевтичною корпорацією «Юрія-фарм» у вигляді розчину для інгаляцій під торговою назвою Небутамол®. Ефективність і безпека препарату Небутамол® у дітей із загостреннями БА була продемонстрована у рандомізованому клінічному випробуванні, що проводилося на базі ДУ «Інститут педіатрії, акушерства і гінекології НАМН України імені академіка О.М. Лук’янової» під керівництвом В.Ф. Лапшина і Т.Р. Уманець. Порівняно з використанням сальбутамолу у формі дозованого аерозольного інгалятора застосування препарату Небутамол® за допомогою небулайзера у дітей шкільного віку з легким і середньотяжким загостренням БА сприяло більш швидкому регресу основних клінічних симптомів, поліпшенню показників функції зовнішнього дихання і зменшенню тривалості перебування в стаціонарі при його високій безпеці і добрій переносимості. Вплив препарату Небутамол® на функцію зовнішнього дихання показаний на рис. 5.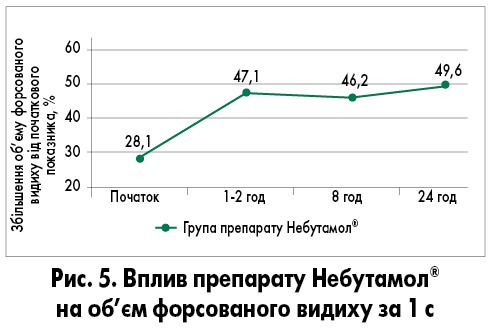
Роль ГКС-терапії у лікуванні БА та візингу у дітей
У разі відсутності ефекту від терапії бронхолітиками впродовж 1 год або у випадку розвитку загрозливого для життя загострення необхідним є ГКС. У лікуванні дітей дошкільного віку перевагу надають пероральному преднізолону, тривалість терапії становить до 5 днів (GINA, 2021). Дітям старше 6 років призначають інгаляційні глюкокортикостероїди (ГКС) у високих дозах і/або системні ГКС. Однак слід підкреслити, що ефект системних ГКС розвивається дещо пізніше (через 6 год і більше), ніж при використанні інгаляційних у високих дозах (до 3 год; G. Rodrigo et al., 1999; ICON, 2012). У низці досліджень було продемонстровано, що застосування небулізованого флутиказону, як мінімум, не поступається за ефективністю пероральним ГКС (A.I. Manjra et al., 2000), а також істотно підвищує ефективність сальбутамолу (E. Estrada-Reyes et al., 2005).
В Україні флутиказону пропіонат для небулайзерної терапії у дітей віком ≥4 років випускається під назвою Небуфлюзон® (ТОВ «Юрія-фарм»). Флутиказону пропіонат має високу спорідненість (приблизно вдвічі вищу, ніж у будесоніду) та тривалий зв’язок із ГКС-рецепторами, що надає йому потужної місцевої протизапальної дії. Згідно з інструкцією, доза препарату Небуфлюзон®, необхідна для досягнення терапевтичного ефекту, є вдвічі меншою у порівнянні з такою при застосуванні будесоніду. Небуфлюзон® є препаратом із високим профілем безпеки та мінімальними побічними ефектами при його застосуванні в терапевтичних дозах. Важливим також є те, що в терапевтичних дозах Небуфлюзон® не знижує рівень остеокальцину і пропептидів проколагену І типу – маркерів формування кісткової тканини – та не впливає на рівень карбокси-С-телопептидів колагену I типу та дезоксипіридиноліну – маркерів резорбції кісткової тканини (G.P. Bootsma, 1996).
Небулізований флутиказону пропіонат не поступається ефективністю пероральному преднізолону в лікуванні загострення БА та ефективний у дозі, що становить половину дози інших інгаляційних ГКС. Небуфлюзон® призначають з перших днів загострення БА по 1 мг (1/2 небули) 2 рази на добу через 15-20 хв після інгаляції з β2-агоністом (Небутамол®) або в одній інгаляції з ним. Комбінація небулізованих форм сальбутамолу і флутиказону (Небутамол® + Небуфлюзон®) впливає одразу на 2 механізми бронхообструкції при загостренні БА – бронхоспазм і набряк слизової оболонки, що дозволяє знизити частоту застосування системних ГКС.
Правила небулайзерної терапії
Одним із основних правил ефективної та безпечної небулайзерної терапії є належний догляд за небулайзером, що дозволяє мінімізувати ризики забруднення та колонізації бактерій у дихальних шляхах. Також міжнародна література рекомендує використовувати стерильні однодозові контейнери (Guidance CDER, 2002; A Guide, 2017).
Є 2 причини цього:
І – використання багатодозових контейнерів асоціюється із можливістю розповсюдження нозокоміальної інфекції внаслідок забруднення.
ІІ – стерильні багатодозові контейнери дають можливість менше використовувати у складі препарату консерванти. Відсутність консервантів є сучасною вимогою до інгаляційних препаратів (табл. 3).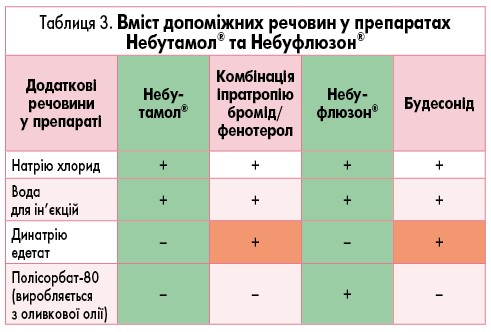
Повідомляється, що багатодозові флакони для ліків були пов’язані з забрудненням небулайзерів і можуть бути джерелом нозокоміальної інфекції (D.S. Gardenhire et al., 2017). Сьогодні, у час пандемії COVID-19, особливу увагу слід приділяти належному очищенню усіх поверхонь кімнати/зони, де проводиться інгаляція. Крім того, принципово важливо слідкувати, щоб не відбувалося обміну пристроями для інгаляцій між пацієнтами. Обов’язковим є миття рук до та після використання обладнання, а також регулярне очищення обладнання після кожного використання з дотриманням усіх інструкцій виробника (M. Cazzola et al., 2021).
Важливим є питання про використання небулайзера в період пандемії. Не існує єдиної думки щодо безпеки такого методу лікування під час пандемії СOVID-19. GINA попереджає про небезпеку інгаляції через небулайзер, оскільки це може сприяти поширенню вірусу. GINA спирається на дослідження, проведене в 2009 р., в якому брав участь тільки 1 пацієнт (D.S. Hui et al., 2009). Але такі авторитетні фахові спільноти, як Всесвітня організація охорони здоров’я, NICE, BTS, під час перегляду рекомендацій 2021 р. говорять про безпеку небулайзерної терапії на підставі результатів сучасніших досліджень і метааналізів за участю більшої кількості пацієнтів.
Чим небезпечна наявність консервантів у складі інгаляційних препаратів?
Відомо, що такі консерванти, як бензалконію хлорид та динатрію едетат, є потужними бронхоконстрикторами. Їх включення у розчин іпратропію броміду для небулайзера призвело до парадоксальної бронхоконстрикції у деяких хворих на БА та загального зниження ефективності бронходилататора. У подвійному сліпому рандомізованому клінічному дослідженні було продемонстровано зниження об’єму форсованого видиху більш ніж на 20% від вихідного рівня у пацієнтів, які отримували інгаляції препаратом, що містить ці консерванти, а вдихання розчину, що не містить консервантів, призвело до швидкої та більшої загальної бронходилатації (рис. 6).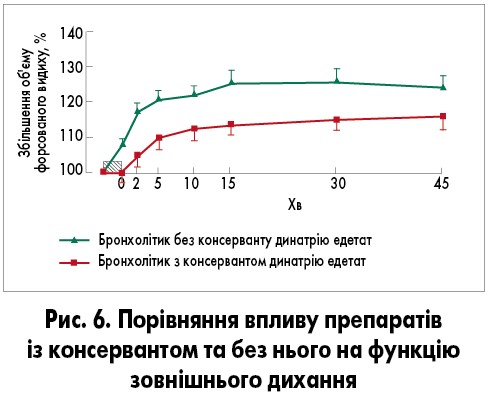
Перевагою препаратів Небутамол® та Небуфлюзон® є відсутність у їх складі динатрію едетату, який спричиняє парадоксальне звуження бронхів у значної частини хворих на БА та знижує ефективність бронхолітиків (R. Beasley et al., 1998). У порівнянні з розчинами іпратропію броміду/фенотеролу та будесоніду відсутність консервантів у складі препаратів дозволяє уникнути впливу на ефективність бронходилатації.
Отже, одночасне використання препаратів Небутамол® та Небуфлюзон® при бронхообструктивному синдромі/вірус-індукованому візингу дозволяє досягти швидкого ефекту, що проявляється усуненням симптомів та покращенням функції легень.
Основною відмінністю Небутамол® і Небуфлюзон® від інших препаратів на ринку України є відсутність у їхньому складі консервантів, які можуть викликати парадоксальний бронхоспазм. Наявність молекул Небутамол® і Небуфлюзон® у сучасних рекомендаціях та оптимальний склад роблять їх препаратами вибору при бронхообструкції у дітей.
Список літератури знаходиться в редакції.
Тематичний номер «Педіатрія» № 2 (58) 2021 р.



