4 липня, 2021
Сучасні рекомендації з діагностики та лікування функціональної диспепсії
У квітні відбувся науковий симпозіум із міжнародною участю – ХХІІІ Національна Школа гастроентерологів, гепатологів України «Коморбідні стани в гастроентерології, мультидисциплінарний підхід. Академія здорового харчування», в якому взяла участь професор кафедри внутрішньої медицини № 3 Національного медичного університету ім. О. О. Богомольця (м. Київ), керівник Гастроцентру клініки «Оберіг», доктор медичних наук Галина Анатоліївна Соловйова з доповіддю «Функціональна диспепсія. Діагностика та лікування сьогодні».
 Професор розпочала свою доповідь із клінічного випадку. Жінка, 27 років, звернулася до центру третинної допомоги з рефрактерними диспепсичними симптомами, які почали проявлятися в шкільному віці та наявні останні 10 років. Домінувальні симптоми: виражена повнота пацієнтки, тяжкість після їжі та нудота. Останнім часом хвора виключила з раціону жирну їжу. У дитинстві перенесла апендектомію. У 13 років страждала на нервову анорексію (розрішення відбулося в 15 років). Єдина дитина в родині, живе з батьками. Після навчання працювала офіс-менеджером, але 5 міс тому була змушена припинити трудову діяльність через диспепсичні скарги. Попередній діагноз – функціональна диспепсія (ФД).
Професор розпочала свою доповідь із клінічного випадку. Жінка, 27 років, звернулася до центру третинної допомоги з рефрактерними диспепсичними симптомами, які почали проявлятися в шкільному віці та наявні останні 10 років. Домінувальні симптоми: виражена повнота пацієнтки, тяжкість після їжі та нудота. Останнім часом хвора виключила з раціону жирну їжу. У дитинстві перенесла апендектомію. У 13 років страждала на нервову анорексію (розрішення відбулося в 15 років). Єдина дитина в родині, живе з батьками. Після навчання працювала офіс-менеджером, але 5 міс тому була змушена припинити трудову діяльність через диспепсичні скарги. Попередній діагноз – функціональна диспепсія (ФД).
Лікарі-гастроентерологи мають справу зі схожими випадками дуже часто, адже, за даними Американської колегії гастроентерологів (2017), періодичні симптоми диспепсії спостерігаються в ≈20% населення, причому більшість із них (70%, а це вже свідчить про ФД) формуються з боку шлунка та дванадцятипалої кишки.
Згідно з Римським консенсусом IV, діагноз ФД встановлюється за наявності ≥1 з таких тез (у разі відсутності органічної патології, тривалості симптомів протягом 3 міс, їх появи не менш ніж 6 міс тому):
- турбує відчуття переповнення шлунка після їжі;
- спостерігається передчасне насичення;
- скарги на епігастральний біль;
- з’являється відчуття епігастрального печіння.
Відповідно до Європейських рекомендацій із ведення диспепсії та гастропарезу (UEG, 2020), ФД – один із найчастіших станів, які трапляються в клінічній практиці. Факторами ризику для ФД є гострі гастроінтестинальні інфекції, антибіотики, нестероїдні протизапальні засоби, тривога, депресія, куріння тощо. ФД – основна причина витрат в охороні здоров’я; для самого пацієнта вона асоціюється зі значним зниженням якості життя, психосоціальною коморбідністю, може бути асоційована зі втратою маси тіла.
Діагноз ФД базується на клінічних симптомах, які свідчать про залучення гастродуоденальної зони: постпрандіальна тяжкість, раннє насичення, епігастральне печіння, нудота, надмірна відрижка, румінація. «Червоні прапорці»: необґрунтована втрата маси тіла, початок захворювання у віці >55 років, дисфагія (особливо прогресивна) та/або одинофагія, стійке блювання, ознаки гастроінтестинальної кровотечі – мелена, гематемезис, залізодефіцитна анемія, сімейний анамнез (рак шлунка чи стравоходу).
У Європейських рекомендаціях із ведення диспепсії та гастропарезу (UEG, 2020) для діагностики ФД пропонується використовувати аналіз крові, УЗД органів черевної порожнини, тест спорожнення шлунка, езофагеальну pH‑метрію для виключення гастроезофагеальної рефлюксної хвороби (ГЕРХ). Маркерами ФД є дуоденальна еозинофілія та порушення переносимості нутрієнтів.
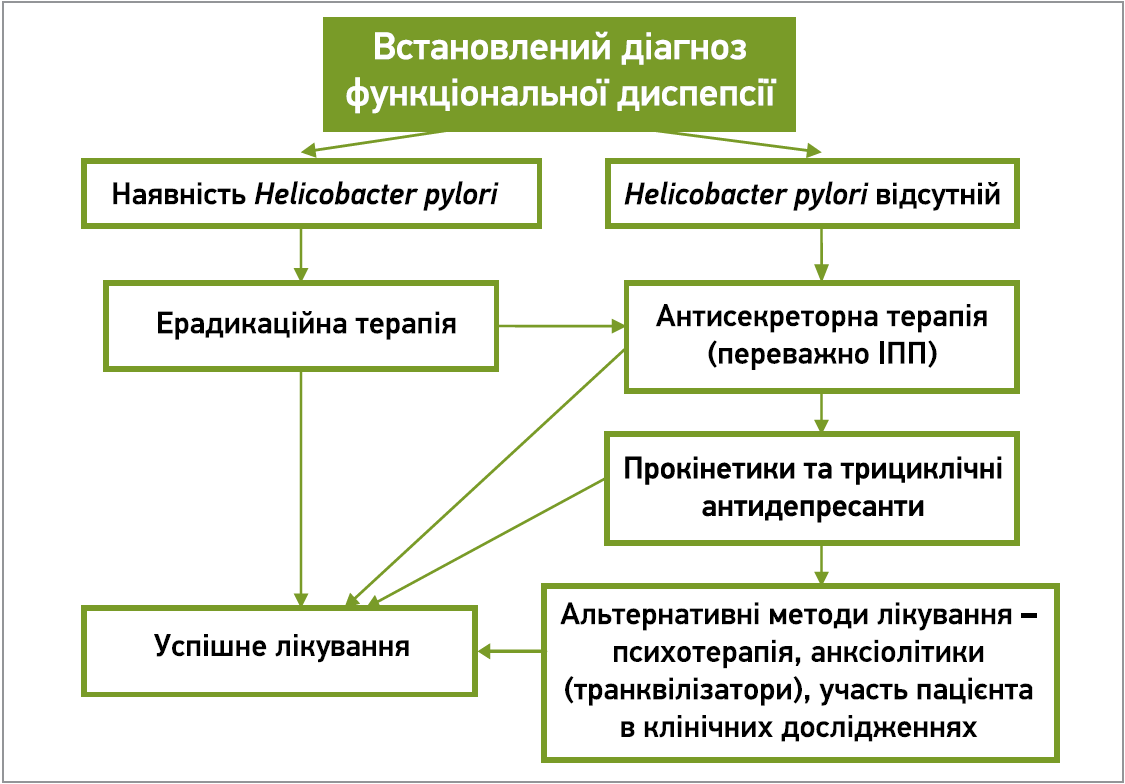
Після встановлення клінічного діагнозу ФД необхідно розпочинати емпіричне лікування; водночас слід пам’ятати, що основною метою лікування ФД є покращення якості життя. Перша лінія терапії за наявності Helicobacter pylori – ерадикаційна терапія; за її відсутності та наявності епігастрального больового синдрому (ЕБС) – інгібітори протонної помпи (ІПП), в разі постпрандіального дистрес-синдрому (ПДС) – прокінетики (рис. 1, 2). За відсутності ефекту від використання терапії першої лінії при ЕБС застосовується амітриптилін, у разі ПДС – міртазапін. За неефективності терапії другої лінії варто переходити до лікування симптомів. Для купірування болю призначаються трициклічні антидепресанти, від нудоти – протиблювальні, від раннього насичення та постпрандіального відчуття насичення – буспірон.
Рис. 1. Алгоритм лікування функціональної диспепсії
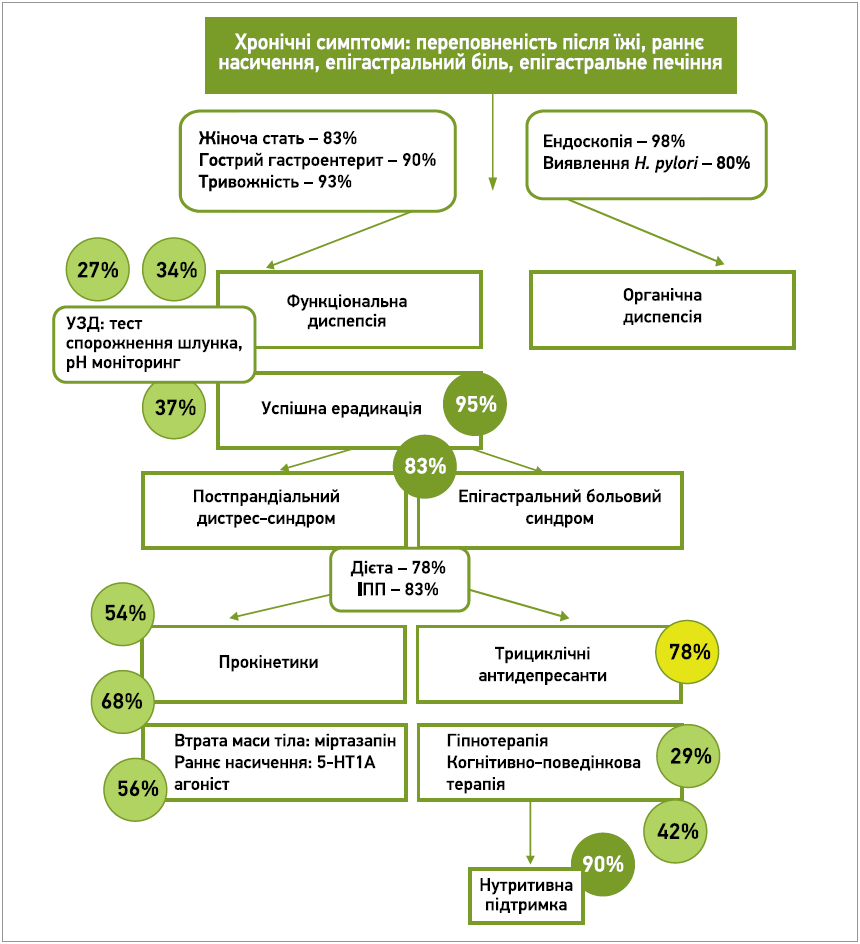 Рис. 2. Проєкт консенсусу з функціональної диспепсії (UEG, 2020)
Рис. 2. Проєкт консенсусу з функціональної диспепсії (UEG, 2020)
Однак сучасна парадигма призначення терапії для купірування симптомів ФД має дещо інший вигляд. Наприклад, останній Американський консенсус із диспепсії пропонує всім пацієнтам призначати спочатку ІПП, згодом – трициклічні антидепресанти, а наприкінці – прокінетики.
Водночас корейські дослідники пропонують тест на інфекцію H. pylori проводити тим пацієнтам із диспепсією, які не реагують на кислотні супресанти чи прокінетики.
Серед типів ФД переважає ПДС (50%); за його наявності вираженіші прояви супутніх симптомів і станів (клінічна депресія, синдром подразненого кишечнику, ГЕРХ) і найнижча оцінка якості життя. Якщо ФД супроводжується гастроезофагеальним рефлюксом, синдромом подразненого кишечнику, частота звернень по допомогу сягає 67%. Окрім того, пацієнти з таким оверлап-синдромом мають вираженіші симптоми.
При ПДС (а також за ПДС-ЕБС‑оверлап) основний фактор патогенезу – утруднення акомодації шлунка, що водночас є фактором патогенезу закрепу з уповільненим транзитом і ГЕРХ. Під терміном ПДС розуміють постпрандіальний епігастральний біль і постпрандіальну нудоту. Це значно збільшує його частку в типах ФД.
Для лікування ПДС використовуються прокінетики. У Європейських рекомендаціях із ведення диспепсії та гастропарезу (UEG, 2020) запропоновано призначення ітоприду, котрий практично не має побічних дій. Проводилися декілька клінічних досліджень, під час яких виявлено його переваги порівняно з іншими прокінетиками при лікуванні ФД, ФД-ГЕРХ. Водночас він здатен купірувати різні супутні симптоми – здуття, нудоту, печію тощо.
Нещодавно на ринку з’явився препарат Мотоприд виробництва Київського вітамінного заводу, який містить 50 мг ітоприду гідрохлориду.
Для оцінки ефективності цього препарату в лікуванні пацієнтів із ФД-ПДС на базі комунального некомерційного підприємства «Київський міський консультативно-діагностичний центр» протягом 2020 року ми провели рандомізоване проспективне дослідження. До нього увійшли 126 дорослих пацієнтів, котрі відповідали таким критеріям включення: діагноз ФД-ПДС відповідно до критеріїв Римського консенсусу IV; наявність інфекції H. pylori; повне розуміння характеру дослідження та надання письмової інформованої згоди на участь у ньому.
Пацієнтів розподілили на 2 групи: група 1 (основна) – 65 осіб, які отримували ерадикаційну терапію і прокінетик Мотоприд по 50 мг тричі на день; група 2 (порівняння) – 61 учасник, котрий отримував тільки ерадикаційну терапію. Тривалість лікування склала 14 днів, сумарна тривалість дослідження – 30 днів.
Для оцінки результатів лікування використовувалися 3 шкали: шкала Лікерта (Likert scale) – для оцінки вираженості диспепсичних і супутніх гастроентерологічних симптомів; госпітальна шкала тривоги і депресії (HADS) – для оцінки ступеня вираженості тривоги та депресії в динаміці; опитувальник SF‑36 – для оцінки показників якості життя.
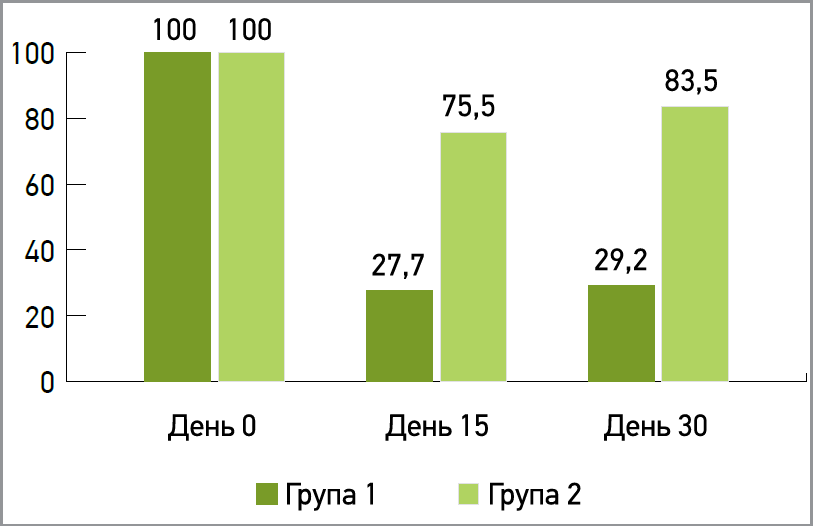
Після закінчення 14-денного курсу лікування в групі 1 наявність симптомів ФД-ПДС спостерігалася у 27,7% пацієнтів, у групі 2 цей показник був статистично значимо вищим – 75,5% (р=0,015). На 30-й день у деяких учасників мав місце рецидив симптомів, однак сумарно в групі 1 симптоми ФД-ПДС були присутні у 29,2%, натомість у групі 2 – у 83,6% включених. Аналіз результатів продемонстрував наявність статистично значимої різниці між групами (р=0,023). Таким чином, додаткове призначення прокинетика сприяє більш ефективному та тривалому зниженню симптомів ФД-ПДС порівняно з тільки ерадикаційною терапією (рис. 3).
Рис. 3. Наявність симптомів ФД-ПДС у досліджуваних групах залежно від типу лікування (%)
На початку дослідження групи були зіставними за ступенем вираженості симптому постпрандіальної тяжкості за шкалою Лікерта. Серед пацієнтів групи 1 цей показник дорівнював 5,8±0,5 бала, в групі 2-5,7±0,4 бала (р>0,05). На 15-й день ступінь вираженості постпрандіальної тяжкості в групі 1 був достовірно нижчим, ніж у групі 2-3,2±0 vs 5,0±0,2 бала відповідно (р=0,046). Ця різниця зберігалася й на 30-й день спостереження: показник у групі 1 становив 2,0±0,1, у групі 2-5,1±0,3 бала (р=0,034). Тренд зниження тяжкості симптому був більш вираженим у групі 1 (рис. 4). Таким чином, ітоприду гідрохлорид у складі комбінованої терапії статистично значимо знижує прояви постпрандіальної тяжкості за шкалою Лікерта.
Рис. 4. Бальна оцінка ступеня вираженості постпрандіальної тяжкості за шкалою Лікерта в досліджуваних групах залежно від типу лікування
На момент початку дослідження групи не відрізнялися за ступенем прояву симптому раннього насичення за шкалою Лікерта. Серед пацієнтів групи 1 цей показник склав 5,6±0,5 бала, в учасників групи 2 – 5,5±0,5 бала (р>0,05). На 15-й день ступінь вираженості раннього насичення в групі 1 був статистично значимо нижчим, ніж у групі 2, – 3,4±0,2 vs 5,1±0,5 бала відповідно (р=0,042). Динаміка зберігалася й на 30-й день: показник вираженості симптому раннього насичення дорівнював 1,7±0,2 та 4,8±0,5 бала в групі 1 та 2 відповідно (р=0,021) (рис. 5).
Рис. 5. Бальна оцінка ступеня вираженості симптому раннього насичення за шкалою Лікерта в досліджуваних групах залежно від типу лікування
Ступінь вираженості печії в групах на момент початку дослідження статистично значимо не відрізнявся, склавши 3,8±0,4 бала в групі 1 і 4,0±0,5 бала в групі 2 (р>0,05). На 15-й день спостерігалося незначне зниження вираженості показника – до 3,0±0,4 бала в групі 1 і до 3,8±0,5 бала в групі 2, проте статистично значимої різниці виявлено не було (р=0,068). На 30-й день ступінь вираженості печії в пацієнтів групи 1 був істотно нижчим порівняно з групою 2: 1,5±0,1 vs 3,5±0,3 бала відповідно (р=0,038). Таким чином, комбінована ерадикаційна і прокінетична терапія статистично значимо знижує ступінь вираженості печії на 30-й день спостереження.
Ступінь вираженості нудоти за шкалою Лікерта на початку дослідження становив 4,9±0,5 бала в групі 1 і 4,8±0,5 бала в групі 2 (р>0,05). На 15-й день спостерігалося статистично значиме зниження показника в групі 1 до 3,0±0,2 бала, в той час як у групі 2 він практично не змінився (4,6±0,4 бала; р=0,042). Подібна тенденція зберігалася й на 30-й день: ступінь вираженості нудоти в групі 1 був статистично значимо нижчим, ніж у групі 2, – 1,2±0,1 vs 4,7±0,6 бала відповідно (р=0,026). Отже, ітоприду гідрохлорид у складі комбінованої терапії статистично значимо знижує ступінь вираженості нудоти за шкалою Лікерта на 15-й і 30-й день спостереження.
Серед учасників дослідження депресія (клінічна і прихована) виявлена в 58,4% пацієнтів групи 1 і 60,6% пацієнтів групи 2 (р>0,05). На тлі лікування на 15-й день показник депресії був статистично значимо нижчим у групі 1 порівняно з групою 2 – 30,8% і 57,4% відповідно (р=0,002). На 30-й день тенденція зберігалася: серед пацієнтів групи 1 депресія спостерігалася у 18,7% учасників, натомість у групі 2 цей показник склав 52,5% (р>0,001). Отримані результати свідчать, що додаткове призначення ітоприду гідрохлориду сприяє зниженню рівня депресії в пацієнтів із ФД-ПДС.
Динаміка показників якості життя за шкалою SF‑36 також достовірно відрізнялася. Так, на 30-й день у групі 1 спостерігалося статистично значиме поліпшення показників якості життя за всіма доменами шкали. Зміни показників якості життя в групі 2 не спостерігалося (р>0,05). Отже, ітоприду гідрохлорид у складі комбінованої терапії сприяв поліпшенню якості життя пацієнтів.
Таким чином, комбінована ерадикаційна і прокінетична терапія в порівнянні з лише ерадикаційною терапією є дієвішою в лікуванні ФД-ПДС. Додаткове призначення препарату Мотоприд сприяє ефективнішому зниженню вираженості та тривалішому усуненню симптомів захворювання, зниженню рівня депресії та поліпшенню показників якості життя.
Під час спостереження в групі Мотоприду було отримано статистично значиме зниження клінічних симптомів, супутніх проявів (печії тощо) та депресії. Також відзначалося значне покращення якості життя пацієнтів, які застосовували Мотоприд.
? Чи варто проводити ерадикаційну терапію за відсутності скарг або в разі, якщо скарги з’являються рідко?
Ерадикаційна терапія – метод лікування хронічного гастриту. Необхідно мати на увазі, що в гастроентерології терміни «скарги» та «захворювання» доцільно розмежовувати. Хронічний гастрит – це виключно морфологічний діагноз; головна мета його лікування – запобігти прогресуванню каскаду Correa – виникнення розповсюдженої атрофії слизової оболонки та розвитку раку шлунка. Саме тому, згідно з Кіотським консенсусом MAPS щодо лікування гастриту та передракових станів, у разі поверхневого гастриту та за відсутності атрофії варто призначати ерадикаційну терапію. За розповсюдженої атрофії терапія також призначається, а атрофічні зміни, як доводять сучасні дослідження, мають тенденцію зникати через декілька років після проведеного лікування. За наявності кишкової метаплазії ерадикаційна терапія здатна зупинити процес, запобігаючи в такий спосіб розвитку раку шлунка. Отже, цей метод лікування варто призначати на всіх етапах розвитку хронічного гастриту. Що стосується «лікування скарг», то тут доречно прислухатися до висновків Кіотського консенсусу, який повідомляє, що ерадикаційна терапія дає ефект у лікуванні скарг в 1 з 14 пацієнтів.
? Чи варто всім хворим із хронічним гастритом проводити антигелікобактерну терапію й намагатися здійснити ерадикацію H. pylori? Можливо, доцільніше визначати патогенність штамів і вже на підставі результатів обстежень призначати лікування?
Деякі дослідження свідчать, що існує зв’язок певних штамів із розвитком патологічних станів у слизовій оболонці шлунка, але, на жаль, на сьогодні доведених рандомізованих досліджень і метааналізів, на які можна було би спиратися, немає. Проте можна сподіватися, що незабаром вони з’являться.
Висновки
- ФД – основна причина витрат в охороні здоров’я; для самого пацієнта асоціюється зі значним зниженням якості життя, психосоціальною коморбідністю, може бути асоційована зі втратою маси тіла.
- Діагноз ФД базується на клінічних критеріях і виключенні симптомів тривоги.
- Першою лінією терапії для пацієнтів із ФД є ерадикаційна терапія й ІПП, другою – прокінетики та трициклічні антидепресанти, третьою – антидепресанти (за втрати маси тіла – міртазапін), буспірон, гіпнотерапія, когнітивно-поведінкова терапія.
- Мотоприд – ефективний препарат для лікування ФД-ПДС, який достовірно зменшував прояви ПДС за шкалою Лікерта на 15-й і 30-й день спостереження (р<0,05), а також достовірно знижував ступінь вираженості нудоти за шкалою Лікерта на 15-й і 30-й день спостереження (р<0,05), печії на 30-й день (р<0,05), сприяв зниженню рівня депресії в пацієнтів із ПДС, але не впливав на рівень тривоги; достовірно покращував якість життя пацієнтів за шкалами болю, загального здоров’я та вітальності.
Підготував Олександр Соловйов
Медична газета «Здоров’я України 21 сторіччя» № 10 (503), 2021 р.