30 липня, 2021
Артеріальна гіпертензія: коморбідність і супутні захворювання
Артеріальна гіпертензія (АГ) останнім часом набула характеру епідемії та є найпоширенішим захворюванням серцево-судинної (СС) системи серед дорослого населення у світі. Це зумовило розробку програми профілактики й лікування цієї недуги в Україні. Нещодавно відбулася онлайн-конференція за темою «Артеріальна гіпертензія – коморбідність і супутні захворювання», на якій було розглянуто важливі моменти щодо факторів, які спричиняють підвищення артеріального тиску (АТ), та оптимальних підходів до терапії. Своїми міркуваннями із приводу зазначених питань поділилися з авдиторією провідні вітчизняні фахівці.
Ведення пацієнтів з АГ: додаткові можливості підвищення ефективності терапії
 Лариса Анатоліївна Міщенко, д. мед. н., професорка, завідувачка відділу гіпертонічної хвороби ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України (м. Київ), на початку доповіді акцентувала, що ефективність лікування АГ необхідно підвищити, оскільки в умовах реальної клінічної практики досягнення цільових рівнів АТ (<140/90 мм рт. ст.) у нашій країні є низьким та становить лише 14,4% (ВООЗ, 2020). Безумовно, дотримання рекомендацій, в яких представлені базові принципи антигіпертензивної терапії, що передбачають призначення інгібіторів ангіотензинперетворювального ферменту (іАПФ), блокаторів рецепторів ангіотензину ІІ (БРА) у комбінації з блокаторами кальцієвих каналів (БКК) та діуретиками – тіазидними або тіазидоподібними, є важливим та обов’язковим (ESC/ESH, 2018). Проте, на жаль, для досягнення пацієнтами дійсно ефективного контролю АТ часто цього недостатньо.
Лариса Анатоліївна Міщенко, д. мед. н., професорка, завідувачка відділу гіпертонічної хвороби ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України (м. Київ), на початку доповіді акцентувала, що ефективність лікування АГ необхідно підвищити, оскільки в умовах реальної клінічної практики досягнення цільових рівнів АТ (<140/90 мм рт. ст.) у нашій країні є низьким та становить лише 14,4% (ВООЗ, 2020). Безумовно, дотримання рекомендацій, в яких представлені базові принципи антигіпертензивної терапії, що передбачають призначення інгібіторів ангіотензинперетворювального ферменту (іАПФ), блокаторів рецепторів ангіотензину ІІ (БРА) у комбінації з блокаторами кальцієвих каналів (БКК) та діуретиками – тіазидними або тіазидоподібними, є важливим та обов’язковим (ESC/ESH, 2018). Проте, на жаль, для досягнення пацієнтами дійсно ефективного контролю АТ часто цього недостатньо.
В організмі людини рівень АТ підтримують дві важливі регуляторні системи: симпатоадреналова і ренінангіотензинова (РАС), які постійно перебувають у стані взаємодії. У контексті активації симпатичної нервової системи розуміють її вплив, як-то (Коваленко та співавт., 2019):
- Безпосередній ефект на серце.
- Ефект на артеріальні резистивні й венозні ємнісні судини.
- Стимуляція симпатичних нервів нирок із наступною активацією РАС, що також додає вазоконстрикторного компоненту і збільшення загального периферичного судинного опору.
Чинники ризику АГ, які є одночасно факторами активації симпатоадреналової системи, – це куріння, ожиріння, стрес та цукровий діабет. На жаль, дані фактори ризику мають значну поширеність у популяції та відіграють певну роль у формуванні й підтриманні високого рівня АТ.
Клінічні ознаки гіперсимпатикотонії – це переважно червоне обличчя, тремор у руках, пітливість, висока частота пульсу. Однак за певних умов таких активних ознак гіперсимпатикотонії немає; наприклад, в осіб з ожирінням спостерігається підвищена ренальна, м’язова і кардіальна симпатична активність. Слід зазначити, що часто навіть у нормотензивних пацієнтів ожиріння є тригером активації симпатичної нервової системи (Grassi et al., 2015).
У контексті патогенетичного зв’язку абдомінального ожиріння і АГ варто зауважити, що абдомінальне ожиріння, з одного боку, є тригером симпатоадреналової активності, а з іншого – прямим стимулятором розвитку інсулінорезистентності та, відповідно, гіперінсулінемії, які своєю чергою також підвищують симпатоадреналову активність. Усе це разом може призводити до розвитку АГ на тлі ожиріння. Саме так реалізується гіпертензивний ефект метаболічного синдрому.
Тому при веденні таких пацієнтів слід застосовувати особливий патогенетичний підхід на основі загальних стратегій, які ґрунтуються на доказових дослідженнях та клінічних рекомендаціях із лікування АГ. Препаратами першої лінії є, безумовно, блокатори РАС – іАПФ та БРА. До них можна додавати дигідропіридинові БКК. Згідно з австралійськими рекомендаціями щодо менеджменту пацієнтів з АГ та ожирінням (2018), вже на другому кроці терапії до іАПФ або сартанів можна додати агоніст імідазолінових рецепторів І1, який патогенетично є більш слушним у цій ситуації. Третім кроком буде вже тіазидний діуретик.
Відтак, з-поміж селективних агоністів імідазолінових рецепторів, препаратом вибору є моксонідин (Фізіотенс®). Він знижує рівень АТ через пригнічення активності симпатичної нервової системи, а з іншого боку – підвищує чутливість тканин до інсуліну. Раннє додавання моксонідину до комбінованої терапії АГ сприяє ефективному зниженню АТ завдяки зменшенню гіперсимпатикотонії.
За даними міжнародного багатоцентрового відкритого обсерваційного дослідження MERSY (2013) тривалістю шість місяців, до якого було включено близько 6 тис. пацієнтів, додавання препарату Фізіотенс® до блокаторів РАС зумовлювало суттєве зниження рівня АТ: систолічного АТ у межах 25 мм рт. ст. та діастолічного АТ – на 13 мм рт. ст.
У випробуванні ALMAZ (2006) порівнювали ефективність застосування моксонідину та метформіну в 202 осіб з АГ та метаболічним синдромом. Було показано, що за впливом на інсулінорезистентність моксонідин у дозі 0,4 мг/добу при тривалості приймання 16 тижнів не поступався метформіну. Крім того, у пацієнтів з ознаками симпатикотонії (частота серцевих скорочень >80 уд./хв) ефект підвищення чутливості тканин до інсуліну під впливом моксонідину був виразнішим порівняно із метформіном.
Лариса Анатоліївна поділилася власним досвідом застосування моксонідину (2018). Так, порівнювали п’ять антигіпертензивних засобів, серед яких еплеренон, спіронолактон, торасемід і два препарати, які впливають на симпатичну нервову активність, – моксонідин та небіволол. Моксонідин був навіть дещо ефективнішим за небіволол щодо досягнення цільового рівня АТ при резистентній АГ, особливо у пацієнтів із цукровим діабетом і центральним ожирінням. Тому моксонідин може бути препаратом вибору при резистентній АГ в осіб із метаболічним синдромом.
На завершення Л.А. Міщенко акцентувала, що препарати центральної дії є корисним доповненням до антигіпертензивної терапії у пацієнтів, в яких АТ не контролюється, особливо за наявності метаболічного синдрому та ознак симпатокотонії.
Оптимізація лікування хворих на АГ: раціональний вибір додаткової терапії
 Микола Валентинович Хайтович, д. мед. н., професор, завідувач кафедри клінічної фармакології та клінічної фармації Національного медичного університету імені О.О. Богомольця (м. Київ), висвітлив проблеми, що зустрічаються при лікуванні пацієнтів з АГ із погляду клінічної фармакології. Спікер зазначив, що проблема СС-патології в Україні залишається гострою й актуальною. Відтак, 67% летальних випадків спричинені серцево-судинними захворюваннями (УУН, 2014). Приміром, у трьох країнах Східної Європи, як-то Україна, Білорусь та Російська Федерація, у чоловіків віком 50‑54 роки ризик смерті від ішемічної хвороби серця перевищував такий у когорті чоловіків 75‑79 років у Франції (Nichols еt al., 2014). Це свідчення того, що все ще не вдається контролювати основні аспекти, які призводять не лише до розвитку АГ, але й до фатальних ускладнень.
Микола Валентинович Хайтович, д. мед. н., професор, завідувач кафедри клінічної фармакології та клінічної фармації Національного медичного університету імені О.О. Богомольця (м. Київ), висвітлив проблеми, що зустрічаються при лікуванні пацієнтів з АГ із погляду клінічної фармакології. Спікер зазначив, що проблема СС-патології в Україні залишається гострою й актуальною. Відтак, 67% летальних випадків спричинені серцево-судинними захворюваннями (УУН, 2014). Приміром, у трьох країнах Східної Європи, як-то Україна, Білорусь та Російська Федерація, у чоловіків віком 50‑54 роки ризик смерті від ішемічної хвороби серця перевищував такий у когорті чоловіків 75‑79 років у Франції (Nichols еt al., 2014). Це свідчення того, що все ще не вдається контролювати основні аспекти, які призводять не лише до розвитку АГ, але й до фатальних ускладнень.
Доповідач озвучив патогенетичні механізми розвитку судинного ремоделювання (як результат імунологічного запалення), що призводить, зокрема, до підвищення АТ. Симпатоадреналова система через гіпоксію впливає на мітохондріальну дисфункцію, внаслідок чого мітохондріальна ДНК або реактивні форми кисню вже виступають як damage-асоційовані молекулярні патерни. Після накопичення вони викликають ендотеліальну дисфункцію та зміни у судинному руслі за рахунок їх ремоделювання. Як відомо, внаслідок ремоделювання судин зростає загальний периферичний опір та, відповідно, відбувається розвиток стійкої АГ (Хайтович та співавт., 2015).
Микола Валентинович зазначив, що все починається ще з дитинства. У 2000-х рр. було проведене дослідження під керівництвом академіка В.Г. Майданника, в якому взяли участь підлітки віком 13‑14 років із короткочасним підвищенням АТ. За результатами, 5‑7% когорти учасників мали АГ. Попередньо вважалося, що це вегетативна дисфункція. Проте виявилося, що товщина комплексу інтима-медіа загальної сонної артерії у дітей значно перевищувала нормативні значення. Тобто вже був наявний каротидний атеросклероз, як у дорослої людини.
Фактори, що модифікують ризик СС-смерті (за шкалою SCORE):
- соціальна депривація – першопричина багатьох ССЗ;
- ожиріння, зокрема центральне, за даними вимірювання індексу маси тіла та окружності талії;
- гіподинамія;
- психосоціальний стрес, включно із життєво важливим виснаженням;
- сімейний анамнез передчасного ССЗ (чоловіки <50 років, жінки <55 років);
- автоімунні та інші запальні захворювання;
- основні психічні розлади;
- лікування ВІЛ-інфекції;
- фібриляція передсердь;
- гіпертрофія лівого шлуночка;
- хронічне захворювання нирок;
- синдром обструктивного апное сну.
Що стосується лікування, на сьогодні є чіткі алгоритми щодо ведення пацієнтів з АГ. Ініціація терапії має включати комбінацію двох антигіпертензивних засобів. Якщо цільового рівня АТ не досягнуто – додають третій препарат.
Важливо пам’ятати, що перш ніж посилювати антигіпертензивну терапію, необхідно з’ясувати, чи приймає хворий нестероїдні протизапальні препарати (НПЗП), чи достатній комплаєнс. Щодо НПЗП – це найбільш часто вживана група ліків, проте на тлі їх приймання порушується утворення простагландинів. У такий спосіб нівелюється ефект антигіпертензивних засобів, що може викликати як гіпертонічні кризи, так і відсутність ефективності лікування.
Окрім того, варто зважати на певні інші фактори: надмірне вживання кухонної солі, приймання психостимуляторів, спосіб життя, лікування хронічних захворювань, надмірне вживання алкоголю, недостатню кількість клітковини в раціоні тощо (Katzung, 2018).
Професор звернув увагу на препарати центральної дії, які впливають на імідазолінові рецептори. Такий препарат, як моксонідин (Фізіотенс®) має низку переваг, зокрема, забезпечує сприятливий ваготропний ефект та асоційований із незначною кількістю побічних явищ за рахунок низької афінності до α2-адренорецепторів та високої афінності до імідазолінових рецепторів.
У дослідженнях було доведено, що препарат чинить кардіо- та васкулопротективну дію, сприяє зниженню кетохоламінів у сечі, має нефропротективні властивості та, що дуже важливо, забезпечує хороший метаболічний профіль, а саме зменшує інсулінорезистентність (Fenton et al., 2006; Sharma et al., 2004). Додавання моксонідину (препарату Фізіотенс®) до комбінації антигіпертензивних засобів суттєво покращує ефективність антигіпертензивної терапії.
Важливі фармакокінетичні особливості препарату Фізіотенс®:
- Біодоступність при пероральному прийманні – 88%.
- Швидкий початок дії: Тmax – 1 год.
- Швидко врівноважувана концентрація у крові: Т1/2 – 2,5 год (5 год).
- Відсутній ефект першого проходження через печінку.
- Вживання їжі суттєво не впливає на біодоступність.
М.В. Хайтович озвучив запитання, яке турбує багатьох: що краще обрати – генерик чи бренд? Велике значення має біоеквівалентність. Тобто генеричний препарат повинен забезпечувати відповідну концентрацію діючої речовини у крові й терапевтичну еквівалентність – зв’язок із рецептором і, відповідно, ефекти, на які очікують від даного лікарського засобу. Також важливо, щоб препарат був виготовлений із застосуванням сучасних фармацевтичних підходів. Якість виробництва субстанції та готових лікарських форм оригінального препарату Фізіотенс® відповідає міжнародному стандарту GMP.
У контексті питання, чи буде генеричний лікарський засіб так само ефективний, як оригінальний препарат, лектор навів дані дослідження, в якому порівнювали ефективність оригінального моксонідину – препарату Фізіотенс® із генеричними засобами при гіпертонічному кризі (АТ – 200/110 мм рт. ст.) (Руксін та співавт., 2015). Загалом було включено 179 пацієнтів (середній вік – 68 років) із тривалим анамнезом АГ (близько 22 років). Згідно з отриманими результатами, Фізіотенс® виявився на 25% ефективніший щодо зниження АТ вже через 30 хв після застосування (рисунок).
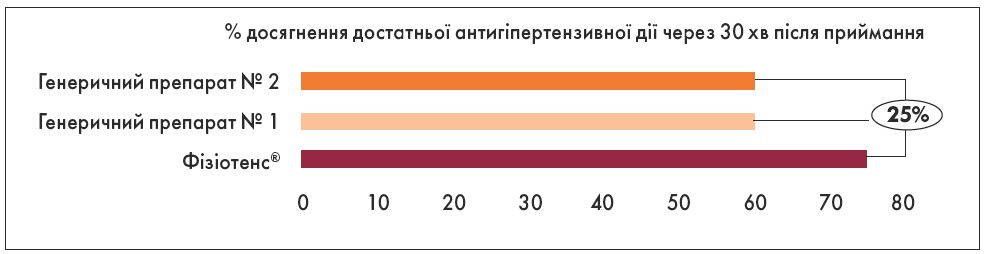 Рис. Ефективність препарату Фізіотенс® порівняно з генеричними лікарськими засобами моксонідину при різкому підвищенні АТ
Рис. Ефективність препарату Фізіотенс® порівняно з генеричними лікарськими засобами моксонідину при різкому підвищенні АТ
Таким чином, відповідно до зазначених даних можна дійти висновків, що моксонідин (Фізіотенс®):
- чинить центральну дію, зменшуючи периферичну симпатичну активність та загальний периферичний судинний опір;
- має сприятливу переносимість;
- характеризується низьким потенціалом щодо взаємодії з іншими ліками;
- відрізняється від генериків за фармакокінетикою;
- може застосовуватися як допоміжний засіб при лікуванні АГ і неускладненому гіпертензивному кризі;
- покращує метаболічний профіль у пацієнтів з АГ та цукровим діабетом, метаболічним синдромом чи порушенням толерантності до глюкози;
- може використовуватися в осіб з АГ і супутніми бронхіальною астмою та/або хронічним обструктивним захворюванням легень.
Підготувала Мар’яна Гнатів
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (76) 2021 р.



