9 вересня, 2021
Ектоін: механізми респіраторної цитопротекції
 Для розуміння механізмів цитопротекції насамперед слід розглянути види клітинної смерті.
Для розуміння механізмів цитопротекції насамперед слід розглянути види клітинної смерті.
Сьогодні виокремлюють декілька типів клітинної смерті: без значних порушень клітинної мембрани (апоптоз, автофагія та аноїкіс (anoikis, із грецької ἀν- «без», οἶκος – «будинок») – окремий випадок клітинної загибелі шляхом апоптозу, яка настає у відповідь на неправильну адгезію клітин або її втрату); з літичною та запальною формами клітинної загибелі (піроптоз, некроптоз і фероптоз) [6].
Неконтрольовано клітини гинуть унаслідок їхнього раптового структурного ушкодження під впливом екстремальних фізико-хімічних або механічних факторів. Такий незворотний біологічно неконтрольований варіант клітинного руйнування зазвичай називають випадковою смертю клітини. Так, некроз – це патологічна форма загибелі клітин, що з’являється при гострому ушкодженні та спричиняє руйнування клітинних і внутрішньоклітинних мембран, у т. ч. мембран лізосом, що обумовлює вихід лізосомальних ферментів, протеоліз і ушкодження ядра клітини – каріолізис [20].
Водночас у більшості випадків смерть клітини ініціюється генетично зумовленим механізмом (регульована загибель клітин – regulated cell death, RCD). RCD може вважатися частиною фізіологічної програми та містить чітко структуровані сигнальні каскади й молекулярно визначені ефекторні механізми, а також використовується організмом у разі неспроможності адаптивної відповіді на вплив несприятливих внутрішньоклітинних і позаклітинних факторів [1].
Нерідко програмована загибель клітин прирівнюється до апоптозу, однак відомі й неапоптичні форми клітинної смерті – автофагія, некроптоз, піроптоз, фероптоз, ентоз, нетоз, партанатос, залежна від лізосом загибель клітин, залежна від автофагії загибель клітин, алкаліптоз, оксейптоз тощо [20]. Поглиблене розуміння кожної з цих летальних підпрограм і їхніх міжклітинних наслідків може виявити нові терапевтичні цілі для уникнення патогенної втрати клітин [9].
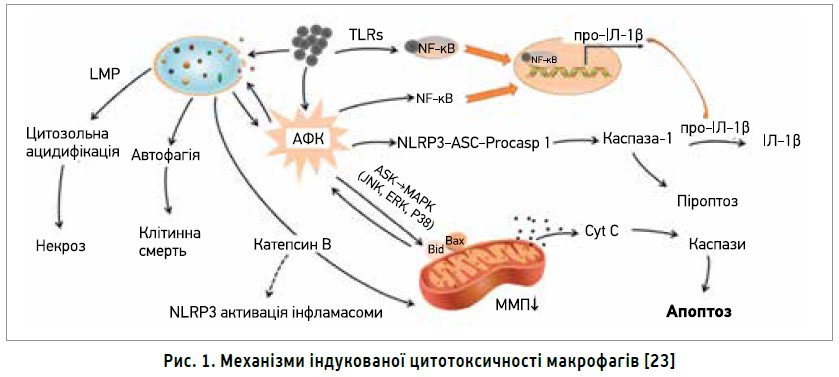
Недостатній транспорт кисню (особливо на тлі високих метаболічних потреб) швидко виснажує енергетичні системи клітини та запускає механізми її загибелі, при цьому гіпоксія є одним з пускових факторів розвитку як апоптозу, так і некрозу клітин [1]. На рисунку 1 продемонстровано каскад клітинних і молекулярних подій, як-от генерація активних форм кисню (АФК) і ушкодження лізосом, які зумовлюють некроз, апоптоз, піроптоз. Через оксидативний стрес MAPK‑шляхом з’являються залежні від мітохондрій апоптичні каскади. АФК активують низку транскрипційних факторів, у т. ч. NF‑κB, який регулює запальну відповідь. Унаслідок індукції проникності лізосомальних мембран (lysosomal membrane permeabilization, LMP) відбувається транслокація катепсинів до цитоплазми.
Відомо про цитопротекторну роль автофагії [11], однак масивна проникність лізосомальних мембран спричиняє дисфункцію автофагії. В результаті активації каспази‑1 вивільняється велика кількість інтерлейкіну 1β, що зумовлює запалення, порушення цілісності плазматичної мембрани та швидке вивільнення назовні вмісту клітини (інфламасома-залежний піроптоз) [23].
Ефективне пригнічення процесів, які зазвичай розглядають як причину регульованої клітинної смерті, як-от активація ефекторних каспаз у процесі апоптозу, не забезпечує справжнього захисного ефекту в організмі ссавців, а лише змінює кінетику смерті клітин унаслідок порушення клітинного морфологічного, а також біохімічного зв’язку [1]. Натомість справжньої цитопротекції можна досягти за допомогою пригнічення летальної сигналізації у ранній фазі процесу, коли адаптивні реакції ще здатні до регулювального впливу [9].
Отже, сучасні уявлення про цитопротекцію припускають можливість і необхідність раннього впливу на фактори, що запускають процеси загибелі клітин.
Різні організми з метою цитопротекції розробили різноманітні механізми захисту від стресу, спричиненого чинниками зовнішнього середовища, як-от посуха чи екстремальні температури. Також відомо, що коливання осмолярності навколишнього середовища є фактором стресу в багатьох природних середовищах існування мікроорганізмів, оскільки вони зумовлюють осмотично спричинені потоки води через напівпроникну цитоплазматичну мембрану. Бактерії (особливо ті, що живуть в екстремальних умовах) мають здатність виробляти сполуки невеликої молекулярної маси, відомі як сумісні розчинені речовини чи осмоліти (осмопротектори), які не перешкоджають клітинним процесам. Натомість через накопичення осмолітів у гіперосмолярних умовах мікроорганізми чинять опір згубним наслідкам виходу із клітини води та подальшого зневоднення цитоплазми і зниження тургору [5].
За структурою сумісні розчинені речовини належать до таких груп: цукри (сахароза, трегалоза), поліоли (сорбіт, гліцерин, маніт, манозилгліцерамід, манозилгліцерин), N‑ацетильовані діамінокислоти (N‑ацетилглутамінілглутаміновий амід), бетаїни (бетаїн, гліцин, деривати), амінокислоти та їхні похідні (пролін, глутамат, глутамін, аланін, ектоін, гідроксиектоін) [3].
Ектоін – це низькомолекулярний циклічний тетрагідропіримідиновий органічний осмоліт, який уперше був ідентифікований у галофільній бактерії Ectothiorhodospira halochloris, але відтоді його знаходили в інших екстремофільних мікроорганізмах (здебільшого аеробних), хемогетеротрофних і галофільних бактеріях, як-от α-, γ-протеобактерії та Actinobacteridae, в яких він стабілізує клітинні мембрани, ферменти, нуклеїнові кислоти при екстремальних температурах або високих концентраціях солі [3].
Синтез ектоіну з його попередника (L‑аспартат-β-семіальдегіду) каталізується ферментами, включаючи ацетилтрансферазу діаміномасляної кислоти (DABA) (ectA), амінотрансферазу DABA (ectB) і синтазу ектоіну (ectC). Гени, що кодують ці ферменти, організовані в оперонах ectABC або ectABC‑ask [3].
Ектоін посилює зв’язки між сусідніми молекулами води та збільшує їхню кількість, перетворюючи воду з хаотичної рідини в структурований гідрокомплекс, що оточує клітини слизових оболонок захисним шаром, забезпечуючи бар’єрний захист слизових оболонок. За результатами низки біофізичних досліджень установлено, що ектоін зв’язує молекули води краще за деякі інші осмопротектори (як-от гліцерин), зберігає потужні гідратаційні властивості навіть при високих концентраціях NaCl, добре переноситься людьми, тваринами та різними культурами клітин [3], зокрема, може запобігти старінню шкіри [16].
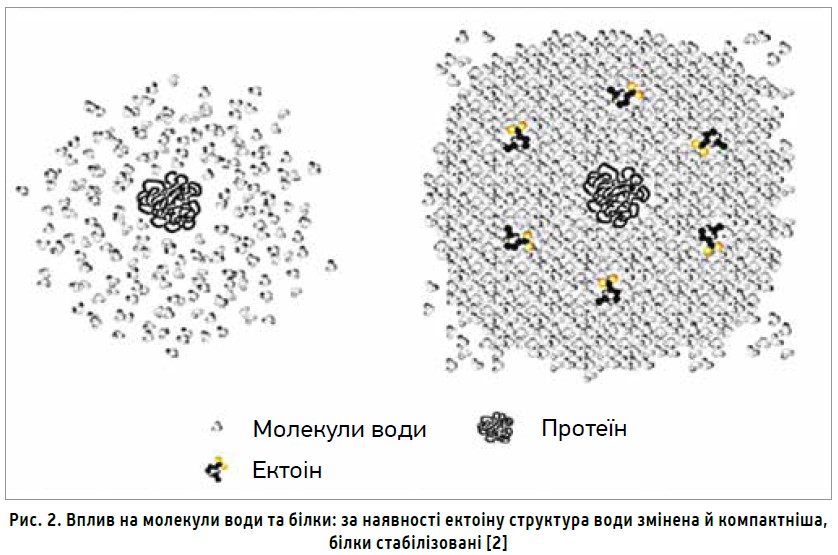
Хоча механізм дії ектоіну остаточно невідомий, існує декілька гіпотез, що пояснюють біофізичні принципи, за якими він діє. Найбільш загальноприйнятою гіпотезою є модель преференційного виключення (або пільгового зволоження), згідно з якою осмопротектори не взаємодіють безпосередньо з макромолекулою у водному розчині, а лише з молекулами води, що прилягають до поверхні білка, збільшуючи гідратацію макромолекули, внаслідок чого спостерігається відштовхування білка, який складається компактніше, краще зберігає свою структуру, менше зазнає термодинамічного зв’язування (рис. 2). Отже, ектоін має стабілізувальну роль у рецепторних структурах [3]. Остаточно не з’ясовано, чи ектоін, який зовнішньо застосовується, діє ззовні, чи поглинається, оскільки здійснює ефективний захист від осмотичного стресу [14].
Проведено багато експериментальних досліджень з вивчення цитопротекторної дії ектоіну. Встановлено, що ектоін (але не гідроксиектоін або бетаїн) за токсичності, спричиненої поліглютаміном, зменшував загальну кількість агрегатів, чисельність великих цитоплазматичних включень та збільшував частоту ядерних включень. Незважаючи на наявність ядерних включень, після застосування ектоіну рідше спостерігалися апоптотичні зміни [23].
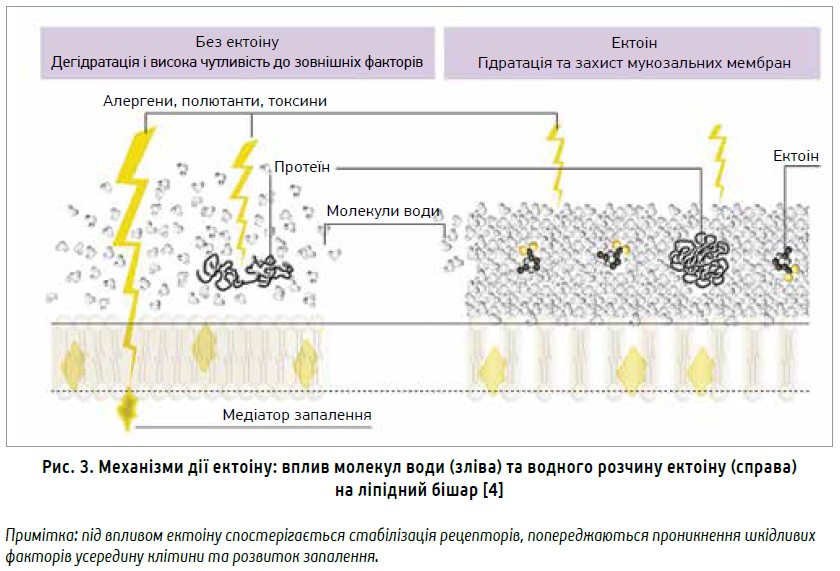
Ектоін ефективно полегшував нейтрофільне запалення легень щурів, зумовлене вуглецевими наночастинками, через пригнічення прозапальної сигналізації [17]; водночас він пом’якшував у мишей запальні реакції в епітеліальних клітинах легень після вдихання вуглецевих наночастинок. Однак цей ефект не спостерігався при запаленні, індукованому бактеріальним ліпополісахаридом [10]. Установлено, що інгаляційний вплив наночастинок вуглецю спричиняв накопичення керамідів у ліпідних плотах клітинних мембран, активацію рецептора епідермального фактора росту (EGFR) і запалення легень [13]. Однак у тварин, які додатково отримували ектоін, спостерігалися м’якіші алергічні реакції, оскільки ектоін пригнічував опосередковане керамідом фосфорилювання EGFR. Знижений рівень IL‑6 у сироватці крові свідчив про вплив ектоіну щодо попередження системного запалення (рис. 3) [22].
Доведено профілактичний ефект ектоіну на індукцію антиапоптотичної сигналізації. Нейтрофільне запалення легень, спричинене одноразовим або багаторазовим впливом на тварин токсичними наночастинками, було зменшено після введення ектоіну. Аналіз нейтрофілів із бронхоальвеолярного промивання свідчить про те, що ефект in vivo обумовлений попередженням апоптозу нейтрофілів [18]. Ці висновки були підтверджені та розширені в експериментах з культивованими клітинами бронхіального епітелію людини, в яких ектоін пригнічував сигналізацію клітин, зумовлену наночастинками, й індукцію IL‑8 [17].
Результати інших досліджень довели, що ектоін і гідроксиектоін підсилювали поверхнево-активні речовини легень, що свідчить про їхнє потенційне використання як допоміжних факторів при інгаляційній терапії [8].
Накопичено результати клінічних досліджень з оцінки ефективності та безпечності застосування ектоіну як допоміжного засобу при лікуванні запальних захворювань верхніх дихальних шляхів, у т. ч. оцінювався вплив на алергічне запалення. Під час порівняння впливу (в пацієнтів з алергічним ринітом) топічних засобів зі вмістом ектоіну, як-от назальний спрей, очні краплі, з впливом засобів на основі азеластину й кромогліцинової кислоти виявлено високу ефективність ектоіну, при цьому не спостерігалося побічних ефектів [21]. За результатами подвійного сліпого рандомізованого плацебо-контрольованого перехресного дослідження 46 пацієнтів з алергічним ринокон’юнктивітом очні краплі та назальний спрей, що містили ектоін, суттєво зменшували такі специфічні симптоми, як чхання, сльозотеча, свербіж очей (p≤0,021), а також «свербіж вуха / піднебіння» (p=0,036). Водночас продемонстровано високий профіль безпеки ектоіну [15]; його ефективність за алергічного риніту доведена й іншими дослідниками [12].
Для оцінки ефективності застосування ектоіну при лікуванні гострого бронхіту до клінічного дослідження було залучено 135 пацієнтів (79 отримували інгаляційний розчин ектоіну, а щодо 56 осіб застосовували сольовий інгаляційний розчин). Після лікування прояви симптомів захворювання суттєво зменшилися в обох групах (p<0,05), але ефект у групі ектоіну був більшим і спостерігався раніше, ніж у групі фізіологічного розчину. Відмінності в площі під кривою симптомів задишки та результатів аускультації були на користь ектоіну (p<0,05). Після лікування більша кількість пацієнтів і лікарів із групи ектоіну оцінювали стан як «повністю відновлений» або «значно покращений» (порівняно із групою фізіологічного розчину). Майже всі хворі та лікарі оцінювали переносимість обох способів лікування як «хорошу» або «дуже хорошу». Було зроблено висновок, що інгаляційний розчин ектоіну є ефективнішим за сольовий розчин при лікуванні бронхіту [19].
Отже, ектоін належить до органічних осмолітів, які широко синтезуються деякими бактеріями у відповідь на високу солоність / осмолярність та/або екстремальне підвищення температури. Перенесений до біологічних систем ектоін через формування «ектоін-гідрокомплексу» оточує себе (як і сусідні білки та клітинні мембрани) водним шаром, протидіючи інтенсивним впливам на клітину несприятливих факторів зовнішнього середовища (попереджуючи некроз). Окрім зволожувальних властивостей, ектоін обмежує каскад запальних реакцій на мембранному рівні (попереджає регульовану загибель клітин), зокрема в клітинах епітелію дихальних шляхів.
Ектобріс (ТОВ «Юрія-Фарм») – перший на фармацевтичному ринку України інгаляційний Ектоін®. Ця натуральна молекула є оригінальною німецькою розробкою в сфері біотехнологій; виробляється компанією Bitop AG Germany з 1993 р. Молекула не взаємодіє з білками, а завдяки утворенню структурованого гідрокомплексу здатна захищати клітини від алергенів, вірусів, бактерій та хімічних агентів.
Література
1. Федорова О. А. Цитопротекция в хирургии. Потенциал клинического применения препарата Метамакс. Український медичний часопис. 2014; 104 (6). https://www.umj.com.ua/article/82937.
2. Bilstein A. et al. Ectoine in the Treatment of Irritations and Inflammations of the Eye Surface. BioMed Research International.2021; 2021. Article ID8885032, 16 pageshttps://doi.org/10.1155/2021/8885032.
3. Bownik A., Stępniewska Z. Ectoine as a promising protective agent in humans and animals Arh Hig Rada Toksikol 2016; 67: 260-265.
4. Casale M. et al. Topical Ectoine: A Promising Molecule in the Upper Airways Inflammation – A Systematic Review. HindawiиBioMed Research International.2019; 2019, Article ID7150942, https://doi.org/10.1155/2019/7150942.
5. Czech L. et al. Role of the Extremolytes Ectoine and Hydroxyectoine as Stress Protectants and Nutrients: Genetics, Phylogenomics, Biochemistry, and Structural Analysis. Genes 2018, 9, 177; doi: 10.3390/genes9040177.
6. FitzGerald E. S. Competitive Cell Death Interactions in Pulmonary Infection: Host Modulation Versus PathogenManipulation. Front. Immunol. 11:814. doi: 10.3389/fimmu.2020.00814.
7. Furusho K. et al. Ectoine alters subcellular localization of inclusions and reduces apoptotic cell death induced by the truncated Machado-Joseph disease gene product with an expanded polyglutamine stretch. Neurobiol Dis. 2005; 20 (1): 170-178. doi: 10.1016/j.nbd.2005.02.011.
8. Harishchandra R.K. et al. Compatible solutes: Ectoine and hydroxyectoine improve functional nanostructures in artificial lung surfactants. Biochim Biophys Acta 2011; 1808: 2830-40. doi: 10.1016/j.bbamem.2011.08.022.
9. Galluzzi L. et al. Molecular mechanisms of cell death: recommendations of the Nomenclature Committee on Cell Death 2018. Cell Death & Differentiation (2018) 25: 486-541. https://doi.org/10.1038/s41418-017-0012-4.
10. Kroker M. et al. Preventing carbon nanoparticleinduced lung inflammation reduces antigen-specific sensitization and subsequent allergic reactions in a mouse model. Part Fibre Toxicol 2015; 12: 20. doi: 10.1186/s12989-015-0093-5.
11. Moreau K. et al. Cytoprotective roles for autophagy. Current Opinion in Cell Biology 2010, 22: 206-211.
12. Mrukwa-kominek E., Janiszewska-Salamon J., Luboń W. Ectoine in the treatment of ocular allergy. Ophthalmol J.2016; 1, supl. 1, 1-3. doi: 10.5603/OJ.2016.0014.
13. Peuschel H. et al. Carbon nanoparticles induce ceramide- and lipid raft-dependent signalling in lung epithelial cells: a target for a preventive strategy against environmentally-induced lung inflammation. Part Fibre Toxicol 2012; 9: 48. doi: 10.1186/1743-8977-9-48.
14. Rieckmann T. et al. The inflammation-reducing compatible solute ectoine does not impair the cytotoxic effect of ionizing radiation on head and neck cancer cells. Scientific RepoRts. 2019; 9: 6594 | https://doi.org/10.1038/s41598-019-43040-w.
15. Salapatek A.M., Werkhäuser N., mail B, Mösges R., Raskopf E., Bilstein A. Effects of ectoine containing nasal spray and eye drops on symptoms of seasonal allergic rhinoconjunctivitis. Clin Transl Allergy. 2021; 11: e12006. https://doi.org/10.1002/clt2.12006.
16. Singh O.V., Gabani P. Extremophiles: radiation resistance microbial reserves and therapeutic implications. Journal of Applied Microbiology.2011. 110, 851-861. doi:10.1111/j.1365-2672.2011.04971.x.
17. Sydlik U. et al. The Compatible Solute Ectoine Protects against Nanoparticle-induced Neutrophilic Lung Inflammation. Am J Respir Crit Care.2009; 180: 29-35. doi: 10.1164/rccm.200812-1911OC.
18. Sydlik U. Recovery of neutrophil apoptosis by ectoine: a new strategy against lung inflammation. Eur Respir J 2013; 41: 433-442. doi: 10.1183/09031936.00132211.
19. Tran B-H. et al. Ectoine-Containing Inhalation Solution versus Saline Inhalation Solution in the Treatment of Acute Bronchitis and Acute Respiratory Infections: A Prospective, Controlled, Observational Study. BioMed Research International. 2019; 2019, Article ID7945091, 8 pages https://doi.org/10.1155/2019/7945091.
20. Tan D. et al. The molecular machinery of regulated cell death. Cell Research. 2019; 29: 347-364; https://doi.org/10.1038/s41422-019-0164-5.
21. Werkhäuser N. et al. Treatment of Allergic Rhinitis with Ectoine Containing Nasal Spray and Eye Drops in Comparison with Azelastine Containing Nasal Spray and Eye Drops or with Cromoglycic Acid Containing Nasal Spray Journal of Allergy.2014; 2014, Article ID176597, 13 pages http://dx.doi.org/10.1155/2014/176597.
22. Unfried К. et al. The Compatible Solute Ectoine Reduces the Exacerbating Effect of Environmental Model Particles on the Immune Response of the Airways. Journal of Allergy.2014; 2014, Article ID708458, 7 pages http://dx.doi.org/10.1155/2014/708458.
23. Yuan X. et al. Cellular Toxicity and Immunological Effects of Carbon-based Nanomaterials Particle and Fibre Toxicology (2019) 16:18 https://doi.org/10.1186/s12989-019-0299-z.