30 жовтня, 2021
Нове в системному лікуванні поширеного та метастатичного нирковоклітинного раку
 Сучасні терапевтичні опції у пацієнтів із поширеним нирковоклітинним раком (НКР) істотно відрізняються від застосовуваних 2 роки тому, що відображено в оновлених клінічних настановах міжнародних організацій. Нещодавно опубліковані результати досліджень KEYNOTE‑564 та KEYNOTE‑426 демонструють ефективність імунотерапії при поширених формах НКР.
Сучасні терапевтичні опції у пацієнтів із поширеним нирковоклітинним раком (НКР) істотно відрізняються від застосовуваних 2 роки тому, що відображено в оновлених клінічних настановах міжнародних організацій. Нещодавно опубліковані результати досліджень KEYNOTE‑564 та KEYNOTE‑426 демонструють ефективність імунотерапії при поширених формах НКР.
У рамках вебінару «Комплексне лікування місцевих, поширених та метастатичних форм пухлин нирки» доповідь на тему «Нове в системному лікуванні поширеного та метастатичного нирковоклітинного раку» представив старший науковий співробітник відділення пластичної та реконструктивної онкоурології Національного інституту раку (м. Київ), кандидат медичних наук Олександр Едуардович Стаховський.
– Одним із ключових факторів, котрі впливають на вибір терапії при метастатичному НКР, є визначення групи ризику. Згідно з оновленими клінічними настановами Національної онкологічної мережі США (NCCN), використовують дві основні моделі ризику: прогностичну модель Меморіального онкологічного центру ім. Слоуна – Кеттерінга (MSKCC) та прогностичну модель Міжнародного консорціуму з метастатичного нирковоклітинного раку (IMDC). У клінічній практиці для визначення групи ризику частіше використовують прогностичну модель IMDC (табл. 1).
За останні 2 роки відбулися значні зміни у лікуванні метастатичного НКР. Згідно з клінічними настановами Європейської асоціації урології (EAU, 2018), для терапії пацієнтів групи сприятливого прогнозу (за IMDC) були рекомендовані сунітиніб або пазопаніб у першій лінії терапії, кабозантиніб або ніволумаб – у другій та третій лінії терапії, для пацієнтів групи проміжного та несприятливого прогнозу – іпілімумаб/ніволумаб або кабозантиніб, сунітиніб чи пазопаніб у першій лінії терапії, кабозантиніб або VERG-таргетна терапія чи ніволумаб у другій лінії терапії, кабозантиніб або альтернативний таргетний препарат чи ніволумаб – у третій лінії терапії. В оновлених рекомендаціях NCCN з’являються нові терапевтичні опції як для пацієнтів зі сприятливим прогнозом, так і для хворих групи проміжного та несприятливого прогнозу у вигляді комбінації таргетних та імунотерапевтичних засобів (табл. 2).
На конгресі Американського товариства клінічної онкології (ASCO), що пройшов на початку червня цього року, були представлені оновлені результати рандомізованого подвійного плацебо-контрольованого багатоцентрового дослідження KEYNOTE‑564 (NCT03142334). Його метою є вивчення безпеки й ефективності застосування пембролізумабу як ад’ювантної терапії у пацієнтів з НКР після нефректомії. У дослідження було включено 994 пацієнти з НКР групи високого ризику, яким виконали нефректомію щонайменше за 12 тижнів до рандомізації та які попередньо не отримували системної терапії. Критеріями помірного високого ризику були pT2 4 ступеня або саркоматоїд N0M0, або pT3 будь-якого ступеня N0M0, критерії високого ризику – pT4 будь-якого ступеня N0M0 чи pT будь-якої стадії та ступеня при N+M0. У дослідження також були включені пацієнти з метастазами (M1 NED – немає ознак захворювання після видалення первинної пухлини + метастази в м’яких тканинах, які були повністю видалені ≤1 року після нефректомії). Учасники були рандомізовані у співвідношенні 1:1 на групи пембролізумабу та плацебо. Первинною кінцевою точкою дослідження була виживаність без хвороби (ВБХ), вторинною кінцевою точкою – загальна виживаність (ЗВ). Згідно з отриманими даними, ад’ювантна терапія пембролізумабом мала перевагу над плацебо як через 12, так і через 24 місяці спостереження (відношення ризиків – ВР – 0,68; 95% довірчий інтервал – ДІ – 0,53-0,87; P=0,0010; рис. 1). Медіана ВБХ не досягнута у жодній з груп.
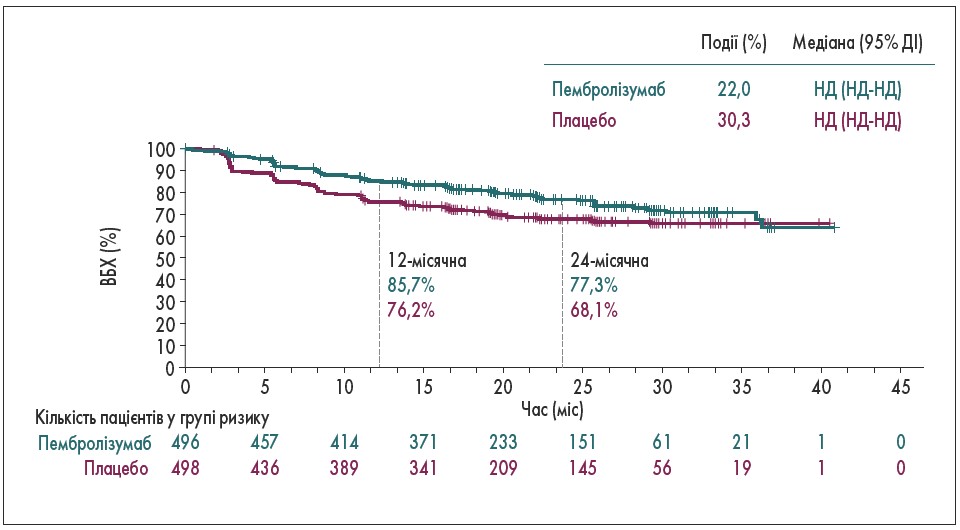 Рис. 1. ВБХ у дослідженні KEYNOTE‑564
Рис. 1. ВБХ у дослідженні KEYNOTE‑564
Що стосується безпеки, то побічні явища (з усіх причин) були зареєстровані у 96,3% учасників групи пембролізумабу проти 91,1% у групі плацебо, зокрема побічні ефекти 3-5 ступеня – у 32,4 та 17,7% пацієнтів відповідно. У групі пембролізумабу були зафіксовані два випадки смерті, у групі плацебо – один випадок. У 20,7% пацієнтів з групи пембролізумабу імунотерапія була припинена через виражену токсичність. Найчастішими побічними ефектами, пов’язаними з лікуванням, були втома, свербіж, гіпо- та гіпертиреоїдизм, діарея, висип, артралгія, нудота, міалгія, астенія (T.K. Choueiri et al., 2021).
Таким чином, результати дослідження KEYNOTE‑564 демонструють істотну перевагу пембролізумабу над плацебо за показником ВБХ у пацієнтів з НКР помірного високого та високого ризику.
В іншому дослідженні KEYNOTE‑426 (NCT02853331) порівнювали ефективність і безпеку комбінації пембролізумабу з акситинібом та монотерапії сунітинібом у пацієнтів з поширеним світлоклітинним раком нирки, які раніше не отримували системного лікування. 861 пацієнт був рандомізований у групи пембролізумабу + акситинібу (n=432) та сунітинібу (n=429). Терапію проводили до прогресування захворювання, появи непереносимої токсичності або відмови лікаря/пацієнта від лікування. Первинними кінцевими точками дослідження були виживаність без прогресування (ВБП) та ЗВ.
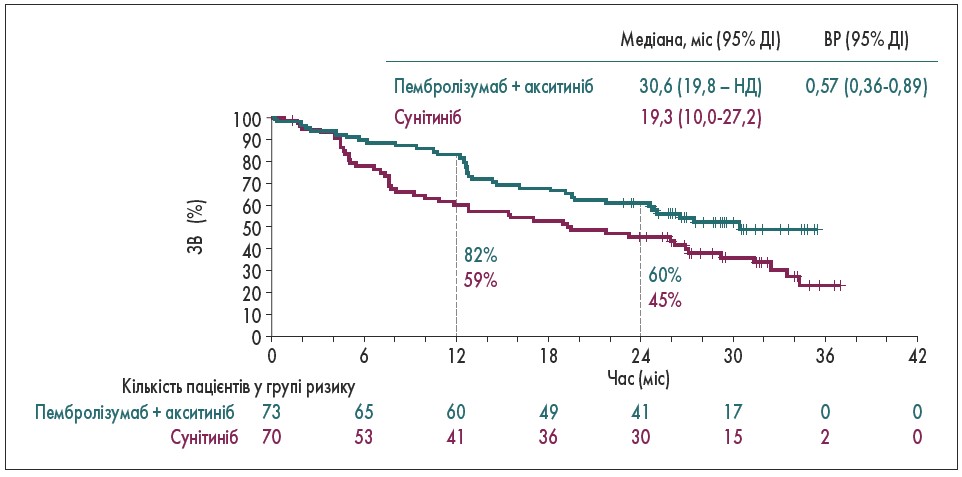
За результатами дослідження, 12-місячна ЗВ у пацієнтів, яким раніше була виконана нефректомія, становила 91% у групі пембролізумаб + акситиніб та 83% – у групі сунітинібу, 24-місячна ЗВ – 77 та 70% відповідно (рис. 2). У хворих, яким не проводили нефректомію, 12-місячна ЗВ дорівнювала 82% у групі пембролізумаб + акситиніб та 59% – у групі сунітинібу, 24-місячна ЗВ – 60 та 45% відповідно (рис. 3). Така ж тенденція прослідковується за показниками ВБП. У пацієнтів після нефректомії 12-місячна ВБП становила 61% у групі пембролізумаб + акситиніб та 50% – у групі сунітинібу, 24-місячна ВБП – 40 та 28% відповідно. У хворих, яким не проводили нефректомію, 12-місячна ВБП дорівнювала 54% у групі пембролізумаб + акситиніб та 35% – у групі сунітинібу, 24-місячна ВБП – 26 та 17% відповідно. У пацієнтів після нефректомії частіше спостерігали повну відповідь на лікування за комбінованою схемою, ніж у пацієнтів, яким не проводили операцію. Побічні явища зафіксовано у 98,4% (≥3 ступеня – 75,8%) пацієнтів групи пембролізумаб + акситиніб та 99,5% (≥3 ступеня – 70,6%) групи сунітинібу (B.I. Rini et al., 2019; D. Soulieres et al., 2020).
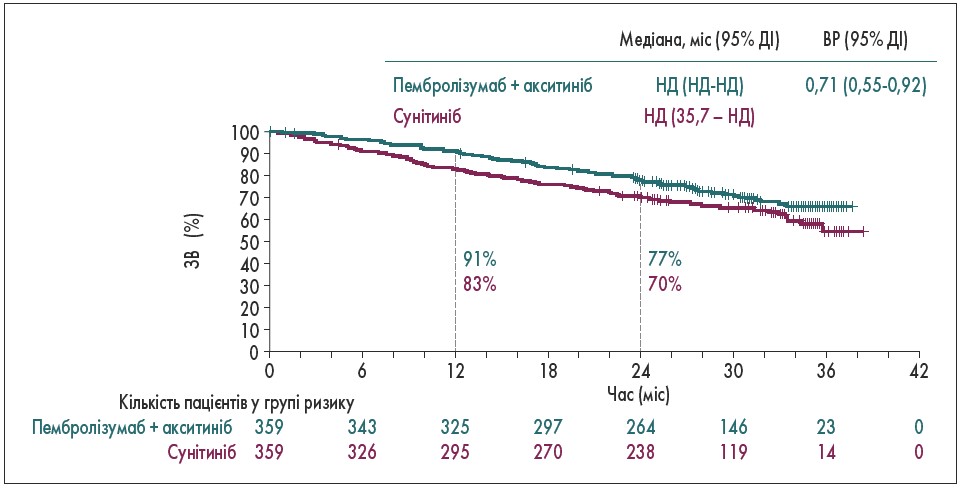 Рис. 2. Криві Каплана – Меєра щодо ЗВ у пацієнтів після нефректомії
Рис. 2. Криві Каплана – Меєра щодо ЗВ у пацієнтів після нефректомії
Рис. 3. Криві Каплана – Меєра щодо ЗВ у пацієнтів, яким не проводили нефректомію
Таким чином, комбінація пембролізумабу та акситинібу показала істотну перевагу над монотерапією сунітинібом за ЗВ і ВБП. Слід зауважити, що у пацієнтів після нефректомії ЗВ була більшою, ніж у хворих, яким операцію не проводили. Тому у пацієнтів, у яких з певних причин не може бути застосована комбінація пембролізумаб + акситиніб, доцільно розглянути можливість виконання нефректомії.
Підготувала Ілона Цюпа
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 4 (71) 2021 р.