15 листопада, 2021
Ацетилсалициловая кислота: проверенная временем, современная, незаменимая
Часть первая
 Ацетилсалициловая кислота (АСК) входит в список важнейших лекарственных средств (ЛС) Всемирной организации здравоохранения (ВОЗ) [1], а также в перечень ЛС, подлежащих реимбурсации по Государственной программе «Доступні ліки» [2]. Она является также одним из самых потребляемых препаратов: ежегодно мировая фарминдустрия производит >40 000 тонн АСК, из которых 35 тонн потребляются каждый день только в США [3, 4].
Ацетилсалициловая кислота (АСК) входит в список важнейших лекарственных средств (ЛС) Всемирной организации здравоохранения (ВОЗ) [1], а также в перечень ЛС, подлежащих реимбурсации по Государственной программе «Доступні ліки» [2]. Она является также одним из самых потребляемых препаратов: ежегодно мировая фарминдустрия производит >40 000 тонн АСК, из которых 35 тонн потребляются каждый день только в США [3, 4].
Чем же объясняется такая популярность препарата? Прежде всего тем, что за более чем 120-летнюю историю существования АСК зарекомендовала себя как высокоэффективное, надежное и доступное средство для профилактики тромбообразования, уменьшающее риск развития тромботических осложнений сердечно-сосудистых заболеваний (ССЗ) и смертность от них, что подтверждено в огромном количестве хорошо организованных клинических исследований (КИ) и обзоров (Physicians’ Health Study, 1989; SAPAT, 1992; Antithrombotic Trialists’ Collaboration, 1994; ISIS‑2, 1998; ASPREE, 2018) [5-10]. Кроме того, преимуществом АСК перед другими дезагрегантами является удобство применения: в отличие от непрямых антикоагулянтов, терапия которыми требует регулярного контроля свертываемости с расчетом Международного нормализованного отношения, при лечении АСК не требуется такой строгий лабораторный контроль [11].
Проблема снижения сердечно-сосудистого риска (ССР) очень актуальна во всем мире. По заключению специалистов Centers for Disease Control and Prevention, средняя продолжительность жизни населения была бы на 10 лет больше при снижении инвалидизации взрослого населения вследствие ССЗ, которые ВОЗ называет эпидемией XXI века [12]. Однако особенно остро стоит эта проблема в странах с низким уровнем дохода: установлено, что доля случаев преждевременной смерти варьирует от 4% в странах с высоким уровнем дохода населения до 42% в странах с низким его уровнем [13].
Украина в этом смысле – не исключение, являясь страной № 1 в Европе и № 2 в мире в рейтинге смертности от ССЗ [14]. Эта ситуация существует давно, сохраняясь и в настоящее время: в соответствии с данными Государственной службы статистики Украины, в январе 2021 г. доля умерших от ишемической болезни сердца (ИБС) и цереброваскулярных заболеваний составляла ≈66% [15]. Особенно на этом фоне огорчает, но и дает надежду, что, по данным ВОЗ, при адекватных профилактических мерах ≈80% инфарктов и инсультов могло быть предотвращено [16]. В абсолютных цифрах это ≈1 млн сосудистых катастроф в год [17].
Определяющим направлением в профилактике тромбозов и тромбоэмболий в терапевтической и хирургической практике, способствующим снижению развития острого коронарного синдрома (нестабильной стенокардии, острого инфаркта миокарда, ИМ) и сердечной смерти, тромбоэмболии легочной артерии, ишемического инсульта (ИИ), критических нарушений микроциркуляции в почках, сетчатке глаза, в периферических сосудах, является использование антиагрегантных препаратов, нарушающих процессы адгезии и агрегации тромбоцитов.
Антитромбоцитарные препараты, доказавшие свою клиническую эффективность, классифицируются на группы в соответствии с их механизмом действия [18]:
- блокаторы циклооксигеназы‑1 (ЦОГ), нарушающие синтез тромбоксана А2, – АСК и другие нестероидные противовоспалительные препараты (НПВП);
- антагонисты рецептора АДФ Р2Y12 – клопидогрель, тикагрелор, прасугрель;
- блокаторы гликопротеиновых рецепторов ІІb/ІІIa – абциксимаб, эптифибатид, тирофибан;
- ингибиторы цАМФ фосфодиэстеразы: дипиридамол, трифлюзал, цилостазол (Плестазол).
Среди них лидирует по частоте применения АСК, которую применяют как для первичной, так и для вторичной профилактики осложнений ССЗ [19]. Так, например, при опросе пациентов 2 семейных клиник Канады оказалось, что лица в возрасте >50 лет в 39% случаев регулярно получают АСК, причем 53% пациентов применяют АСК для первичной профилактики сердечно-сосудистых осложнений (ССО) и 46% – с целью вторичной их профилактики [20].
Фармакодинамика АСК
Еще в 1967 г. Quiсk обнаружил, что АСК увеличивает время кровотечения; тогда же было установлено, что АСК ингибирует агрегацию тромбоцитов [21]. J. H. Smith и A. L. Willis описали механизм действия АСК, связанный с ингибированием ЦОГ‑1 тромбоцитов [22] путем ацетилирования специфических остатков серина в изоферментах COX‑1, а в 1971 г. J. R. Vane предположил, что результатом этого является угнетение синтеза простагландинов (ПГ) [23].
В настоящее время эффекты АСК достаточно хорошо изучены, однако исследования продолжаются и находятся все новые грани действия этого известного препарата. Только в PubMed имеется >72,5 тыс. публикаций, посвященных различным аспектам действия АСК.
На какие патогенетические механизмы тромбообразования она влияет?
В основе макро- и микротромбообразования лежат многочисленные механизмы, стимулирующие агрегационную активность тромбоцитов; в частности, наблюдается ускоренный и турбулентный ток крови в суженном атеросклеротической бляшкой участке сосуда, что способствует повреждению эндотелия с развитием эндотелиальной дисфункции и «обнажению» коллагена, который является одним из главных факторов агрегации и адгезии тромбоцитов. Тромбоциты активируются метаболитом арахидоновой кислоты тромбоксаном А2 (ТхА2), а также другими проагрегантами [19]. Выработанный при активации тромбоцита ТхА2 действует на тромбоциты двояко, вызывая изменения их конфигурации (из диска тромбоцит превращается в шар), способствует образованию отростков, а также активации гликопротеновых комплексов (рецепторов) IIb/IIIa. Последние связывают фибриноген, который, образуя мостики между отдельными тромбоцитами, обеспечивает образование тромбоцитарных конгломератов (агрегация) и приклеивание их (адгезия) к стенке сосуда, образуя белый тромб [24]. Кроме того, во многих работах показана роль ТхА2 как мощного медиатора, повышающего капиллярную проницаемость и дестабилизацию клеточных мембран, стимулирующего цитолиз миоцитов и эндотелиальных клеток, провоцирующего вазоконстрикцию [25], что также способствует тромбообразованию.
Основной механизм действия АСК на свертываемость крови (как и других обладающих антиагрегантным эффектом НПВП) состоит в инактивации ключевого фермента метаболизма арахидоновой кислоты – ЦОГ, а именно ее изофермента ЦОГ‑1, локализованной в тромбоцитах, следствием чего является уменьшение образования из арахидоновой кислоты циклических эндоперекисей ПГ G2 и ПГ H2, служащих предшественниками ТхА2 [26].
В отличие от других НПВП, АСК обладает необратимым действием на ЦОГ‑1, которое клинически может быть оценено по удлинению времени кровотечения [27]. Однажды попав под действие АСК, ацетилирующей его ферменты, тромбоцит теряет способность к синтезу TхA2 и агрегации до окончания своего жизненного цикла, составляющего 9-11 суток, поскольку он является безъядерной клеткой и не ресинтирует новые ферменты [28].
ЦОГ‑2 в 50-100 раз менее чувствительна к действию АСК [29], поэтому влияние АСК на изоформы ЦОГ (ЦОГ‑1 и ЦОГ‑2) имеет дозозависимый характер:
- малые дозы (до 325 мг) оказывают дезагрегационное действие (тормозят агрегацию тромбоцитов), при этом уровень простациклина, который является мощным естественным вазодилататором и антиагрегантом, сохраняется достаточно высоким. В более высоких дозах АСК вызывает подавление обоих изоферментов и снижение образования простациклина [30];
- средние дозы (1,5-2 г) оказывают аналгезирующее и жаропонижающее действие;
- большие дозы (4-6 г) обладают противовоспалительным эффектом.
Бытует мнение, что селективность малых доз АСК также обусловлена наибольшим воздействием препарата на ЦОГ‑1 тромбоцитов в системе портального кровообращения, поэтому больший ингибирующий эффект оказывается именно на тромбоциты, а не на сосудистую стенку, где происходит образование простациклина; антитромбоцитарный эффект препарата проявляется до его распределения в системном кровотоке [31].
В связи с новыми находками в биохимии атеросклероза в последние годы значительно возрос интерес к роли в атерогенезе и тромбогенезе противовоспалительных факторов – липоксинов, резолвинов, протектинов. Есть мнение, что дисбаланс между ними, с одной стороны, и провоспалительными лейкотриенами, с другой, способствует повреждению сосудистой стенки, в т. ч. атеросклеротической бляшки, и, как следствие, – образованию тромба.
В этом отношении интересен еще один тип фармакологических эффектов АСК, который является результатом модулирования (не торможения!) активности ЦОГ‑2 и превращения ее в липоксигеназу. Последняя продуцирует из арахидоновой кислоты 15(R)-гидроксиэйкозатетраеновую кислоту (15R-HETE) вместо предшественника ПГ – ПГ H2. 15R-HETE в дальнейшем метаболизируется в липоксин A4, известный как аспирин-индуцированный липоксин [32], причем другие НПВП такого действия не оказывают.
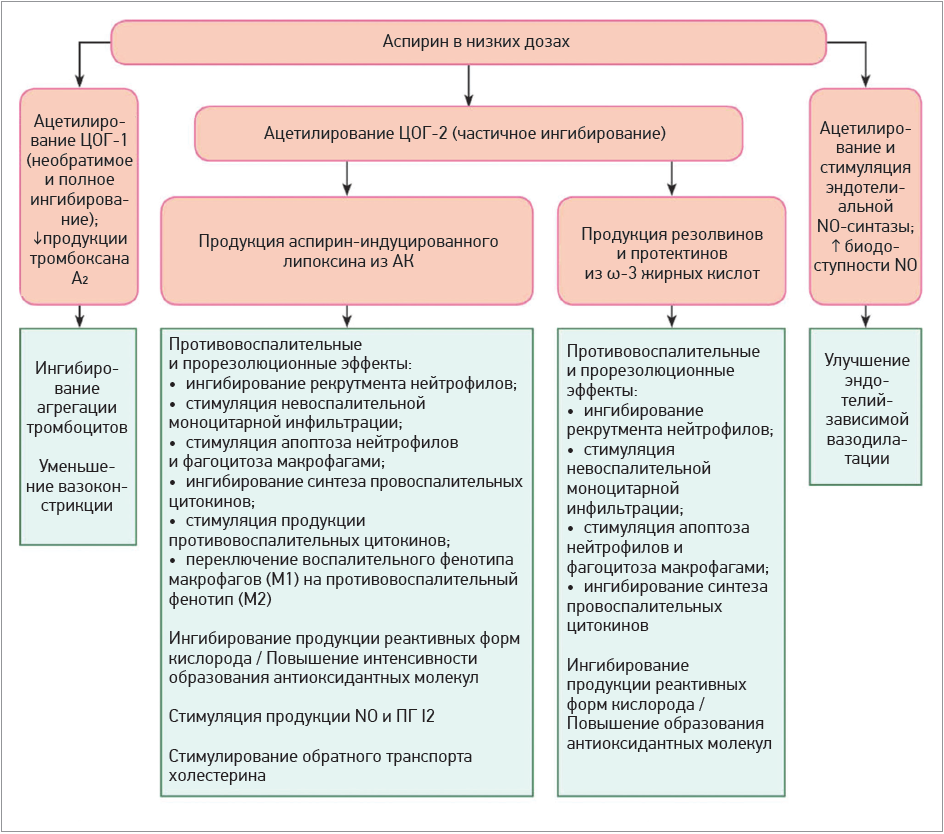
Этот липоксин обладает противовоспалительными свойствами; он относится к семейству специализированных медиаторов, которые играют ключевую роль в разрешении воспаления и регенерации тканей [33]. Кроме того, аспирин-индуцированный липоксин может также уменьшать эндотелиальную дисфункцию, стимулируя NO-синтазу в эндотелии, а также тормозить атерогенез благодаря антиоксидантному действию и усилению обратного транспорта холестерина [34]. Помимо липоксина, ацетилированная ЦОГ‑2 способствует продукции резолвинов и протектинов из ω‑3 полиненасыщенных жирных кислот, которые (как и липоксины) проявляют противовоспалительные эффекты и способствуют нормализации окислительно-восстановительного статуса [33]. Схематически эффекты АСК представлены на рисунке 1.
Рис. 1. Основные протекторные эффекты низких (антитромбоцитарных) доз АСК [36, 37]
Примечания: АК – арахидоновая кислота; ПГ I2 – простагландин I2 (простациклин); NO – оксид азота.
Роль гидроксида магния в препаратах АСК
Как показано в ряде исследований, гидроксид магния, входящий в состав некоторых препаратов АСК в качестве вспомогательного вещества, может снижать вероятность развития побочных явлений со стороны желудочно-кишечного тракта. Так, в одном из исследований [38] было проведено сравнение основных и побочных эффектов различных форм АСК. В исследовании участвовали пациенты в возрасте 18-60 лет с повышенной спонтанной и индуцированной агрегацией тромбоцитов, 286 человек из которых получали желудочнорастворимую форму АСК (150 мг/сут), 57 – желудочнорастворимую форму АСК + оксид магния 75 мг/сут, 36 – кишечнорастворимую форму АСК 100 мг/сут. Контрольную группу составили 127 здоровых людей такого же возраста.
Было установлено, что независимо от дозы препараты сопоставимо подавляли агрегацию тромбоцитов, при этом переносимость была лучше у АСК + оксид магния: диспептические расстройства отмечались почти у половины пациентов, получавших желудочнорастворимую АСК, а также в 14 и 5% случаев соответственно при приеме кишечнорастворимой формы АСК и желудочнорастворимой комбинации АСК + оксид магния.
В исследовании А. Л. Верткина и соавт. (2009) [39] также изучался профиль безопасности желудочнорастворимой АСК относительно других форм АСК по развитию и динамике симптомов диспепсии и эндоскопической картины лекарственной гастропатии на фоне лечения в течение 12 нед. Была показана более низкая частота и выраженность диспепсий и эрозивно-язвенных поражений слизистой оболочки желудка и двенадцатиперстной кишки у больных ИБС с высоким риском развития гастропатий на фоне приема желудочнорастворимой формы АСК с добавлением оксида магния, чем при применении кишечнорастворимой формы АСК.
Есть КИ по сравнительной безопасности применения АСК в кишечнорастворимой и желудочнорастворимой формах с добавлением оксида магния (АСК – соответственно 100 и 150 мг/сут) на протяжении 12 мес [40]. Побочные эффекты чаще развивались при использовании кишечнорастворимой АСК: боль и желудочные диспептические расстройства – в 54 и 30% случаев соответственно, при этом в группе пациентов, принимавших желудочнорастворимую АСК, была отмечена меньшая частота как эрозий, так и язв, чем в группе Тромбо АСС (16,2 и 23,4% для эрозий; 4,4 и 10,9% для язв соответственно), однако эти различия не были статистически значимыми.
Подобные результаты отмечались и в других исследованиях [41, 42].
Помимо гастропротекторного действия оксида магния, которое характерно для буферных антацидов [43], магнию свойственны и другие полезные эффекты; его роль в организме человека хорошо изучена. Он является кофактором >300 ферментов, регулирует проницаемость клеточных мембран и органелл клетки (в т. ч. митохондриальных), является антагонистом кальция, защищает клетку от его избытка, повышает активность антиоксидантной системы и т. д., поэтому 15,2 и 30,39 мг гидроксида магния соответственно в составе препаратов Магникор и Магникор форте в качестве вспомогательного вещества (АО «Киевский витаминный завод») могут иметь дополнительное положительное значение и быть полезными при длительной антитромбоцитарной терапии [44].
Негативным последствием магниевого дефицита является повышенная агрегация тромбоцитов и увеличение риска тромбоэмболических осложнений. На фоне дефицита магния дисбаланс Ca2+: Mg2+ приводит к избыточному тромбообразованию. На клеточном уровне Mg2+ сдерживает образование артериального тромба путем ингибирования активности тромбоцитов, тем самым потенцирует антикоагулянтные эффекты АСК и позволяет минимизировать ее дозу [45].
Фармакокинетика и лекарственные формы АСК. Преимущества желудочнорастворимой формы
Желудочнорастворимая (простая) форма АСК хорошо всасывается в желудке благодаря тому, что низкий рН предотвращает ее деацетилирование и сохраняет АСК в неионизированной форме, которая лучше всасывается. Кишечнорастворимые формы обеспечивают высвобождение действующего вещества в верхней части тонкого кишечника, где уровень рН почти нейтральный, следовательно, инактивация АСК происходит быстрее; биодоступность препарата составляет ≈50% [46, 47].
При использовании АСК в желудочнорастворимой форме концентрация в плазме крови достигает пика через 30-40 мин, а подавление функции тромбоцитов наблюдается через 1 ч после приема, при этом антитромботическое действие АСК наблюдается в интервале от 24 до 48 ч после приема, что позволяет назначать ее 1 р/сут [48].
Особенности фармакокинетики АСК определяют преимущества простой формы АСК перед ее кишечнорастворимыми формами в антиагрегантной активности [49]: были подтверждены в 3 раза более быстрое достижение пика концентрации и в 5 раз более высокая максимальная концентрация действующего вещества в плазме крови после приема простой АСК по сравнению с кишечнорастворимой формой, что способствовало более предсказуемому и быстрому (через 60 мин) развитию антиагрегантного эффекта.
Кишечнорастворимые формы (энтерики) за счет более медленного всасывания формируют максимальную концентрацию АСК в плазме крови через 3-4 ч; это время может быть существенно увеличено при хронических воспалительных процессах в желудочно-кишечном тракте, сахарном диабете (СД) и др.) [50].
Если разжевать таблетку кишечнорастворимой формы АСК, скорость развития максимального антиагрегационного действия наступает, как и при использовании желудочнорастворимых форм [51].
Дозы АСК
В соответствии с данными известного метаанализа 2002 г. Antithrombotic Trialists’ Collaboration, наиболее высокий протекторный эффект относительно снижения риска ССО на фоне применения АСК отмечался при ее использовании в низких дозах (75-150 мг), составляя 32%. В высоких (500-1500 мг) и средних (160-325 мг) дозах он составлял 19 и 26% соответственно [7].
Подобное явление некоторые авторы связывают с тем, что дозы АСК >300 мг/сут способствуют снижению синтеза простациклина (антиагреганта и вазодилататора) за счет ингибирования ЦОГ‑2, что увеличивает риск тромбообразования и, как следствие, сосудистых событий [52].
Кроме того, в статье [53] было показано, что увеличение дозы АСК >100 мг/сут сопровождается повышением риска геморрагических осложнений, а прием АСК в дозах <75 мг/сут недостаточно эффективно предотвращает ИМ и инсульты, поэтому в настоящее время большинством экспертов доза АСК 75-100 мг/сут признана оптимальной для вторичной профилактики ИИ и других ССО.
В то же время в последние годы появились данные, что на выбор дозы АСК определенное влияние может оказать масса тела пациента и, соответственно, распределение препарата: при увеличенной массе тела для создания эффективной концентрации могут потребоваться более высокие дозы АСК (при массе >120 кг – 150 мг АСК), однако они могут оказаться чрезмерными у пациентов с низкой массой тела из-за снижения выработки эндотелиального простациклина на фоне избыточной концентрации АСК. Эти особенности следует учитывать в практике, поскольку масса тела может быть одним из факторов, определяющих клиническую эффективность АСК [54, 55].
Режим применения АСК
Наиболее часто рекомендуемая схема применения АСК для планового лечения включает однократный прием 75-150 мг препарата в день. Если требуется быстрое и полное ингибирование тромбоцитов (например, при ангинозном приступе), первая доза АСК должна составлять 150-300 мг [56].
Когда наиболее рационально принимать АСК? Поскольку было показано, что риск инфарктов и инсультов достигает пика в утренние часы [57], утвердилась рекомендация принимать препарат для антиагрегантной терапии в вечернее время, чтобы к утру был достигнут максимум профилактического эффекта [58].
Учитывая то, что АСК действует на тромбоцит необратимо (все время его жизни), разовое нарушение режима при приеме препарата не приведет к синдрому рикошета, однако курсами принимать АСК опасно: такой режим может привести к возрастанию риска тромбоза. В исследовании [59] показано, что активация тромбоксанзависимой агрегации тромбоцитов после прекращения приема АСК происходит быстро, причем имеется нелинейная зависимость между активностью тромбоцитарной ЦОГ и синтезом тромбоксана. С другой стороны, была отмечена способность даже небольших количеств тромбоксана, продуцируемого незаблокированными тромбоцитами, индуцировать агрегацию тромбоцитов и повышать риск тромбообразования через 1-2 нед. Такая тенденция сохранялась и спустя более продолжительное время: через 31-180 дней после прекращения приема АСК значимо (почти в 1,5 раза) повышается риск развития ИМ и смерти от ИБС [60].
Разъяснительная работа с пациентами (многие считают целесообразным самостоятельно начинать профилактический курсовой прием АСК), выбор категории пациентов, которым действительно нужна терапия АСК, а также формирование приверженности к ее приему является важной задачей работы с больными, которые должны получать антиагреганты (особенно для вторичной профилактики). Подтверждением этого являются результаты шведского исследования (2017). Были проанализированы данные Шведского регистра, куда вошли 601 527 больных, принимавших ≈3 лет с целью первичной или вторичной профилактики АСК в низких дозах со средней приверженностью к лечению >80%. Было показано, что у пациентов в возрасте >70 лет с предшествующими ССЗ риск развития сердечно-сосудистых событий (ССС) (сразу после прекращения лечения и в дальнейшем) из-за прекращения приема препарата оказался выше на 46%. Среди больных, которые использовали АСК в качестве первичной профилактики, прекращение терапии АСК также сопровождалось увеличением риска ССО, но меньшим (на 28%) [61].
Первичной профилактике ССЗ посвящен целый ряд КИ, в которых были получены достаточно противоречивые результаты: очень оптимистичные в 1988-2005 гг., однако показавшие меньшую эффективность и небезопасность в последующие годы [62].
Однако в последнем обзоре 2019 г. (13 рандомизированных КИ (РКИ), n=164 225, средний возраст – 62 года) была подтверждена эффективность первичной профилактики АСК (с учетом рисков, особенностей сопутствующей патологии, возраста и т. п.), превышающая в ряде клинических ситуаций риски развития кровотечений [63].
Первичная профилактика АСК у относительно здоровых людей без ССЗ
В большинстве случаев назначение АСК здоровым людям не рекомендуется как рутинная мера, однако есть ряд исследований, в которых отмечаются позитивные результаты ее приема.
В 1989 г. в исследовании Physicians’ Health Study (США), в которое было включено 22 000 врачей-мужчин в возрасте 40-84 года, в группе здоровых лиц, принимавших АСК (325 мг/сут), в среднем через 5 лет отмечено уменьшение риска развития ИМ на 44% (по сравнению с аналогичной группой обследуемых без приема АСК) [5].
В крупное рандомизированное исследование Women’s Health Study, в котором, напротив, не получили таких впечатляющих результатов по снижению риска развития ССЗ и сердечной смерти. В исследовании приняли участие 39 876 здоровых женщин в возрасте >45 лет, которые в течение 10 лет принимали по 100 мг АСК через день. Назначение препарата способствовало снижению на 17% риска развития любого инсульта (ишемического – на 24%) и на 22% – транзиторной ишемической атаки (ТИА), не влияя при этом достоверно на нефатальный ИМ и смерть от сердечно-сосудистых причин. Частота желудочно-кишечных кровотечений была несколько выше, чем в плацебо (4,6 и 3,8% соответственно). Интересен был анализ результатов в различных возрастных группах: в группе женщин в возрасте >65 лет АСК снижала риски более активно (количество основных ССС – на 26%, риск ИИ – на 30%, ИМ – на 34%) [64].
В последующем результаты нескольких крупных исследований были обобщены в систематическом обзоре (95 тыс. участников), в котором показано, что польза от длительного приема АСК лицами без клинических проявлений атеросклероза сомнительна, так как продемонстрировано снижение риска ишемических событий с 0,57 до 0,51%, но при этом частота желудочно-кишечных и экстракраниальных кровотечений повысилась на 0,03% в год [53]. Не улучшала прогноз и комбинированная терапия АСК с клопидогрелем у пациентов без клинических проявлений атеросклероза (даже при наличии множественных факторов риска) [65].
В одном из последних исследований (ASPREE, Австралия, США; 19 114 относительно здоровых людей в возрасте >70 лет, наблюдение длилось 4,7 года) изучалась роль низкой дозы АСК в первичной профилактике ССЗ (фатальные и нефатальные ИМ и инсульт, госпитализация по поводу сердечной недостаточности). Исследование показало, что частота ССС была недостоверно меньшей в группе получавших АСК, однако при этом достоверно (коэффициент рисков (КР) 1,38) повышались риски серьезных кровотечений, а также (в сравнении с плацебо) повышалась смертность (КР 1,14), что авторы объясняли онкологическими причинами [9].
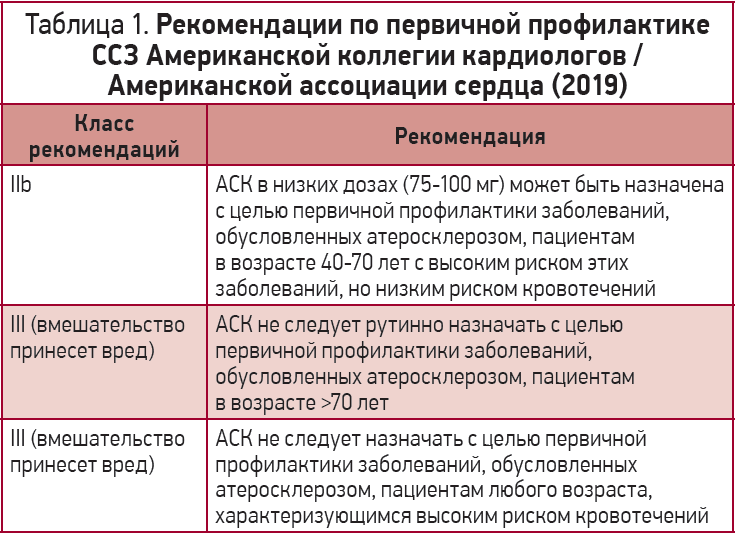
Мнение экспертов по первичной профилактике ССЗ, изложенное в рекомендациях Американской коллегии кардиологов / Американской ассоциации сердца (2019) [66], представлено в таблице 1.
Для определения риска у пациентов без ССЗ традиционно используют шкалу SCORE (пол, возраст, курение, АДс и уровень общего холестерина). При очень высоком риске смерти от ССЗ в течение 10 лет показатель SCORE >10%, при высоком – 5-9%, умеренном – 1-4%, низком – <1%. В соответствии с рекомендациями, при организации профилактических мероприятий наибольшее внимание следует уделять пациентам высокого и очень высокого риска (≥5%) [67].
Однако шкала SCORE и некоторые другие (Фремингемская и ASCVD) включают только такие факторы, как показатели артериального давления (АД), курение, холестерин, пол и возраст, наличие СД. Другие показатели (семейный анамнез, наличие хронической болезни почек, некоторые виды терапии, данные других биохимических и инструментальных исследований) они не учитывают, хотя есть данные об их влиянии на прогноз. Существуют данные о более точной оценке риска при учете информации о толщине комплекса интима-медиа и наличии атеросклеротических бляшек в сонных артериях [68], а также индекса коронарного кальция (ИКК) как маркера тяжести коронарного атеросклероза [69]. В отношении последнего показателя показано, что для больных с ИКК >100 (высокая вероятность тяжелого стенозирующего коронарного атеросклероза) назначение АСК было более эффективным, чем для больных с ИКК <100, у которых геморрагический риск от назначения АСК оказался выше, чем польза от ее назначения. Оценка риска развития артериального тромбоза возможна также с помощью показателей гемокоагуляции (время свертывания крови, активированное частичное тромбопластиновое время, международное нормализованное отношение), гомоцистеина, С-реактивного белка – лабораторных тестов, помогающих принять решение о назначении антиагрегантов для первичной профилактики больным, у которых риск тромбозов превышает риск кровотечений [62].
В последнее время для выявления пациентов высокого риска все шире применяются КИ, в которых анализируются его генетические маркеры. Так, в исследованиях CURE и ACTIVE-A показано, что полиморфизм гена ЦОГ коррелирует с риском неблагоприятных исходов ССЗ и с эффективностью терапии АСК: при наличии редких (минорных) аллелей полиморфного маркера rs20417 гена ЦОГ‑2 и соответственно низкой активности ЦОГ достоверно ниже было образование тромбоксана и простациклина, меньше – число ССО и выше – эффективность АСК, а при гомозиготном носительстве мажорного аллеля, напротив, отмечалось почти 2-кратное увеличение риска ССС [70].
Первичная профилактика АСК при хроническом коронарном синдроме (ХКС)
В плацебо-контролируемом КИ SAPAT (Swedish Angina Pectoris Aspirin Trial) 2035 пациентов со стабильной стенокардией получали в течение 15 мес соталол в сочетании с АСК 75 мг или плацебо (первичная профилактика). Суммарная частота ИМ и внезапной смерти в группе АСК снизилась на 34% (р=0,003), а других сосудистых событий и сердечно-сосудистой смертности – на 22-32% [6].
Данные метаанализа, в который входили 5 РКИ по первичной профилактике (52 251 участник, дозы АСК составляли 75-650 мг/сут, средний период наблюдения – 4,6 года), свидетельствуют, что не выявлено значимого влияния на инсульт (относительный риск (ОР) 1,08) в отличие от достоверного уменьшения риска ИМ (ОР 0,74), при этом риск внутричерепного кровоизлияния увеличивался [71], что, возможно, связано с применением достаточно больших доз АСК.
Первичная профилактика АСК при гипертонических болезнях
Одним из первых исследований, в котором изучались вопросы профилактики ССС при артериальной гипертензии (АГ), было исследование НОТ (Hypertension Optimal Treatment Trial, 18 790 пациентов в возрасте 50-80 лет), где оценивали влияние приема АСК в дозе 75 мг/день (по сравнению с плацебо) на течение АГ у пациентов с различными уровнями АД. Показано, что АСК достоверно уменьшала риск серьезных ССС на 15% и ИМ на 36% без влияния на частоту инсультов и увеличения риска внутричерепных кровотечений, но с возрастанием частоты других серьезных кровотечений без повышения (по сравнению с плацебо) риска фатальных кровотечений.
Установлено, что наибольшую пользу АСК может принести:
- у больных с умеренным повышением уровня креатинина сыворотки (>115 мкмоль/л), у которых наблюдалось большее снижение риска ССО и ИМ (-13 и -7 событий на 1000 пациенто-лет) без увеличения риска кровотечений, чем в целом у включенных в исследование пациентов;
- у пациентов с высоким и очень высоким общим ССР, а также с более высокими исходными цифрами систолического и диастолического АД, тогда как у больных с исходно низким риском побочные эффекты АСК нивелировали прогностическую выгоду лечения [72].
И в выводах по результатам НОТ, и в руководстве по менеджменту АГ Европейского общества гипертензии / Европейского общества кардиологов [73] специально подчеркнуто, что для уменьшения риска геморрагического инсульта АСК должна назначаться только после достижения адекватного контроля АД.
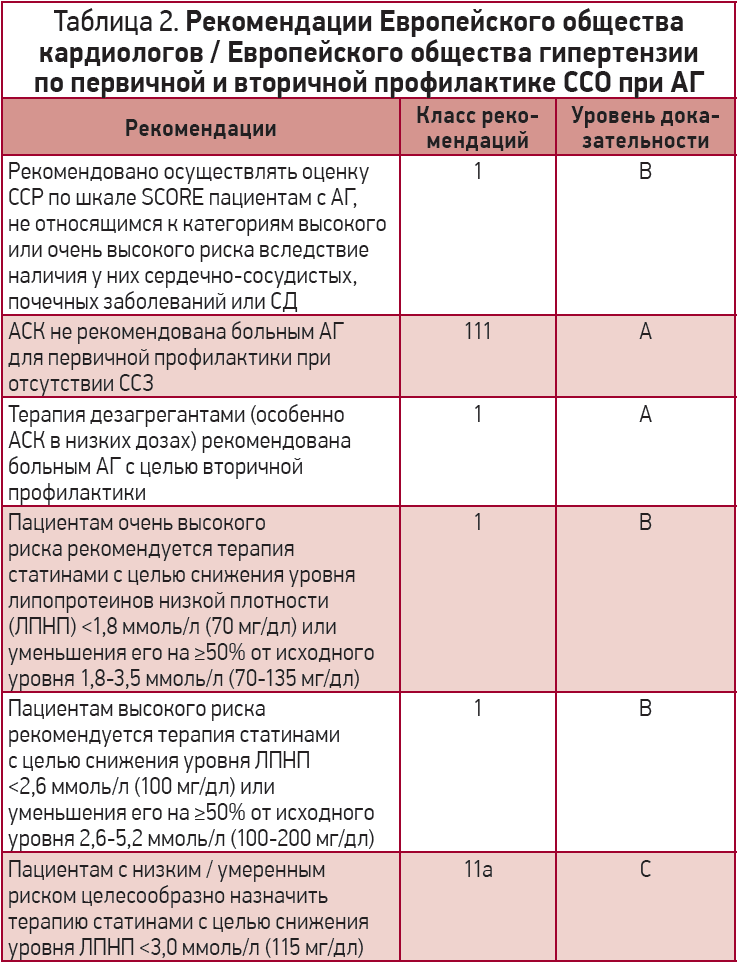
В последних рекомендациях Европейского общества кардиологов / Европейского общества гипертензии (2018) по лечению больных с АГ [76] сформулированы положения по целесообразности медикаментозной профилактики ССО с учетом степени их риска (табл. 2).
Первичная профилактика АСК в неврологии
Опубликованные в последние годы данные о низкой эффективности АСК в первичной профилактике инсульта (в т. ч. – см. выше) не отменяют необходимости в антитромботической терапии у больных с высоким ССР [62, 71]. Одним из важных (но не учитываемых в шкале SCORE факторов риска) является, как отмечается в последние годы, состояние атеросклеротической бляшки. Считают, что, кроме больных с высоким риском по шкале EURO SCORE, антитромботическую терапию должны получать все пациенты с доказанным атеросклерозом независимо от степени стенозирования артерий, если общая площадь атеросклеротических повреждений значительна, а структура атеросклеротической бляшки гетерогенна и нестабильна [77].
Первичная профилактика АСК при болезнях почек
Специалисты Американской ассоциации сердца и Американской ассоциации по борьбе с инсультом рекомендуют прием АСК с целью первичной профилактики больным хронической болезнью почек со скоростью клубочковой фильтрации (СКФ) <45 мл/мин/1,73 м2, однако не <30 мл/мин/1,73 м2 [78, 79].
Первичная профилактика АСК при СД
Атеротромботические осложнения – главная причина смерти пациентов с СД; усиление агрегационной активности тромбоцитов – один из возможных факторов, увеличивающих риск их возникновения.
По данным популяционных исследований, ≈50% лиц с СД 2 типа в момент установления диагноза имеют клинически значимые ССЗ и/или не менее 1 фактора риска ССЗ помимо гипергликемии (гипертензию, гиперлипидемию, инсулинорезистентность, избыточный вес), в связи с чем риск смерти от сердечно-сосудистых причин у больных СД выше, чем в популяции [80]. Коррекция агрегационных свойств крови у больных с СД имеет очень большое значение, поскольку при этом заболевании риски тромбообразования повышаются по целому ряду причин; прежде всего это эндотелиальная дисфункция, с которой и начинается атерогенез, а также увеличение выработки тромбоксана А2, повышение фибрина, снижение фибринолиза, чувствительности к тромболизису и др. [81]. У таких больных отмечается повышение риска кардиоваскулярных событий в 2-4 раза в сравнении с пациентами без диабета, причем ⅔ смертей у них в возрасте >65 лет обусловлены ИБС, 16% – инсультом [82]. Однако исследование JPAD, в котором принимали участие пациенты с СД с очень невысоким уровнем риска развития ССС (0,25% в год), не показало эффективности АСК в первичной профилактике у таких больных [83]. В РКИ, опубликованном в 2018 г. (ASCEND, 15 480 пациентов с СД без ССЗ; сравнивали эффективность АСК 100 мг/сут vs плацебо в течение 7,4 года и отмечали невысокую умеренную эффективность АСК в предупреждении первого ССС), снижение серьезных событий (ИМ, инсульта, ТИА или смерти по любой сосудистой причине) в группе приема АСК составляло 12% [84].
С учетом этих и других исследований, в рекомендациях Американской ассоциации сердца / Американской диабетической ассоциации (2016, 2017) указан прием АСК 75-160 мг/сут с целью первичной профилактики больным СД 1 и 2 типов, у которых 10-летний риск ССЗ составляет >10% (большинство мужчин в возрасте >50 лет и женщин в возрасте >60 лет при наличии минимум 1 дополнительного фактора риска – курение, семейный анамнез ССЗ, АГ, гиперлипидемия, альбуминурия) (табл. 3), а также отсутствуют риски кровотечений.
Отмечают также, что прием АСК возможен у пациентов среднего риска (мужчины в возрасте <50 лет и женщины в возрасте <60 лет при наличии 1 дополнительного фактора риска или лица более пожилого возраста с их отсутствием, а также при 10-летнем риске ССО 5-10%) [86, 87]. В соответствии с рекомендациями Европейского общества кардиологов (2019) [85], с целью первичной профилактики рекомендованы дозы АСК 75-100 мг/сут при высоком и очень высоком ССР, а также при отсутствии противопоказаний; при умеренном риске прием АСК не показан.
Первичная профилактика АСК при заболеваниях периферических сосудов
В последнее время периферический атеросклероз приобретает масштаб глобальной проблемы ввиду своей широкой распространенности: в экономически развитых странах ≈10% взрослого населения страдает ишемией нижних конечностей, на долю облитерирующего атеросклероза при этом приходится 80-90% случаев [88, 89]. В многочисленных рекомендациях по терапии периферического атеросклероза превалирует мнение о необходимости пожизненного назначения антитромбоцитарной терапии [90].
Подобная терапия с АСК (75-325 мг/сут) или клопидогрелем (75 мг/сут) с целью снижения риска ИМ, инсульта, сосудистой смерти с высоким уровнем доказательности (1А) рекомендуется пациентам с симптоматическими проявлениями заболеваний сосудов. У асимптомных пациентов она также считается рациональной, но с меньшей степенью доказательности (11а), однако в рекомендациях Американской ассоциации сердца / Американской коллегии кардиологов (2011) отмечается ее целесообразность у пациентов с верифицированным атеросклерозом артерий брахиоцефальной зоны вне зависимости от клинических проявлений [91]. У симптомных пациентов после реваскуляризации рекомендуют двойную антиагрегантную терапию (ДААТ) – АСК + клопидогрель (в течение не менее 1 мес после эндоваскулярных вмешательств независимо от типа стента). После операции по паховому шунтированию рекомендуют антиагрегантную монотерапию, а при шунтировании ниже колена с протезным протезом можно рассмотреть возможность проведения ДААТ (11b) [92, 93].
При решении о назначении антиагрегантной терапии необходимо учитывать, что заболевание артерий нижних конечностей (ЗАНК) является маркером распространенного атеросклеротического процесса, часто затрагивающего несколько сосудистых русел за пределами нижних конечностей и повышающего риск общей и сердечно-сосудистой смертности. Антитромботическая терапия является краеугольным камнем ведения этих пациентов для предотвращения ишемических ССЗ, событий на конечностях и смерти.
Стоит ли усиливать противосвертывающие вмешательства при ЗАНК?
При симптоматическом ЗАНК добавление антикоагулянтов (антагонистов витамина K) к антиагрегантной терапии увеличивало риск обширного и опасного для жизни кровотечения без пользы в отношении сердечно-сосудистых исходов. В недавнем исследовании низкая доза перорального антикоагулянта прямого действия ривароксабана + АСК показала хорошие результаты не только в отношении снижения смертности и серьезных ССС, но также и в отношении серьезных событий со стороны конечностей, включая ампутацию, в связи с чем эту комбинацию особенно рекомендуют у пациентов с очень высоким риском [93].
Применение АСК в акушерстве
Преэклампсия является серьезным осложнением 3-4% всех беременностей и причиной ≈50 тыс. случаев ежегодной материнской смертности [94].
Поскольку патофизиология преэклампсии до конца не изучена, профилактических мер для ее предупреждения по-прежнему недостаточно. Есть данные, что использование АСК или низкомолекулярного гепарина может помочь снизить вероятность развития данной патологии. Например, использование низких доз АСК у женщин с высоким хорионическим гонадотропином и аномальными показателями при допплеровском исследовании маточных артерий позволило увеличить вес младенца при рождении, а также снизить заболеваемость гестационной АГ [95], комбинация гепарина (НФГ или НМГ) с АСК во время беременности – увеличить частоту живорождений у женщин со стойким антифосфолипидным синдромом [96].
Из-за своего антитромбоцитарного действия АСК в низких дозах в настоящее время рекомендуется для предотвращения тромботических проявлений у беременных с синдромом антифосфолипидных антител, механическими сердечными клапанами или с промежуточным / высоким риском преэклампсии [97, 98]. Получены результаты [99], позволяющие авторам рекомендовать женщинам с высоким риском преэклампсии с целью ее профилактики малые дозы (150 мг) АСК с 12-й недели беременности и до 36-й недели (при условии низкого риска желудочно-кишечных кровотечений).
Вторичная профилактика АСК
В отличие от первичной профилактики, целесообразность применения которой при ССЗ обсуждается и зависит от выраженности рисков осложнений, вторичная профилактика инфаркта, инсульта и сердечной смерти является общепризнанной тактикой лечения с высоким уровнем доказательности по эффективности.
Вторичная профилактика после ИМ
Одним из крупнейших обзоров, посвященных проблеме вторичной профилактики при ССЗ, является опубликованный в 1994 г. обзор Antiplatelet Trialists’ Collaboration, включающий >50 исследований на 100 тыс. больных с ИБС. В соответствии с его заключением длительное применение АСК с целью вторичной профилактики снижает частоту сердечно-сосудистой смерти на 15%, несмертельных сосудистых событий – на 30% [100].
В последующий метаанализ, выполненный этой же Группой совместных исследований по антитромботической терапии (Antithrombotic Trialists’ Collaboration) (2002), были включены данные 287 исследований о лечении 220 тыс. пациентов высокого риска, перенесших ранее острый ИМ, инсульт, ТИА, с текущим инфарктом или инсультом, стабильной стенокардией. 135 тыс. больных, участвовавших в исследованиях и вошедших в этот метаанализ, принимали АСК ≥75 мг в режиме монотерапии или в составе комбинированного антитромбоцитарного лечения. Результаты анализа подтвердили, что применение антитромбоцитарных препаратов является эффективной мерой вторичной профилактики ССЗ, уменьшая ОР смерти от любых причин на 16%, серьезные сосудистые осложнения и инсульты – на 25%, ИМ – на 34%. Для всех пациентов с высоким риском серьезных ССС абсолютная польза лечения достоверно превосходила абсолютный риск больших геморрагических осложнений, который составил 1,13% на фоне применения антиагрегантов и 0,71% в группе без лечения [7].
Эффективность АСК при вторичной профилактике не зависела от клинических форм ХКС: острый ИМ, нестабильная стенокардия или стабильно протекающий ХКС, поэтому ее применение в виде монотерапии или в комбинации с другими антиагрегантами в настоящее время имеет убедительные доказательства эффективности, а также является стандартом для вторичной профилактики у больных с атеросклеротическим поражением коронарных и других артерий.
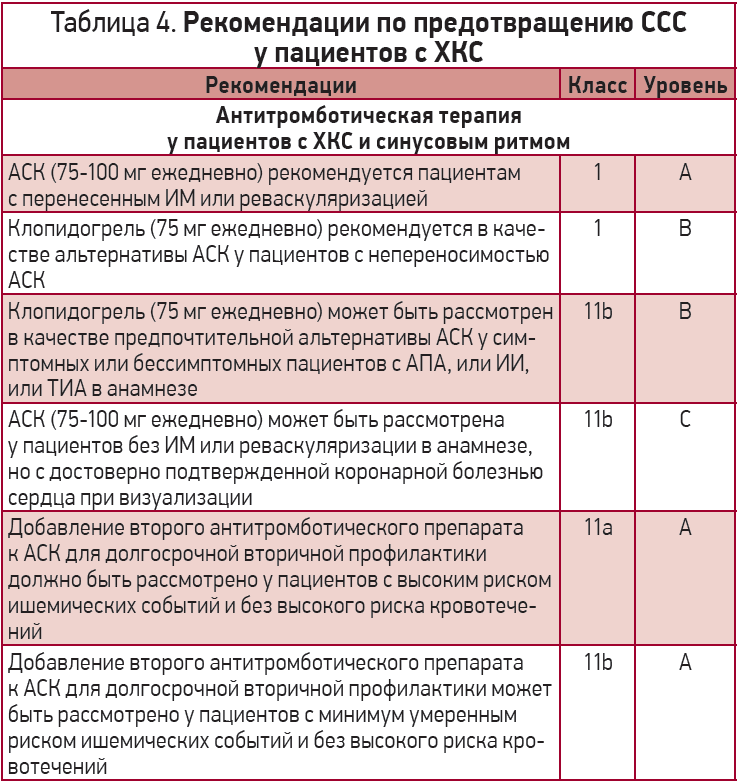
В рекомендациях Европейского общества кардиологов по диагностике и лечению ХКС (2019) имеется ряд положений относительно применения АСК у пациентов с ХКС (табл. 4) [101].
Вторичная профилактика после инсульта и ТИА
Инсульт не только занимает второе место среди причин смерти от ССЗ, но и считается ведущей причиной инвалидизации у лиц пожилого возраста, причем преобладают ИИ (70-85%), возникающие вследствие атеросклеротического поражения церебральных артерий [102].
Вторичная профилактика при инсульте является столь же обязательным показанием к лечению АСК, как и ИМ, при этом также ведущее место занимает антитромбоцитарная терапия.
Известный метаанализ исследований, посвященных оценке эффективности антитромбоцитарных средств у больных, перенесших ИИ или ТИА (Antithrombotic Trialists’ Collaboration), показал, что длительный (2-3 года) прием антитромбоцитарных средств снижает риск развития повторного инсульта, ИМ и острой сосудистой смерти в среднем на 20-22%, позволяя предотвратить у 36 из 1000 больных повторные ишемические события [7]. В исследованиях IST и CAST, вошедших в этот метаанализ, отмечалась не только высокая профилактическая эффективность АСК (более высокая, чем при первичной профилактике), но и возможность повышения риска геморрагических инсультов, однако сравнение рисков свидетельствовало о преобладании пользы над риском при применении антитромбоцитарной терапии [103, 104].
В последнем обзоре [105] приведены рекомендации по вторичной профилактике инсультов и ТИА, разработанные на основании многочисленных КИ:
- всем лицам с ИИ/ТИА рекомендуется использовать антиагрегантную терапию для профилактики повторного инсульта, если нет показаний для назначения антикоагулянтной терапии (CSBP, 2017) [106];
- АСК (80-325 мг) или клопидогрель (75 мг) могут быть вариантами выбора, который зависит от клинических обстоятельств (CSBP, 2017) [106];
- выбор антиагрегантного препарата для вторичной профилактики инсульта у лиц с некардиоэмболическим инсультом должен быть индивидуализированным с учетом факторов риска, стоимости, переносимости, относительной известной эффективности препаратов и других клинических характеристик (AHA/ASA, 2019) [107].
В соответствии с рекомендациями Европейской организации по изучению инсульта (ESO, 2021), для некоторых людей с высоким риском инсульта, у которых ТИА не связана с сердечными заболеваниями, двойная антитромбоцитарная терапия с клопидогрелем и АСК в виде таблеток в течение 24 ч после ТИА и в течение 3 нед после него выраженно снижает риск инсульта (на 19 из 1000 населения). При начале приема АСК или клопидогреля рекомендуется ввести однократную нагрузочную дозу (не менее 150 мг АСК и 300 мг клопидогреля) с последующим переходом на ежедневные стандартные поддерживающие дозы [108].
Применение АСК в остром периоде ИМ, ИИ, после аортокоронарного шунтирования (АКШ)
АСК при нестабильной стенокардии и в остром периоде острого ИМ
Активация тромбоцитов при повреждении атеросклеротической бляшки играет ключевую роль в патогенезе острых коронарных синдромов (ОКС). Кроме антиагрегантного действия, положительную роль при ОКС имеет торможение синтеза медиаторов воспаления благодаря противовоспалительному действию АСК: редуцируется мононуклеарная инфильтрация, снижается активность воспалительного процесса в сосудистой стенке и тем самым повышается стабильность бляшки [109].
При отсутствии противопоказаний АСК является обязательным средством неотложной и последующей терапии ОКС, а также обязательным компонентом комбинированной антитромбоцитарной терапии; целесообразность этих рекомендаций имеет хорошую доказательную базу.
Хотя исследований по прямому сравнению различных доз АСК не проводилось, в настоящее время при ОКС рекомендуется первую дозу (150-325 мг АСК) разжевать для более быстрого всасывания, достижения эффективной концентрации в плазме и уменьшения времени до ингибирования тромбоцитарной ЦОГ‑1 [110].
В рекомендациях по ведению пациентов с ОКС и ИМ, изданных в Финляндии, отмечается такое: если ИМ или ОКС развились у пациента, который уже принимает АСК постоянно, в момент приступа ее целесообразно назначить в дозе 100 мг [111]. Применяемая таким образом АСК обеспечивает достоверное (на 40%) уменьшение смертности и риска ИМ у больных нестабильной стенокардией [112].
В КИ ISIS‑2, рандомизированном сравнительном исследовании эффективности стрептокиназы, АСК (160 мг/сут в течение 1 мес), комбинированного лечения (стрептокиназа и АСК) или плацебо при ИМ в группе больных, получавших АСК, отмечено снижение сосудистой смертности в течение 5 нед на 23%. Эффект АСК был сопоставим с эффектом тромболитической терапии (снижение смертности на 25%) и усиливался до 42% снижения смертности при комбинированном лечении стрептокиназой и АСК [8]. Именно результаты исследования ISIS‑2 послужили основанием для включения АСК в официальные руководства по лечению ОКС [113, 114].
При ОКС эффективно применение в комбинации с АСК ингибиторов рецепторов P2Y12: клопидогреля [115], или прасугреля, или тикагрелора в течение 12 мес [26]. С теоретической точки зрения одновременное применение комбинации антиагрегантов с разным механизмом действия может привести к суммированию или потенцированию их эффектов. Высокая клиническая эффективность такой двойной антитромбоцитарной терапии была подтверждена, например, в исследовании CURE (The Clopidogrel in Unstable angina to prevent Recurrent Events) у пациентов с ОКС без подъема сегмента SТ, в котором на фоне двойной терапии АСК + клопидогрель наблюдалось снижение числа неблагоприятных исходов в группе низкого риска на 29%, в группе среднего риска – на 15%, в группе высокого риска – на 27% [116].
После ОКС при отсутствии побочных реакций рекомендуется назначение АСК на неопределенно длительное время [117].
АСК в остром периоде ИИ
В остром периоде ИИ только два метода лечения приносят очевидную пользу больным, а также имеют самую большую доказательную базу – внутривенная тромболитическая терапия рекомбинантными тканевыми активаторами плазминогена и АСК (класс I, уровень А) [62].
В 2014 г. опубликованы результаты систематического Кокрановского обзора, объединившего 8 исследований (41 183 пациента), при этом наибольшая часть из них были участниками двух крупных рандомизированных плацебо-контролируемых исследований – IST (1997) и CAST (1997) [118]. Дозы АСК в этих работах варьировали от 160 до 325 мг/сут, а длительность приема АСК/плацебо составила 4-24 нед. Анализ этих исследований показал, что в сравнении с плацебо терапия АСК приводит к уменьшению повторных ИИ на 13% [104], дополнительно предотвращая 9 смертельных исходов от любых причин на 1000 пролеченных и способствуя полному восстановлению неврологического статуса в течение 30 дней после ИИ дополнительно у 7 человек на 1000 пролеченных. Подобный эффект достигается за счет небольшого увеличения риска нефатального большого внечерепного кровотечения (дополнительно 4 случая кровотечения на 1000 пролеченных). Кроме этого, польза АСК у больных с ИИ проявляется в снижении частоты венозных тромбоэмболических осложнений [119].
Сведения о результатах применения АСК в первые часы инсульта крайне ограничены, но одно из последних прямых сравнений тромболитической терапии и АСК в остром периоде ИИ с негрубым неврологическим дефицитом (среднее время начала лечения составляло 2,7 ч; тяжесть по шкале National Institutes of Health Stroke Scale, NIHSS‑2 – Шкала тяжести инсульта Национальных институтов здоровья CША) показало преимущества АСК по исходам (у 3,2% пациентов, получавших альтеплазу, развился геморрагический инсульт против 0% пациентов, получавших АСК), а также по восстановлению функций при лучшем профиле безопасности [120].
Прием АСК целесообразно начинать как можно раньше с момента появления симптомов инсульта, но лишь после исключения внутричерепного кровоизлияния. Однако не следует использовать АСК за и через 24 ч соответственно до и после тромболитической терапии [121].
На основании результатов проведенных исследований Европейская инициатива борьбы с инсультом (EUSI) и Американская ассоциация сердца в рекомендациях по ведению больных с мозговым инсультом констатировали, что большинству больных необходимо назначение АСК не позднее 24-48 ч после возникновения инсульта. АСК (100‑300 мг/сут) может быть назначена в первые 48 ч после ИИ [121]. С целью снижения риска геморрагических осложнений через 1-2 нед от начала лечения доза АСК для длительного приема может быть уменьшена до 75-100 мг/сут, ведь не отмечается больших различий в эффективности лечения в зависимости от применения больших (до 1500 мг/сут) и малых доз АСК, хотя осложнения со стороны желудочно-кишечного тракта достоверно чаще отмечаются при приеме больших доз. Эффективность монотерапии клопидогрелем и другими антиагрегантами в остром периоде инсульта окончательно не подтверждена [122].
В последнем обзоре 2021 г. [105] также отмечается целесообразность применения АСК в остром периоде ИИ, поскольку безопасность и преимущества АСК как способа лечения острого ИИ не только были засвидетельствованы в исследованиях (IST, 1997; CAST, 1997), но и подтверждены выводами более позднего Кокрановского обзора [118]. На сегодня АСК – антиагрегант, эффективность и безопасность которого в остром периоде ИИ доказаны в крупных РКИ. Согласно международным рекомендациям, больным с острым ИИ следует проводить раннюю (в течение 48 ч) терапию АСК (предпочтительнее в желудочнорастворимых формах) [62, 123, 124].
Применение АСК при АКШ/стентировании
В 1986 г. был имплантирован первый интракоронарный стент; это породило новую проблему – повышение риска как острого, так и отсроченного тромбоза стента (ТС), частота которых до появления ДААТ (комбинация АСК и клопидогреля) достигала 9% [125]. Повышение риска тромбообразования отмечается и после баллонной пластики коронарных артерий, что также требует проведения агрессивной антитромботической терапии [28].
Применение монотерапии АСК у пациентов после АКШ, по данным крупного метаанализа Antithrombotic Trialists’ Collaboration, сопровождалось снижением риска отдаленных кардиоваскулярных событий на 53% (p=0,004) [126]. Аналогичные результаты были представлены в обзоре данных 8 РКИ по рациональности применения АСК (325-1200 мг/сут) у 2500 больных с ИБС после АКШ, у которых также отмечалось существенное снижение частоты повторных окклюзий [127]. С постепенным совершенствованием технологий и обязательного приема ДААТ (АСК + тиенопиридин) в течение 1 мес с последующим продолжением приема АСК без ограничений по времени частота развития ТС снизилась до приемлемого 1% [128].
Возможно применение также иной схемы профилактики тромбоза: после планового стентирования коронарных артерий у больных со стабильной ИБС и низким риском кровотечений рекомендуется сочетание АСК с клопидогрелем в течение 6 мес с возможностью пролонгирования до 12 мес вне зависимости от типа стента. При наличии высокого риска кровотечений пациентам показана длительность двойной терапии от 1 до 3 мес с периодической оценкой риска кровотечений и ишемических событий [129].
После прекращения комбинированной антиагрегантной терапии прием АСК в дозах, рекомендованных для проведения вторичной профилактики, должен сохраняться пожизненно [130].
Больным после стентирования или шунтирования очень важно добросовестно выполнять рекомендации врача: прекращение приема антиагрегантов является важным фактором развития поздних тромбозов у больных с голометалическим стентом. В исследовании у пациентов с ангиографически документированным поздним ТС ни у одного из больных, продолжавших прием ДААТ, тромбоз не развился. В другом 9-месячном исследовании, где зарегистрировано 14 подострых и 15 поздних тромбозов, самым важным фактором риска развития указанных событий было преждевременное прекращение приема антиагрегантов, что повышало риск его развития в 90 раз [131].
Нужно ли прекращать плановый прием АСК перед оперативными вмешательствами? Имеются данные КИ о возможности не прерывать прием препарата, используя АСК в дозе 75-150 мг у пациентов с ИБС до самого дня проведения АКШ. Как следствие, отмечается снижение риска периоперационных ишемических событий, а при соблюдении мер профилактики геморрагических осложнений не наблюдается значительного повышения частоты больших кровотечений в течение и после оперативного лечения [132]. В настоящее время такой подход закреплен в ряде зарубежных клинических рекомендаций [133].
Довідка «ЗУ»
На українському ринку ацетилсаліцилова кислота представлена вітчизняним препаратом Магнікор виробництва АТ «Київський вітамінний завод». Цей лікарський засіб відповідає світовим стандартам ефективності та безпеки. Магнікор випускається в таблетках, вкритих плівковою захисною оболонкою, в зручному дозуванні (150 та 75 мг ) для навантажувальної та підтримувальної терапії.
Магнікор показаний до застосування:
- при гострій та хронічній ІХС;
- з метою профілактики повторного тромбоутворення;
- для первинної профілактики тромбозів, серцево-судинних захворювань, як-от гострий коронарний синдром, у пацієнтів віком від 50 років, у яких наявні фактори ризику розвитку захворювань серцево-судинної системи: АГ, гіперхолестеринемія, цукровий діабет, ожиріння, спадковий анамнез.
Читати продовження >>
Медична газета «Здоров’я України 21 сторіччя» № 19 (512), 2021 р.