30 листопада, 2021
Територія правильного ритму: безпека, доведена практикою
Однією із найпоширеніших стійких аритмій є фібриляція передсердь (ФП), що пов’язана з розвитком небезпечних ускладнень та погіршенням якості життя хворих. Відновлення та підтримка нормального синусового ритму – бажана мета для багатьох пацієнтів із ФП, однак ця стратегія обмежена відносно невеликою кількістю антиаритмічних препаратів (ААП), доступних для контролю ритму при ФП. Тож як обрати ефективний і безпечний шлях розв’язання цієї проблеми? Та що насамперед контролювати при ФП – частоту серцевих скорочень (ЧСС) чи ритм? Провідний науковий співробітник відділу реанімації та інтенсивної терапії, д. мед. н. Олег Ігорович Іркін та старша наукова співробітниця відділу аритмій серця (ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України», м. Київ), к. мед. н. Олена Миколаївна Романова детально розглянули ці питання в межах ХІІ Національного конгресу кардіологів України, що відбувся цьогоріч у вересні.
Порівняння підходів до контролю ЧСС та ритму: результати досліджень
На сьогодні існує два підходи щодо лікування ФП: перший – це збереження синусового ритму за допомогою медикаментозної чи електричної кардіоверсії, другий – терапія, спрямована на контроль ЧСС, але таке лікування не впливає на порушення ритму. Ще 2002 р. у дослідженні AFFIRM порівнювали ефективність цих двох стратегій. За результатами випробування, автори не виявили суттєвої різниці щодо ефективності між двома підходами до лікування ФП. Також було показано, що в пацієнтів, у яких контролювали ритм, а не ЧСС, спостерігалося більше побічних ефектів, таких як брадикардія, подовження інтервалу QT та гастроінтестинальні порушення.
Сучасні дослідження демонструють дещо інші результати. Так, за даними великого метааналізу J.P. Kelly (2019), контроль ритму, а не частоти, достовірно знижував такі показники, як:
- ризик госпіталізації;
- ймовірність розвитку інсульту;
- ризик серцевої недостатності (СН);
- загальна смертність.
Результати дослідження CASTLE-AF (2018) показали, що на тлі більш радикального методу відновлення ритму – процедури катетерної абляції, у хворих на ФП та СН зі зниженою фракцією викиду (СНзнФВ) уповільнювалося прогресування СН, зменшувалася імовірність госпіталізації з приводу СН і смерті від усіх причин.
У рандомізованому випробуванні, присвяченому контролю ритму за допомогою абляції та ЧСС у пацієнтів із СН та ФП, було з’ясовано, що в осіб із СНзнФВ <45% процедура абляції та утримання синусового ритму суттєвіше покращувала виживаність хворих, ніж у таких зі збереженою ФВ (Parkash et al., 2021). Окрім того, у міжнародному відкритому дослідженні EAST-AFNET 4, в якому взяли участь 2789 пацієнтів із ФП зі 135 медичних центрів, також було доведено, що саме жорстке і раннє відновлення й утримання синусового ритму за допомогою ААП або катетерної абляції, а не контроль ЧСС пов’язані із достовірно нижчим ризиком розвитку несприятливих серцево-судинних подій (як-то госпіталізація, пов’язана із СН, гострий коронарний синдром), інсульту або серцево-судинної смерті (Galiuto et al., 2020).
Олена Миколаївна зупинилася на деяких положеннях настанов ESC щодо ведення пацієнтів із ФП 2020 р. Так, рекомендованою є стратегія «АВС», де:
- А – антикоагулянтна терапія з метою запобігання інсульту; в межах цього напряму запропоновано оцінити ризики кровотеч та підібрати оптимальний антикоагулянт;
- В – кращий контроль симптомів, коли слід оцінити симптоми, якість життя і уподобання пацієнта, а також оптимізувати контроль клінічних показників та обрати стратегію контролю серцевого ритму.
- С – коморбідність, моніторинг факторів ризику серцево-судинних захворювань.
Стратегія контролю ритму
Стратегія контролю ритму стосується спроб відновити/підтримувати синусовий ритм і також може включати комбінацію терапевтичних підходів, зокрема кардіоверсію, ААП і катетерну абляцію разом із належним контролем ЧСС, антикоагулянтною та комплексною серцево-судинною профілактичною терапією (ESC, 2020).
Показаннями для застосування ААП є наявність симптомів, їх тяжкість та асоційовані з ними стани, що прогнозують погану переносимість епізодів ФП. При виборі ААП головним критерієм є мінімізація протиаритмогенного ризику й органотоксичності. Як зазначено в рекомендаціях Європейського товариства кардіологів (ESC, 2020), з метою зменшення ймовірності протиаритмогенних ускладнень слід оцінювати динаміку електрокардіограми після лікування.
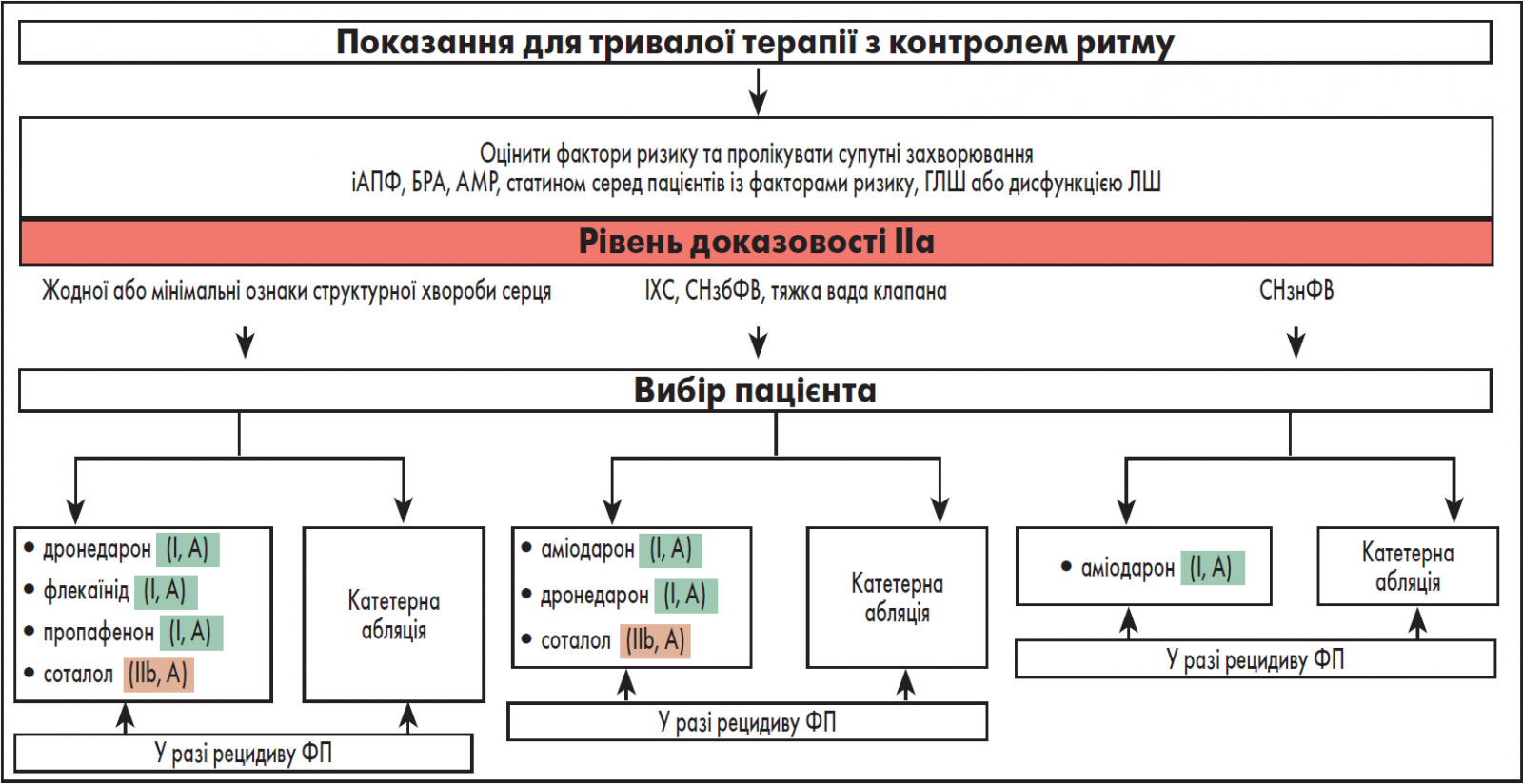
Тактику початку довгострокового контролю ритму в симптомних пацієнтів із ФП відображено на рисунку.
Рисунок. Тактика початку довгострокового контролю ритму в симптомних пацієнтів із ФП
Примітки: іАПФ – інгібітор ангіотензинперетворювального ферменту, БРА – блокатор рецепторів ангіотензину ІІ,
АМР – антагоніст мінералокортикоїдних рецепторів, ГЛШ – гіпертрофія лівого шлуночка, СНзбФВ – серцева недостатність зі збереженою фракцією викиду.
Олег Ігорович наголосив, що у пацієнтів зі структурними ураженнями серця стратегією вибору для відновлення та утримання синусового ритму є насамперед катетерна абляція, а медикаментозна палітра засобів для таких хворих є вкрай обмеженою. На противагу, спектр ААП для відновлення синусового ритму в осіб із мінімальними структурними змінами серця або без таких є значно ширшим. Зокрема, доступні такі ААП ІС класу, як флекаїнід (І, А), пропафенон (І, А) і ААП ІІІ класу – дронедарон (І, А), соталол (ІІb, А).
Також спікери детальніше зупинилися на ефективності та особливостях застосування молекули флекаїніду. На сучасному фармацевтичному ринку України флекаїнід, зокрема, представлений препаратом Ліксарит («Асіно») у дозі 100 мг. Флекаїнід виводиться нирками, а отже, при його застосуванні слід контролювати кліренс креатиніну. Якщо цей показник становить <50 мл/хв, дозування потрібно зменшити вдвічі. З метою запобігання розвитку проаритмогенних ефектів флекаїніду необхідний регулярний моніторинг електрокардіограми, та у разі подовження комплексу QRS ˃25% від вихідного рівня застосування препарату слід припинити.
Порівняння флекаїніду із пропафеноном
Як зазначив Олег Ігорович, є досить показові відмінності між цими двома препаратами.
Так, період напіввиведення флекаїніду становить 20 год. У пропафенону цей час коротший – 5‑8 год, тому варто розуміти, що кратність призначення препаратів буде різною. Біодоступність флекаїніду складає 90%. Таке чітке окреслення даного показника свідчить про те, що діяти він буде у кожного пацієнта приблизно однаково. Своєю чергою біодоступність пропафенону – 25‑75%, а це означає, що у кожного пацієнта він може діяти по-різному. Як зазначалося, шлях елімінації у флекаїніду – нирки, у пропафенону ж – печінка.
Необхідно пам’ятати, що на відміну від флекаїніду, пропафенон має достатньо виразний β-блокувальний ефект, через який наявні певні обмеження його застосування при таких станах, як дисфункція синоатріального чи атріовентрикулярного вузла, блокада ніжок пучка Гіса, подовження інтервалу QT, синдром Бругада, ІХС, декомпенсована хронічна СН. До відносних протипоказань також можна віднести хронічне обструктивне захворювання легень і бронхіальну астму.
Цікаво, що пік концентрації пропафенону становить 1‑3 год, флекаїніду – 3‑4 год. Однак у дослідженні D.S. Echt et al. (2019), в якому порівнювали ці препарати, було продемонстроване переважання швидкості настання клінічного ефекту вже протягом 1 год у флекаїніду порівняно із пропафеноном.
Ліксарит: протирецидивна терапія
Звичайна доза флекаїніду (Ліксариту) становить 100 мг двічі на добу, і за відсутності рецидивів порушення ритму протягом трьох місяців її можна зменшувати вдвічі. У разі зриву ритму на тлі планової протирецидивної терапії доцільно застосовувати стратегію «таблетка в кишені», яка передбачає наступний алгоритм дій: спочатку хворий має прийняти 200 мг флекаїніду для переривання повторних епізодів ФП, а за умови збереження ФП – повторно у дозі 100 мг через 2 год. Незалежно від того, відновився синусовий ритм чи ні, вечірнє планове приймання 100 мг препарату слід пропустити, оскільки його добова доза не повинна перевищувати 400 мг. Після відновлення ритму пацієнт має продовжити планову протирецидивну терапію.
О.М. Романова також акцентувала увагу на таких перевагах підходу «таблетка в кишені»:
- висока ефективність у відновленні синусового ритму (90%);
- швидке відновлення ритму після приймання флекаїніду;
- низький ризик тяжких побічних реакцій;
- відсутність потреби у госпіталізації, що дає змогу значно зменшити витрати на медичне обслуговування;
- покращення якості життя пацієнта.
О.І. Іркін зауважив, що стратегію «таблетка в кишені» можна застосовувати тоді, коли ефективність і безпеку препарату було попередньо встановлено в лікарні. Контроль ритму після використання даної схеми проводять через 24 год.
Олена Миколаївна нагадала присутнім про спільне засідання ради експертів із порушень ритму серця Асоціації кардіологів та президії аритмологів України, яке відбулося 11‑12 жовтня 2018 р. в Одесі. На цьому засіданні практично всі експерти погодилися з тим, що протирецидивну терапію слід застосовувати, якщо пароксизми ФП виникають частіше ніж один раз на місяць. За кратності пароксизмів від одного разу на місяць до одного разу на рік тактика може бути спрямована на подолання приступу («таблетка в кишені»).
Окрім того, на вказаному заході був погоджений важливий аспект застосування флекаїніду, а саме те, що його комбінація із β-блокаторами вважається доцільною.
Висновки
- Стратегія контролю синусового ритму, а не ЧСС є першочерговою при веденні хворих на ФП.
- Інвазивні методи лікування ФП мають переваги в осіб із виразними структурними ураженнями серця.
- Представник ІС класу ААП флекаїнід (Ліксарит) має високу ефективність як для протирецидивної терапії, так і фармакологічної кардіоверсії у пацієнтів без виразних структурних змін серця.
- У разі призначення флекаїніду необхідно оцінювати кліренс креатиніну для вибору ефективної та безпечної дози з метою використання в межах протирецидивної терапії та для відновлення синусового ритму.
- На підставі світових наукових даних і власного досвіду клінічного застосування флекаїніду (Ліксариту) лектори підсумували, що: препарат демонструє високу ефективність при відновленні пароксизмів ФП, а також забезпечує відновлення синусового ритму протягом 3‑8 год у 94% пацієнтів. Окрім того, стратегія «таблетка в кишені» із застосуванням флекаїніду є зручною та ефективною.
Підготувала Мар’яна Гнатів
UA-LICS-PUB-112021-024